Analizar la repercusión del antidepresivo vortioxetina sobre la función sexual, frente a inhibidores selectivos de la recaptación de serotonina (ISRS) e inhibidores selectivos mixtos de la recaptación de serotonina y noradrenalina (IRSN o Duales) en pacientes con depresión.
Material y métodosEstudio analítico, observacional, longitudinal y prospectivo en el que se incluyeron hombres y mujeres mayores de 18años con trastorno depresivo y actividad sexual en pareja, separándolos en dos grupos: 1)de estudio: inician tratamiento con vortioxetina; 2)control: mantienen tratamiento con ISRS o Duales. Se realizaron tres visitas: inclusión, seguimiento a las 4semanas y final 3meses desde la inclusión. El periodo total de seguimiento fue de 3meses.
ResultadosSe incluyeron 87 pacientes (edad media, 46,85años). Al final del estudio se hallaron diferencias significativas (DS) en el valor medio de la suma de las puntuaciones de los dominios evaluadores de la respuesta sexual del cuestionario de Función Sexual de la Mujer (FSM-2) entre el grupo de estudio y el de control (22,42±4,39 y 16,13±7,76, respectivamente), con menor riesgo de disfunción sexual en las mujeres tratadas con vortioxetina. También menor riesgo de disfunción sexual en estas mismas mujeres en los dominios de deseo, lubricación, orgasmo, frecuencia sexual y satisfacción sexual. Estas diferencias no se hallaron al evaluar la función sexual masculina.
ConclusionesLas mujeres tratadas con vortioxetina presentaron mejor función sexual que las tratadas con ISRS o Duales y menor riesgo de disfunción sexual.
To analyze the impact of the antidepressant vortioxetine on sexual function, compared to selective serotonin reuptake inhibitors (SSRIs) and mixed selective serotonin and norepinephrine reuptake inhibitors (IRSN or Dual) in patients with depression.
Material and methodsAnalytical, observational, longitudinal and prospective study, which included men and women over 18years of age, with depressive disorder and sexual activity with a partner, separating them into two groups: (i)study, starting treatment with vortioxetine; (2)control, maintaining treatment with SSRIs or Duals. Three visits were made: inclusion, follow-up at 4weeks and final 3months from inclusion. The total follow-up period was 3months.
ResultsA total of 87 patients were included (mean age 46.85years). At the end of the study, significant differences (SD) were found in the mean value of the sum of the scores of the evaluative domains of the sexual response of the Women's Sexual Function Questionnaire (FSM-2) between the study group and the control (22.42±4.39 and 16.13±7.76, respectively), with a lower risk of sexual dysfunction in women treated with vortioxetine. Also, lower risk of sexual dysfunction in these same women in the domains of desire, lubrication, orgasm, sexual frequency and sexual satisfaction. These differences were not found when assessing male sexual function.
ConclusionsWomen treated with vortioxetine presented better sexual function than those treated with SSRIs or Duals and a lower risk of sexual dysfunction.
A nivel mundial, los trastornos mentales suponen el 22,8% del total de enfermedades, siendo la depresión el más frecuente, estimándose en 350 millones el número de personas afectadas en todo el mundo1. Los trastornos depresivos (TD) constituyen un grupo de entidades clínicas que en su mayor parte son diagnosticadas y tratadas en atención primaria, remitiéndose a atención especializada los cuadros más graves o cuando la respuesta al tratamiento antidepresivo instaurado no ha sido satisfactoria.
El consumo de antidepresivos en España en 2015 fue de 73,1 dosis diarias por cada 1.000 habitantes, que pasaron a ser 92 dosis diarias en 20212. Este aumento se ha producido en la mayoría de los países y se relaciona con la pandemia por coronavirus. Los antidepresivos más prescritos en nuestro país son los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores selectivos mixtos de la recaptación de serotonina y noradrenalina (Duales o IRSN), pero es conocido que pueden provocar disfunciones sexuales3. La disfunción sexual es uno de los efectos secundarios más duraderos en los pacientes tratados con antidepresivos, a pesar de que su aparición se subestima en las fichas técnicas de estos fármacos, en donde se informa de una incidencia entre el 1 y el 10%4. Estos porcentajes son muy bajos al compararlos con los estimados en la práctica clínica diaria, así como en estudios específicos5, incluidas revisiones sistemáticas3,6 y metaanálisis7. El motivo de esta subestimación se debe a que la incidencia de disfunción sexual que figura en las fichas técnicas ha sido obtenida mediante ensayos de fármacos registrados y estudios de eficacia a corto plazo, a menudo poco fiables al incluir pacientes muy seleccionados y sexualmente no activos4. También, porque no se han utilizado cuestionarios validados para llevar a cabo dichos ensayos, recurriendo a menudo a informes poco fiables. Utilizando grandes muestras de pacientes y recurriendo a cuestionarios validados y fiables, numerosos estudios demuestran que la prevalencia real de disfunción sexual es del 50-75% en pacientes tratados con los antidepresivos más prescritos en las consultas de medicina de familia y de psiquiatría, sin distinción entre hombres y mujeres, siendo mayor entre quienes recibieron tratamiento con ISRS8. En voluntarios sanos, que tomaron un ISRS durante al menos 8semanas, la prevalencia fue superior al 80%9.
Vortioxetina, un antidepresivo de características especiales10, no parece tener efectos adversos sobre la función sexual11. Introducido en el mercado farmacéutico en 2016, se trata de un inhibidor de la recaptación de serotonina que actúa como agonista o antagonista en función del receptor serotoninérgico (agonista 5-HT1A, agonista parcial 5-HT1B y antagonista 5-HT1D, 5-HT3 y 5-HT7), modulando la neurotransmisión también en otros sistemas (noradrenalina, dopamina, histamina, acetilcolina, GABA y glutamato), actividad responsable de sus efectos antidepresivos y ansiolíticos. Sin embargo, hay pocos estudios que evalúen la función sexual en pacientes tratados con vortioxetina frente a los antidepresivos antes referidos12, motivo por el cual nos animamos a realizar este estudio.
Con la intención de aportar datos sobre la efectividad y la tolerabilidad de los antidepresivos, en un área terapéutica en la cual los médicos de familia están muy implicados, creímos pertinente realizar esta investigación. Además, existe una limitación de la evidencia actual en este campo, al faltar estudios comparativos entre vortioxetina y los antidepresivos más habitualmente prescritos en cuanto a efectividad y tolerabilidad13. Por todo lo cual consideramos justificada su realización.
Nuestro objetivo en este estudio ha sido analizar la repercusión de vortioxetina sobre la función sexual, frente a ISRS y Duales, en pacientes afectados por TD en el ámbito de la medicina de familia (atención primaria), partiendo de la hipótesis de que el riesgo de disfunción sexual con su uso es menor, tal y como algunos estudios previos indican14.
Material y métodosEstudio analítico, observacional, longitudinal y prospectivo en el que se incluyen pacientes mayores de 18años con TD que acudieron a la consulta de su médico de familia, desde marzo a junio de 2021, y que mantenían actividad sexual en pareja. Mediante muestreo consecutivo, los investigadores ofrecieron cada día participar en el estudio a los dos primeros pacientes mayores de 18años en tratamiento con antidepresivos que acudían a la consulta por cualquier motivo. Del mismo modo, a aquellos subsidiarios de ser tratados con dichos fármacos por presentar TD. Las personas incluidas procedían de seis centros de salud de la provincia de Valencia (España) pertenecientes a las poblaciones de Xàtiva, Rotglá-Corbera, L’Alcúdia, Alzira, Guadassuar y Alaquàs, siendo excluidas quienes tomaban más de un fármaco antidepresivo o fármacos antipsicóticos, los afectados por enfermedades graves y los tratados con hormonas u otros medicamentos que pudieran interferir en la respuesta sexual. También se excluyó a los consumidores excesivos de alcohol o de otras sustancias de abuso.
Como criterio médico para diagnosticar el TD y su gravedad se consideraron las puntuaciones obtenidas mediante la Montgomery-Asberg Depression Rating Scale (MADRS)15 y la Escala de Impresión Cínica Global de Gravedad de la Enfermedad (CGI)16. Para valorar la función sexual se tuvieron en cuenta los valores obtenidos con los cuestionarios validados de Función Sexual del Hombre (FSH)17 y de Función Sexual de la Mujer (FSM-2)18, según fuera el sexo del paciente.
Mediante muestreo consecutivo se separaron los pacientes en dos grupos:
- •
Grupo 1, o de estudio. Se incluyen pacientes que inician tratamiento con vortioxetina por una de estas causas: a)son diagnosticados de novo de TD (MADRS ≥7), y b)están siendo tratados con ISRS o Duales, pero la mejoría del TD es insuficiente, según criterio del médico investigador, considerando los resultados obtenidos con las escalas MADRS y CGI, o el paciente se muestra insatisfecho, bien respecto a la eficacia del tratamiento antidepresivo anterior, bien por alguno de sus efectos adversos.
- •
Grupo 2, de control. Pacientes tratados previamente con ISRS o Duales que siguen con el mismo tratamiento por mejoría suficiente del TD, según criterio del médico investigador, considerando los resultados obtenidos con las escalas MADRS y CGI, y satisfacción del paciente con el tratamiento antidepresivo anterior respecto a su eficacia y su tolerancia.
Para el cálculo del tamaño de la muestra, a fin de realizar un contraste de hipótesis bilateral entre los pacientes de ambos grupos, suponiendo un descenso de los valores medios de la MADRS en el grupo1 de 1,5 puntos respecto al descenso obtenido con los tratados del grupo2, y una desviación típica en ambos grupos de 4, se obtendría un «tamaño del efecto d» de 0.375. Considerando un nivel de significación α (error tipoI) de 0,05 y una potencia estadística de 0,95 (1: error β o tipoII), se obtuvo una muestra mínima para cada grupo de 186 individuos y un total de 372. Suponiendo una proporción de pérdidas del 15%, se esperó alcanzarla mediante la selección inicial de 450 individuos.
Se realizaron tres visitas en ambos grupos. Una primera (V1) de inclusión; la segunda (V2), de seguimiento 4semanas después, y la tercera (V3), visita final 3meses después de V1.
El análisis estadístico de los valores obtenidos en ambos grupos se realizó por comparación de medias mediante la t de Student, si la distribución de la muestra era normal. En caso de no distribución normal de la muestra, se recurrió a la comparación de medianas mediante las pruebas no paramétricas de Kruskal-Wallis y U de Mann-Whitney.
ResultadosPacientes incluidos: 87 (31 hombres y 56 mujeres). Edad media: 46,85años ±12,52 (máximo 76años, mínimo 19).
En V1 se incluyen en el grupo1: 51 pacientes (58,6%), 18 hombres y 33 mujeres; en el grupo2 se incluyen 36 pacientes (41,4%), 13 hombres y 23 mujeres. Dosis media inicial de vortioxetina en el grupo1: hombres 10,28mg ±2,69; mujeres 10,50mg ±2,73.
En V3, finalizan el estudio en el grupo1: 42 pacientes (56,7%), 19 hombres y 23 mujeres; finalizan el estudio en el gupo2: 32 pacientes (43,2%), 9 hombres y 23 mujeres. Dosis media final de vortioxetina en el grupo1: hombres 13,42mg ±3,74; mujeres 12,27mg ±4,28.
No finalizan el estudio 13 pacientes: 2 hombres y 9 mujeres por náuseas y vómitos, y 1 hombre y 1 mujer por pérdida de seguimiento. En total, problemas de tolerabilidad o acontecimientos adversos en 14 pacientes: 5 hombres y 9 mujeres (náuseas y vómitos leves), todos ellos pertenecientes al grupo1.
Análisis de efectividadEn V1 la puntuación de MADRS fue: en el grupo1 (n=51): 27,69±7,94; en el grupo2 (n=36): 20,39±11,70; t de Student entre ambos grupos: 0,01, diferencias significativas (DS), con puntuaciones menores (menor gravedad del TD) en el grupo2 (tratados previamente con antidepresivos).
En V3 la puntuación de MADRS fue: en el grupo 1 (n=43): 13,40±9,33; en el grupo2 (n=32): 13,81±7,69; t de Student entre ambos grupos: 0,83 (no DS).
Evaluación de la función sexual en los hombresEn V1, los valores medios de la suma de las puntuaciones de los seis dominios evaluadores de la respuesta sexual (DERS) del cuestionario FSH fueron: en el grupo1 (n=18): 15,19±4,38; en el grupo2 (n=13): 15,50±3,17; t de Student entre ambos grupos: 0,83 (no DS).
En V3, los valores medios de la suma de las puntuaciones de los seis DERS fueron: en el grupo1 (n=19): 16,36±3,51; en el grupo2 (n=9): 17,88±2,20; t de Student entre ambos grupos: 0,24 (no DS). Los valores medios de la suma de los DERS en el subgrupo de pacientes del grupo2 tratados con ISRS (n=8): 17,68±2,26; al compararlos con los valores en los tratados con vortioxetina (ya expuesto), no se hallaron DS (t de Student: 0,34).
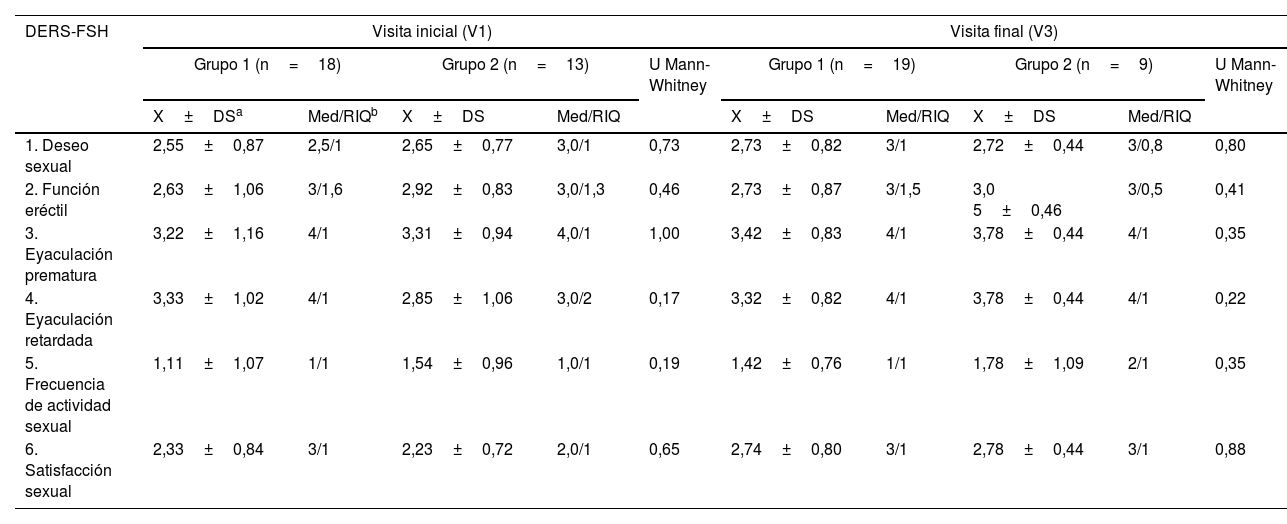
Respecto a las puntuaciones en cada uno de los seis DERS del cuestionario FSH, en V1 no se hallaron DS entre los hombres incluidos en el grupo1 (n=18) y los incluidos en el grupo2 (n=13) (ver valores medios y medianas en la tabla 1). Tampoco DS entre ambos grupos en V3 (tabla 1).
Valor medio de las puntuaciones y mediana en cada uno de los seis DERS del cuestionario FSH en hombres
| DERS-FSH | Visita inicial (V1) | Visita final (V3) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Grupo 1 (n=18) | Grupo 2 (n=13) | U Mann-Whitney | Grupo 1 (n=19) | Grupo 2 (n=9) | U Mann-Whitney | |||||
| X±DSa | Med/RIQb | X±DS | Med/RIQ | X±DS | Med/RIQ | X±DS | Med/RIQ | |||
| 1. Deseo sexual | 2,55±0,87 | 2,5/1 | 2,65±0,77 | 3,0/1 | 0,73 | 2,73±0,82 | 3/1 | 2,72±0,44 | 3/0,8 | 0,80 |
| 2. Función eréctil | 2,63±1,06 | 3/1,6 | 2,92±0,83 | 3,0/1,3 | 0,46 | 2,73±0,87 | 3/1,5 | 3,0 5±0,46 | 3/0,5 | 0,41 |
| 3. Eyaculación prematura | 3,22±1,16 | 4/1 | 3,31±0,94 | 4,0/1 | 1,00 | 3,42±0,83 | 4/1 | 3,78±0,44 | 4/1 | 0,35 |
| 4. Eyaculación retardada | 3,33±1,02 | 4/1 | 2,85±1,06 | 3,0/2 | 0,17 | 3,32±0,82 | 4/1 | 3,78±0,44 | 4/1 | 0,22 |
| 5. Frecuencia de actividad sexual | 1,11±1,07 | 1/1 | 1,54±0,96 | 1,0/1 | 0,19 | 1,42±0,76 | 1/1 | 1,78±1,09 | 2/1 | 0,35 |
| 6. Satisfacción sexual | 2,33±0,84 | 3/1 | 2,23±0,72 | 2,0/1 | 0,65 | 2,74±0,80 | 3/1 | 2,78±0,44 | 3/1 | 0,88 |
En V1, los valores medios de la suma de las puntuaciones de los ocho DERS del cuestionario FSM-2 fueron: en el grupo1 (n=33): 17,18±6,99, mediana 19,00 y rango intercuartil (RIQ) 8; en el grupo2 (n=23): 15,13±8,43, mediana 19,00 y RIQ 18; U de Mann-Whitney: 0,45 (no DS entre ambos grupos).
En V3, los valores medios de la suma de los DERS fueron: en el grupo1 (n=23): 22,42±4,39, mediana 23,00 y RIQ 7; en el grupo2 (n=23): 16,13±7,76, mediana 19,00 y RIQ 12; U de Mann-Whitney: 0,003; hay DS, con puntuaciones más altas (y por tanto menor riesgo de disfunción sexual), en mujeres tratadas con vortioxetina. Al comparar los valores medios de la suma de los DERS en las mujeres del grupo1 (n=23) (antes referidos) con las del grupo2, tratadas específicamente con ISRS (n=10): 18,00±5,94, mediana 19,50 y RIQ 10, se hallaron DS (U de Mann-Whitney: 0,042), con puntuaciones más altas (menor riesgo de disfunción sexual) en mujeres tratadas con vortioxetina. Al comparar los valores medios de la suma de los DERS en las mujeres del grupo1 (n=23) (antes referidos) con las del subgrupo de pacientes del grupo2 tratadas específicamente con desvenlafaxina (n=9): 15,00±10,11, mediana 22,00 y RIQ 21, se hallaron DS (U de Mann-Whitney: 0,032), con puntuaciones más altas (menor riesgo de disfunción sexual) en mujeres tratadas con vortioxetina.
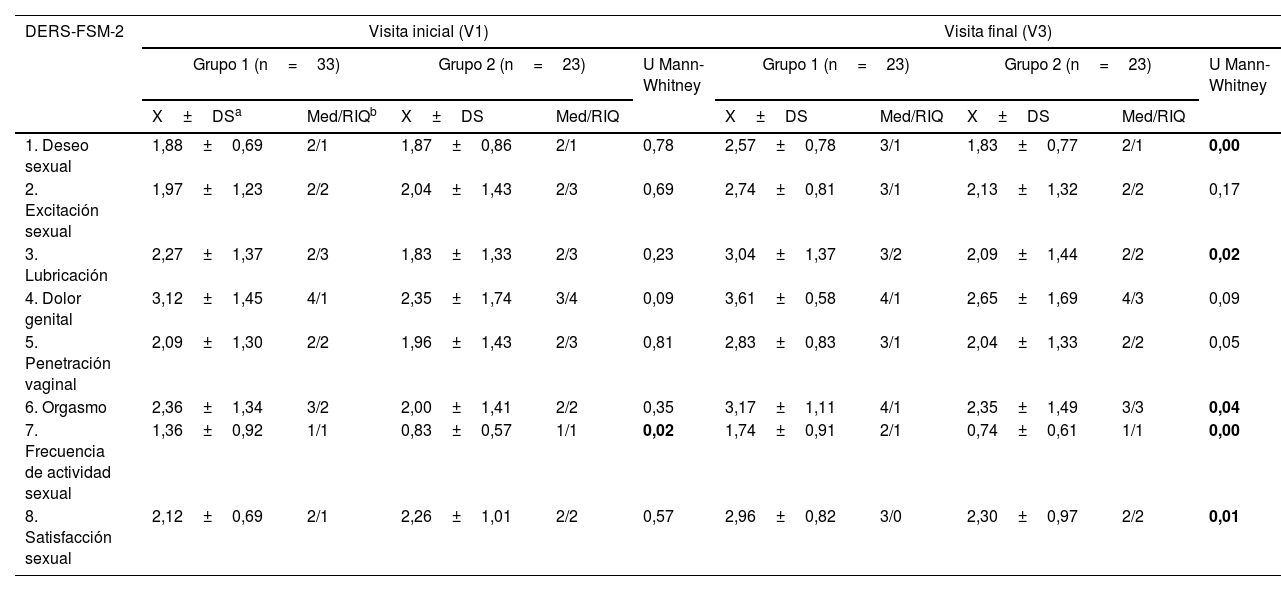
Respecto a las puntuaciones en cada uno de los ocho DERS del cuestionario FSM-2, la frecuencia sexual en V1 fue significativamente mayor entre las mujeres del grupo1 (n=33) al compararlo con las del grupo2 (n=23) (ver valores medios y medianas en tabla 2). También se hallaron DS entre ambos grupos en V3 en los dominios de deseo, lubricación, orgasmo, frecuencia de actividad sexual y satisfacción sexual, con puntuaciones más altas (menor riesgo de disfunción sexual) en las mujeres del grupo1 (tabla 2).
Valor medio de las puntuaciones y mediana en cada uno de los ocho DERS del cuestionario FSM-2 en mujeres
| DERS-FSM-2 | Visita inicial (V1) | Visita final (V3) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Grupo 1 (n=33) | Grupo 2 (n=23) | U Mann-Whitney | Grupo 1 (n=23) | Grupo 2 (n=23) | U Mann-Whitney | |||||
| X±DSa | Med/RIQb | X±DS | Med/RIQ | X±DS | Med/RIQ | X±DS | Med/RIQ | |||
| 1. Deseo sexual | 1,88±0,69 | 2/1 | 1,87±0,86 | 2/1 | 0,78 | 2,57±0,78 | 3/1 | 1,83±0,77 | 2/1 | 0,00 |
| 2. Excitación sexual | 1,97±1,23 | 2/2 | 2,04±1,43 | 2/3 | 0,69 | 2,74±0,81 | 3/1 | 2,13±1,32 | 2/2 | 0,17 |
| 3. Lubricación | 2,27±1,37 | 2/3 | 1,83±1,33 | 2/3 | 0,23 | 3,04±1,37 | 3/2 | 2,09±1,44 | 2/2 | 0,02 |
| 4. Dolor genital | 3,12±1,45 | 4/1 | 2,35±1,74 | 3/4 | 0,09 | 3,61±0,58 | 4/1 | 2,65±1,69 | 4/3 | 0,09 |
| 5. Penetración vaginal | 2,09±1,30 | 2/2 | 1,96±1,43 | 2/3 | 0,81 | 2,83±0,83 | 3/1 | 2,04±1,33 | 2/2 | 0,05 |
| 6. Orgasmo | 2,36±1,34 | 3/2 | 2,00±1,41 | 2/2 | 0,35 | 3,17±1,11 | 4/1 | 2,35±1,49 | 3/3 | 0,04 |
| 7. Frecuencia de actividad sexual | 1,36±0,92 | 1/1 | 0,83±0,57 | 1/1 | 0,02 | 1,74±0,91 | 2/1 | 0,74±0,61 | 1/1 | 0,00 |
| 8. Satisfacción sexual | 2,12±0,69 | 2/1 | 2,26±1,01 | 2/2 | 0,57 | 2,96±0,82 | 3/0 | 2,30±0,97 | 2/2 | 0,01 |
Al prescribir un fármaco antidepresivo, tanto los médicos de atención primaria como los de atención especializada tienen en cuenta su eficacia y su tolerabilidad19, pero en pocas ocasiones su posible repercusión sobre la función sexual20, aspecto relevante para la calidad de vida21 en cualquier persona interesada en disfrutar de una vida sexual satisfactoria, que es la mayoría y, por supuesto, entre quienes sufren depresión22.
Pese a su importancia, ni los médicos de familia ni los psiquiatras suelen interesarse por las cuestiones sexuales de los pacientes con TD en la práctica clínica diaria23, y tampoco estos suelen exponer sus problemas sexuales al médico, ya que la comunicación espontánea de los mismos no supera el 20-40%8. Todo esto hace que se subestime la prevalencia de disfunción sexual secundaria al tratamiento antidepresivo en las consultas.
Sin embargo, los pacientes tratados con antidepresivos toleran mal la disfunción sexual, ya que, según los resultados de un estudio bien elaborado24, solo el 24,5% de ellos mostraron buena tolerancia al problema sexual, mientras que el 42,5% y el 32,9%, respectivamente, manifestaron tolerancia regular o mala. Así pues, considerar esta cuestión a la hora de prescribir fármacos antidepresivos, y preguntar a los pacientes ya tratados sobre la posible presencia de disfunción sexual, es importante para alcanzar un adecuado cumplimiento terapéutico25, así como una buena adherencia al tratamiento26.
A la hora de hacerlo, se ha de manifestar la preocupación por el bienestar y la calidad de vida del paciente, informándole de manera neutral sobre los posibles efectos adversos de estos medicamentos en la esfera sexual, preguntándole con claridad si ha notado alguna merma en su respuesta sexual. Solicitar la cumplimentación de los cuestionarios autoadministrados FSH y FSM-2 puede ser una estrategia útil para desenmascarar, con garantías, cualquier problema sexual, especialmente en pacientes que se muestran remisos a responder a nuestras preguntas, dada la privacidad que dichos instrumentos psicométricos ofrecen, su fiabilidad y su rápida cumplimentación (entre 5 y 10minutos).
Aunque las náuseas y los vómitos sean un efecto adverso frecuente al utilizar vortioxetina27, hecho que hemos podido confirmar en este estudio, nuestros resultados coinciden con otros que demuestran la ventaja de utilizar dicho fármaco como antidepresivo, al preservar mejor la función sexual que ISRS o Duales28.
Una limitación importante del estudio ha sido en relación al tamaño de la muestra inicialmente prevista, muy superior a la obtenida finalmente. No alcanzarlo se ha debido, sobre todo, por coincidir el desarrollo del mismo con el periodo más álgido de la pandemia por COVID-19, lo cual ha dificultado sobremanera la captación de pacientes a incluir por parte de los investigadores, que por la misma razón al final se han reducido a 11 de los 50 que se preveía participasen. Como consecuencia, el número de hombres estudiados ha sido corto, lo que tal vez explique que, en ellos, a diferencia de lo hallado en las mujeres estudiadas, no existan diferencias significativas en las puntuaciones del cuestionario de función sexual del hombre (FSH) en relación con haber sido tratados con antidepresivos ISRS, Duales o vortioxetina.
Otra posible limitación, frecuente en cualquier estudio sobre sexualidad humana, es que algunos pacientes se muestren reticentes a responder con sinceridad a los cuestionarios de evaluación sexual que han de cumplimentar. Para evitarlo, los investigadores apelaron a su sinceridad, garantizándoles la confidencialidad y el anonimato, imprescindible para que las respuestas a los cuestionarios de función sexual, FSH y FSM-2, fueran veraces. Consideramos, además, que este posible sesgo es asumible, conociendo las características de dichos instrumentos que han sido diseñados para minimizar tal circunstancia. Por todas estas razones, creemos que los datos obtenidos son fiables.
Estos resultados favorables en la respuesta sexual de mujeres tratadas con vortioxetina, respecto a ISRS y Duales, se han de confirmar en un futuro estudio en el que la muestra de personas incluidas sea más cuantiosa. Esto nos permitirá analizar si tales beneficios se producen también en hombres, y si se mantienen cuando se recurre a dosis de vortioxetina más altas que las utilizadas en la presente investigación.
ConclusionesEn la muestra analizada no se hallaron diferencias significativas en la efectividad de vortioxetina, al compararla con la de ISRS y Duales. Tampoco en la función sexual de los hombres estudiados por el mismo motivo. Sin embargo, las mujeres tratadas con vortioxetina presentaron mejor función sexual que las del grupo control (que fueron tratadas con ISRS o Duales) en los dominios de deseo sexual, lubricación, frecuencia de actividad sexual y satisfacción sexual del cuestionario de función sexual FSM-2. Por lo tanto, las mujeres tratadas con vortioxetina tenían menor riesgo de sufrir disfunción sexual que las tratadas con ISRS o Duales.
Consideraciones éticasEste estudio se ha realizado de conformidad con el Código de Ética de la Asociación Médica Mundial (Declaración de Helsinki) para experimentos con seres humanos. Se ha obtenido el consentimiento informado de los pacientes incluidos en él. Ha sido aprobado por el Comité Ético de la Investigación con Medicamentos del Hospital Arnau de Vilanova-Liria de Valencia (España), código del protocolo FSSVOR-2020-01.
FinanciaciónLa presente investigación ha sido subvencionada por la Fundación SEMERGEN como «Ayuda a Proyectos de Investigación» al recibir el premio al Mejor Proyecto de Investigación en Atención Primaria (primer accésit) en 2020.
Conflicto de interesesALMG ha sido consultor o ha recibido honorarios o fondos de investigación en los últimos 5años de Julius, Lundbeck, Otsuka, Janssen Cilag, Pfizer, Roche, EISAI, Instituto de Salud CarlosIII, Junta de Castilla y León y ANECA. Todos los demás autores informan que no tienen relaciones financieras con intereses comerciales.
A los siguientes médicos de familia por su participación como investigadores en el estudio: Bárbara Castells Surián, María Teresa Tortosa Carreres, Vanessa Domínguez Úbeda, Esperanza Eulalia Montava Jiménez, Álvaro Sánchez Vicens y Belén Serrano-Chornet.