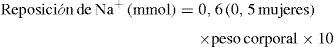El síndrome de secreción inadecuada de hormona antidiurética o vasopresina (SIADH) es una entidad de etiología muy variada que cursa con hiponatremia, hipoosmolalidad plasmática, osmolalidad urinaria inadecuadamente elevada y natriuresis altas. Al tratarse de un diagnóstico por exclusión, se precisa descartar previamente estados que cursan con disminución de la volemia eficaz, y polidipsia primaria. Además, el estado ácido-base, el potasio, la función cardiaca, renal, suprarrenal y tiroidea deben ser normales. Junto con las neoplasias e infecciones, los fármacos son una causa habitual, y con incidencia en aumento, de este síndrome. Tanto su diagnóstico como su tratamiento suelen ser poco complejos, y conciernen con frecuencia al ámbito de la Atención Primaria. Se describen cuatro casos de SIADH atribuido a fármacos, y se revisan las características generales de la entidad.
The syndrome of inappropriate antidiuretic hormone (or vasopressin) secretion (SIADH) has a very varied aetiology which presents with hyponatraemia, low plasma and urine osmolality, and an inappropriately high natriuresis. on being a diagnosis by exclusion, it is important to rule out states that present with decreased effective blood volume, and primary polydipsia. In addition, the acid-base, potassium, cardiac, renal, adrenal and thyroid function should be normal. Along with malignancies and infections, drugs are a common and increasing cause of this syndrome. Its diagnosis and treatment are often straightforward, and are often dealt with in primary care. We describe four cases of SIADH attributed to drugs, and review the general characteristics of the condition.
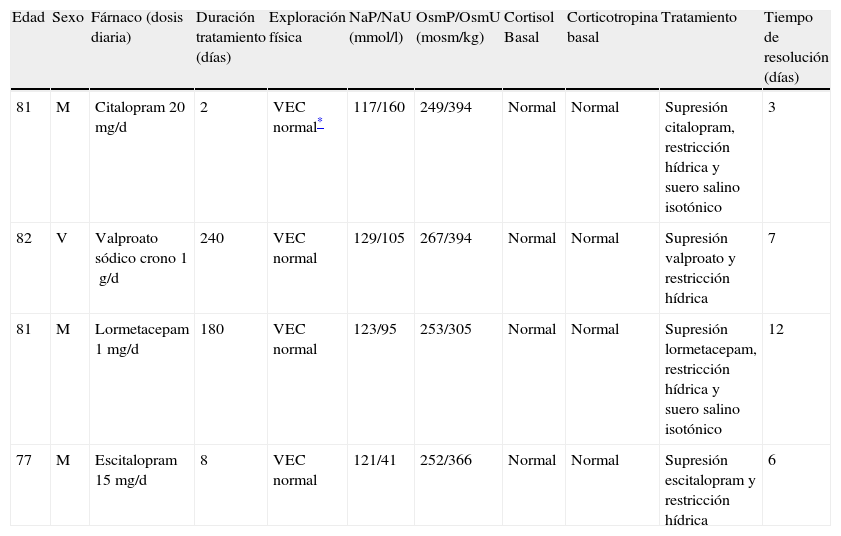
El síndrome de secreción inadecuada de hormona antidiurética o vasopresina (SIADH) es la causa más frecuente de hiponatremia1, y se define por la liberación mantenida de ADH en ausencia de sus estímulos habituales (hiperosmolalidad, hipotensión e hipovolemia). Cursa con hiponatremia, hipoosmolalidad plasmática, osmolalidad urinaria (OsmU) inadecuadamente elevada y natriuresis superior a 40mmol/l, todo ello derivado de la alteración en la excreción renal de agua libre. Para su diagnóstico, es preciso descartar situaciones que cursen con disminución de la volemia eficaz (insuficiencia cardiaca −IC−, cirrosis con ascitis, hipovolemia, etc.), y demostrar la normalidad del estado ácido-base, del potasio, de la función cardiaca, renal, suprarrenal y tiroidea2. De entre los agentes etiológicos, los fármacos son causa conocida y frecuente de SIADH. Su incidencia, por ello, es creciente —también en Atención Primaria (AP)—, y tanto su diagnóstico como su manejo terapéutico suelen ser poco complejos y, por lo general, al alcance de este ámbito asistencial. Describimos 4 casos de SIADH atribuido a fármacos (tabla 1); y revisamos las características generales de la entidad.
Características generales de los pacientes
| Edad | Sexo | Fárnaco (dosis diaria) | Duración tratamiento (días) | Exploración física | NaP/NaU (mmol/l) | OsmP/OsmU (mosm/kg) | Cortisol Basal | Corticotropina basal | Tratamiento | Tiempo de resolución (días) |
| 81 | M | Citalopram 20mg/d | 2 | VEC normal* | 117/160 | 249/394 | Normal | Normal | Supresión citalopram, restricción hídrica y suero salino isotónico | 3 |
| 82 | V | Valproato sódico crono 1g/d | 240 | VEC normal | 129/105 | 267/394 | Normal | Normal | Supresión valproato y restricción hídrica | 7 |
| 81 | M | Lormetacepam 1mg/d | 180 | VEC normal | 123/95 | 253/305 | Normal | Normal | Supresión lormetacepam, restricción hídrica y suero salino isotónico | 12 |
| 77 | M | Escitalopram 15mg/d | 8 | VEC normal | 121/41 | 252/366 | Normal | Normal | Supresión escitalopram y restricción hídrica | 6 |
Observación 1. Mujer de 81 años en tratamiento, desde 2 días antes, con 20mg/día de citalopram. Consulta por somnolencia y mareo. La exploración física fue normal. Los parámetros bioquímicos, incluidos el cortisol basal y la tirotropina (TSH) fueron también normales, salvo: sodio plasmático ([Na+]p): 117mmol/l (valor normal —vn–: 135–145), osmolalidad plasmática (OsmP): 249mosm/kg (vn 280–295), Na urinario (NaU): 160mmol/l y OsmU: 394mosm/kg (vn: 300–900mosm/kg). Tras suspensión del citalopram, restricción hídrica y aporte de suero salino isotónico, a las 72h quedó asintomática y con un [Na+]p de 135mmol/l.
Observación 2. Varón de 82 años con antecedentes de adenocarcinoma de próstata sin datos de recidiva y enfermedad pulmonar obstructiva crónica. Tres meses antes había sido diagnosticado de esofagitis por Candida albicans, y tratado con fluconazol. Consulta por reaparición de la odinofagia. Seguía tratamiento con tiotropio, fluticasona, salmeterol y, desde 8 meses antes, 1 gramo diario de valproato sódico crono por un episodio maníaco en el contexto de un trastorno bipolar. La exploración física y los parámetros bioquímicos elementales, cortisol basal y TSH fueron normales, excepto: [Na+]p: 129mmol/l, OsmP: 267mosm/kg, NaU: 105mmol/l y OsmU: 394mosm/kg. Se indicó nuevamente fluconazol oral, con lo que desapareció la sintomatología digestiva. Ante la persistencia de la hiponatremia, y la constatación de su existencia en relación temporal con el inicio del tratamiento con valproato, se suspendió el mismo, normalizándose la natremia (137mmol/l) a los 7 días.
Observación 3. Mujer de 81 años, con antecedentes de hipertensión arterial, asma bronquial y déficit de vitamina B12 por gastritis crónica atrófica. Seguía tratamiento con formoterol y budesonida inhalados, montelukast, simvastatina, 1mg/d de lormetacepam, amiloride a días alternos y vitamina B12. Desde varios meses antes se habían detectado hiponatremias moderadas (en torno a 123mmol/l) con natriuresis y OsmU elevas (62mmol/l y 418mosm/kg), y normalidad de las funciones cardiaca, renal, suprarrenal y tiroidea. Se atribuyeron a SIADH por un infarto lacunar antiguo. Consulta por disnea y bradipsiquia. La exploración física reveló sibilancias dispersas. No había edemas ni signos de deshidratación. Analíticamente destacaba un [Na+]p de 123mmol/l y una OsmP de 253mosm/kg, con OsmU de 109mosm/kg y NaU de 95mmol/l. Se revisó la relación de sus hiponatremias con la situación clínica y los fármacos utilizados en cada momento. Con el diagnóstico de sospecha de SIADH secundario al uso de lormetacepan, se suspendió el mismo, normalizándose la natremia (140mmol/l) a los 12 días.
Observación 4. Mujer de 77 años en tratamiento desde dos semanas antes con 15mg/día de escitalopram. Acude a revisión relativamente asintomática. La exploración física fue normal. Entre los parámetros analíticos destacaba: [Na+]p de 121mmol/l y OsmP de 252mosm/kg, con OsmU de 366mosm/kg y NaU de 80mmol/l. Con la sospecha de SIADH secundario al uso de escitalopram, se suspendió el mismo, normalizándose la natremia (136mmol/l) a los 6 días.
DiscusiónLa natremia ([Na+]p) es el principal determinante de la osmolalidad plasmática. En consecuencia, la mayoría de las hiponatremias ([Na]p<135mmol/l) se acompañan de hipoosmolalidad plasmática (<280mOsm/kg), lo cual es relevante, ya que dicho estado provoca el paso de agua a las células cerebrales, lo que condiciona la mayoría de sus síntomas3. En otras situaciones más raras, la hiponatremia puede acompañarse de osmolalidad elevada —es el caso, por ejemplo, de las hiperglucemias graves, en las que la natremia baja 2,4mmol/l por cada 100mg/dl que sube la glucemia— o normal. En ambos supuestos se habla de seudohiponatremia. En la hiperglucemia existe paso de agua intracelular al plasma y, como resultado, hiponatremia por dilución. En las hiperproteinemias o hipertrigliceridemias graves puede verse hiponatremia, que no requiere tratamiento, debido a que la concentración de sodio, medida por litro de plasma, disminuye al estar, en estas circunstancias, reducida el agua plasmática.
La hiponatremia es el trastorno hidroelectrolítico más frecuente, y las entidades causantes son numerosas. Quizá el primer dato que haya de investigarse sea el estado del volumen circulante eficaz (VCE), entendido como aquel que perfunde adecuadamente los tejidos. El VCE puede estar bajo tanto en situaciones de disminución del volumen extracelular (VEC) —por pérdida gastrointestinal, renal o cutánea de líquidos— como de aumento del mismo. Es lo que ocurre, por ejemplo, en la IC con edema o en la cirrosis con ascitis, en los que existe una hipoperfusión tisular por disminución del gasto cardiaco o de las resistencias vasculares respectivamente. En estas situaciones, la hiponatremia se produce por hipersecreción de ADH e incremento de la reabsorción tubular de agua. Al tiempo, aumenta la reabsorción proximal de Na+ y agua, que explicaría —además de la hiponatremia— el edema y las natriuresis bajas ([Na+]u<20mmol/l).
Al margen del SIADH, son también causas conocidas de hiponatremia el hipotiroidismo, la insuficiencia suprarrenal, la insuficiencia renal, los diuréticos —especialmente las tiazidas (que también provocan SIADH)—, la polidipsia primaria, la pérdida cerebral de sal (en enfermedades cerebrales, especialmente hemorragias subaracnoideas) y el reajuste del osmostato (suelen ser pacientes con hiponatremia estable, debido a que tienen el umbral para la liberación de ADH más bajo).
El SIADH es un proceso frecuente, de etiología muy variada, y caracterizado por la liberación de ADH no mediada por sus estímulos habituales. Cursa con hiponatremia, normovolemia, hipoosmolalidad plasmática, OsmU inadecuadamente elevada (más de 100mosm/kg) y natriuresis superior a 40mmol/l. Con frecuencia, se acompaña de hipouricemia por excreción aumentada de uratos. Ya se ha dicho, por otra parte, que es preciso descartar previamente situaciones que cursen con disminución de la volemia eficaz (IC, cirrosis con ascitis, hipovolemia…) y la polidipsia primaria. Al tiempo, se requiere demostrar la normalidad del estado ácido-base, del potasio, de la función cardiaca, renal, suprarrenal y tiroidea1. En el trastorno subyace una incapacidad para excretar agua libre, de lo que se deduce una retención del agua ingerida y una expansión de los líquidos corporales. La inexistencia de edema se explica por la activación de los receptores de volumen, que conducen a una excreción urinaria de sodio y de agua.
Las causas del SIADH son múltiples (tabla 2). Entre ellas, destacan, por su frecuencia, los tumores, especialmente el carcinoma pulmonar de células pequeñas, en el que se ha documentado producción ectópica de ADH4; los fármacos —según autores, la causa más frecuente5— y las infecciones. Aunque la mayoría de sustancias que provocan SIADH lo hacen de manera excepcional, la lista de fármacos implicados —algunos de ellos de uso habitual— ha ido en progresivo aumento. El mecanismo de producción del SIADH por fármacos no es del todo conocido, pero parece múltiple. Se ha descrito, por ejemplo, el efecto directo sobre las células tubulares renales6, el papel de la serotonina en la síntesis de vasopresina7, el aumento de la producción hipotalámica8 de ADH o el incremento del efecto de la vasopresina9. Al igual que en nuestros pacientes —cuya media de edad fue de 80 años— está descrita una mayor incidencia del síndrome en personas de edad avanzada. Así lo atestigua el trabajo de Pedrós C et al10, en el que la edad mediana de las hiponatremias por inhibidores selectivos de la recaptación de serotonina fue de 75 años, y el 84% de los pacientes eran mayores de 64 años.
Causas de SIADH
| Oncológicas |
| Carcinoma microcítico de pulmón, timoma, mesotelioma, tunor gastrointestinal, páncreas, vejiga, uréter, uretra, próstata, útero, recto, linfoma, neuroblastoma, sarcoma de Ewing, nasofaringe. |
| Neurológicas |
| Infecciones (encefalitis, absceso, meningitis), accidente cerebrovascular, traumatismo craneoencefálico, tumores cerebrales, hematoma subdural, hemorragia subaracnoidea, esclerosis múltiple, arteritis de la temporal, epilepsia, síndrome de Guillain-Barré, lesiones de la médula espinal, sección del tallo pituitario, adenomectomía transesfenoidal, hidrocefalia. |
| Neumológicas |
| Infecciones (tuberculosis, neumonía bacteriana y vírica, absceso, empiema), aspergilosis, asma, atelectasia, fallo respiratorio agudo, neumotórax, ventilación mecánica con presión positiva, fibrosis quística. |
| Farmacológicas |
| Oxitocina, clorpropamida, tolbutamida, rosiglitazona, clofibrato, enalapril, teofilina, carbamacepina, oxcarbacepina, citalopram, escitalopram, fluoxetina, sertralina, paroxetina, levetiracetam, venlafaxina, viloxazina, haloperidol, valproato, quetiapina, barbitúricos, lormetazepam, morfina, antidepresivos tricíclicos, inhibidores de la monoamino oxidasa, nicotina, «éxtasis», tiazidas, vincristina, vimblastina, ciclofosfamida, cotrimoxazol, ciprofloxacino, etionamida, omeprazol, piroxicam, diclofenaco, indometacina. |
| Posquirúrgicas |
| Cirugía mayor abdominal o torácica, e hipofisiaria transesfenoidal. |
| Infecciosas |
| Virus de la inmunodeficiencia humana, varicela, listeriosis, mononucleosis infecciosa, criptococosis, lepra. |
| Otras |
| Enfermedades psiquiátricas (psicosis aguda, etc.), delirium tremens, autoinmunitarias (lupus eritematoso sistémico, síndrome de Sjögren), porfiria aguda intermitente, pericarditis, estrés, dolor, náuseas, atrofia senil, ejercicio muy prolongado, idiopático. |
La clínica de la hiponatremia se debe a la disfunción neurológica provocada por la sobrehidratación neuronal secuente a la hipoosmolalidad. En general, es poco expresiva, y depende de la intensidad de la misma y de su velocidad de instauración11. Oscila desde náuseas o malestar hasta cefalea, hipotermia, letargia, convulsiones, parálisis seudobulbar o coma (éstas, generalmente con natremias por debajo de 115–110mmol/l). La hiponatremia aguda sintomática, especialmente en mujeres premenopáusicas, puede causar déficits neurológicos permanentes o la muerte12.
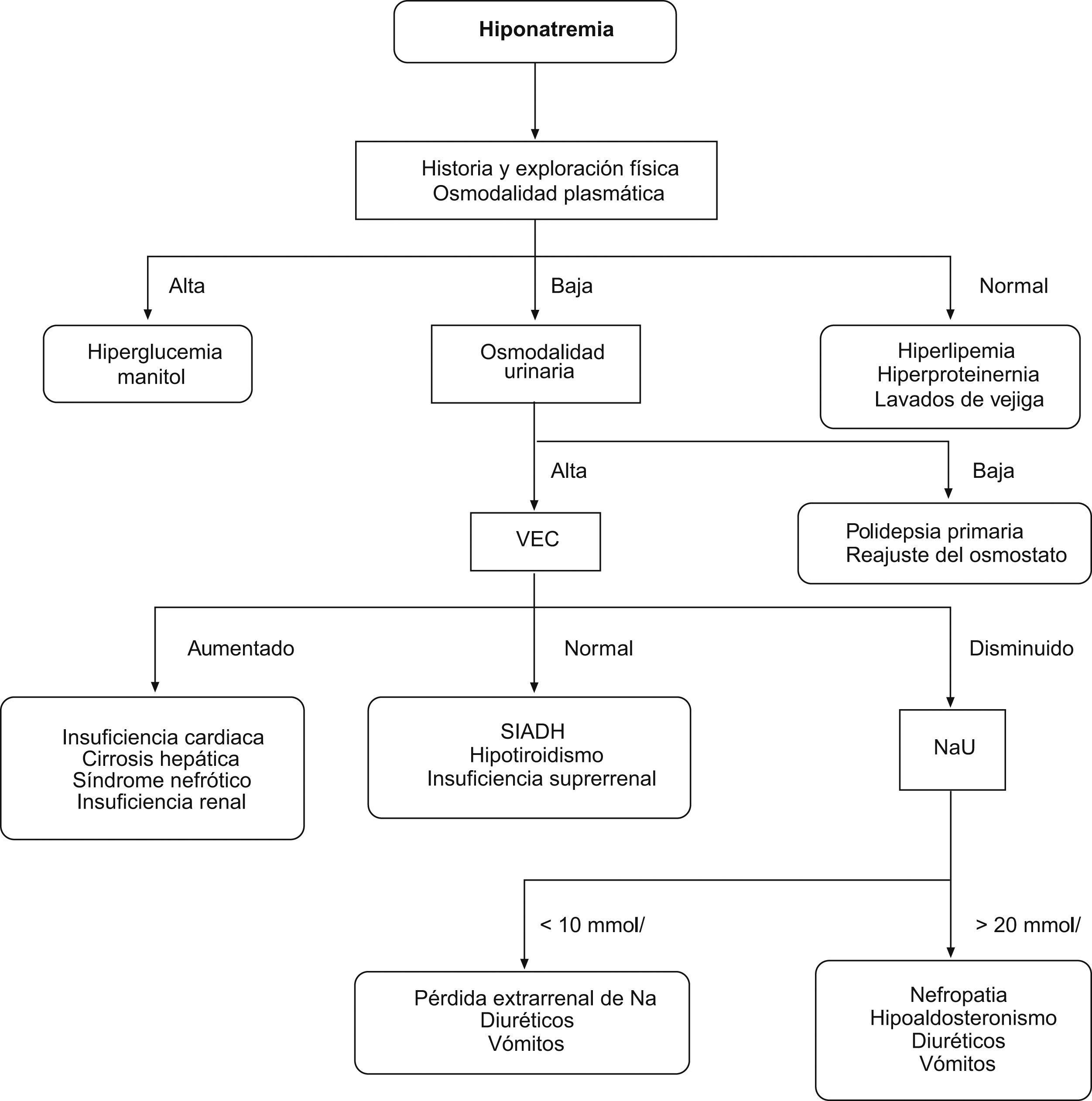
El diagnóstico de la hiponatremia requiere de una adecuada historia clínica (antecedentes de vómitos, diarrea, quemaduras, tratamiento diurético o de alguna causa de SIADH) y exploración física (normovolemia, signos de deshidratación o edema). Además, es preciso conocer la osmolalidad plasmática, ya que de estar normal o elevada, hay que dirigir el estudio hacia las causas de seudohiponatremia13. Es importante conocer que en casos de administración de glicina, sorbitol o manitol (generalmente tras resecciones transuretrales), hiperlipemias e hiperproteinemias, existe un hiato osmolal —diferencia entre la osmolalidad plasmática medida en el laboratorio y la calculada (Posm=2×Nap+[glucemia]/18+BUN/2,8)—. Una vez confirmado el estado de hipoosmolalidad plasmática, se necesita conocer la osmolalidad urinaria (en el SIADH >100mosm/kg), ya que, de ser inferior, orienta hacia un reajuste del osmostato o una polidipsia primaria. Finalmente, una natriuresis superior a 40mmol/l es coherente con el SIADH, aunque también con los estados pierde-sal (diuréticos, insuficiencia renal, insuficiencia suprarrenal) y el hipotiroidismo. Adjuntamos algoritmo de actuación frente a la hiponatremia (fig. 1).
Aunque los valores plasmáticos de ADH estarán inadecuadamente elevados respecto de la hipoosmolalidad plasmática, esta determinación ni se considera necesaria para el diagnóstico ni suele ser de ayuda para diferenciar las distintas situaciones que cursan con hiponatremia. Por ello, su aplicación en la clínica es limitada.
Existen algunas consideraciones fundamentales respecto del tratamiento de la hiponatremia. En primer lugar, que el objetivo prioritario no es normalizar la natremia, sino conseguir valores de sodio dentro de unos límites razonablemente seguros (por lo general, superiores a 120mmol/l). En segundo lugar, que la administración de suero salino hipertónico sólo está indicada ante hiponatremias graves (110–115mmol/l) o con sintomatología llamativa. Y finalmente, que es fundamental tratar la causa de la hiponatremia. De igual trascendencia resulta insistir en que la corrección excesivamente rápida puede provocar, especialmente en formas crónicas graves, grandes quemados, desnutridos y alcohólicos crónicos, una desmielinización osmótica preferentemente de la protuberancia. Esta grave complicación se caracteriza por paraparesia o cuadriparesia, disartria, disfagia, convulsiones o coma. Por ello, no se debe elevar la natremia más de 10–12mmol/l en las primeras 24h ni más de 18mmol/l en los primeros 2 días. No obstante, se requiere extremar la prudencia, ya que, incluso a este ritmo, puede aparecer sintomatología neurológica.
En el SIADH, donde la hiponatremia se debe inicialmente a retención de agua, la terapia fundamental14 es —además del tratamiento causal— la restricción de agua. Si con ello no fuera suficiente, o ante casos de hiponatremia grave, puede administrarse suero salino hipertónico acompañado de diuréticos de asa, para inducir una diuresis hipotónica. Como recordatorio, cabe insistir en que 1 litro de suero salino isotónico contiene 154mmol/l de sodio, y un vial de 10ml de cloruro sódico al 20%, 34mmol de sodio. Una fórmula general adecuada para plantear el ritmo de la reposición de sodio en las primeras 24h (10mmol) sería:
Ante situaciones de gravedad, hay que considerar un aumento en el ritmo de infusión inicial. Otras sustancias, como el litio o la demeclociclina, no suelen utilizarse, y actúan sobre el efecto de la ADH en los túbulos colectores. Muy recientemente, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha aprobado el uso de tolvaptán en el SIADH. Se trata de un antagonista de la vasopresina o ADH que bloquea la unión de vasopresina a los receptores V2 de las porciones distales de la nefrona, y que induce un aclaramiento de agua libre sin depleción de electrolitos, reducción de la osmolalidad urinaria y aumento de la natremia15,16.
Para finalizar, nos parece importante insistir en que el SIADH debido a fármacos es un trastorno frecuente y de ningún modo ajeno al ámbito de la AP. Una historia clínica y una exploración física adecuadas suelen resultar muy clarificadoras; y los datos de laboratorio precisos para el diagnóstico están al alcance de este nivel asistencial, al igual que algunas de las medidas terapéuticas.