la información que aporta el proteinograma y su asociación con diferentes enfermedades.
Para la separación de las proteínas del suero se han utilizado a lo largo del tiempo diferentes soportes (papel, acetato de celulosa, agarosa) que han ido mejorando la calidad de la separación. En estos métodos se depositaba la muestra sobre el soporte y se sometía a éste a una corriente eléctrica de tal manera que las proteínas se separaban en función de su carga eléctrica; posteriormente, se sumergía el soporte en un colorante (negro amido, rojo Congo) para que éste se fijase a las diferentes fracciones electroforéticas y, posteriormente, se cuantificaban de forma semicuantitativa en un densitómetro.
Recientemente, se dispone de un sistema de realización de los proteinogramas, utilizando una técnica diferente, denominada electroforesis capilar, donde la muestra se hace pasar por un capilar y las proteínas se separan debido a un fuerte voltaje electroosmótico y las bandas se estiman mediante la medición a 214 nm del enlace peptídico. La introducción de esta tecnología ha permitido aumentar la calidad del proteinograma y una mayor rapidez, comodidad y precisión.
Valoración del proteinograma
Hay que tener presente que el proteinograma proporciona la información correspondiente a las proteínas mayoritarias de cada banda y que, por tanto, la información que parece aportar sobre una proteína específica puede estar distorsionada en presencia de concentraciones aumentadas de las otras proteínas que comparten la zona de migración. La valoración cuantitativa de cada una de las principales proteínas plasmáticas se
realizan por otros procedimientos analíticos.
En el proteinograma realizado por electroforesis capilar se definen las siguientes bandas:
Banda de la prealbúmina
Es una banda difusa, por delante de la albúmina, poco visible y que está constituida por dos proteínas con un gran interés para la valoración nutricional como son la prealbúmina y la proteína fijadora del retinol. Por sus bajas concentraciones, se requieren técnicas inmunológicas para valorar su cuantía.
Banda de la albúmina
Es la banda más importante del proteinograma, representando más del 50% del mismo en condiciones normales. Está integrada por la proteína más abundante del plasma. Su interés se centra en las hepatopatías (cirrosis) y nefropatías (síndrome nefrótico), donde está disminuida. Se eleva en situaciones de deshidratación y por prolongación del tiempo del torniquete a la hora de la extracción de la muestra. Una alteración cualitativa sin significado patológico que se puede presentar es la bisalbuminemia, que puede tener un origen genético o adquirido (generalmente debido a la toma de medicamentos).
Banda de la *1-globulina
Esta banda está formada por un conjunto de proteínas como la *1-antitripsina, la *1-glucoproteína, la transcortina, la *1-lipoproteína, y la *-fetoproteína, siendo las dos primeras las que representan el mayor porcentaje de la misma. Esta banda se eleva en los procesos inflamatorios agudos, por lo que las proteínas que la integran se denominan reactantes de fase aguda.
Mayor interés tiene su disminución, ya que indica un déficit de *1-antitripsina, sobre todo en la deficiencia homocigota (PiZZ) en donde la concentración plasmática de esta proteína está por debajo del 10-15% de su concentración en los sujetos sanos (MM). En ausencia de proceso inflamatorio agudo, los sujetos homocigotos SS y los heterocigotos MS, MZ y SZ tienen alrededor del 50% de las concentraciones encontradas en los sujetos con el fenotipo MM.
Banda de la *2-globulina
Las tres principales proteínas que la integran son la *2-macroglobulina, la haptoglobina y la ceruloplasmina. Se comportan también como reactantes de la fase aguda positivos; la *-2 macroglobulina tiene una función de antiproteasa sérica; la haptoglobina se une a la hemoglobina en los procesos hemolíticos intravasculares donde está disminuida y la ceruloplasmina tiene una misión transportadora del cobre, siendo sus concentraciones bajas en la enfermedad de Wilson.
Bandas de las ß-globulinas
Las proteínas más importantes son la transferrina, la hemopexina, la ß-lipoproteína y el c3 nativo.
La transferrina se eleva en situaciones de déficit de hierro y desciende en el síndrome nefrótico y las hepatopatías; la hemopexina desciende en las anemias hemolíticas y se eleva en las reacciones agudas; el c3 desciende en el LES activo y se eleva como reactante de fase aguda positivo.
En esta banda pueden aparecer otras extras correspondientes a la hemoglobina de los sueros hemolizados, el fibrinógeno (cuando el proteinograma se realiza con plasma) y las gammapatías monoclonales, sobre todo IgA.
Banda de la *-globulina
Está formada por las tres principales inmunoglobulinas: IgG, IgA e IgM; en ausencia de una gammapatía monoclonal, su estimación electroforética solamente aportará información sobre la concentración sérica, sobre todo de la IgG. Su elevación puede ser policlonal, donde todas las inmunoglobulinas se elevan dando lugar a una curva simétrica, o bien monoclonal donde aparece un pico correspondiente a la síntesis de una sola cadena de inmunoglobulinas. La elevación policlonal de la IgA da lugar a lo que se llama puente ß*-globulina.
Las elevaciones policlonales suelen deberse a una activación de la inmunidad humoral, inducida por múltiples mecanismos patológicos, como las infecciones, las enfermedades autoinmunes, las hepatopatías y los procesos inflamatorios agudos y crónicos.
Las elevaciones monoclonales se deben, sobre todo, al mieloma múltiple, la enfermedad de Waldeströn, la enfermedad de las cadenas pesadas y, con mucha frecuencia, a las denominadas gammapatías monoclonales de significado incierto (GMSI) (tabla 1).
La historia clínica, la exploración y la utilización de diferentes parámetros de laboratorio y la aplicación de los criterios diagnósticos son necesarios para hacer un correcto diagnóstico diferencial de las gammapatías monoclonales (tabla 2).
La proteína C-reactiva, cuando su aumento es muy manifiesto, aparece como una pequeña banda en la región gamma del proteinograma.
Patrones electroforéticos
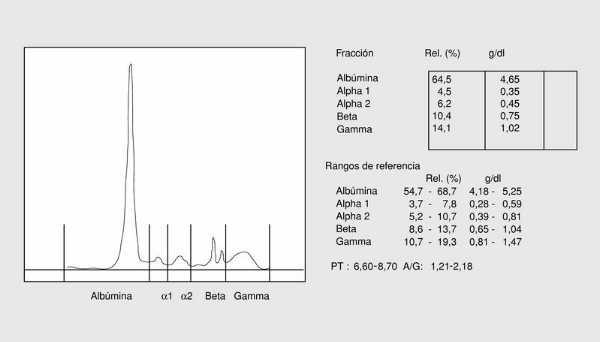
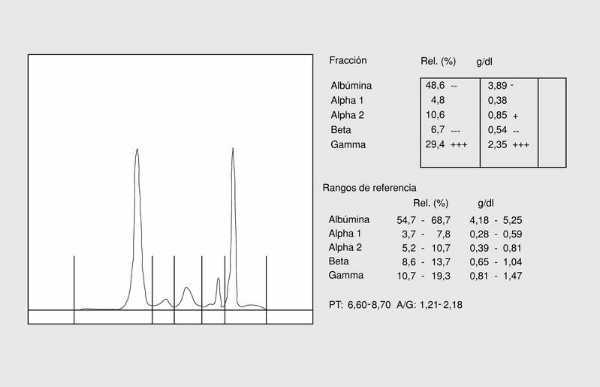
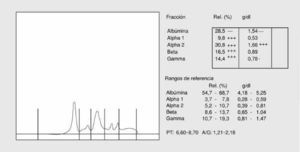
Los patrones electroforéticos surgieron de la asociación que se observó entre las diversas enfermedades y determinadas alteraciones en el proteinograma. Actualmente, con la posibilidad de cuantificar las proteínas individuales, el interés por el conocimiento de los patrones electroforéticos ha disminuido; no obstante, no hay que olvidar que una observación detallada del proteinograma aporta una información semicuantitativa sobre las proteínas mayoritarias de cada banda (fig. 1).
Fig. 1. Proteinograma normal.
Patrón asociado a la cirrosis hepática
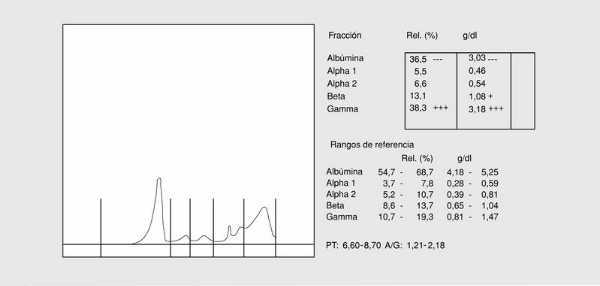
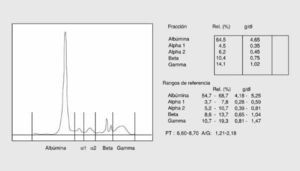
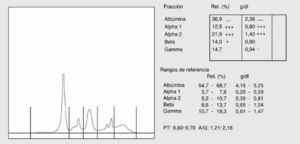
Se presenta con una disminución de todas la proteínas sintetizadas por el hígado, fundamentalmente de la albúmina y un aumento de la banda de las inmunoglobulinas como consecuencia de la falta de degradación de la IgA de origen digestivo, unido a una síntesis importante de inmunoglobulinas como consecuencia del material antigénico procedente del tubo digestivo (fig. 2).
Fig. 2. Proteinograma de cirrosis hepática.
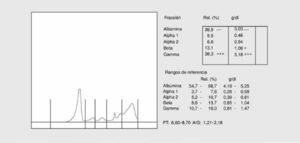
Patrón del síndrome nefrótico
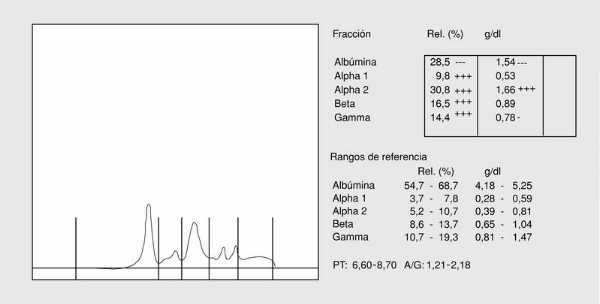
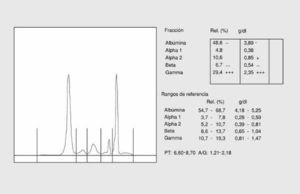
Se caracteriza por una disminución de la albúmina, un aumento de la *2-globulina, una disminución de las *-globulinas como consecuencia de las pérdidas renales de las proteínas de menor peso molecular y el aumento compensatorio de las de mayor peso molecular a fin de mantener el poder oncótico del plasma (fig. 3).
Fig. 3. Proteinograma de síndrome nefrótico.
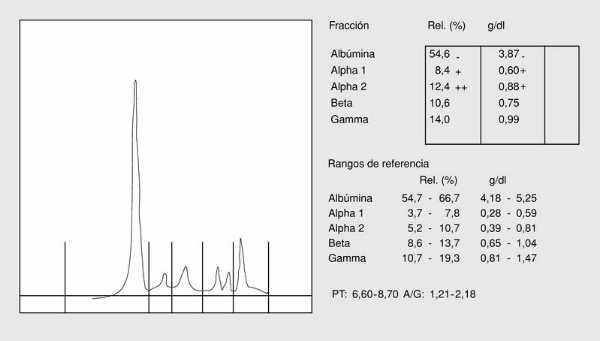
Patrón inflamatorio
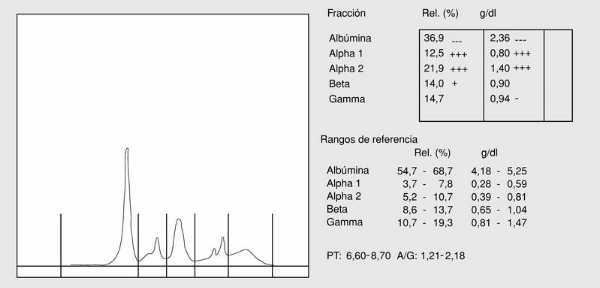
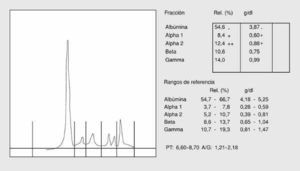
Algunas proteínas plasmáticas se comportan como reactantes de fase aguda de la inflamación; estos reactantes de fase aguda pueden agruparse en dos categorías: reactantes de fase aguda positivos, que aumentan su concentración en respuesta al estímulo inflamatorio, y reactantes de fase aguda negativos, que disminuyen su concentración plasmática en respuesta a la inflamación. Entre los primeros se encuentra la *1-antitripsina, la ceruloplasmina, la haptoglobina y el c3; entre los segundos, la prealbúmina, la albúmina y la transferrina. El patrón electroforético de la inflamación se caracteriza por un aumento de las bandas de la *1-globulina, *2-globulina y si el proceso se cronifica, un incremento de la banda de la *-globulina. La disminución de la síntesis de la prealbúmina, albúmina y transferrina tiene escasa repercusión electroforética en la inflamación aguda (fig. 4).
Fig. 4. Proteinograma de inflamación aguda.
Patrón electroforético del embarazo
Se presenta con una disminución de la albúmina por hemodilución y una elevación de la *-macroglobulina y de la transferrina, posiblemente como consecuencia del aumento de los estrógenos y del déficit férrico asociados al embarazo.
Patrón de gammapatía monoclonal
En la región gamma o en la región beta-gamma aparece un pico monoclonal correspondiente a la presencia en el suero de una inmunoglobulina monoclonal completa o de una de sus cadenas. La identificación de la paraproteína se efectúa por inmunoelectroforesis, inmunofijación o inmunosustracción (figs. 5 y 6).
Fig. 5. Proteinograma de mieloma múltiple.
Fig. 6. Gammapatía monoclonal de significado incierto.
En resumen, el patrón electroforético observado en la enfermedad dependerá de los mecanismos fisiopatológicos activados inflamación, respuesta inmunológica humoral, aumento o disminución de la síntesis proteica, pérdidas de proteínas (riñón, intestino, piel) y hemólisis intravascular, así como de su grado de activación en el momento que se realiza el proteinograma. Resulta casi imposible obtener un proteinograma patognomónico y precoz de una enfermedad, excepto las que cursan con alteraciones estructurales o de la regulación de la síntesis de alguna proteína, como la bisalbuminemia y, fundamentalmente, las gammapatías monoclonales.
Utilidad clínica del proteinograma
El proteinograma es el método de análisis con mayor sensibilidad clínica para la detección de una gammapatía monoclonal, por lo que la sospecha de una gammapatía monoclonal es la principal indicación a la hora de solicitar un proteinograma. No se debe utilizar el proteinograma para la medición de proteínas específicas ni para el seguimiento de los valores de su magnitud, así como su utilización como estudio previo para la selección de las proteínas individuales a cuantificar por otros procedimientos. No obstante, no parece justificada la sustitución del proteinograma por un perfil de proteínas, por lo que el cuadro clínico del individuo debe ser el que condicione las proteínas individuales que tengan que ser estudiadas en función de las alteraciones patológicas que se quieran valorar. Su observación detallada es imprescindible para su correcta interpretación, por lo que es recomendable adjuntar, con el mismo, un informe interpretativo del facultativo del laboratorio sobre las alteraciones con interés clínico observadas en el proteinograma.
Bibliografía general
Bergon E. Utilidad de la electroforesis de las proteínas séricas en el laboratorio clínico. Rev Diagn Biol 1998; 47: 10-18.
Beses C, Sans-Sabrafen J. Introducción al estudio de las hemopatías disglobulinémicas. En: Hematología clínica. Ed. Mosby/Doyma Libros, 1994; 448-456.
McPherson R. Proteínas específicas. En: Henry JB, editores. Diagnóstico y tratamientos clínicos por el laboratorio. Masson-Salvat, 1993; 223-236.
Patel S, Lott JA. Electroforesis de proteínas séricas. En: Kaplan-Pesce, editor. Química clínica. Ed. Panamericana, 1988; 1547-1554.
Wolf PL. Interpretation of electrophoretic patterns of serum proteins. Clin Lab Med 1986; 6: 441-455.