El dolor es el síntoma más importante de la artrosis. Es, casi siempre, de comienzo subagudo e insidioso aunque en algunos casos aparece de forma aguda en general, después de un traumatismo y a continuación persiste crónicamente. Tiene características mecánicas y, por tanto, se exacerba con la función de la articulación enferma y mejora o desaparece en reposo. Con frecuencia existe el llamado «ritmo artrósico»: dolor que aparece al utilizar la articulación tras un período de reposo y que alivia después de un tiempo de uso, pero que reaparece si se la sobrecarga en exceso. En las fases avanzadas, especialmente en la cadera, hay también dolor nocturno o de reposo.
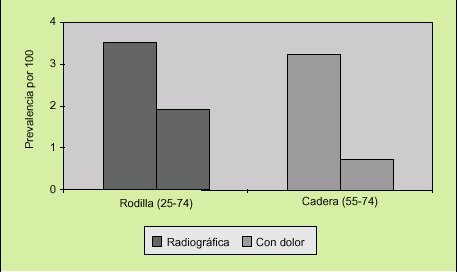
Los factores asociados, con mayor frecuencia, con la presencia de dolor en artrosis son: el sexo (las mujeres refieren dolor con más frecuencia que los varones), la localización articular de la enfermedad (la rodilla y la cadera son más dolorosas que las manos), y la gravedad de los cambios radiográficos (a mayor deterioro radiológico, mayor probabilidad de dolor)1. No obstante, una de las características más sorprendentes, y más comúnmente detectadas, es la escasa consistencia que existe entre dolor y artrosis radiológica. Así, en el estudio NHANES-I, se examinó a 6.913 individuos entre 25-74 años y se encontró que sólo el 44% de los 319 que tenían artrosis radiológica de rodilla referían dolor2,3 (fig. 1).
Fig. 1. Correlación entre dolor y artrosis radiográfica de rodilla y cadera en el estudio NHANES-I (Lawrence, 1998).
Complejidad de los mecanismos del dolor en la artrosis
El dolor es el síntoma por el que principalmente los pacientes artrósicos acuden a su médico. Sin embargo, conocer la causa del dolor en esta enfermedad no es un asunto sencillo (tabla 1).
En primer lugar, el dolor es una sensación displacentera que tiene por función detectar procesos potencialmente patógenos para el organismo y que implica un sentimiento de ansiedad y de huida. Por ello, es tanto una sensación como una emoción. La IASP (International Association of the Study of Pain) describe el dolor como «una experiencia desagradable sensorial y emocional que va ligada a una lesión real o potencial de los tejidos»4.
En la sensación dolorosa se imbrican procesos de transmisión (neurofisiología), a través de un circuito de neuronas y vías nerviosas, y procesos de modulación (neurobiología) mediante el cual la sensación se inhibe o se amplifica. La primera neurona tiene su soma en el ganglio raquídeo. La prolongación periférica de su axón da lugar a las fibras aferentes de los nervios periféricos, que son de tres grupos distintos: fibras Aß (gruesas y mielinadas), fibras A* (delgadas y mielinadas) y fibras C (no mielinadas). Las fibras Aß se activan por estímulos inocuos, como el movimiento normal de la articulación, y son las encargadas de la propiocepción. Las fibras A* (rápidas y que transmiten el dolor agudo) y las fibras C (más lentas y que transmiten el dolor difuso) se activan con estímulos potencialmente dañinos para la articulación y son, por tanto, los nociceptores, los cuales pueden ser activados tanto por estímulos químicos (presencia de prostaglandinas, sustancia P, bradicinina o histamina) como por estímulos mecánicos (alteraciones de la forma articular o tensiones anómalas sobre las estructuras inervadas). La prolongación central del axón de la primera neurona se dirige hacia el asta posterior de la médula, donde hace sinapsis con la segunda neurona, y desde ahí la sensación asciende a los núcleos centrales y a la corteza cerebral.
Las articulaciones reciben inervación sensorial y autonómica de las ramas articulares de los nervios periféricos adyacentes y de los musculares cercanos. Los estudios histológicos de inervación del tejido articular han demostrado una extensa inervación en las estructuras articulares (cápsula, ligamentos, meniscos, periostio, sinovial y médula ósea hasta la placa subcondral). Nunca, sin embargo, se han identificado elementos ner viosos en el cartílago, tanto humano como de experimentación animal y, por tanto, el cartílago no puede ser fuente de dolor. Recientes estudios detectan la presencia de sustancia P en el cartílago que podría pro venir de los propios condrocitos, por lo que, si bien el cartílago no puede ser doloroso, sí podría producir sustancias algógenas5. Junto con ello, se conoce que en la sinovial han de existir receptores opioides, cuya estimulación inhibe la transmisión del dolor, ya que la morfina intraarticular produce reducción del dolor, especialmente en las articulaciones inflamadas, y se han detectado opioides endógenos como betaendorfina y metencefalina (no dinorfina) en las células sino-
viales6,7.
Desde un punto de vista práctico, la mencionada complejidad de la etiología del dolor en la artrosis podría resumirse en dos tipos de mecanismos: mecanismos periféricos y centrales (tabla 2).
Mecanismos periféricos en el origen del dolor artrósico
Inflamación sinovial
Aunque la artrosis no es considerada como una enfermedad articular primariamente inflamatoria, los estudios histológicos demuestran prácticamente siempre la presencia de inflamación en la sinovial: edema, proliferación e infiltrados mononucleares. En la artroscopia, se encuentra inflamación en todos los pacientes, que es máxima en la unión cartílago sinovial y disminuye al alejarse de esta zona8. Las causas de dicha inflamación son traumatismos, detritus y restos del cartílago que son vistos habitualmente en el líquido sinovial de artrosis, mecanismos inmunes (depósitos de inmunoglobulinas y complemento en el cartílago) y, finalmente, la presencia de cristales: pirofosfato o hidroxiapatita que se observan en el 60-75% de las artrosis.
La inflamación puede producir dolor por diversos mecanismos:
Estímulo de los nociceptores por la liberación celular de prostaglandinas, leucotrienos, interleucinas, bradicinina y serotonina.
Los nociceptores de la cápsula pueden estimularse mecánicamente por el edema y la distensión de partes blandas.
Inflamación neurogénica («reflejo axonal»): en los fenómenos inflamatorios se puede producir la liberación de péptidos fundamentalmente vasodilatadores y proinflamatorios, como la sustancia P, producidos en las células del ganglio de la raíz, y transportados por los axones hasta los tejidos periféricos y las terminaciones sinápticas, donde incrementan el grado de inflamación. Por ello, la capsaicina, que induce la depleción de sustancia P, ha sido empleada con éxito en el tratamiento local de la artrosis.
Dolor de origen óseo
Varios mecanismos han sido implicados en la aparición de dolor óseo en la artrosis:
En la artrosis de cadera se ha visto reducción del drenaje venoso del hueso demostrado por flebografía y aumento de la presión femoral intramedular9 que mejora con la osteotomía10. Asimismo, se ha podido demostrar hipertensión medular mediante la colocación de un catéter, con una intervención quirúrgica menor, en la cabeza femoral a 5-10 mm del espacio articular11. Ésta podría ser la etiología del dolor nocturno en la artrosis de cadera.
El crecimiento de los osteófitos motiva una activación del periostio, lugar donde han sido demostrados nociceptores acompañando a los ejes vasculares5.
Finalmente, una posibilidad más rara, pero bien descrita en la bibliografía son las fracturas de estrés de la tibia12 como causa de dolor en la artrosis de rodilla. Suelen cursar con un súbito deterioro del dolor y el diagnóstico puede precisar una gammagrafía. Son fracturas estables, con poca tendencia a desplazarse, en las que reducir actividad es la mejor opción terapéutica.
Dolor de origen en partes blandas
Los tejidos blandos articulares y periarticulares pueden ser fuente de dolor. Las alteraciones en la forma sinovial, los osteófitos y, en los casos avanzados, la destrucción e inestabilidad, conducen a la aplicación de fuerzas anómalas a la cápsula, ligamentos, bolsas, tendones, etc., y otras estructuras inervadas, y motivan elongamientos, fibrosis, contracturas, e incluso reducción del flujo vascular, todo lo cual puede producir dolor13. En este sentido, uno de los tejidos más importantes en la génesis del dolor podría ser el músculo. O'Reilly et al14 han comprobado recientemente que en la artrosis de rodilla la fuerza del cuádriceps y la activación muscular es significativamente más baja en los pacientes con dolor que en los controles. El posible mecanismo del dolor en estos pacientes es debido a la inestabilidad articular que motiva la debilidad muscular; el estrés sobre articulaciones inestables motiva aumento de la tensión sobre los nociceptores de la cápsula y los ligamentos y, por tanto, dolor e incapacidad. Lo importante, en este caso, es que un estudio15 ha demostrado que pacientes aleatorizados a recibir un programa de 12 semanas de puesta a punto en caminar, mejoraban esta capacidad en un 18,4%, mejoraban también la funcionalidad articular y apreciaban una disminución en el grado de dolor.
Mecanismos centrales del dolor en la artrosis
Son tres los mecanismos fundamentales de origen central por los que el sistema nervioso puede influir en la sensación dolorosa de la artrosis.
Sensibilización central
En las neuronas del sistema nervioso central ocurre un proceso de sensibilización que hace que tejidos normales, situados alrededor de los inflamados, sean frecuentemente dolorosos. El fenómeno más conocido es el llamado win up, por el que los impulsos continuados y mantenidos de las fibras C incrementan el número y el grado de la excitabilidad de las neuronas del asta posterior de la médula. Esto conduce a una reducción del umbral del dolor e incremento de la sensación dolorosa, tanto en el lugar de la lesión (hiperalgesia primaria) como en las áreas circundantes (hiperalgesia secundaria). Por otro lado, puede incluso aparecer alodinia, es decir, dolor con estímulos habitualmente inocuos y no dolorosos. Ésta es la causa de que, en ocasiones, aparezcan como dolorosos los músculos y otras áreas vecinas de la articulación.
Amplificación central: fibromialgia
Moldofsky16 constata en sus estudios que la fibromialgia puede verse entre un 7-14% de los pacientes con artrosis; para este autor el sueño tiene la capacidad de modular el dolor y se ha comprobado que la deprivación del sueño desciende el umbral del dolor en humanos.
Dolor de origen psicológico y social
O'Reilly et al14 y Summers et al17 encuentran una clara asociación del dolor en artrosis con la presencia de ansiedad o depresión, sin tener en cuenta factores radiológicos. Las intervenciones psicosociales18 como la del Arthritis Self-Management Program (un curso de educación de pacientes de base comunitaria) proporcionan a los enfermos una capacidad de afrontar la enfermedad y un menor grado de dolor y de incapacidad. Asimismo, los contactos telefónicos mensuales producen mejoría del dolor y de la función articular en comparación con los controles19. Esto podría deberse a que hubiera un mejor cumplimiento del tratamiento por parte de los pacientes que recibían la intervención, pero la mejoría también se producía en aquellos que no modificaban la medicación. Finalmente, hemos de concluir que, aunque los factores psicosociológicos pueden tener importancia en la artrosis, y algunas intervenciones dirigidas a este fin han demostrado ser efectivas (controles telefónicos, programas de autocontrol, intervenciones cognitivoconductales, programas con la participación del cónyuge, etc.), estas intervenciones tienen un alto efecto placebo y se desconoce el grado en el que el paciente mejora únicamente por sentirse más atendido.
En conclusión, el dolor no demuestra una perfecta correlación con la artrosis radiográfica, pero su estu dio es necesario al ser uno de los factores pronósti cos más importantes en la evolución de la enfermedad. La etiología del dolor en la artrosis es compleja y no bien conocida, e influyen causas periféricas (tejidos y nociceptores) y centrales (mecanismos de amplificación).