Recientes cambios en la legislación española obligan a los centros de reproducción asistida españoles a comunicar al Registro Nacional de Actividad-Registro SEF su actividad y los resultados obtenidos a partir del año 2014. El objetivo de este trabajo es analizar la repercusión que los cambios legislativos recientes hayan podido tener en la estimación de las especificaciones de 32 indicadores de calidad descritos en la UNE 179007 para el Laboratorio de Repoducción Humana Asistida (LRHA) mediante el método del estado del arte.
Material y métodosSe utilizó el método basado en el estado del arte a partir de datos del Registro SEF (2010-2013) de participación voluntaria y del Registro Nacional de Actividad-Registro SEF del Registro de Interés por el Ministerio de Sanidad, Servicios Sociales e Igualdad de 2014 de participación obligatoria. En todos los años se utilizó la metodología descrita por Buño et al. (2008) para el cálculo de la especificación de calidad a nivel deseable, la cual, de modo resumido, corresponde al nivel de calidad alcanzado por el 75% de los mejores laboratorios (percentil 25 de la distribución de valores de cada uno de los indicadores analizados). Se calcula el IC 95% del percentil 25 para determinar la imprecisión de dicha estimación.
ResultadosLa imprecisión de las especificaciones estimadas ha disminuido al poder disponer de información de casi todos los centros de TRA nacionales. Nuestros resultados han puesto de manifiesto la consistencia del método del estado del arte, pues el 85% (26/32) de las especificaciones de los indicadores de calidad permanecen estables a lo largo del tiempo. Solo se han observado cambios significativos en 6 especificaciones de los indicadores. Las 2 especificaciones de los indicadores que han aumentado significativamente son «Tasa de supervivencia a la crioconservación de embriones procedentes de ovocitos frescos propios y donados» y «Porcentaje de embriones evolutivos o utilizados»; disminuyendo significativamente «Número medio de preembriones transferidos en fresco procedentes de ovocitos propios», «Porcentaje de gestación por transferencia de embriones procedentes de ovocitos propios frescos» y «Tasa de gestación múltiple en ciclos de FIV/ICSI».
DiscusiónLos cambios observados en las especificaciones de algunos indicadores que aumentan de forma significativa reflejan cambios en la práctica clínica. Aun así es necesario mejorar la validez de algunos indicadores de calidad de la UNE, ya que su formulación actual no permite estimar la calidad de la prestación asistencial que pretende analizar.
Under recent changes in Spanish law, assisted reproduction centres must inform the National Registry of Activity-SEF Registry of their activity and of the results obtained since 2014. The present study analyses the repercussions of these legislative changes on determining the specifications for 32 quality indicators described in the UNE 179007 standard.
Material and methodsA state-of-the-art method was applied to data obtained from the SEF Register (2010-2013), participation in which is voluntary, and from the National Registry of Activity-SEF Registry administered by the Ministry of Health, Social Services and Equality, participation in which has been mandatory since 2014. For each year of the study period, the method used was that described by Buño et al. (2008) for calculating the quality specification at a desirable level. In short, this corresponds to the quality level reached by 75% of the best laboratories (the 25th percentile of the distribution of values for each of the indicators analysed). The 95% confidence interval of the 25th percentile was calculated to determine the margin of error of this estimate.
ResultsThe imprecision of the studied specifications has decreased, as information was available from almost all the ART centres in Spain. Our results corroborate the robustness of the state-of-the-art method, with 85% (26/32) of the quality indicator specifications remaining stable over time. Significant changes were only observed in 6 indicator specifications. The 2 specifications that increased significantly were “Survival rate to cryopreservation of embryos from donated and own fresh oocytes” and “Percentage of embryos in evolution or used”. On the other hand, there were significant decreases for “Mean number of pre-embryos transferred fresh from own oocytes”, “Percentage of gestation by embryo transfer from fresh own oocytes” and “Multiple gestation rate in IVF/ICSI cycles”.
DiscussionThe significant increases observed in the specifications of some indicators reflect changes in clinical practice. Nevertheless, it is necessary to improve the validity of some UNE quality indicators, since with their current formulation, the quality of the treatment provided cannot be determined.
Cualquier prestación sanitaria debe estar centrada en el paciente, lo que obliga a los profesionales sanitarios a utilizar herramientas para asegurar que su actividad satisface las necesidades de este. Los indicadores de calidad son una herramienta clave para asegurar la calidad de este servicio (Castilla et al., 2016). En lo que respecta al laboratorio de reproducción humana asistida (RHA), la norma UNE 179007 (2013) «Sistemas de gestión de la calidad para laboratorios de reproducción asistida» establece los indicadores de calidad para el aseguramiento de esta en los laboratorios de reproducción asistida. Las especificaciones de estos indicadores de calidad desde el año 2010 se han establecido utilizando el método del estado del arte a partir de los datos obtenidos del Registro SEF, de participación voluntaria y declarado registro de interés sanitario por el Ministerio de Sanidad, Servicios Sociales e Igualdad en 2009. Anualmente se actualizan dichas especificaciones de calidad, pues el estado del arte cambia con base en los avances tecnológicos. Mantilla et al. (2015) analizaron la evolución de estas especificaciones desde los años 2010-2012, comprobando que se mantenían para todos los indicadores, excepto para aquellos relacionados con la crioconservación de ovocitos y embriones, lo que atribuyeron a la implantación de la vitrificación en los centros españoles. En el caso del laboratorio de andrología, existe literatura sobre las especificaciones de calidad de indicadores de la fase técnica de la determinación de parámetros seminales, las cuales han sido calculadas con base en la variación biológica (Álvarez et al., 2003), en el estado del arte (Castilla et al., 2005) y en la opinión de los clínicos (Aguilar et al., 2008).
En julio de 2015 se hizo efectiva una modificación de la Ley 14/2006, de 26 de mayo, sobre técnicas de RHA en relación con el registro obligatorio de actividad y resultados de los centros y servicios de RHA. Debido a este cambio legislativo, el Registro SEF fue declarado en septiembre de 2015 como Registro Nacional de Actividad-Registro SEF (RNA-RSEF), y su participación para los centros de RHA españoles pasó de voluntaria a obligatoria, lo que debería lógicamente repercutir en la tasa de participación de centros de RHA en este registro. Por tanto, el último Registro Nacional de Actividad-Registro SEF, realizado en el año 2016 (que corresponde a la actividad de 2014), es el primer registro de RHA de participación obligatoria realizado en España desde la creación del registro de RHA en la primera Ley de Reproducción Humana Asistida de 1988. En este estudio nos proponemos analizar la evolución de las especificaciones de los indicadores en los últimos 5 años y determinar el impacto que han tenido en ellas los cambios legislativos recientes que obligan a los centros nacionales a participar en el RNA-RSEF.
Material y métodosSe compararon las especificaciones de indicadores de calidad de la UNE 179007 (2013) a nivel deseable obtenidos por el método del estado del arte (tabla 1) a partir de los datos del RNA-RSEF del año 2016, correspondiente a la actividad nacional del año 2014 de participación obligatoria, con las obtenidas en los años 2010-2013, de participación voluntaria. En todos los años analizados se auditaron los datos reportados a cada registro por el 15% de los centros participantes. Los datos de participación de los años 2010-2014 se obtuvieron de los informes de los años 2010 a 2014 de la página web del Registro de la Sociedad Española de Fertilidad (2017) (www.registrosef.com). Las especificaciones de calidad de los años 2010-2014 se obtuvieron de la página web del grupo de interés de calidad de la Asociación para el Estudio de la Biología de la Reproducción (2017) (www.asebir.com). En todos los años se utilizó la metodología descrita por Buño et al. (2008) para el cálculo de la especificación de calidad a nivel deseable, la cual de modo resumido corresponde al nivel de calidad alcanzado por el 75% de los mejores laboratorios (percentil 25 de la distribución de valores de cada uno de los indicadores analizados).
Lista de indicadores de calidad del laboratorio de reproducción asistida humana (UNE 179007) analizados
| Indicador |
|---|
| 1. Porcentaje de fecundación normal FIV/ICSI en ciclos con ovocitos propios en fresco |
| 2. Porcentaje de fecundación normal FIV/ICSI en ciclos con ovocitos donados en fresco |
| 3. Porcentaje de gestación clínica por transferencia en ciclos de FIV/ICSI con ovocitos propios en fresco |
| 4. Porcentaje de gestación clínica por transferencia en ciclos de FIV/ICSI con ovocitos propios crioconservados |
| 5. Porcentaje de gestación clínica por transferencia en ciclos de FIV/ICSI con ovocitos donados en fresco |
| 6. Porcentaje de gestación clínica por transferencia en ciclos de FIV/ICSI con ovocitos donados crioconservados |
| 7. Tasa de implantación en ciclos de FIV/ICSI con ovocitos propios en fresco |
| 8. Tasa de implantación en ciclos de FIV/ICSI con ovocitos donados en fresco |
| 9. Tasa de implantación en ciclos de preembriones crioconservados con ovocitos propios |
| 10. Tasa de implantación en ciclos de preembriones crioconservados con ovocitos donados |
| 11. Porcentaje de gestación clínica por transferencia de preembriones crioconservados procedentes de ovocitos propios |
| 12. Porcentaje de gestación clínica por transferencia de preembriones crioconservados procedentes de ovocitos donados |
| 13. Número de preembriones transferidos por embarazo en ciclos de FIV/ICSI con ovocitos propios en fresco |
| 14. Número de preembriones transferidos por embarazo en ciclos de FIV/ICSI con ovocitos donados en fresco |
| 15. Número de preembriones transferidos por embarazo en ciclos de criotransferencias con ovocitos propios |
| 16. Número de preembriones transferidos por embarazo en ciclos de criotransferencias con ovocitos donados |
| 17. Porcentaje de preembriones utilizados en ciclos de FIV/ICSI con ovocitos propios en fresco |
| 18. Porcentaje de preembriones utilizados en ciclos de FIV/ICSI con ovocitos donados en fresco |
| 19. Porcentaje de supervivencia ovocitaria tras descrioconservación en ciclos con ovocitos propios |
| 20. Porcentaje de supervivencia ovocitaria tras descrioconservación en ciclos con ovocitos donados |
| 21. Porcentaje de supervivencia preembrionaria tras descrioconservación en ciclos con ovocitos propios |
| 22. Porcentaje de supervivencia preembrionaria tras descrioconservación en ciclos con ovocitos donados |
| 23. Porcentaje de gestación clínica en ciclos de inseminación artificial conyugal |
| 24. Porcentaje de gestación clínica en ciclos de inseminación artificial de donante |
| 25. Tasa de gestación múltiple en ciclos de FIV/ICSI con ovocitos propios |
| 26. Tasa de gestación múltiple en ciclos de FIV/ICSI con ovocitos donados |
| 27. Tasa de gestación múltiple en ciclos de inseminación artificial conyugal |
| 28. Tasa de gestación múltiple en ciclos de inseminación artificial de donante |
| 29. Número medio de preembriones por transferencia en ciclos de FIV/ICSI con ovocitos propios en fresco |
| 30. Número medio de preembriones por transferencia en ciclos de FIV/ICSI con ovocitos donados en fresco |
| 31. Porcentaje de preembriones crioconservados por ciclo con ovocitos propios en fresco |
| 32. Porcentaje de preembriones crioconservados por ciclo con ovocitos propios donados |
Se calculó el porcentaje relativo de participación respecto al año anterior. Para el cálculo del porcentaje absoluto de participación se utilizó el Registro Nacional de centros del Ministerio de Sanidad, Servicios Sociales e Igualdad (2015). Se utiliza el test χ2 para comparar la evolución del porcentaje absoluto de participación de centros en el Registro SEF a lo largo de los diferentes años. Una vez actualizadas estas especificaciones y para ver la repercusión de la participación obligatoria en el RNA-RSEF, se compararon estas especificaciones a nivel deseable, correspondiente al percentil 25, con las obtenidas los años anteriores, 2010-2013, a partir del Registro SEF de participación voluntaria. La comparación de las especificaciones entre años se realiza mediante comparación de los intervalos de confianza al 95% del percentil 25 de cada indicador analizado. Para el análisis estadístico y la construcción de las gráficas, las especificaciones y sus intervalos se utilizó el programa estadístico IBM SPSS Statistics 20.
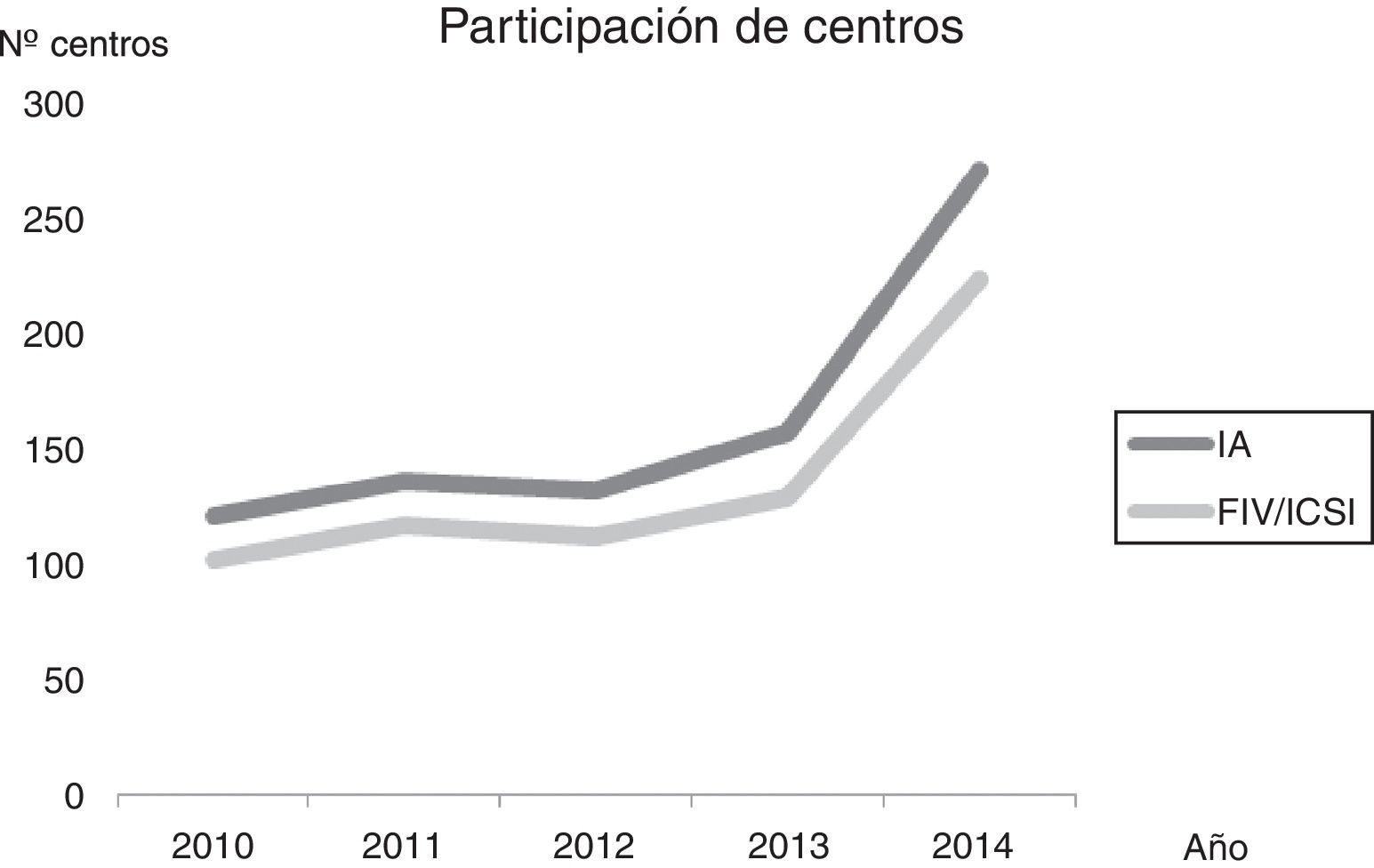
ResultadosParticipación en el registroSe observa un gran aumento en el número de centros participantes en 2014 (fig. 1), siendo este de un 73,1% respecto al 2013. El porcentaje absoluto de participación en el RNA-RSEF fue significativamente superior al de los años 2010-2013 (p<0,001), pasando del 63,7% en 2013 de los centros del Registro Nacional de centros de reproducción asistida del Ministerio de Sanidad, Servicios Sociales e Igualdad al 91,8% en 2014 (p<0,001).
Evolución de las especificaciones de calidadDe los indicadores descritos en la tabla 1, solo en 6 se observaron diferencias estadisticamente significativas en las especificaciones. Las 2 especificaciones de los indicadores que han aumentado significativamente fueron «Tasa de supervivencia a la crioconservación de embriones procedentes de ovocitos frescos propios y donados» y «Porcentaje de embriones evolutivos o utilizados», y las 3 especificaciones que han disminuido significativamente fueron «Número medio de preembriones transferidos en fresco procedentes de ovocitos propios», «Porcentaje de gestación por transferencia de embriones procedentes de ovocitos propios frescos» y «Tasa de gestación múltiple en ciclos de FIV/ICSI». En el resto de los indicadores no se observaron cambios destacados.
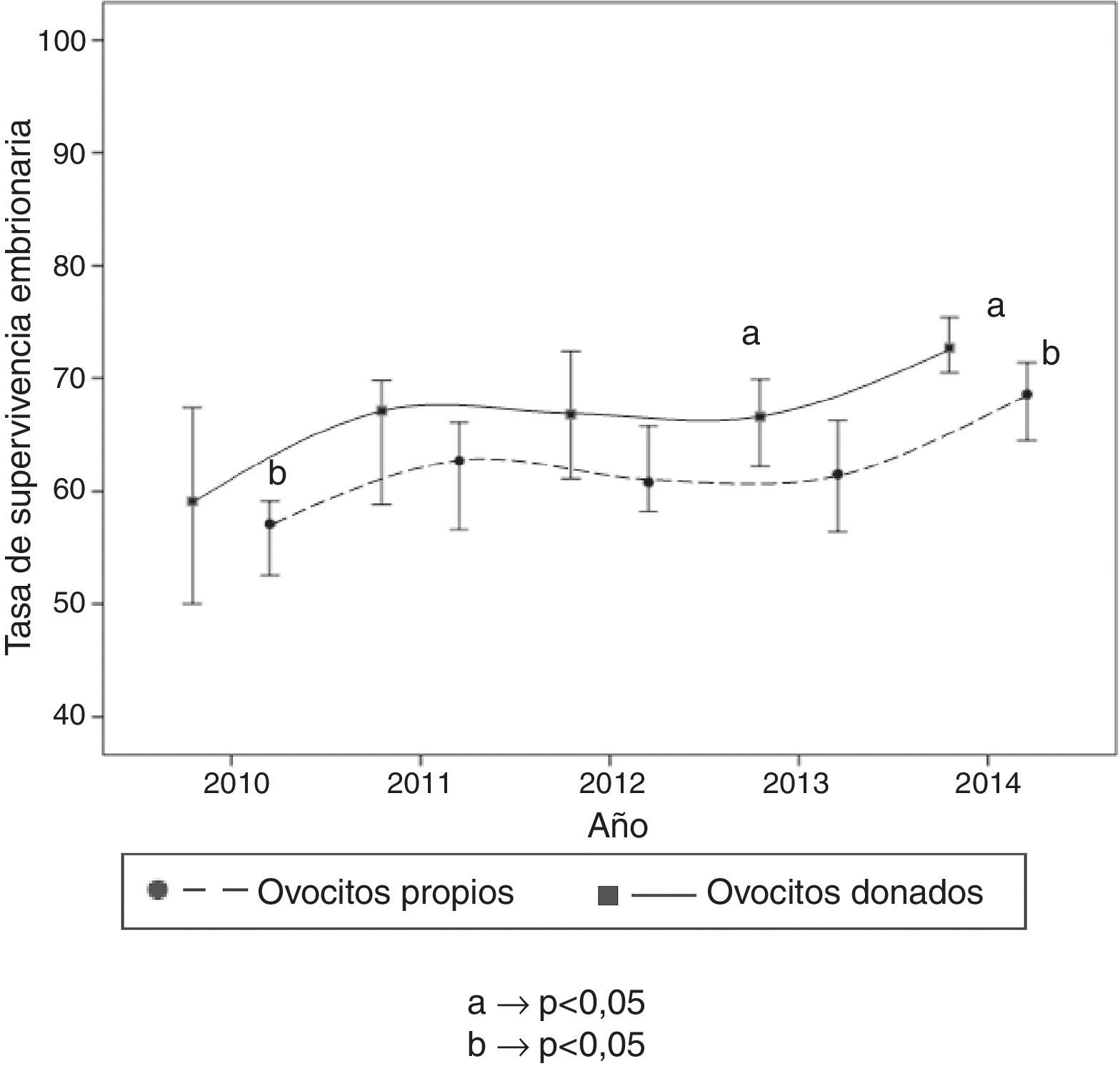
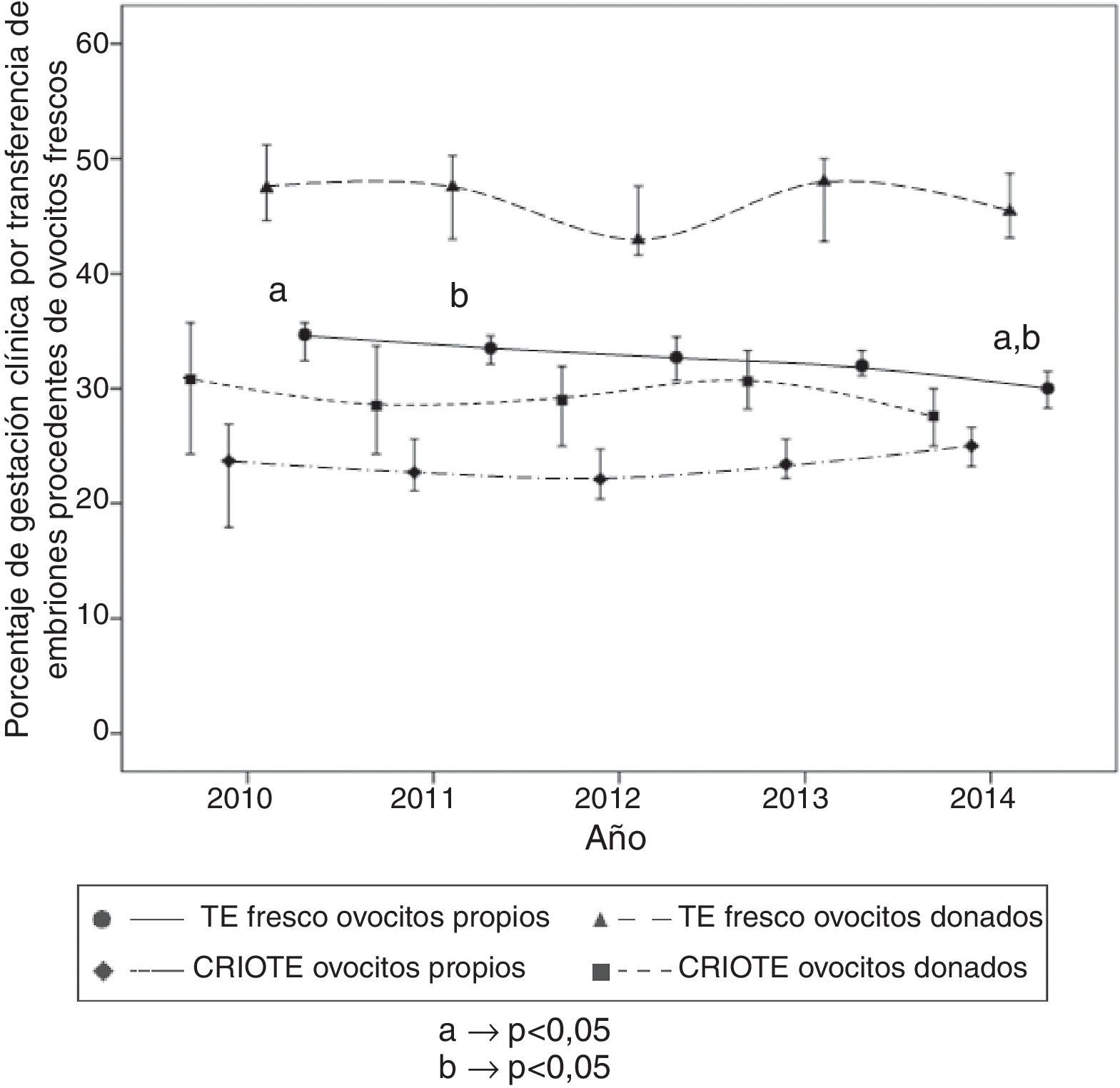
Se observó un aumento significativo en la especificación del indicador «Tasa de supervivencia embrionaria» de embriones procedentes de ovocitos donados del año 2014 respecto al 2013 y de embriones procedentes de ovocitos propios del año 2014 respecto al 2010 (fig. 2). No se observan diferencias significativas en la especificación del indicador «Porcentaje de gestación clínica por transferencia de embriones frescos procedentes de ovocitos frescos donados», ni para embriones crioconservados procedentes de ovocitos frescos propios y donados a lo largo de los años. Sin embargo, se observa una disminución significativa en esta especificación en la transferencia embrionaria de embriones frescos procedentes de ovocitos propios entre los años 2010 y 2014 (fig. 3).
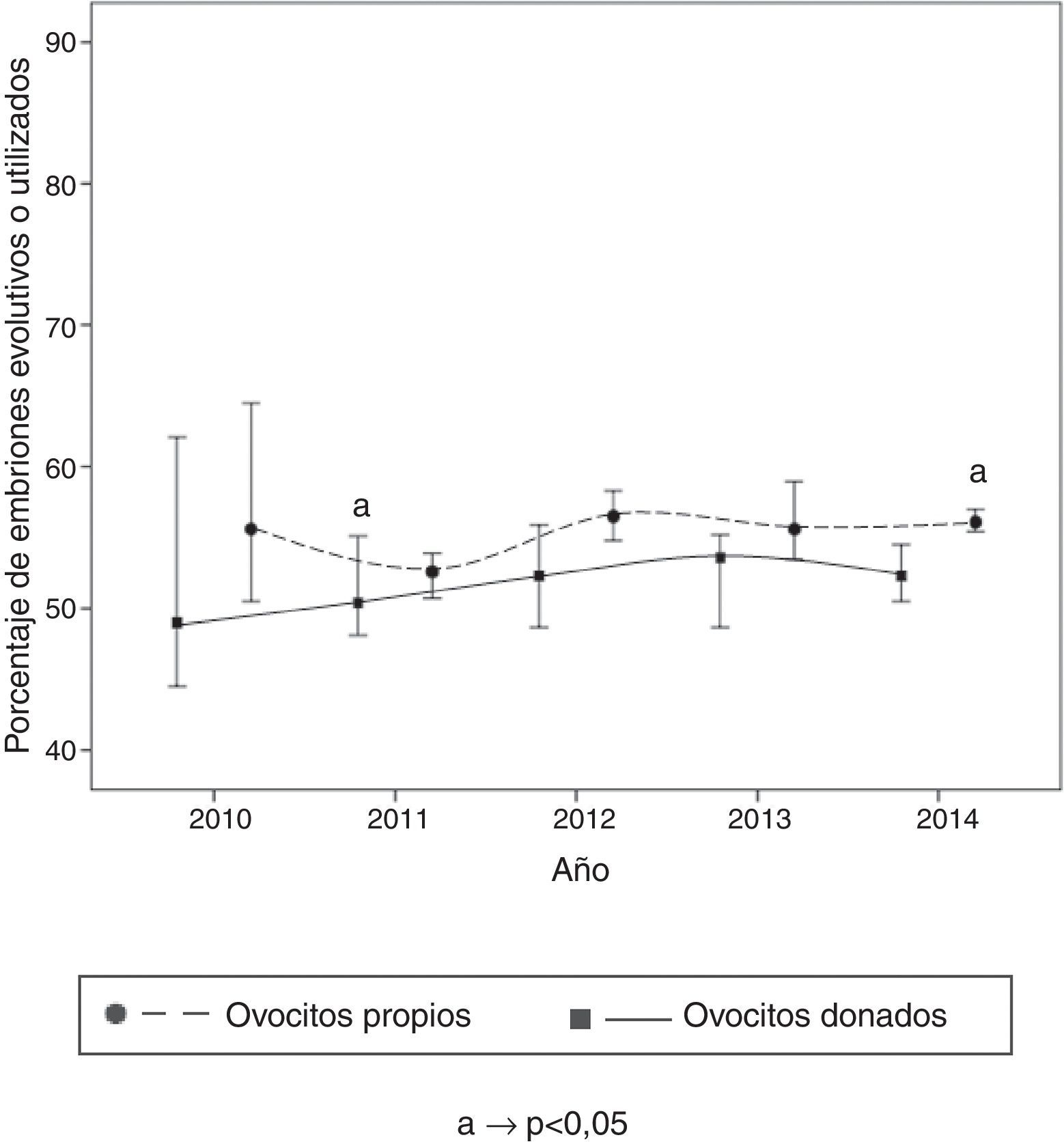
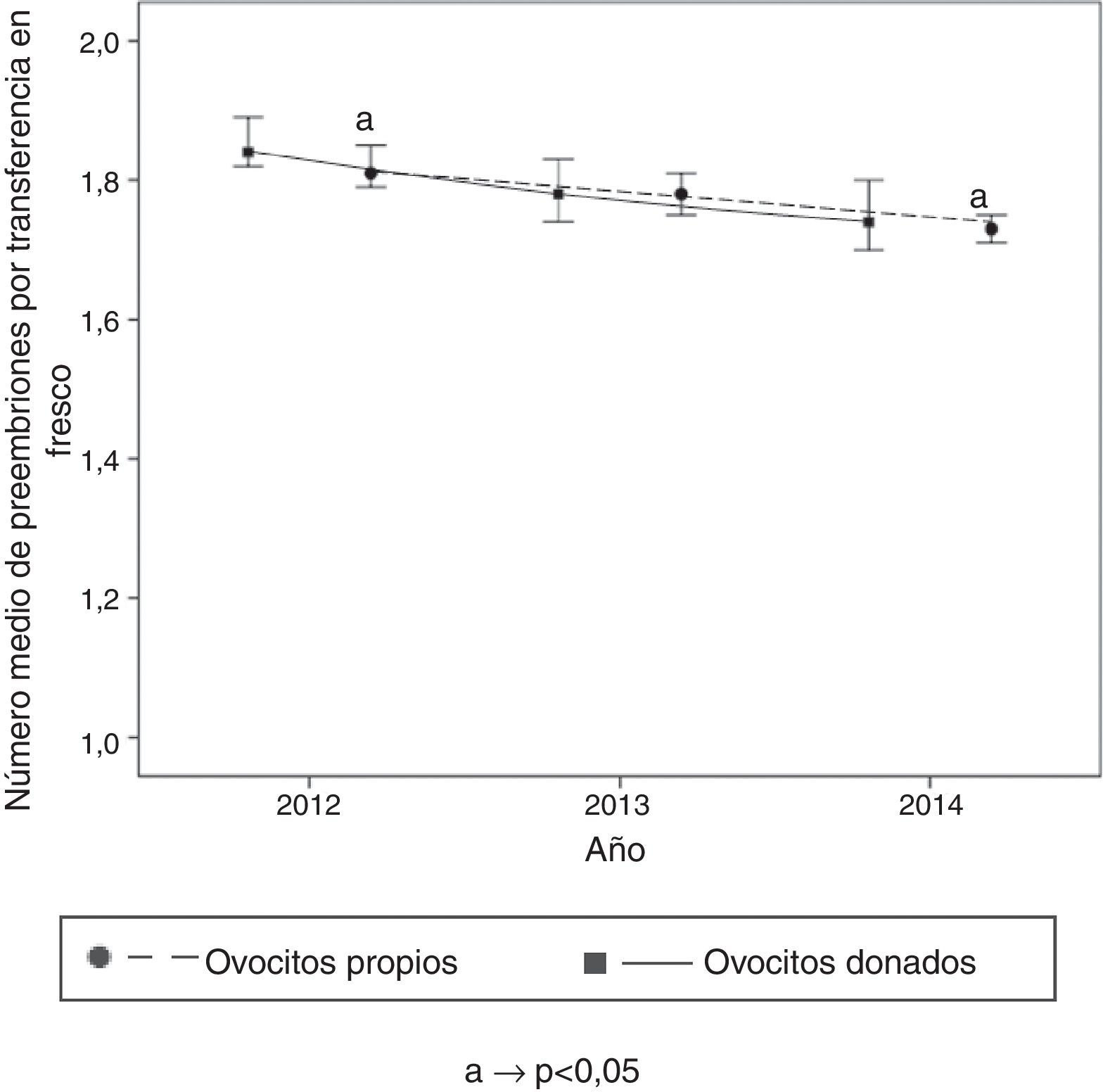
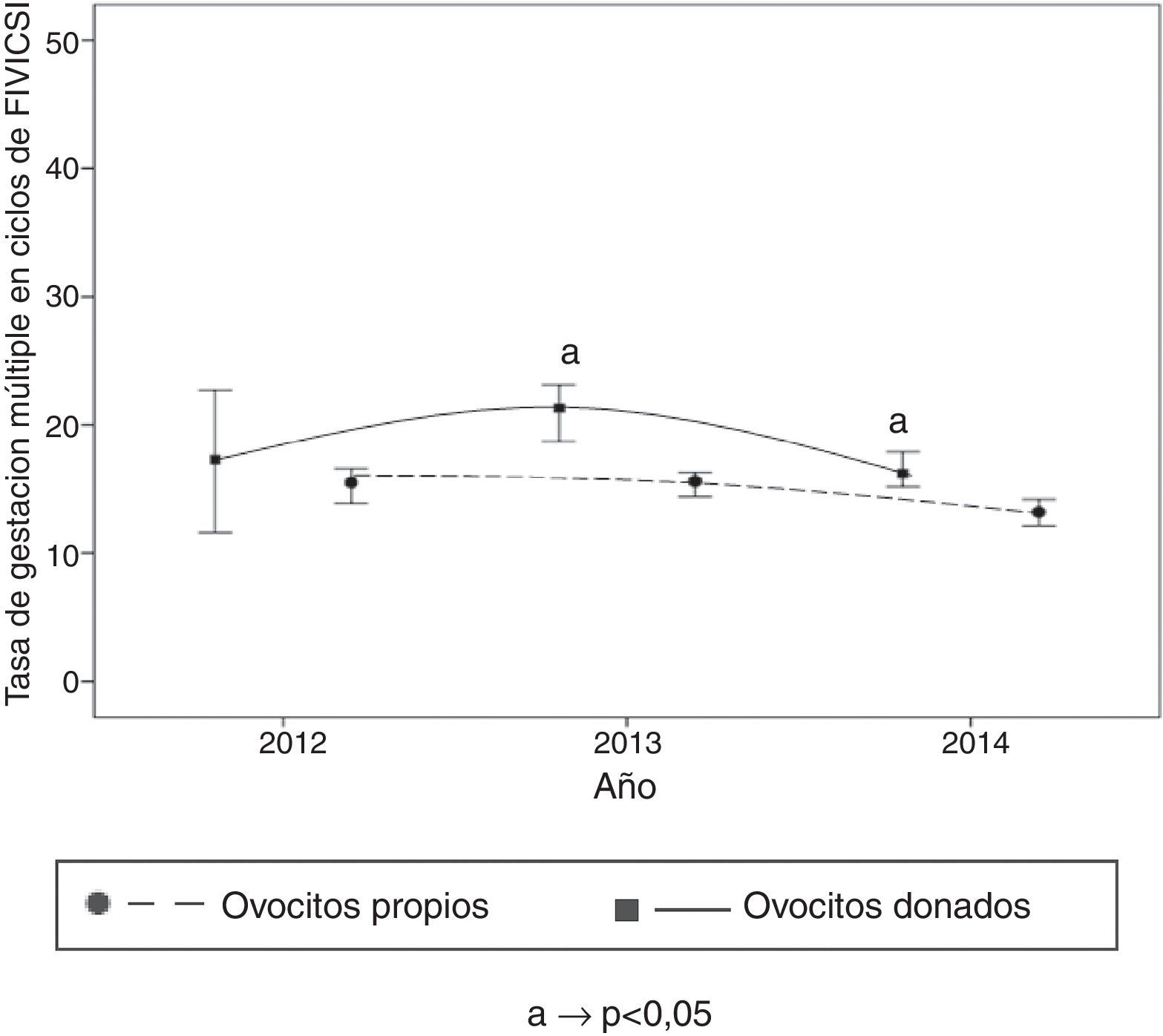
Se observa un aumento significativo en la especificación del indicador «Porcentaje de embriones evolutivos o utilizados» procedentes de ovocitos propios en el año 2014 respecto al 2011 (fig. 4). Se observa una disminución significativa en la especificación del indicador «Número medio de preembriones por transferencia en fresco» a lo largo de los años, tanto en ovocitos propios como donados (fig. 5). Se observa un descenso significativo en la especificación del indicador «Tasa de gestación múltiple en ciclos de FIV/ICSI» con ovocitos donados frente a la de ovocitos propios del año 2014 respecto al 2013 (fig. 6).
En la mayoría de las especificaciones de los indicadores de calidad descritas se observa una reducción de la amplitud del intervalo de confianza de la estimación de la especificación (percentil 25) en el año 2014.
DiscusiónNuestros resultados han puesto de manifiesto la consistencia del método del estado del arte en el establecimiento de especificaciones de indicadores de calidad del Laboratorio de Reproducción Asistida, ya que a pesar de haberse producido un incremento relativo en el porcentaje de centros participantes del 73,1% en el año 2014, estas especificaciones apenas han variado. Por lo tanto, los valores establecidos en años anteriores son válidos para el 85% (26/32) de los indicadores. Este incremento de centros participantes coloca a España a la cabeza de Europa en TRA (Calhaz-Jorge et al., 2017) y en los primeros puestos a nivel mundial (Dyer et al., 2016). No cabe duda de que este incremento ha estado relacionado con los cambios legislativos que han obligado a los centros españoles a participar.
Como era de esperar, por el aumento del número de centros considerados en la estimación de la especificaciones, se ha observado una disminución considerable en la amplitud de los intervalos de confianza de la mayoría de las especificaciones, lo que hace que estas sean más precisas. Mantilla et al (2015) observaron una tendencia a aumentar la especificación del indicador de calidad «Tasa de supervivencia a la crioconservación de embriones procedentes de ovocitos frescos propios y donados» entre los años 2010-2012. Nuestros resultados confirman esa tendencia, alcanzando la significación. Esto parece deberse a la plena incorporación de la vitrificación embrionaria en los laboratorios nacionales. Esta mejora en la calidad de esta prestación se produce tanto para ovocitos propios como donados, confirmando la mayor eficacia de esta técnica con respecto a la utilizada hace unos años basada en la congelación lenta (Levron et al., 2014; Fasano et al., 2014).
Otro indicador en el cual se observa variación en su especificación a lo largo de los años es en el «Número medio de preembriones transferidos en fresco procedentes de ovocitos propios», en que se observa un número significativamente inferior en 2014 que en 2012. Esta disminución podría reflejar la implantación de políticas de transferencia embrionaria encaminadas a disminuir la tasa de embarazo múltiple. Entre estas estrategias se encuentra la tendencia actual a realizar transferencias electivas de embrión único (eSET) tanto en ciclos de FIV/ICSI de ovocitos propios como donados, así como a disminuir el porcentaje de transferencias de 3 embriones (Zamora et al., 2014). Estas tendencias coinciden con lo descrito en otros países de nuestro entorno (Calhaz-Jorge et al., 2017).
La disminución observada en la especificación del indicador «Porcentaje de gestación por transferencia de embriones procedentes de ovocitos propios frescos» puede relacionarse con la disminución de la eficacia asociada a la eSET debida a la ya comentada disminución del número de embriones transferidos. Para mantener una eficacia similar a la obtenida con transferencias de 2 embriones es necesario considerar las gestaciones obtenidas con el eSET en fresco, más las obtenidas tras una criotransferencia de uno o 2 embriones crioconservados (López-Regalado et al., 2016). Con esta última estrategia se consigue igualar la tasa de gestación sin obtener apenas embarazos múltiples. No obstante, también podría relacionarse la disminución observada en la especificación del indicador «Porcentaje de gestación por transferencia de embriones procedentes de ovocitos propios frescos» con la implantación de políticas de transfer diferido (freeze all) en los centros españoles. Esta estrategia de cancelar la transferencia de embriones frescos y vitrificar todos los embriones suele aplicarse a pacientes con sospecha de síndrome de hiperestimulación ovárica o con luteinización precoz, las cuales son pacientes que tienen buenas respuestas a la estimulación ovocitaria, lo que se asocia a un mayor número de embriones disponibles, permitiendo realizar una adecuada selección embrionaria antes de la transferencia (Ata et al., 2012Labarta et al., 2017). Por tanto, es lógico que esto repercuta negativamente en la especificación del indicador de calidad de la gestación por transferencia de embriones en fresco, ya que las pacientes de mejor pronóstico son excluidas de su cálculo. Además, el no haber observado ninguna variación en las especificaciones del indicador «Tasa de implantación» nos hace descartar la hipótesis de una reducción en la calidad embrionaria como explicación de la comentada disminución de la tasa de gestación por transferencia.
Otra consecuencia de la progresiva implantación del eSET en ciclos de ovocitos propios es la observada disminución significativa en la especificación del indicador «Tasa de gestación múltiple en ciclos de FIV/ICSI». Dada la relevancia clínica de este indicador de calidad, consideramos muy destacado que haya descendido su especificación, pues pequeñas disminuciones en el porcentaje de embarazos múltiples tienen una gran repercusión en la seguridad y en los costes asociados a las TRA (Cabello et al., 2010). El no haber observado ninguna variación en la especificación del mismo indicador pero con embriones procedentes de ovocitos donados frescos se explica porque la práctica de eSET estaba ya más implantada en ciclos de donación de ovocitos (Zamora et al., 2014) y porque en los ciclos de recepción de estos embriones no se da la práctica de freeze all, pues no se estimula la ovulación, no existiendo riesgo de síndrome de hiperestimulación ovárica ni efecto negativo sobre el endometrio. Creemos necesario incorporar indicadores a los sistemas de calidad del laboratorio de RHA que describan la incorporación de las 2 políticas de transferencia embrionaria comentadas anteriormente en ciclos con embriones procedentes de ovocitos propios: eSET y freeze all.
Por otro lado, el aumento observado en la especificación del indicador «Porcentaje de embriones evolutivos o utilizados» (transferidos+crioconservados) en ovocitos propios se podría relacionar con la tendencia a aumentar con los años el porcentaje de embriones crioconservados en ciclos de ovocitos propios, y que nos vuelve a demostrar como la llegada de la vitrificación ha cambiado claramente el destino clínico de muchos embriones al mejorar el pronóstico de supervivencia de aquellos de calidad C o D. Hay que destacar que la especificación del indicador «Porcentaje de supervivencia ovocitaria a la crioconservación» es significativamente superior cuando los ovocitos son donados que cuando son propios. Este resultado se asociaría a la mejor calidad ovocitaria de ovocitos procedentes de mujeres jóvenes donantes que de ovocitos procedentes de mujeres de más edad infértiles. Esta mayor calidad se refleja también en que la mayoría de las especificaciones de indicadores de calidad son más altas en embriones procedentes de ovocitos de donante que propios. Actualmente existe una gran controversia sobre el rendimiento de los ovocitos crioconservados comparado con el de ovocitos frescos, existiendo autores que hablan de una eficacia similar (Rienzi et al., 2010; Rienzi et al., 2012) y otros que demuestran un rendimiento inferior en los crioconservados (Potdar et al., 2014). Nuestros resultados obtenidos con la especificación del indicador de calidad «Tasa de gestación por transferencia» evidencian que el rendimiento es menor, pues observamos una tasa de gestación por transferencia embrionaria significativamente menor cuando los embriones proceden de ovocitos crioconservados. No obstante, a pesar de esta menor eficacia creemos que los beneficios logísticos de usar ovocitos crioconservados compensan este pequeño menor rendimiento.
Entre las limitaciones de nuestro estudio encontramos que dado que el RNA-RSEF utilizado para establecer la especificación de los indicadores de calidad es un registro centro a centro, no hemos podido ajustar las especificaciones por distintas variables que repercuten en el resultado de las TRA, como edad, años de esterilidad, etc. Esto hubiera sido posible realizarlo si se dispusiera de datos de un registro de TRA ciclo a ciclo. Sin embargo, creemos que dado el elevadísimo número de ciclos realizados en España y recogidos por el RNA-RSEF, los valores obtenidos son representativos de la calidad de las TRA en España. Otra limitación de nuestro estudio es que las especificaciones de los indicadores de calidad obtenidas se basan en datos de actividad de hace 2 años, lo cual es debido a que es necesario esperar al resultado de las gestaciones obtenidas en los últimos meses del año. Además, hay que añadir un periodo de recogida y análisis de datos de al menos 6-12 meses, por lo que cada año se publican datos correspondientes como mínimo a la actividad realizada 2 años antes.
En resumen, la precisión de las especificaciones de los indicadores de calidad de la UNE 179007 (2013), basados en el estado del arte, ha aumentado considerablemente debido a los cambios legislativos a nivel nacional, que han favorecido la participación de centros en el RNA 2014-RSEF. La mayoría de las especificaciones de calidad basadas en el estado del arte de los indicadores de la UNE se mantienen estables a nivel deseable durante los últimos 5 años, demostrándose la firmeza de este método de cálculo de especificaciones de calidad. Además, la única área del laboratorio de RHA en la cual se ha producido un aumento significativo en la calidad de sus prestaciones es en la crioconservación de embriones y ovocitos, lo que ha repercutido en el aumento de las especificaciones basadas en el estado del arte de los indicadores relacionados con esta área. Estos cambios han permitido disminuir el número de embriones transferidos procedentes de ovocitos propios y, consecuentemente, disminuir la especificación del indicador de calidad «Porcentaje de gestación múltiple en ciclos de FIV/ICSI», de gran transcendencia clínica. Por último, es necesario mejorar la validez de algunos indicadores de calidad de la UNE 179007 (2013), pues su formulación actual no permite estimar la calidad de la prestación de las actividades que se pretendía medir; además, es necesario incorporar nuevos indicadores de las políticas de transferencia embrionaria.
AutoríaTodos los autores contribuyeron a la concepción y el diseño del estudio, al análisis e interpretación de los datos, a la redacción del artículo, a la revisión crítica de los contenidos y dieron su aprobación final a la versión que se publica.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.