El estatus epiléptico no convulsivo (SENC) es una entidad subdiagnosticada. Hay datos limitados sobre el rol de levetiracetam vía oral (LEV-VO) en el manejo del SENC.
Objetivo: Analizar la respuesta del LEV-VO en pacientes con SENC.
Materiales y métodosRetrospectivamente se analizaron los casos de SENC tratados con LEV-VO entre 2007- 2008 de nuestro registro. Se definió SENC como actividad epiléptica continua o recurrente, generalizada o focal, de 30 minutos o más de duración, acompañada con signos motores sutiles y/o alteración del estado de conciencia-conducta. Utilizamos los criterios de Chong-2005 para definir actividad epiléptica. Se definió respuesta al tratamiento al observar mejoría clínica y electroencefalográfica (desaparición del estatus epiléptico). Se definió SENC refractario (SENC-R) como aquel sin respuesta completa al uso apropiado de dos fármacos antiepilépticos (fármaco de primera línea: benzodiacepina+fármaco segunda línea: fenitoína). La dosis total de LEV-VO usada fue 3.000mg, administrando 500mg cada 15-20 minutos.
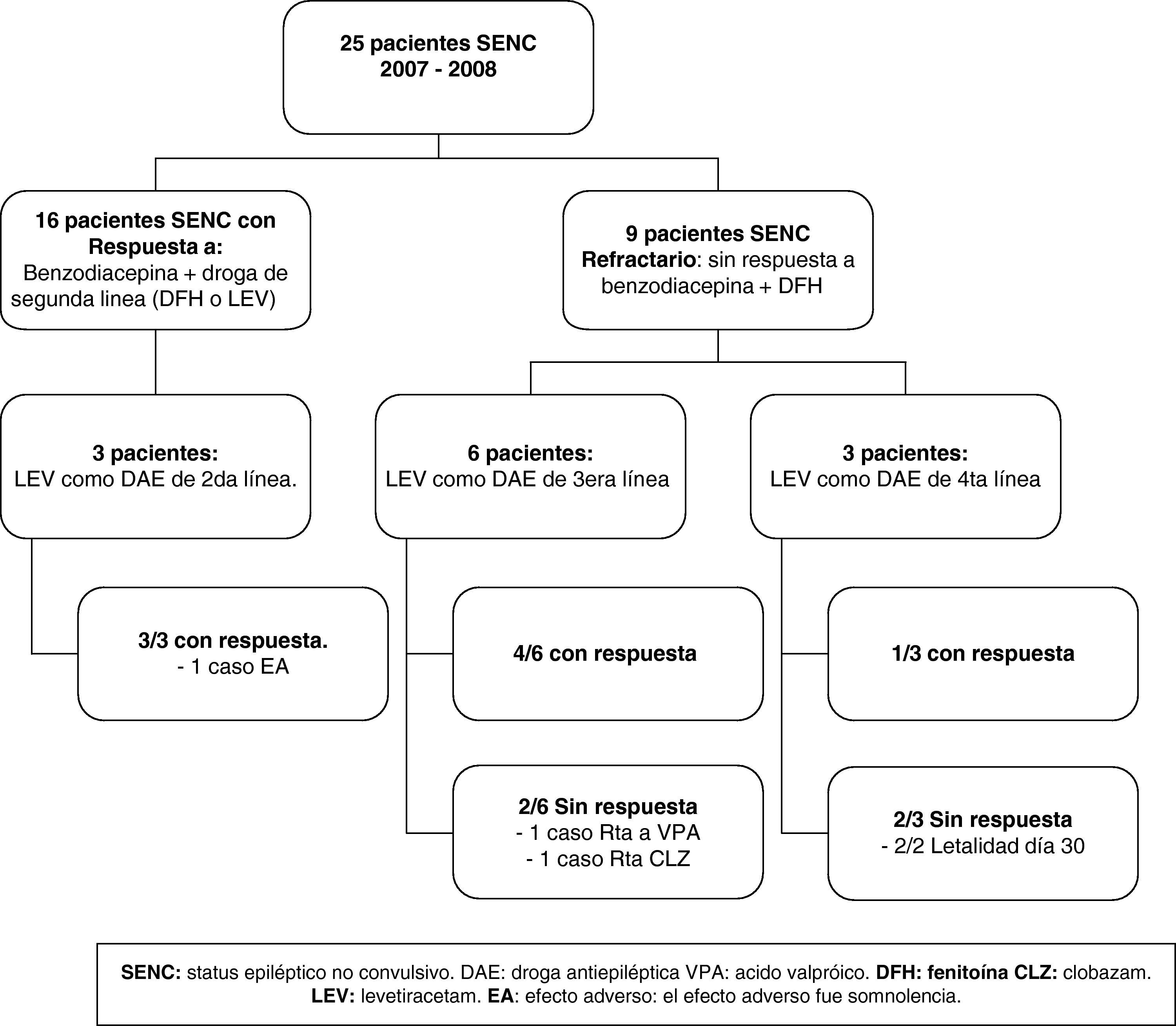
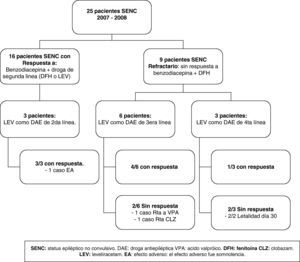
ResultadosSe incluyeron 12 pacientes con SENC tratados con LEV-VO de un total de 25. Se utilizó como fármaco de segunda línea para el tratamiento inicial SENC en tres pacientes y como fármaco de tercera o cuarta línea en el SENC-R en 9. Hubo una respuesta en el 100% de los casos (3/3) del SENC inicial. La tasa de respuesta en los SENC-R como fármaco de tercera y cuarta línea fue del 66% (4/6) y del 33% (1/3) respectivamente.
ConclusiónEl uso LEV-VO tiene un potencial rol en el tratamiento del SENC inicial como refractario, el cual debería ser confirmado en estudios prospectivos, controlados y aleatorizados.
Nonconvulsive status epilepticus (NCSE) is an underdiagnosed condition. There is limited information about treatment with oral levetiracetam (LEV-VO) for NCSE.
ObjectiveTo analyze NCSE response to LEV-VO treatment.
Materials and MethodsWe retrospectively analyzed NCSE cases treated with LEV-VO, between 2007-2008, in our record. NCSE was defined as continuous or recurrent seizure activity, generalized or focal, 30minutes or longer, accompanied by subtle motor signs and/or altered state of consciousness, behavior. Chong-2005 criteria were used for defining epileptic activity. We defined response to treatment if there were clinical and EEG improvement (disappearance of the status epilepticus). Refractory was defined (NCSE-R) when NCSE had no complete response to the appropriate use of two antiepileptic drugs (first-line drug: benzodiazepine+second-line drug: phenytoin). The total dose used (LEV-VO) was 3,000mg, 500mg administered every 15-20minutes.
ResultsWe identified 25 patients with NCSE, 12 treated with LEV-VO. LE-VO was used as second-line drug for initial treatment in 3 NCSE patients, and as a drug of third or fourth line in NCSE-R in 9 patients. There was a response in 100% cases (3/3) of the initial NCSE. The response rate in the NCSE-R as a drug of third and fourth line was 66% (4/6) and 33% (1/3) respectively.
ConclusionLEV-VO has a potential role in the treatment of refractory and initial SENC, which should be confirmed in prospective, randomized and controlled studies.
El estatus epiléptico no convulsivo (SENC) es una entidad heterogénea con una gran variedad de manifestaciones clínicas. En el año 1800 médicos franceses describieron cuadros epilépticos con manifestaciones no convulsivas1,2, y en la década de los ochenta del siglo pasado aparecieron las primeras descripciones de series de pacientes con SENC. A partir de entonces ha habido grandes avances en la comprensión de esta entidad y de su fisiopatología y pronóstico3-6. La incidencia varía según las diferentes series; se estima entre 5,6 y 18,3/100.000 personas/año7. En nuestra población la incidencia ajustada anual de estatus epiléptico (SE) es de 24,3 SE/100.000 habitantes/año, correspondiendo el 48% a SENC (incidencia ajustada anual de SENC de 11.6 SE/100.000 habitantes/año)8.
Sin embargo, y a pesar de su alta incidencia, no existen guías acerca del tratamiento específico para el SENC, y en guías recientes su tratamiento continúa siendo igual al del SE generalizado9-11.
Levetiracetam (LEV) es un derivado de la pirrolidona aprobado para tratamiento concomitante de crisis de inicio parcial, crisis mioclónicas y crisis generalizadas en síndromes idiopáticos, y como monoterapia en pacientes con crisis parciales con un nuevo diagnostico de epilepsia12. Levetiracetam vía oral (LEV-VO) tiene una biodisponibilidad del 95%13.
Diferentes series publicadas mostraron la eficacia del uso de levetiracetam de forma endovenosa para el tratamiento del SE, con una tasa global de respuesta del 65%14-18. En un trabajo reciente, que incluyó 4 pacientes con SENC, fue utilizado como primera línea de tratamiento, logrando la remisión en el 100% de los 4 casos17.
En relación con la eficacia del LEV-VO en el tratamiento del SE los datos son insuficientes debido a la escasez de publicaciones19-23. Un estudio retrospectivo realizado en 8 pacientes con SENC mostró la terminación del mismo dentro de los tres días, cuando se usó LEV-VO como terapia añadida a otro anticonvulsivante21. No hemos encontrado series publicadas en nuestro país acerca del tratamiento con este fármaco VO en pacientes con SENC.
El objetivo de este estudio es analizar la respuesta del tratamiento con LEV-VO en pacientes con SENC inicial y refractario en nuestra población.
Material y métodosSe registraron prospectivamente todos los casos de SENC consecutivos entre el 1 de marzo de 2007 y el 31 de junio del 2008, ambos inclusive, en pacientes de 21 años o más.
Se incluyeron a todos los pacientes que cumplían criterios para SENC tratados con LEV-VO y a todos los pacientes con diagnóstico de SENC no tratados con LEV-VO como grupo de control durante el periodo de estudio.
El hospital cuenta con 240 camas, 19 camas de terapia intensiva, 9 camas propias de internación neurológica y 22 boxes para la atención en sala de urgencias. Los potenciales casos de SENC fueron identificados por neurólogos en la sala de urgencias, sala de internación, sala neurológica, consulta neurológica y registros de EEG en consultorio. El hospital brinda atención neurológica y cuenta con la posibilidad de realizar EEG durante las 24 horas del día los 7 días de la semana, es decir, ofrece vigilancia completa para la identificación de los posibles casos. La información respecto al tipo, duración, semiología, tratamiento y etiología del SE, así como enfermedades asociadas, complicaciones, desenlace al día 30, resultados de estudios (laboratorio, EEG, TAC o RMN), datos demográficos y la historia médica del paciente fue recabada en una base de datos electrónica.
La recolección retrospectiva se basó en la Clasificación Internacional de Enfermedades, se revisaron y evaluaron todos registros al alta hospitalaria con códigos positivos para epilepsia (ICD-9: 345 y subgrupos) durante el periodo de estudio.
Se definió el SENC como actividad epiléptica continua en el EEG de 30 minutos o más de duración, generalizada o focal, en pacientes sin presencia de síntomas ictales evidentes (por ejemplo clonus epiléptico)7. Se usaron los criterios de Young modificados para definir actividad epiléptica continua en el EEG24. El patrón EEG fue clasificado según definiciones internacionales25. El tipo de SENC fue clasificado en parcial o generalizado, basado en la Clasificación Internacional de las epilepsias y los síndromes epilépticos (ILAE) de las crisis epilépticas26-28. Las etiologías del SENC se clasificaron en sintomática aguda, sintomática remota y de causa desconocida, usando la definición propuesta por Hauser29 y utilizadas en estudios previos.
Se definió respuesta al tratamiento a la presencia de mejoría clínica y electroencefalográfica2,30.
Mejoría clínica se definió como mejoría del estado de conciencia o los síntomas por los cuales fue admitido en paciente, y mejoría electroencefalográfica a la desaparición del patrón compatible con estatus no convulsivo.
Las benzodiacepinas fueron consideradas de primera línea de tratamiento para todos los pacientes. El fármaco de segunda línea de elección fue fenitoína cuando no se utilizó LEV-VO. La elección del fármaco de tercer o cuarta línea estuvo a cargo del criterio del médico tratante, de acuerdo con las guías vigentes y teniendo en cuenta antecedentes y características particulares de cada caso.
Se definió como SENC refractario a los pacientes sin respuesta completa al uso apropiado con dos fármacos antiepilépticos (primera y segunda línea). Se definió como SENC inicial (SENC-I) a los pacientes que respondieron al fármaco de primera y segunda línea (benzodiacepina+fenitoína o levetiracetam)31,32.
La letalidad al día 30 fue definida como muerte asociada con el SENC entre el inicio del cuadro hasta 30 días posteriores al diagnóstico.
La historia previa de epilepsia fue definida como la presencia de dos o más episodios de crisis en su vida.
La dosis total usada de LEV-VO fue 3.000mg, administrando 500mg cada 15-20 minutos por vía oral o sonda nasogástrica. La dosis total y la vía de administración del LEV-VO se basó en estudios de biodisponibilidad publicados33.
Análisis estadísticoSe realizó estadística descriptiva de la población cautiva y de los pacientes con SENC, medianas, cuartiles y límites inferior y superior. La prueba de Chi cuadrado y la prueba exacta de Fisher fueron empleadas para comparar frecuencias de variables categóricas entre los dos grupos bajo estudio, y la de Mann-Whitney para comparar diferencias en la distribución entre ambos grupos en mediciones con variables ordinales y variables interválicas sin distribución normal. El programa estadístico utilizado fue el Arcus Quickstat (Biomedical).
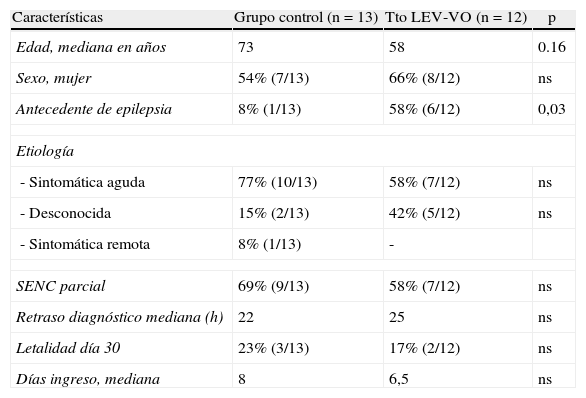
ResultadosSe identificaron 12 pacientes con SENC tratados con LEV-VO de un total de 25 pacientes con diagnóstico de SENC durante el periodo de estudio. La mediana de edad fue de 58 años y el 66% fueron mujeres. Las características basales del grupo de pacientes tratados con LEV-VO y del grupo control figuran en la tabla 1 y en la figura 1.
Comparación de las características clínicas
| Características | Grupo control (n=13) | Tto LEV-VO (n=12) | p |
| Edad, mediana en años | 73 | 58 | 0.16 |
| Sexo, mujer | 54% (7/13) | 66% (8/12) | ns |
| Antecedente de epilepsia | 8% (1/13) | 58% (6/12) | 0,03 |
| Etiología | |||
| - Sintomática aguda | 77% (10/13) | 58% (7/12) | ns |
| - Desconocida | 15% (2/13) | 42% (5/12) | ns |
| - Sintomática remota | 8% (1/13) | - | |
| SENC parcial | 69% (9/13) | 58% (7/12) | ns |
| Retraso diagnóstico mediana (h) | 22 | 25 | ns |
| Letalidad día 30 | 23% (3/13) | 17% (2/12) | ns |
| Días ingreso, mediana | 8 | 6,5 | ns |
SENC: estatus epiletico no convulsivo; Tto LEV-VO: grupo tratado con levetiracetam vía oral.
En el grupo tratado con levetiracetam hubo más pacientes con antecedentes de epilepsia (p=0,03). En el grupo LEV-VO el 42% presentaron etiología desconocida y sintomática aguda el 58%. De esta última el 10% por traumatismo de cráneo, el 34% fue por enfermedad cerebrovascular, el 14% por suspensión del antiepiléptico, el 12% de causa tumoral, el 10% por traumatismo de cráneo, el 10% por alteraciones metabólicas y el 8% por tóxicos. La letalidad al día 30 fue del 17% para el grupo de pacientes tratados con LEV-VO y del 22% para el grupo control.
Las manifestaciones clínicas al ingreso del grupo de pacientes SENC tratados con LEV-VO fueron: trastornos conductuales en el 33%, síndrome confusional en el 25%, afasia en el 17%, alteración de la conciencia en el 17% y coma en en el 8%.
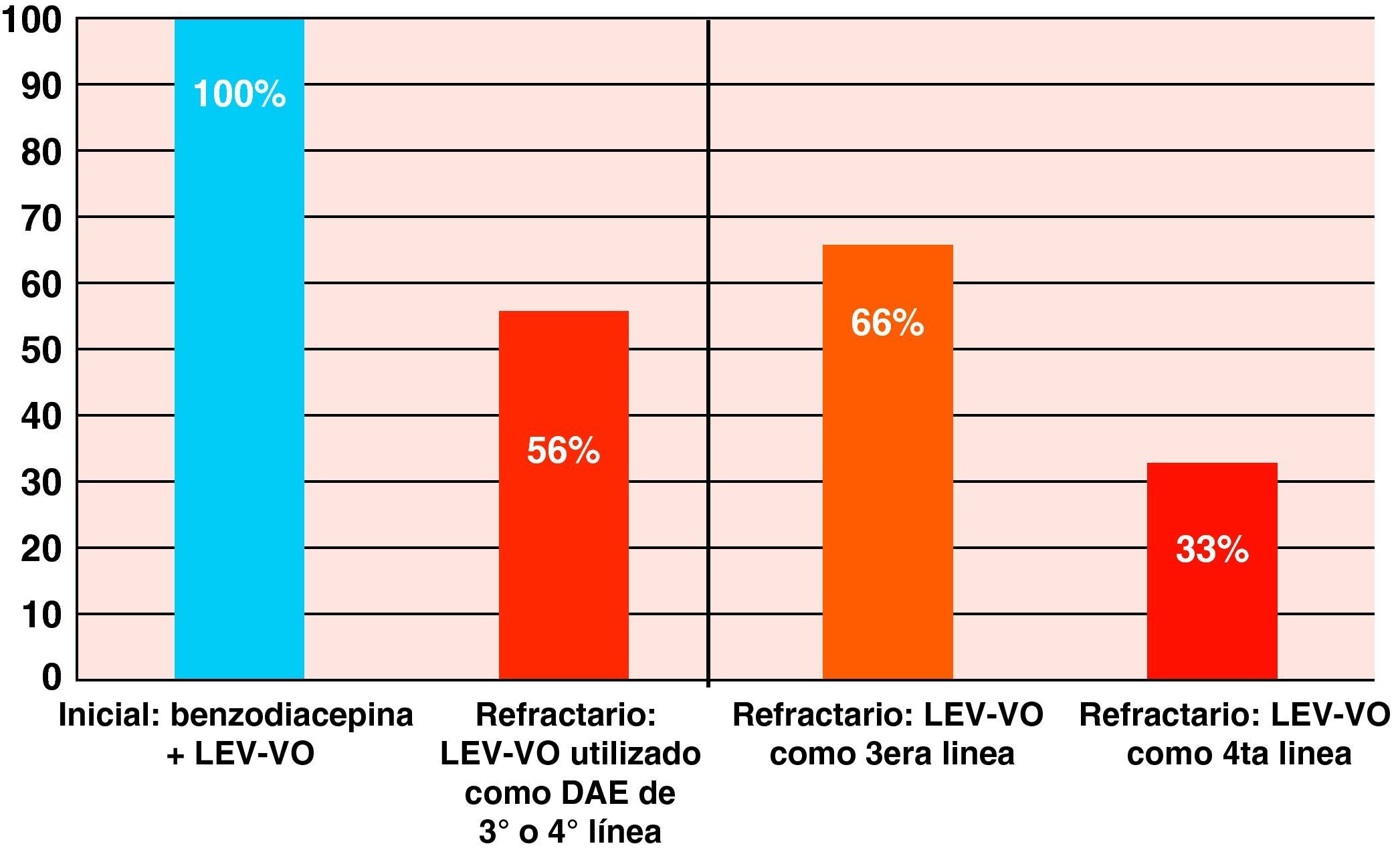
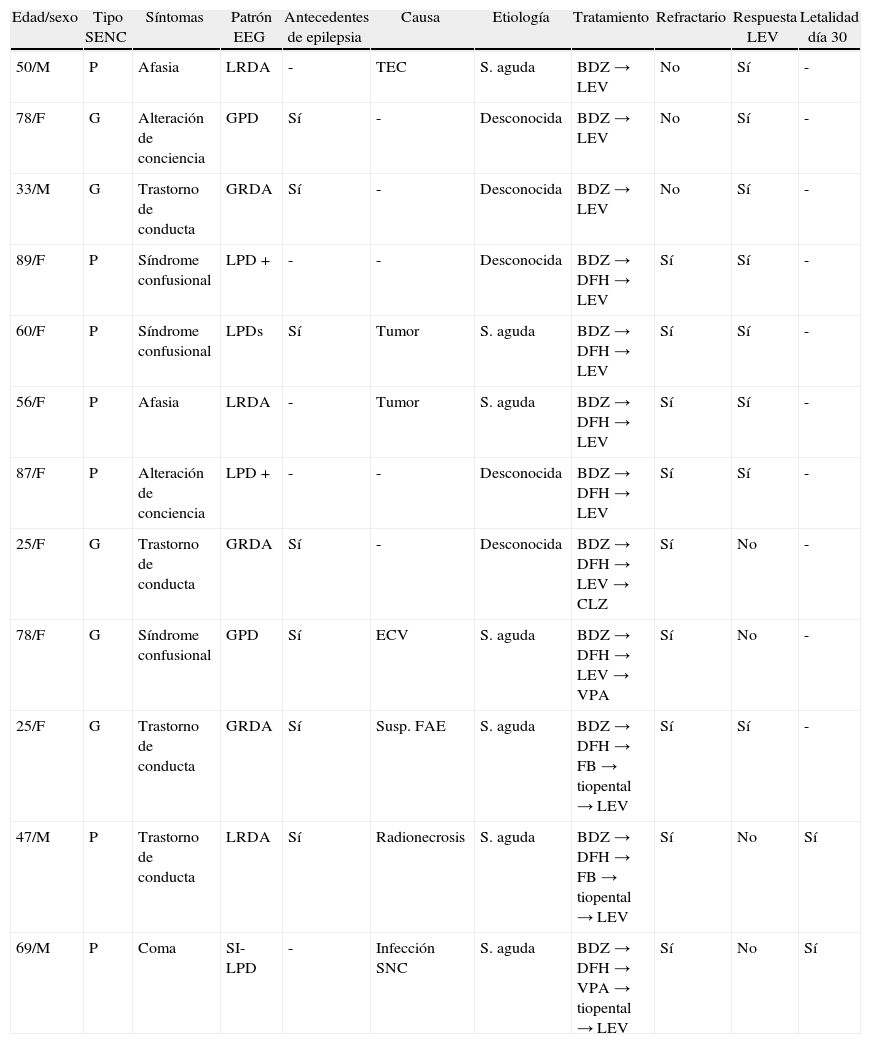
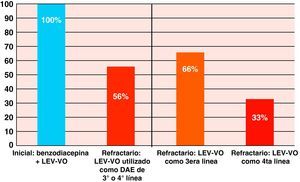
Todos los pacientes con SENC-I, en los cuales el LEV-VO fue administrado como fármaco de segunda línea después de una benzodiacepina, respondieron al tratamiento. La tasa de respuesta global de los pacientes con SENC-R tratados con LEV-VO fue del 56%. Cuando el LEV-VO fue usado como fármaco de tercera línea se observó un 66% de respuesta, mientras que cuando se utilizó como cuarto fármaco respondió solo un 33% de los pacientes (fig. 2). La secuencia de fármacos antiepilépticos administrados se muestra en tabla 2.
Características clínicas de los SENC tratados con LEV-VO
| Edad/sexo | Tipo SENC | Síntomas | Patrón EEG | Antecedentes de epilepsia | Causa | Etiología | Tratamiento | Refractario | Respuesta LEV | Letalidad día 30 |
| 50/M | P | Afasia | LRDA | - | TEC | S. aguda | BDZ→LEV | No | Sí | - |
| 78/F | G | Alteración de conciencia | GPD | Sí | - | Desconocida | BDZ→LEV | No | Sí | - |
| 33/M | G | Trastorno de conducta | GRDA | Sí | - | Desconocida | BDZ→LEV | No | Sí | - |
| 89/F | P | Síndrome confusional | LPD + | - | - | Desconocida | BDZ→DFH→LEV | Sí | Sí | - |
| 60/F | P | Síndrome confusional | LPDs | Sí | Tumor | S. aguda | BDZ→DFH→LEV | Sí | Sí | - |
| 56/F | P | Afasia | LRDA | - | Tumor | S. aguda | BDZ→DFH→LEV | Sí | Sí | - |
| 87/F | P | Alteración de conciencia | LPD + | - | - | Desconocida | BDZ→DFH→LEV | Sí | Sí | - |
| 25/F | G | Trastorno de conducta | GRDA | Sí | - | Desconocida | BDZ→DFH→LEV→CLZ | Sí | No | - |
| 78/F | G | Síndrome confusional | GPD | Sí | ECV | S. aguda | BDZ→DFH→LEV→VPA | Sí | No | - |
| 25/F | G | Trastorno de conducta | GRDA | Sí | Susp. FAE | S. aguda | BDZ→DFH→FB→tiopental→LEV | Sí | Sí | - |
| 47/M | P | Trastorno de conducta | LRDA | Sí | Radionecrosis | S. aguda | BDZ→DFH→FB→tiopental→LEV | Sí | No | Sí |
| 69/M | P | Coma | SI-LPD | - | Infección SNC | S. aguda | BDZ→DFH→VPA→tiopental→LEV | Sí | No | Sí |
+: componente plus; BDZ: diazepam-lorazepam; CLZ: clobazam; DFH: fenitoína; ECV: enfermedad cerebrovascular; EEG: electroencefalograma; FAE: fármacos antiepilépticos; FB: fenobarbital; G: generalizado; L: lateralizada; LEV: levetiracetam; P: parcial; PD: descargas periódicas; RDA: actividad delta rítmica; S. aguda: sintomática aguda; SENC: estatus epiléptico no convulsivo; SI: inducida por estímulo; SNC: sistema nervioso central; TEC: traumatismo encéfalocraneano; VPA: ácido valproico.
En cuanto a los pacientes que no requirieron tratamiento con anestésicos solo uno presentó como efecto adverso sedación.
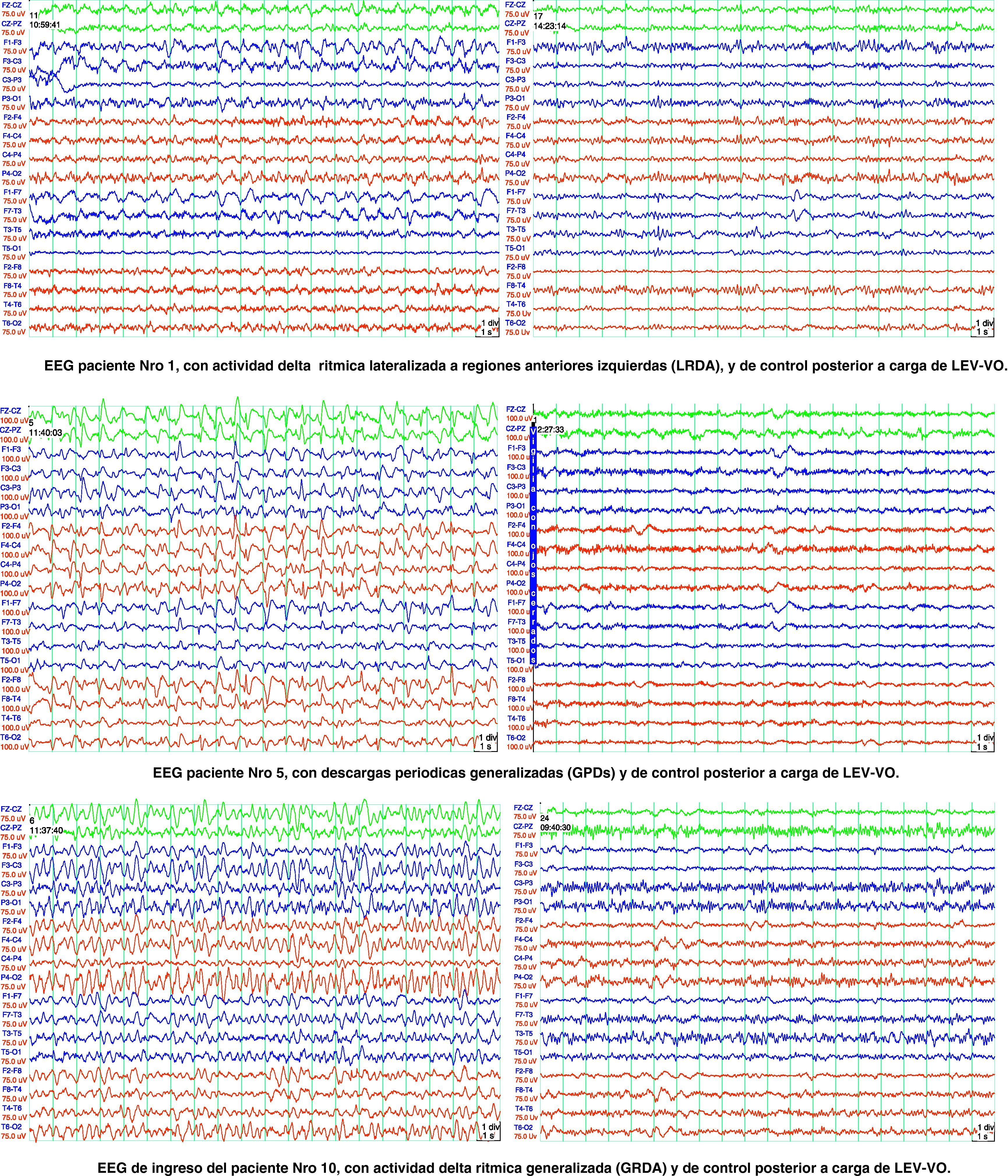
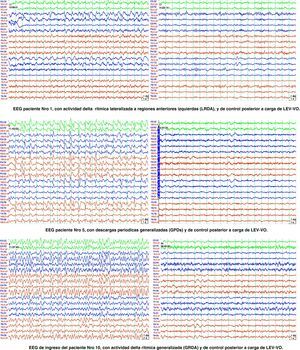
La figura 3 muestra el patrón de EEG al ingreso y posterior al tratamiento con LEV-VO de los pacientes 1, 3 y 10 correspondientes a la tabla 2.
DiscusiónExisten escasas series de casos de pacientes tratados con LEV-VO en el tratamiento del estatus. Una revisión del 2009, que incluyó 58 casos de SE tratados con LEV-VO, mostró una tasa de respuesta del 69%18. En nuestra serie la tasa de respuesta fue del 100% para los pacientes con SENC-I en los cuales LEV-VO se utilizó como fármaco después de las benzodiacepinas, similar a la reportada en otro estudio21. Al igual que en estudio de Rupprecht et al.21, no se encontraron diferencias estadísticamente significativas en cuanto a letalidad o a días de ingreso entre el grupo LEV-VO y el grupo tratamiento con fármacos convencionales.
En cuanto a efectos adversos un estudio demostró que LEV endovenoso es seguro en el tratamiento del SE, no hallando efectos adversos serios en su infusión34. Está demostrada la bioequivalencia de la administración de este fármaco cuando se administra por vía oral o endovenosa33.
El tratamiento con LEV-VO en nuestra cohorte de pacientes con SENC fue seguro y con una baja tasa de efectos adversos, incluso en población anciana. Similar perfil fue observado en una reciente publicación de pacientes con SE tratados con LEV de forma endovenosa17.
Como conclusión, el uso de LEV-VO aparece como una opción terapéutica segura, con tasas de respuesta similares a las de otros tratamientos, tanto como terapia inicial como en terapia de tercera o cuarta línea, con baja tasa de interacciones medicamentosas. Esto plantea la necesidad de futuros estudios prospectivos, controlados y aleatorizados para establecer la eficacia de este fármaco en el tratamiento del SENC.
FinanciaciónNo se recibió ningún apoyo financiero para la realización del trabajo por parte de entidades públicas o privadas.
Ninguno de los autores que subscriben está en condición de becario por parte de entidades públicas o privadas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.