El estatus epiléptico es uno de los mayores problemas en la salud pública de todo el mundo. Constituye una emergencia médica frecuente, con costes elevados para la salud y elevada morbimortalidad. El advenimiento de nuevos fármacos antiepilépticos y formulaciones farmacéuticas nos obliga a revisar permanentemente las estrategias terapéuticas.
ObjetivoActualizar las guías terapéuticas de estatus epiléptico publicadas por el Grupo de Trabajo de Epilepsia de la Sociedad Neurológica Argentina en el año 2007, con información adicional y nuevos resultados hasta la fecha, basándonos en la mejor evidencia médica disponible.
Material y métodosSe seleccionaron artículos de relevancia clínica de bases MEDLINE y Cochrane que incluyeron: estudios clínicos aleatorizados, metaanálisis, guías terapéuticas, revisiones sistemáticas, estudios no aleatorizados, de casos y opiniones de expertos.
ResultadosSe establecieron y seleccionaron aquellos fármacos más eficaces para crisis que perduran más allá de los 5 minutos. Se determinó el tratamiento específico según etapas: prehospitalaria, hospitalaria y en terapia intensiva. Se tuvieron en cuenta los estadios evolutivos, la respuesta clínica y la necesidad de monitorización electroencefalográfica en instancias avanzadas.
ConclusiónSeguimos recomendando iniciar la terapéutica en toda crisis que se extienda más allá de los 5 minutos.
Aún no contamos con la evidencia suficiente que nos permita recomendar fuertemente un fármaco anestésico para el tratamiento del estatus refractario, así como tampoco para establecer el tiempo óptimo de duración del mismo. la monitorización electroencefalográfica continua es necesaria para un mejor manejo terapéutico del estatus epiléptico en etapas avanzadas. La mayor disponibilidad de la electroencefalografía permitirá detectar casos de estatus no convulsivos en los cuales las manifestaciones clínicas de crisis no son evidentes.
Status epilepticus is a major public health problem along the world. It represents a frequently medical emergency with elevated costs and high morbimortality. The prognosis depends on the duration and the phase in which the appropriate treatment is, age, ethiology, comorbidities and complications.
ObjetivesTo establish therapeutic guidelines for those physicians who treat status epilepticus according to medical evidence available to date.
To update the previous guidelines published in 2007 with additional information and new results.
Material and methodsWe selected articles of clinical relevance from databases MEDLINE and Cochrane.
Randomized clinical trials, meta - analyses, therapeutic guidelines, systematic reviews, cases series and experts opinions were included.
ResultsAfter an individualized assessment of different drugs useful for treatment of status epilepticus, we selected those more efficacious for seizures lasting more than 5minutes. After the analysis, we designed an algorithm according to time of evolution, clinical response and electroencephalography monitoring.
ConclusionConsensus has emerged concerning initial treatment of status epilepticus. For practical purposes treatment should be started after 5minutes of continuous seizure activity. Treatment of refractory status was established according to the evidence available but the are not enough randomized trials that compare different therapeutic agents for this instance. Continuous EEG monitoring is needed for better management of status epilepticus in advance stages. The alarming high mortality rate of status epilepticus emphasizes the need of an high suspicion index with rapid recognition and urgent treatment.
El estatus epiléptico (SE) es uno de los mayores problemas en la salud pública de todo el mundo. Las cifras de incidencia y prevalencia no son fáciles de precisar. La realización de estudios epidemiológicos presenta una serie de dificultades metodológicas que explican la disparidad de los datos y resultados existentes entre las diferentes publicaciones. El SE representa aproximadamente el 3,5% de los ingresos a las Unidades de Terapia Intensiva (UTI) y hasta el 15% de los pacientes internados en Servicios de Neurología. La tasa de incidencia anual del SE basada en diferentes estudios realizados en Europa y Estados Unidos varía de 6,2 a 41 por 100.000, incrementándose hasta 15,1 a 86 por 100.000 en adultos mayores, que constituyen junto con los niños menores de 5 años la población de mayor riesgo de incidencia1–4. En la Argentina, un estudio basado en población cautiva de adultos, mostró una incidencia ajustada anual de SE: fue de 24,3/100.000 habitantes año5.
El pronóstico varía respecto de la causa del SE. El SE originado como consecuencia de los niveles plasmáticos bajos de fármacos antiepilépticos (FAE) y el abuso de alcohol tiene un buen pronóstico, con una mortalidad reportada en series de casos menor al 10%, en relación con los SE debidos a las alteraciones metabólicas, la enfermedad cerebrovascular y en particular la anoxia/hipoxia, que se asocian a peor evolución6.
La mortalidad a largo plazo aumenta en los casos de etiología sintomática aguda con respecto de los casos de SE idiopáticos o criptogénicos, y el riesgo de déficits neurológicos después de sufrir un SE es más alto en los casos de SE de etiología aguda sintomática o causados por patología neurológica progresiva, comparado con el SE de causa idiopática/criptogénica o con los casos de SE febril7.
Esta revisión se va a concentrar en actualizar aspectos clínicos y terapéuticos en función de recomendaciones basadas en consensos y evidencia médica disponible. Se actualizaran las guías publicadas por nuestro grupo en el año 2007, con la inclusión y agregado de información de relevancia hasta la fecha.
ObjetivoOrientar a los profesionales en la toma de decisiones clínicas y elección de estrategias terapéuticas para el mejor manejo del SE según los siguientes tópicos a analizar:
- 1.
Fármacos más eficaces en las diferentes etapas del SE.
- 2.
Complicaciones asociadas a la administración de FAE utilizados para el tratamiento del SE.
- 3.
Diferencias de eficacia y tolerabilidad entre los distintos fármacos.
- 4.
Actualización de la guía previa realizada por este grupo en el año 2007.
Medline. Palabras clave: Status epilepticus, estudios clínicos aleatorizados, metaanálisis, revisiones sistemáticas, estudios no aleatorizados, estudios de casos y opinión de expertos.
Cochrane. Estudios clínicos aleatorizados.
1++: metaanálisis de gran calidad, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con muy bajo riesgo de sesgos.
1+: metaanálisis de gran calidad, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con bajo riesgo de sesgos.
1-: metaanálisis de gran calidad, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con alto riesgo de sesgos.
2++: revisiones sistemáticas de alta calidad de estudios de cohortes o de casos-controles, o estudios de cohortes o de casos-controles de alta calidad, con muy bajo riesgo de confusión, sesgos o azar y una alta probabilidad de que la relación sea causal.
2+: estudios de cohortes o de casos-controles bien realizados, con bajo riesgo de confusión, sesgos o azar y una moderada probabilidad de que la relación sea causal.
2-: estudios de cohortes o de casos y controles con alto riesgo de sesgo.
3: estudios no analíticos, como informe de casos y series de casos.
4: opinión de expertos8,9.
A: al menos un metaanálisis, revisión sistemática o ensayo clínico aleatorizado calificado como 1++ y directamente aplicable a la población objeto, o una revisión sistemática de ensayos clínicos aleatorizados o un cuerpo de evidencia consistente principalmente en estudios calificados como 1+, directamente aplicables a la población objeto y que demuestren globalmente consistencia de los resultados.
B: un volumen de evidencia que incluya estudios calificados como 2++ directamente aplicables a la población objeto y que demuestren globalmente consistencia de los resultados, o extrapolación de estudios calificados como 1++ o 1+.
C: un volumen de evidencia que incluya estudios calificados como 2+ directamente aplicables a la población objeto y que demuestren globalmente consistencia de los resultados, o extrapolación de estudios calificados como 2++.
D: Niveles de evidencia 3 o 4, o evidencia extrapolada desde estudios clasificados como 2+.
El grupo de trabajo sobre SE de la Epilepsy Foundation of America (EFA) y la Liga Internacional contra la Epilepsia describen al SE como a la persistencia de actividad ictal continua de 30 minutos o más, o 2 o más crisis sin recuperación total de la conciencia entre ellas10–13. Lowenstein et al. proponen una definición operativa para el SE generalizado convulsivo de 5 minutos, tiempo en el cual la crisis debiera ser interrumpida para evitar mayor morbimortalidad y que derive en un SE refractario14.
Estatus epiléptico refractarioPara definir SE refractario (SER) se suelen utilizar conceptos temporales y/o farmacológicos. Este último permite en la práctica un manejo más concreto para la instauración del tratamiento establecido para dicha etapa, y la mayoría de los expertos ya no consideran el criterio temporal para la clasificación de SER15.
Las definiciones de SER incluyen crisis que persistan por más de 60 a 90 minutos después de iniciada la terapia (concepto temporal), o tras el tratamiento adecuado con benzodiazepinas más una dosis adecuada de fármacos de segunda línea (concepto farmacológico)16,17.El SE súper refractario (SESR) se define como aquel que continúa o se repite 24 horas o más después del inicio del tratamiento anestésico, incluidos los casos en que reaparece el SE en la disminución o suspensión de la anestesia. El término SESR fue usado por primera vez durante el iii coloquio sobre Estatus Epiléptico llevado a cabo en Inglaterra durante el año 2011. No es infrecuente encontrar esta entidad en la Unidad de Terapia Intensiva, pero se desconoce concretamente su frecuencia; alrededor del 15% de los SER evolucionan a SESR. Es una emergencia neurológica con alta morbimortalidad18,19. Recomendamos que en la práctica se considere SE si la crisis persiste por más de 5 minutos. Solo un bajo porcentaje de crisis que se van a autolimitar se extienden más allá de este lapso de tiempo, y sugerimos utilizar el concepto farmacológico para la consideración del SE como refractario.
Clasificación del estatus epilépticoAún no hay consenso general sobre una clasificación sistematizada del SE, y desde lo teórico habría tantos tipos distintos de SE como tipos de crisis epilépticas (tabla 1)20. Sin embargo, sería de mucha utilidad contar con una clasificación para un mejor y adecuado manejo terapéutico, dado que el pronóstico varía según los distintos tipos de SE.
Clasificación del estatus epiléptico según Gastaut
| I- Convulsivo |
| Generalizado: |
| Tónico-clónico |
| Tónico |
| Clónico |
| Mioclónico |
| Parcial: |
| Simple motor |
| Afásico |
| Epilepsia parcial continua |
| II- No convulsivo |
| Generalizado: estatus de ausencia |
| Parcial complejo, simple sensitivo |
Fuente: Gastaut20.
Por lo tanto, a la hora de clasificar el SE recomendamos considerar:
- 1.
Si es convulsivo o no convulsivo (SENC): basándose en la presencia o no de elementos clínico-semiológicos evidentes o sutiles respectivamente.
El SE convulsivo en general es de fácil reconocimiento.
El SENC requiere de un mayor índice de sospecha y ocurre en situaciones clínicas como: pacientes con ruptura de contacto y/o síndromes confusionales inespecíficos (estos suelen presentar mejores resultados terapéuticos) y otra como pacientes en coma, gravemente comprometidos cuyo pronóstico es desalentador21–23.
- 2.
Si es parcial o generalizado: será parcial complejo o parcial simple según haya o no ruptura de contacto con el medio respectivamente.
En caso de SE generalizados el diagnóstico diferencial más importante y con connotaciones terapéuticas será entre los SE generalizados convulsivos (por ejemplo tónico-clónicos) y el SE de ausencia.
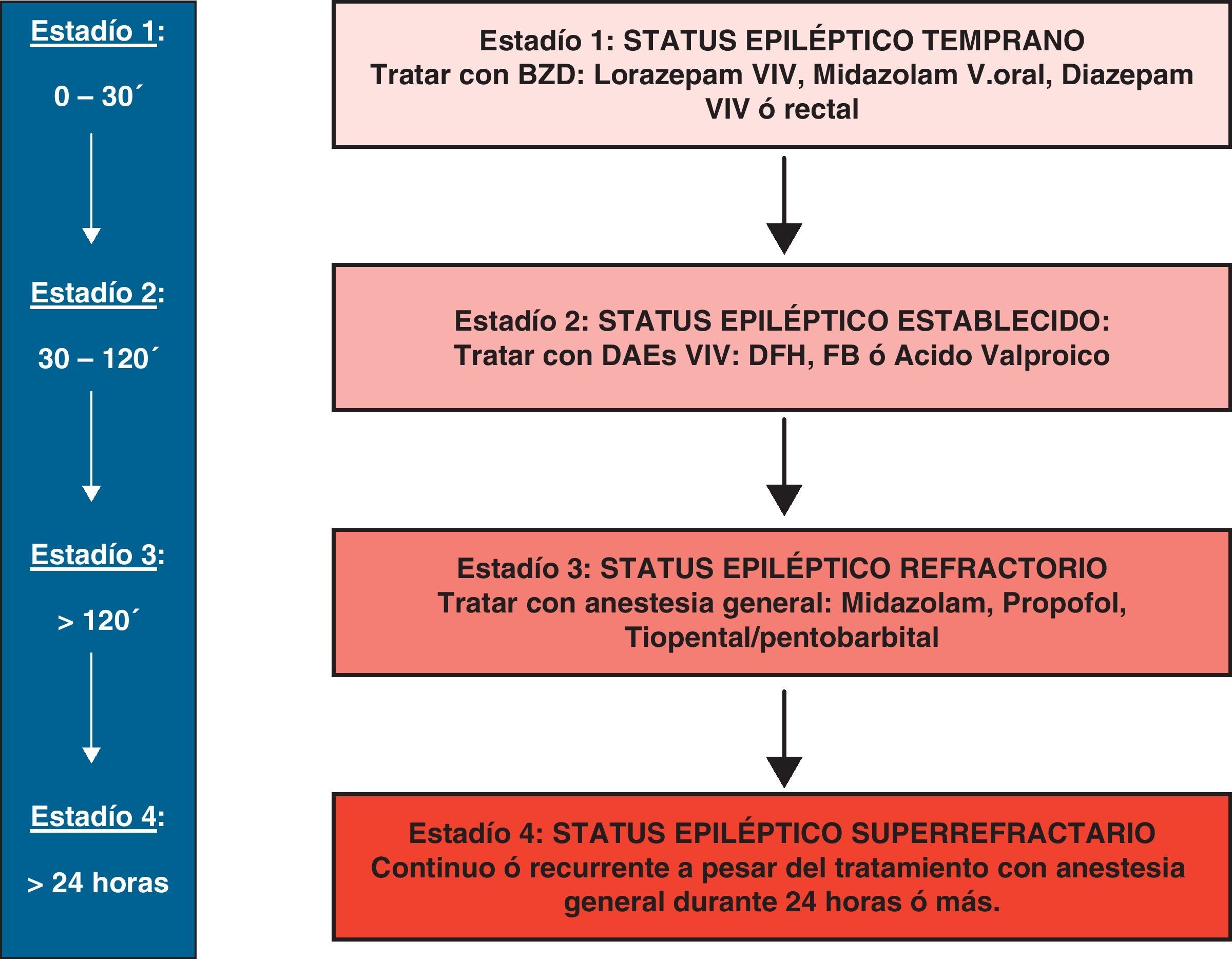
Etapa prehospitalaria24,25: lorazepam intravenoso (IV) (grado de recomendación A), diazepam IV (grado de recomendación A), midazolam intramuscular (IM) (grado de recomendación A)
Etapas del tratamiento del SE. Si el tratamiento en el estadio 1 no es efectivo después de los primeros 30 minutos se pasa al tratamiento de la etapa 2, y si a las 2 h es inefectivo, se pasa al estadio 3, cuyo tratamiento se basa en la administración de anestesia general. El SE que no responde a esta etapa o recurre transcurridas 24 horas de iniciado el tratamiento anestésico se lo considera SE súper refractario.
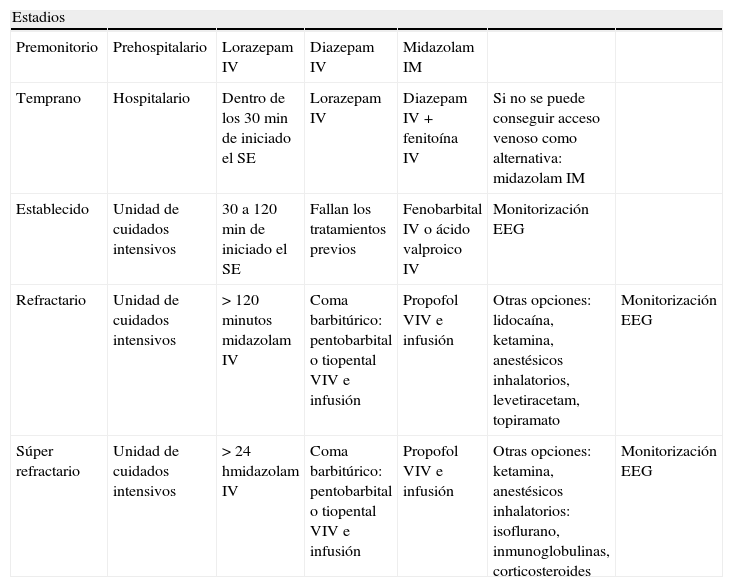
Pautas de tratamiento según los estadios del estatus epiléptico
| Estadios | ||||||
| Premonitorio | Prehospitalario | Lorazepam IV | Diazepam IV | Midazolam IM | ||
| Temprano | Hospitalario | Dentro de los 30 min de iniciado el SE | Lorazepam IV | Diazepam IV + fenitoína IV | Si no se puede conseguir acceso venoso como alternativa: midazolam IM | |
| Establecido | Unidad de cuidados intensivos | 30 a 120 min de iniciado el SE | Fallan los tratamientos previos | Fenobarbital IV o ácido valproico IV | Monitorización EEG | |
| Refractario | Unidad de cuidados intensivos | >120 minutos midazolam IV | Coma barbitúrico: pentobarbital o tiopental VIV e infusión | Propofol VIV e infusión | Otras opciones: lidocaína, ketamina, anestésicos inhalatorios, levetiracetam, topiramato | Monitorización EEG |
| Súper refractario | Unidad de cuidados intensivos | >24 hmidazolam IV | Coma barbitúrico: pentobarbital o tiopental VIV e infusión | Propofol VIV e infusión | Otras opciones: ketamina, anestésicos inhalatorios: isoflurano, inmunoglobulinas, corticosteroides | Monitorización EEG |
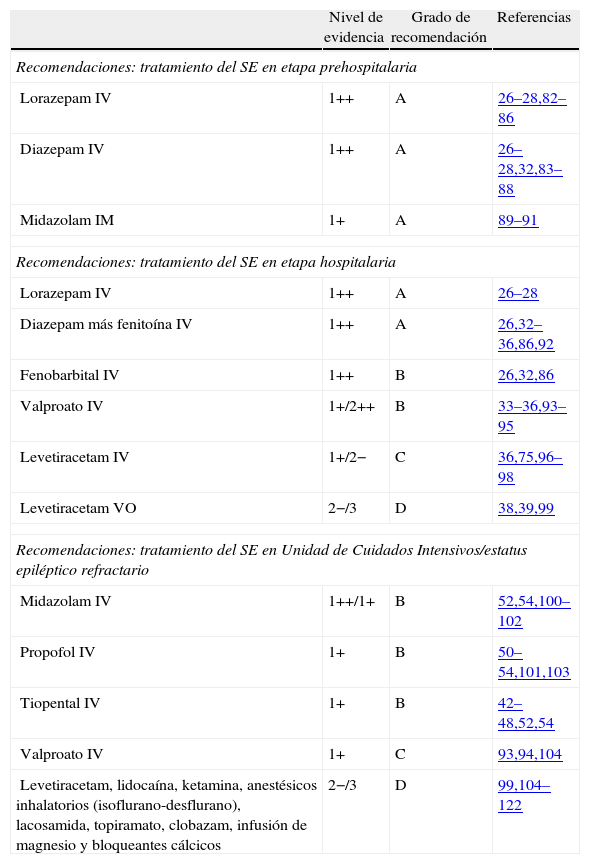
Resumen de niveles de evidencia y grados de recomendaciones de las distintas etapas del estatus epiléptico
| Nivel de evidencia | Grado de recomendación | Referencias | |
| Recomendaciones: tratamiento del SE en etapa prehospitalaria | |||
| Lorazepam IV | 1++ | A | 26–28,82–86 |
| Diazepam IV | 1++ | A | 26–28,32,83–88 |
| Midazolam IM | 1+ | A | 89–91 |
| Recomendaciones: tratamiento del SE en etapa hospitalaria | |||
| Lorazepam IV | 1++ | A | 26–28 |
| Diazepam más fenitoína IV | 1++ | A | 26,32–36,86,92 |
| Fenobarbital IV | 1++ | B | 26,32,86 |
| Valproato IV | 1+/2++ | B | 33–36,93–95 |
| Levetiracetam IV | 1+/2− | C | 36,75,96–98 |
| Levetiracetam VO | 2−/3 | D | 38,39,99 |
| Recomendaciones: tratamiento del SE en Unidad de Cuidados Intensivos/estatus epiléptico refractario | |||
| Midazolam IV | 1++/1+ | B | 52,54,100–102 |
| Propofol IV | 1+ | B | 50–54,101,103 |
| Tiopental IV | 1+ | B | 42–48,52,54 |
| Valproato IV | 1+ | C | 93,94,104 |
| Levetiracetam, lidocaína, ketamina, anestésicos inhalatorios (isoflurano-desflurano), lacosamida, topiramato, clobazam, infusión de magnesio y bloqueantes cálcicos | 2−/3 | D | 99,104–122 |
Etapa hospitalaria (dentro de los 30 minutos de iniciada la crisis)26–28: lorazepam IV (grado de recomendación A), diazepam más fenitoína IV (grado de recomendación A), fenobarbital IV (grado de recomendación B), valproato IV (grado de recomendación B), levetiracetam IV (grado de recomendación C).
Las líneas de tratamiento descriptas han sido establecidas como eficaces para controlar crisis con duración mayor a 5 minutos en adulto.
Etapa en la Unidad de Cuidados Intensivos (más de 30 minutos de iniciada la crisis)/SE refractario29: midazolam IV (grado de recomendación B), tiopental (o su metabolito pentobarbital) IV (grado de recomendación B), propofol IV (grado de recomendación B).
Otras opciones terapéuticas: valproato (grado de recomendación C), lidocaína (grado de recomendación D), ketamina (grado de recomendación D), anestésicos inhalatorios (isoflurano-desflurano) (grado de recomendación D), levetiracetam (grado de recomendación D), lacosamida (grado de recomendación D), otros FAE: carbamazepina, topiromato, clobazam (grado de recomendación D), infusión de magnesio (grado de recomendación D), bloqueantes cálcicos (grado de recomendación D).
Alternativas no farmacológicas para el tratamiento del SE refractario (grado D): dieta cetogénica, tratamientos inmunológicos (corticoides, inmunoterapia), hipotermia, terapias de estimulación eléctrica y magnética (estimulación vagal, terapia electroconvulsiva, estimulación magnética transcraneana [TMS], estimulación cerebral profunda [DBS]), cirugías resectivas.
Estatus epiléptico refractarioEl SE refractario tiene una mortalidad 3 veces mayor que el SENR. Existe poca evidencia respecto a la elección del fármaco anestésico para su tratamiento. Los 3 fármacos más usados son el tiopental sódico, el midazolam y el propofol. No existen estudios aleatorizados que comparen distintos agentes terapéuticos, así como tampoco la duración del tratamiento. La anestesia debería mantenerse por el mínimo período necesario para lograr el control del SE más allá del fármaco elegido30.
El VPA y el levetiracetam son alternativas potencialmente tanto efectivas como seguras, pero hay limitados datos comparativos. En varios trabajos realizados fueron de utilidad sobre todo en pacientes añosos con múltiples patologías concomitantes en estatus no convulsivos y refractarios. En casos de pacientes que poseían alguna contraindicación, o riesgo elevado de recibir la terapia convencional, fueron administrados de forma temprana con buenos resultados.
Si bien no existen hasta la fecha estudios aleatorizados que comparen diferentes estrategias terapéuticas para el tratamiento de SE refractario, hay resultados promisorios con fármacos no anestésicos utilizados de forma temprana, como es el caso del VPA, levetiracetam y posiblemente la lacosamida.
En casos de estatus de ausencia pueden considerarse el VPA y posiblemente el levetiracetam como de primera línea.
Con respecto al pronóstico del SE refractario y SESR, a pesar de que el SE de larga duración implica generalmente un mal pronóstico, existen algunas excepciones, y pacientes con SE refractario de varios días, semanas e incluso meses de duración pueden en ocasiones alcanzar una buena recuperación funcional. De este modo, el tratamiento de soporte (incluyendo repetidos ciclos de anestésicos de ser necesario) no debería ser interrumpido simplemente por la duración prolongada del cuadro, de no existir causa subyacente que augure de cualquier manera un pronóstico catastrófico o evidencia de daño cerebral irreversible. Esta conducta se aplica especialmente a pacientes jóvenes, quienes presentan una mejor tolerancia a los efectos secundarios cardiovasculares de la anestesia prolongada31.
Complicaciones asociadas con el tratamiento de crisis que duran más de 5 minutosLa depresión respiratoria es más frecuente en pacientes con crisis persistentes que en pacientes que recibieron benzodiazepinas por dichas crisis26. Por lo tanto, el no tratar acarrearía mayor riesgo de compromiso respiratorio. No hay diferencias entre lorazepam, diazepam, fenitoína o fenobarbital en la incidencia de reacciones adversas respiratorias o cardíacas26.
Diferencias en eficacia y tolerabilidadDiazepam vs. lorazepamLeppik et al.28 compararon lorazepam (4mg) vs. diazepam (10mg) IV como fármacos de primera línea para el tratamiento del SE en un trabajo aleatorizado doble ciego.
No hubo diferencias significativas en la eficacia. Las crisis fueron controladas en el 76% de los episodios en pacientes que recibieron diazepam, y en el 89% de los episodios de pacientes que recibieron lorazepam. No hubo diferencias significativas en la latencia para el comienzo de acción.
En otro estudio prehospitalario el SE fue controlado a la llegada a la sala de emergencias en más pacientes tratados con lorazepam (59,1%) que con diazepam (42,6%) y menos con placebo (21,1%)26.
Se concluye que ambos fármacos son aceptados como de primera línea para el tratamiento del SE prefiriéndose el lorazepam (grado A)17.
El estudio cooperativo de veteranos comparó la respuesta a 4 tratamientos diferentes en 384 pacientes con SE evidente y 134 pacientes con SE sutil26. Las 4 ramas de tratamiento fueron: diazepam 0,15mg/kg más fenitoína 18mg/kg, lorazepam 0,1mg/kg, fenobarbital 15mg/kg o fenitoína 18mg/kg.
Para el SE evidente la mayor respuesta fue para el lorazepam (64,9%), seguida de fenobarbital (58,2%), diazepam más fenitoína (55,8%) y luego monoterapia con fenitoína (43,6%)27. El SE sutil o no convulsivo tuvo una respuesta menor en todas las líneas de tratamiento: fenobarbital 24,2%, lorazepam 17,9%, diazepam más fenitoína 8,3% y monoterapia con fenitoína 7,7%.
Las diferencias no fueron estadísticamente significativas entre los distintos tratamientos, tanto para el SE evidente como sutil. Tampoco hubo diferencias con respecto a la recurrencia o a la incidencia de eventos adversos.
Diferencias entre lorazepam y diazepam en adultos con crisis de duración mayor a 5 minutos: en adultos no hay diferencias entre lorazepam y diazepam en eficacia y tolerabilidad (grado A); lorazepam tiene mayor duración de acción (grado D)26–28, en adultos la fenitoína intravenosa está más frecuentemente asociada con irritación venosa y flebitis26,28,32.
Fenitoína vs. ácido valproicoMisra et al. realizaron un estudio aleatorizado controlado para comparar la eficacia de ácido valproico (VPA) y de fenitoína (PHT) como fármacos de primera y de segunda línea en el tratamiento del SE convulsivo33. Con un total de 68 pacientes, 35 recibieron VPA y 33 PHT. Los resultados fueron control de las crisis en el 66% de los pacientes tratados con VPA y en el 42% de los pacientes tratados con PHT, cuando recibieron VPA o PHT como tratamiento inicial. En aquellos pacientes que fallaron al primer esquema recibido, en el 79% se logró posteriormente el control del SE usando VPA como segunda opción (pacientes que habían fallado al tratamiento inicial con PHT), mientras que el porcentaje de pacientes que fallaron al VPA como fármaco de inicio, pero respondieron a PHT como segunda opción, fue solo del 25%. La eficacia y tolerabilidad de VPA y PHT en el SE se evaluó también de forma comparativa en los estudios de Agarwal et al.34 y de Gilad et al.35. El primero de ellos compara VPA y PHT en SE refractario al tratamiento inicial con benzodiacepinas (diazepam IV), y el segundo trabajo los compara como fármacos de inicio. El trabajo de Agarwal, un estudio aleatorizado con 50 pacientes en cada rama, obtuvo control del SE en el 88% de los pacientes tratados con VPA y en el 84% de los pacientes tratados con PHT. La tolerabilidad al fármaco fue similar en ambos grupos.
El trabajo de Gilad fue un estudio retrospectivo en el cual se analizaron 49 pacientes que recibieron VPA y 25 pacientes que recibieron PHT como fármaco de inicio, por SE o por crisis agudas repetitivas. Los resultados mostraron una eficacia similar de ambos fármacos para el control de la crisis (87,8% para VPA y 88% para PHT), con tolerabilidad similar. Se concluye que VPA y PHT tienen una eficacia y tolerabilidad similar en el tratamiento del SE (grado B).
Fenitoína vs. levetiracetamEl trabajo de Alvarez et al.36 fue el primero en comparar la eficacia de levetiracetam (LEV) en SE con respecto a otro fármaco. Se analizaron de forma retrospectiva datos que se obtuvieron en un registro prospectivo, para comparar la eficacia de VPA, PHT y LEV en SE como fármacos de segunda línea en pacientes que habían fallado al tratamiento inicial con benzodiacepinas. Evaluaron 198 episodios de SE en 167 pacientes que habían requerido fármacos de segunda línea para el control del SE, tras haber fallado al tratamiento inicial con clonazepam IV o lorazepam IV. Setenta episodios de SE (37%) fueron tratados con PHT, 59 episodios (32%) con VPA y 58 episodios (31%) con LEV. Los resultados (tras un análisis ajustado a la severidad y a la etiología del SE) mostraron que un 16,8% de los casos que fallaron al tratamiento de segunda línea con LEV hubieran podido controlarse utilizando VPA; la eficacia de la PHT como tratamiento de segunda línea fue mayor a la de LEV, pero menor que la de VPA. Pese a las limitaciones metodológicas del estudio, es el primero en comparar la eficacia de LEV en SE con respecto a otro fármaco, y sus resultados sugieren precaución con el uso de LEV en el SE, al tiempo que señala la necesidad de un estudio comparativo bien diseñado. Se concluye que como fármaco de segunda línea tras el fracaso del tratamiento del SE con benzodiacepinas, LEV tiene menor eficacia que PHT (grado C).
Protocolo de tratamiento sugerido de estatus epilépticoA través de varios estudios controlados se ha investigado y establecido la primera línea de tratamiento por niveles de evidencia; sin embargo, las etapas de tratamiento posteriores siguen siendo controvertidas, ya que hasta la fecha no hay registro de ningún estudio clase i que avale estas terapéuticas.
Etapa prehospitalaria. Lorazepam: 2mg IV o diazepam: 5mg IV o midazolam: 5-10mg IM.
Si las crisis persisten por más de 4 minutos se pueden repetir las dosis.
Etapa hospitalaria. Mantenimiento de la circulación y oxigenoterapia; acceso venoso; determinar la etiología; laboratorio; importancia de contar con registro electroencefalográfico (ECG); inicio de tratamiento.
Minuto 0. Mantenimiento de la vía aérea: respiración (oxígeno nasal, tubo de mayo, ARM), soporte hemodinámico (monitorización ECG, control de presión arterial y temperatura); obtener historia; examen neurológico; acceso venoso: solución salina isotónica; administrar 100mg de tiamina más suero glucosado hipertónico: deberán realizarse controles de glucemia periódicos mientras persistan las crisis, ya que hay una tendencia a la hiperglucemia en esta fase inicial del estatus, pero posteriormente, puede haber una tendencia a la hipoglucemia que debe ser corregida; extracción sanguínea y orina: hemograma, urea, glucemia, electrolitos, creatinina, hepatograma, calcio, fósforo, magnesio, gases arteriales, tóxicos; toma de muestra para dosificación de niveles séricos de FAE en pacientes que vienen medicados con dichos fármacos, cuando se sospechan interacciones farmacodinámicas o cinéticas relevantes, pacientes embarazadas o con patología concomitante que interfiera con los FAE (por ejemplo insuficiencia hepática, insuficiencia renal); el EEG permite confirmar la naturaleza epiléptica de las crisis (diagnóstico de estatus convulsivos y no convulsivos) y evaluación de la respuesta al tratamiento antiepiléptico; estudios por imágenes (TC y/o resonancia magnética): su indicación quedará supeditada a las potenciales causas que llevaron al paciente al estatus.
Si al cabo de 5 minutos la crisis persiste iniciar tratamiento con: a) lorazepam: 0,1-0,15mg/kg IV, con una velocidad de infusión de 1-2mg/minuto; ob) diazepam: 0,2-0,3mg/kg IV con una velocidad de infusión de 2-5mg/minuto + PHT: dosis de carga 20mg/kg IV con una velocidad de infusión de 50mg/minuto.
Se recomienda realizar la infusión con monitorización ECG continuo y control de presión arterial (por la posibilidad de desarrollo de arritmias y/o hipotensión o hipertensión).
Otras opciones previo al inicio del tratamiento anestésico: a)fenobarbital 10-20mg/kg diluido en suero fisiológico o dextrosa 5% a pasar 100mg/min (1.000mg en 15 min); b) o ácido valproico: 25-30mg/kg IV: velocidad de infusión aprobado hasta 3mg/kg/min. Probablemente seguro hasta 5-6mg/kg/min. Esta opción puede considerarse en especial en casos de estatus no convulsivos; o c) LEV: 20-60mg/kg IV: velocidad de infusión 15 a 60 min (2-5mg/kg/min). Se han realizado estudios con infusiones más rápidas, de hasta 5 minutos con buena tolerabilidad. Una opción con bioequivalencia similar a la formulación IV es la preparación oral (VO), siendo esta última mejor tolerada a mayores dosis y velocidad de infusión37. Los datos muestran similar eficacia38,39; d) lacosamida: 50-200mg IV cada 15 minutos o velocidad de infusión 40-80mg/min. Mantenimiento 400-600mg/día40,41.
Etapa en Unidad de Cuidados Intensivos/SE refractario42–54: tubo endotraqueal; sondaje vesical; control de presión arterial y temperatura, si transcurridos 30 minutos desde el inicio de la actividad epiléptica no se ha conseguido controlar las crisis se debe considerar el ingreso en terapia intensiva; es recomendable que la infusión de fenobarbital ya se realice en terapia intensiva.
Cuarenta-60 minutos: midazolam (dosis de carga: 0,2mg/kg IV). Mantenimiento: 0,2-0,6 mg/kg/hora o o propofol (dosis de carga 1-2mg/kg IV). Mantenimiento: 2-4mg/kg/hora (hasta 15mg/kg/hora) o coma barbitúrico: pentobarbital (dosis de carga 5-20mg/kg IV). Mantenimiento: 1-3mg/kg/hora,precaución: depresión miocárdica y edema pulmonar o tiopental: 100-250mg en 2 min IV, añadiendo bolos de 50mg cada 2-3 min hasta el control de las crisis o patrón brote supresión. Mantenimiento: 3-5mg/kg/hora.
Monitorización electroencefalográfica continuaEl control electroencefalográfico es imprescindible para evaluar el nivel de inducción del coma, como para descartar la presencia de crisis no convulsivas o status no convulsivos en pacientes en coma55–60. El grado óptimo de supresión electroencefalográfica de la actividad cerebral (supresión de crisis, patrón de paroxismo-supresión, o registro plano) no ha sido evaluado en estudios prospectivos, y los estudios retrospectivos no favorecen claramente ninguna de estas opciones. La misma incertidumbre se aplica a la duración del tratamiento anestésico y al esquema de suspensión del fármaco31. Dependiendo del anestésico utilizado, se recomienda la titulación hasta un patrón EEG de paroxismo-supresión con propofol y barbitúricos. Si se administra midazolam la supresión de las crisis eléctricas es el objetivo recomendado44,52,61,62.
La referencia básica es el trazado llamado paroxismo supresión, que se define por la presencia de períodos entre 2 a 10 segundos de actividad de fondo plana o casi plana, menor a 5μV, interrumpidos por una actividad irregular de ondas lentas y punta onda de gran voltaje, de pocos segundos de duración44,52,62. La supresión dura aproximadamente 5 seg y los brotes incluyen una irregular y amplia variedad de formas de espigas, ondas agudas y ondas lentas. La infusión se continúa durante 4 horas, luego se desciende la velocidad y se monitoriza con el EEG. Si la actividad epileptiforme aún persiste se repite el procedimiento durante otras 4 h. Si no, se suspende el fármaco en 12-24 h gradualmente52,63,64. La duración óptima del control electroencefalográfico de las crisis en pacientes con SE refractario es desconocida, debido a la poca información respecto a cuál sería la duración del tratamiento necesaria para mantener dicho control. Habitualmente, el control de las crisis se mantiene por 24-48 h, seguido de un descenso gradual de la infusión continua de antiepilépticos. Los pacientes pueden presentar recurrencia del SE refractario con el descenso de la infusión continua, requiriendo retornar a igual o mayor dosis del antiepiléptico en infusión continua por un período de tiempo adicional, con o sin el agregado de otro agente terapéutico15.
Estatus epiléptico no convulsivoEl SENC se define como cambios conductuales y/o compromiso de conciencia respecto al estado basal, asociado a actividad epiléptica continua en el EEG de 30min o más de duración, generalizada o focal65. Para definir actividad epiléptica continua en el EEG se usaron los criterios de Young modificados66. Está claro que aún no existe una definición universal del SENC, si bien lo descrito anteriormente beneficia al diagnóstico, una respuesta electroclínica positiva al tratamiento agudo con FAE puede ayudar al proceso diagnóstico, aunque la falta de respuesta no lo excluye.
En relación con el SE sutil, se trata de una forma del SENC que involucra desde el estado de mal convulsivo generalizado que ha sido tratado de forma insuficiente o no ha sido tratado y la principal característica es «estado de coma y ausencia de signos motores»; sin embargo, puede haber alguna sacudida, con descargas del EEG periódicas generalizadas o lateralizadas y regionales. Es así que algunos autores prefieren definir al SE sutil como aquel que presenta cambios en el EEG pero con evidencia de crisis epilépticas previas o estado de mal previo67.
Tratamiento del estatus epiléptico no convulsivoEn la actualidad no existe ninguna guía o consenso de tratamiento para el SENC, debido a la falta de estudios y datos de eficacia. En la actualidad la mayor parte de la información disponible proviene de estudios retrospectivos y series de casos. Tampoco se han realizado ensayos clínicos controlados y aleatorizados, diseñados específicamente que evalúen este tipo de situación, por lo que se utilizan las mismas recomendaciones indicadas para el SE convulsivo en relación con el protocolo de tratamiento, pero con un nivel de evidencia bajo (grado de recomendación D)68–72.
Consideraciones en el adulto mayor y otras poblaciones especialesEn el anciano el diagnóstico puede ser difícil por sus varias formas de aparición clínica73. El SE parcial complejo es la forma más común de presentación, con confusión, alteración del estado de conciencia o síntomas psiquiátricos. Los factores de riesgo son: accidentes cerebrovasculares, epilepsia, demencia, neoplasias del SNC y alteraciones metabólicas sistémicas. Las múltiples comorbilidades de este grupo etario pueden complicar el tratamiento y empeorar el pronóstico. El uso de PHT, fenobarbital y anestésicos en el anciano está asociado a mayor riesgo de complicaciones cardiovasculares, respiratorias y las interacciones con otros fármacos es elevada. En esta población la utilización de valproato y LEV puede ser una alternativa terapéutica74–76.
Estatus epilépico en insuficiencia hepáticaLa incidencia de crisis en pacientes con hepatopatías es del 2 al 33%77. Sin embargo, los reportes de SENC son aislados78. El SENC podría ser una manifestación común dentro del cuadro de encefalopatía hepática. No hay estudios que definan el tratamiento y pronóstico del SE en esta población.
El manejo farmacológico es complejo. Puede haber niveles elevados de FAE por la alteración de la metabolización (reducción de la enzima citocromo P450, alteración de la glucuronización) y por hipoalbuminemia. Se sugiere utilizar FAE sin metabolismo hepático y escasa unión a proteínas plasmáticas, como el LEV.
Estatus epiléptico en insuficiencia renalLas crisis son frecuentes en pacientes con fallo renal agudo y encefalopatía urémica, que suele asociarse a otras alteraciones metabólicas. La incidencia de crisis en pacientes en hemodiálisis por fallo renal es del 2 al 10%79. Los fármacos con alta unión a proteínas (PHT, VPA) no son afectados por la diálisis. El LEV sufre una reducción del 50% posdiálisis, por lo que se debe ajustar la dosis80,81.
Recomendaciones generales- 1.
Considerar diagnósticos diferenciales con eventos no epilépticos de origen psiquiátrico, migraña, amnesia global transitoria, encefalopatía metabólica o tóxica.
- 2.
Utilizar dosis adecuadas según kg de peso y garantizar un correcto acceso intravenoso.
- 3.
Estar preparado para asistencia respiratoria inminente.
- 4.
Determinar y tratar la etiología del SE.
- 5.
Tratar las complicaciones del SE a la mayor brevedad.
- 6.
Recordar que cuanto más se prolongue el SE mayor es la posibilidad de evolucionar hacia la refractariedad.
- 7.
Considerar la evolución hacia un SE no convulsivo en: pacientes con deterioro de sensorio y/o alteración de la conciencia prolongada, automatismos, mioclonías sutiles, trastorno del lenguaje persistente, movimientos oculares involuntarios.
- 8.
Individualizar casos que requieran terapia crónica con FAE.
El SE es una emergencia neurológica frecuente cuyo diagnóstico temprano y rápido inicio del tratamiento son tan importantes como la elección del fármaco a utilizar.
Continuamos recomendando la terapéutica agresiva, al menos en las primeras instancias terapéuticas, e iniciar el tratamiento según el protocolo sugerido en toda crisis que se extienda más allá de los 5 minutos.
La evidencia clínica en los últimos años nos brindó información acerca del tratamiento inicial del SE convulsivo a través de la comparación de las líneas terapéuticas aquí expuestas.
Los fármacos antiepilépticos y anestésicos han demostrado históricamente su eficacia, sin embargo un 30% de los pacientes pueden ser refractarios al tratamiento convencional.
En las 2 últimas décadas se han hecho grandes esfuerzos por mejorar los esquemas de manejo en estadios refractarios del SE. Asimismo, se incorporó el concepto previamente descrito de súper refractario. Se introdujeron nuevos fármacos de uso intravenoso como el ácido valproico, el LEV y más recientemente la lacosamida.
Si bien no contamos con grados altos de evidencias brindados por estudios aleatorizados, comparativos, la indicación de estos medicamentos no-anestésicos cada vez gana más aceptación en los diagramas de flujo de tratamiento del SE.
Aún se requiere de estudios que también determinen y recomienden los tiempos de la supresión electroclínica en estas instancias.
Se establece cada vez con mayor firmeza el rol fundamental de los registros vídeo-electroencefalográficos prolongados o continuos para detectar actividad epiléptica subclínica o sutil, y monitorizar la respuesta al tratamiento en pacientes con sedación farmacológica.
Seguimos haciendo hincapié en que la mayor información y divulgación acerca de la prevalencia y características del SENC es de suma importancia para evitar demoras diagnósticas que deriven en una mayor morbimortalidad.
Se deberá seguir trabajando en objetivos concretos para favorecer la aproximación y el diagnóstico precoz, mejorar la disponibilidad y lectura de la electroencefalografía, mejorar diseños de estudios que evalúen el tratamiento prehospitalario, en la sala de emergencias y la terapia intensiva y líneas de investigación que incluyan comparación de fármacos en períodos refractarios y súper refractario.
Se espera que la actualización de las guías y las nuevas recomendaciones sean consideradas en todos aquellos niveles que de alguna u otra manera estén involucrados en el manejo de pacientes con SE.
Conflicto de interesesRicardo Bernater ha recibido apoyo de las siguientes industrias farmacéuticas para asistir a jornadas y congresos: Laboratorio Abbott, Laboratorio Glaxo SmithKline Argentina, Laboratorio Janssen Argentina.
Analía Calle ha recibido apoyo de las siguientes industrias farmacéuticas para asistir a jornadas y congresos: Laboratorio Glaxo SmithKline Argentina, Laboratorio Bagó Argentina, Laboratorio Abbott Argentina, Laboratorio Raffo Argentina, Laboratorio Novartis Argentina.
Verónica Campanille declara no tener conflictos de intereses.
Oscar Martinez declara no tener conflictos de intereses.
Natalia Paoli ha recibido apoyo del laboratorio Novartis para la realización de una beca en epilepsia.
Mónica Perassolo ha recibido apoyo de las siguientes industrias farmacéuticas para asistir a jornadas y congresos internacionales: Laboratorio Glaxo SmithKline Argentina.
Lucas Romano ha recibido apoyo de las siguientes industrias farmacéuticas para asistir a jornadas y congresos: Laboratorio Bagó Argentina, Laboratorio Glaxo SmithKline Argentina, Laboratorio Novartis Argentina y Laboratorio Raffo Argentina.
María Belén Viaggio ha recibido apoyo de las siguientes industrias farmacéuticas para asistir a jornadas y congresos: Laboratorio Glaxo SmithKline Argentina, Laboratorio Janssen Argentina, Laboratorio Astra Zéneca Argentina.