En este trabajo investigamos la literatura existente acerca de la posibilidad de que algunos hallazgos clínicos puedan ser de utilidad para el diagnóstico de la presencia de contenido de conciencia en los pacientes con alteraciones crónicas de la misma. A partir de la evaluación neurológica de ciertas características de los pacientes en forma sistematizada, se intenta detectar la presencia de contenido de conciencia en aquellos casos en los que las herramientas clínicas recomendadas, como la escala de recuperación de coma revisada, no logran desenmascarar contenido de conciencia y estemos en presencia de casos de la llamada «conciencia encubierta». Aunque el diagnóstico de estos estados se realiza con estudios neurológicos funcionales, se presenta una estrategia de detección de hallazgos fenotípicos para los pacientes que puede ser útil para el diagnóstico correcto.
In this paper we investigate the existing literature on the possibility that some clinical findings may be useful for the diagnosis of the presence of conscious content in patients with chronic alterations of consciousness. From the neurological evaluation of certain characteristics of the patients in a systematized way, we try to detect the presence of content of consciousness in those cases in which the recommended clinical tools, such as the revised coma recovery scale, fail to unmask content of consciousness and we are in the presence of cases of the so-called “covert consciousness”. Although the diagnosis of this type of states is, to date, performed with functional neurological studies, a strategy for detecting phenotypic findings is presented for these patients that may be useful for the correct diagnosis.
La clásica definición de la presencia de conciencia que utilizamos en neurología, entendida como el reconocimiento de uno mismo y de su entorno, a partir del enfoque original de James1 quizá no sea la más adecuada a la hora de la evaluación de pacientes que presentan alteraciones crónicas de la misma. Consideramos de utilidad para el enfoque de estos trastornos, otra definición clásica también, pero desde la filosofía, que es la propuesta por Nagel planteando que un ser es consciente si hay «algo que es como estar» en ese estado en el que se encuentra ese ser2. Un trastorno de la conciencia es un estado en el que la conciencia se ha visto afectada por un daño cerebral difuso o multifocal. Debido a los avances en el cuidado de la salud en las unidades de cuidados intensivos, algunos de los pacientes en coma secundario a un traumatismo craneoencefálico grave y/o a otras enfermedades neurológicas críticas sobreviven y pasan a una etapa de trastorno de conciencia prolongado. La cronicidad del trastorno de conciencia se explica por el daño persistente de las estructuras y funciones de los circuitos neurobiológicos de la conciencia. Se ha postulado que el diferente grado de afectación del circuito cortico-talamocortical explica, por lo menos en parte, la magnitud de la alteración de conciencia3.
Por definición, los trastornos prolongados de conciencia son aquellos que evolucionan después de un coma secundario a un daño cerebral agudo grave y se prolongan más allá de cuatro semanas. Es importante entender la diferencia entre la definición conceptual de cada uno de los trastornos de la conciencia y el conjunto de criterios diagnósticos con los que se va a trabajar4. La definición conceptual implica entender la presencia o ausencia de conciencia en forma binaria, lo cual es objeto de algunas controversias y los criterios diagnósticos se refieren a las características empíricas por las que se reconoce a cada entidad.
Clásicamente, los trastornos crónicos de la conciencia se categorizan en dos estados, el síndrome de vigilia sin respuesta (SVSR), antes llamado estado vegetativo y el estado de conciencia mínima (ECM). La identificación clínica de la conciencia y la que a la fecha permite clasificar a los trastornos de conciencia incluye la respuesta a estímulos y la observación de comportamientos espontáneos. El estado de coma5 puede definirse como un estado de profunda alteración de la conciencia del que el paciente no puede ser despertado. Fundamentalmente, los ojos están cerrados y no existe un ciclo normal de sueño-vigilia. Suele durar solo unos días o semanas tras una lesión cerebral aguda. El SVSR denota una condición de vigilia sin signos clínicos evidentes de conciencia. Estos pacientes pueden abrir los ojos, pero solo muestran comportamientos reflejos (no intencionados), por lo que no habría evidencia clínica de conciencia de sí mismos ni de lo que les rodea, es decir, que en este caso y tomando la definición de Nagel, no existiría nada como estar en ese estado. Por el contrario, los pacientes con ECM muestran signos inequívocos de conductas no reflejas mediadas por la corteza cerebral, que se producen de forma inconsistente, aunque reproducible, en respuesta a estímulos ambientales6. Algunos pacientes con ECM pueden seguir indicaciones hasta con marcadas limitaciones, aunque la comunicación funcional no es posible. Justamente es la comunicación funcional y/o el uso funcional de objetos lo que determina la emergencia o salida del ECM. En la actualidad, se reconoce la heterogeneidad del ECM y, en consecuencia, los pacientes pueden clasificarse según el grado de sus respuestas conductuales en ECM «plus» (si son capaces de seguir órdenes, producir palabras inteligibles y/o mostrar comunicación intencional) o ECM «minus» (si solo muestran signos voluntarios de conciencia, como localización del dolor o seguimiento visual, con ausencia de conductas sugestivas de procesamiento del lenguaje)7–9. En ocasiones, la distinción clínica entre el SVSR y el ECM puede ser sutil en muchos pacientes. De hecho, se reportó que alrededor del 40% de los pacientes con diagnóstico clínico de SVSR pueden diagnosticarse erróneamente, ya que pueden ser conscientes, pero no manifestar signos de conciencia10–13. La dificultad para diferenciar clínicamente los diferentes tipos de trastornos de conciencia e incluso para excluir otros trastornos neurológicos como el síndrome de enclaustramiento o el mutismo acinético, explica la alta tasa de errores diagnósticos que se encuentra en esta población, lo cual interfiere en la toma de decisiones de tratamiento, en la asignación de recursos de diagnóstico y de rehabilitación y en el asesoramiento a las familias acerca del pronóstico funcional de estos pacientes12,14–16. La precisión diagnóstica mejora significativamente cuando se usan escalas estandarizadas12,16,17, cuando se evalúa a los pacientes de forma seriada y en distintos momentos del día18, dadas las fluctuaciones normales de conciencia y cuando se incorporan estudios complementarios funcionales19–22.
En los últimos 20 años, se ha descripto una nueva categoría diagnóstica que ha forzado un cambio de paradigma en la interpretación clínica de los trastornos crónicos de la conciencia. La presencia de actividad cerebral encubierta ante órdenes, utilizando paradigmas avanzados de resonancia magnética y de neurofisiología en algunos pacientes de SVSR y ECM ha permitido introducir el termino de disociación cognitivo–motora23–31 para describir a aquellos que no pueden expresar conductualmente procesos cognitivos residuales o indemnes mediante respuestas motoras. Por lo tanto, podríamos decir que, la disociación cognitivo-motora, también llamada conciencia encubierta, es un estado de conciencia residual tras una lesión cerebral grave o un trastorno neurológico que escapa a la detección rutinaria del comportamiento en la cabecera del paciente23. La sensibilidad relativamente limitada de la evaluación clínica y de las escalas estandarizadas para detectar y valorar la capacidad de respuesta conductual en relación con la presencia de conciencia depende de que dicha evaluación se basa en la respuesta motora del paciente10,31,32.
Los signos residuales de conciencia en aquellos pacientes sin movimiento o sin respuesta motora al comando pueden ser muy sutiles para que se identifiquen con el examen neurológico tradicional o incluso con las escalas estandarizadas propuestas para el diagnóstico del tipo de trastorno de conciencia. Se necesitan propuestas de diagnóstico clínico para identificar pacientes con disociación cognitivo–motora durante el proceso de recuperación del estado de coma y que podrían recuperarse23.
Por todo lo expuesto, consideramos que es muy importante diferenciar fenotipos clínicos de los trastornos crónicos de conciencia, ya que cada uno debería tener un enfoque terapéutico distinto. El objetivo de este artículo es proporcionar un protocolo de valoración neuroconductual estandarizada que permita una correcta interpretación clínica al lado de la cama del paciente con trastorno crónico de la conciencia, incluyendo el reconocimiento de signos neurológicos sutiles indicadores de función cognitiva residual en el contexto de rehabilitación.
MétodosCriterios de elegibilidadSe realizó una búsqueda bibliográfica cuyo principal objetivo fue describir estrategias clínicas para la valoración neuroconductual junto a la cama del paciente con trastorno crónico de la conciencia, según la evidencia publicada, las recomendaciones de la Academia Americana de Neurología21, de la Academia Europea de Neurología22 y varias recomendaciones basadas en la evidencia11,33–36 y una revisión de la literatura científica disponible, otorgando preferencia a los trabajos recientes y a la actualización de mayor relevancia clínica en el campo de la neurorrehabilitación.
Se diseñó una estrategia de búsqueda en las bases de datos PubMed, Research gate, Scopus y Acumulative Index to Nursing and Allied Health Literature, para obtener todos aquellos artículos publicados entre 2014 y 2024. Se utilizaron como palabras clave: «Disorders of consciousness» AND «brain injury» AND/OR «Covert cognition» OR «Cognitive Motor Dissociation».
Se seleccionaron aquellos artículos que cumplían los siguientes criterios de inclusión: 1) artículos en inglés o español; 2) pacientes adultos con trastornos de conciencia secundario a lesión cerebral adquirida; y 3) todo tipo de documentos debido a la escasa literatura por la especificidad de los objetivos: estudios originales, reportes de casos, revisiones o guías de recomendaciones.
Los criterios de exclusión fueron aquellos artículos que abordaban otras enfermedades (enfermedades neurodegenerativas, por ejemplo), que incluyeran pacientes pediátricos o que se hayan publicado antes del 2015, es decir con anterioridad a la descripción original de cognición encubierta o disociación cognitiva-motora30.
Proceso de extracción de datos y síntesis de informaciónLos datos de interés fueron extraídos de los estudios y guías de revisión con el objetivo de responder las siguientes preguntas clínicas:1 ¿cuáles son los aspectos clínicos para tener en cuenta para una adecuada valoración neuroconductual de los trastornos crónicos de la conciencia?;2 ¿cuáles son las dificultades y los factores de confusión para tener en cuenta en la valoración neuroconductual de los trastornos crónicos de la conciencia? Finalmente, se propone un algoritmo de interpretación clínica dirigido a todos los médicos, enfermeros, kinesiólogos, terapistas ocupacionales, fonoaudiólogos, psicólogos, musicoterapeutas y profesionales relacionados con la rehabilitación y cuyo alcance implica a todos los pacientes con trastorno crónico de conciencia que se encuentran en un programa de rehabilitación.
ResultadosEn la presente revisión en la cual basamos el desarrollo de la propuesta de evaluación clínica estandarizada al lado de la cama para pacientes con trastornos crónicos de la conciencia secundarios a una lesión cerebral adquirida se han incluido información relevante de 68 artículos.
Aspectos clínicos para tener en cuenta ante la valoración neuroconductual de los trastornos crónicos de la conciencia.Una valoración neuroconductual eficaz comienza con un enfoque interdisciplinario que promueva el trabajo en equipo y la comunicación entre los profesionales de las distintas especialidades asistenciales, incluidas la medicina, la enfermería y las diferentes áreas terapéuticas. Las medidas de resultado (outcomes) en las escalas de valoración neuroconductual deben ser obtenidas por múltiples disciplinas, en diferentes entornos, a diferentes horas del día y en distintas condiciones para mejorar la precisión diagnóstica al evitar o minimizar efecto de intercurrencias agudas sobreagregadas12,14,17,37.
La evaluación neuroconductual en un programa de rehabilitación debe estandarizarse, administrada por especialistas en todo el proceso asistencial, y realizada por profesionales con experiencia en la evaluación de trastornos crónicos de conciencia y que hayan recibido formación especializada en la herramienta utilizada. Un plan de educación y formación de los profesionales debe siempre incluir una visión general de los trastornos crónicos de conciencia, el alcance una valoración neuroconductual pormenorizada al lado de la cama y una formación práctica para garantizar un estándar de atención en todas las disciplinas34,38. Cuando sea necesario y cuando desde el punto de vista clínico haya dudas acerca del verdadero estado de conciencia del paciente, debe emplearse un enfoque multimodal para mejorar la sensibilidad y especificidad de los resultados de la valoración neuroconductual al lado de la cama de los pacientes con trastornos crónicos de la conciencia, mejorando así la precisión diagnóstica16,29,34,39,40.
La tabla 1 presenta un resumen de las estrategias recomendadas para optimizar al paciente y el entorno con el fin de garantizar la precisión de los resultados de la valoración neuroconductual del paciente con trastorno crónico de la conciencia en el contexto de rehabilitación.
Checklist sugerido para la evaluación neuroconductual con fines diagnósticos en pacientes con trastorno crónico de la conciencia en el contexto de rehabilitación
| Previo a la evaluación | Durante la evaluación | Después de la evaluación |
|---|---|---|
| Leer la historia clínica de la UCIDescartar confundidores médicos, revisando:- laboratorio- neuroimagen- EEGConsiderar esquema farmacológico:- Sedativos- estimulantesConsiderar posibles déficits sensoriales previos y condiciones premórbidasEstimar reserva cognitivaPlanificar al menos 5 sesiones de evaluación en el término de 2 semanas | Revisar confort del paciente:- adecuado posicionamiento de cabeza, miembros y tronco- remover splints o cualquier equipamiento (si no hay contraindicación)- reducir los distractores ambientalesAsegurar una luz y temperatura ambiental apropiadasIniciar estrategias facilitadoras del nivel de alertaObservar comportamiento espontáneo del paciente (movimientos propositivos, intento de sacarse sondas o catéteres; sacar las sábanas; luego de cambiar de lado de la cama, evaluar si hay seguimiento visual o fijación)Evaluar respuestas conductuales del paciente a la orden verbal y frente a estímulos nociceptivosCompletar examen neurológico tradicional, con énfasis en la pesquisa de signos sutiles de conciencia encubierta o cognición residualInterrogar a la familia de manera dirigida para la pesquisa de respuestas del paciente (estímulos emocionales)Continuar evaluando posibles confundidores y corregirlos (si es posible) | Recolectar las puntuaciones de las escalas estandarizadas utilizadas según esquema planificadoRealizar diagnóstico clínico según los criterios internacionales, el examen neurológico, las escalas estandarizadas y neuroimágenesSi la respuesta conductual es ambigua o inconsistente considerar otras evaluaciones (otras escalas, estudios funcionales como RMN-f, EEG-f o PET-FDG)Integrar la información de manera interdisciplinaria para comunicar el diagnóstico y planificar el tratamiento (farmacológico y no farmacológico)Registrar la interpretación clínica, la conducta sugerida de estudios y de tratamiento, la información brindada a la familia y las preguntas que hayan surgido con sus correspondientes respuestas |
UCI: unidad de cuidados intensivos.
Los pasos para una valoración estandarizada del paciente con trastorno crónico de conciencia incluyen:
- 1.
Leer la historia clínica de derivación (unidad de terapia intensiva y sala general) con el objetivo de analizar y descartar confundidores médicos, revisando el último laboratorio (trastornos metabólicos, hidroelectrolíticos, endócrinos), las neuroimágenes disponibles en forma comparativa (carga lesional, presencia de hematomas, lesiones isquémicas secundarias, hidrocefalia, lesiones focales sugestivas de déficit conductual focal, por ejemplo, afasia en pacientes con lesiones en el hemisferio cerebral dominante, síndrome de enclaustramiento en pacientes con lesiones del tronco, principalmente pontinas, síndrome de mutismo acinético en pacientes con lesiones de la corteza cingulada anterior y frontal medial, etc.) y los registros de electroencefalograma (EEG) (actividad epiléptica no convulsiva)41.
- 2.
Ver antecedentes de deficiencia sensorial (visuales, auditivos, enfermedades previas que afecten la sensibilidad superficial y/o profunda) que limite el examen neurológico o la comprensión.
- 3.
Determinar factores premórbidos que disminuyan o incrementen la reserva cognitiva42.
- 4.
Evaluar efectos de fármacos sedativos y estimulantes del sistema nervioso central36–43.
- 5.
Planificar al menos cinco sesiones de evaluación en el término de dos semanas21,22.
- 6.
Revisar el confort del paciente34:
- •
adecuado posicionamiento de cabeza, miembros y tronco,
- •
remover valvas o cualquier equipamiento y/o contenciones (si no hay contraindicación),
- •
reducir los distractores ambientales.
- •
- 7.
Asegurar una luz y temperatura ambiental apropiadas34.
- 8.
Iniciar estrategias facilitadoras del nivel de alerta21.
- 9.
Observar al paciente.
- •
Evaluar movimientos espontáneos propositivos22.
- •
Prestar atención si se intenta quitar los catéteres (sonda nasogástrica, vesical, acceso venoso), sacar sábanas, variabilidad de la frecuencia cardiaca ante estímulos relevantes (no diagnóstico, pero sugestivo).
- •
Luego de cambiar de lado de la cama, evaluar si hay seguimiento visual o fijación (la fijación sola no es suficiente, pero puede ser indicio de contenido de conciencia).
- •
- 10.
Evaluar la respuesta conductual frente a estímulos44.
- •
Llamar por el nombre, en voz alta y clara. Intentar desde ambos laterales del paciente.
- •
Pedir que cierre los ojos y esperar cinco segundos, reiterar la orden. Mismo procedimiento para que cierre la boca y que saque la lengua.
- •
Observar movimientos sutiles a la orden de mover el miembro superior.
- •
Aplicar estímulos dolorosos periféricos44: esta técnica se utiliza para provocar una respuesta de apertura ocular. Aplicar una presión en la articulación interfalángica con un lápiz o bolígrafo en la cara lateral externa de la articulación interfalángica proximal o distal durante 10-15 segundos para obtener una respuesta. Tener en cuenta que un estímulo doloroso periférico puede provocar un reflejo espinal, causando la flexión del miembro examinado; un reflejo espinal no es una indicación de una función cerebral intacta.
- •
Aplicar estímulos dolorosos centrales44: esta técnica se utiliza para provocar una respuesta motora. Se realiza estimulando un nervio craneal, evitando así la posibilidad de provocar un reflejo espinal.
- •
Presión supraorbitaria (nervio craneal V): en primer lugar, colocar la parte plana del pulgar sobre el reborde supraorbitario (pequeña muesca situada debajo la parte interna de la ceja), mientras que la otra mano descansa sobre la cabeza del paciente. A continuación, aplicar gradualmente una presión creciente durante 10-20 segundos para obtener una respuesta. Es importante asegurarse de que el paciente no tenga fractura orbitaria, fracturas faciales o craneotomías frontales
- •
Maniobra de Foix (nervio craneal V): dolor provocado por presión detrás del ángulo mandibular en dirección profunda hacia la apófisis estiloides. Aplicar gradualmente una presión creciente durante 10-20 segundos para obtener una respuesta. Es una maniobra más útil para despertar si no hay respuesta a estímulos menos intensos y dolorosos.
- •
Presión esternal: esta técnica suele realizarse cuando los estímulos mencionados anteriormente no consiguen provocar una respuesta. Aplicar un estímulo en la línea media utilizando los nudillos de un puño cerrado sobre la parte media del esternón del paciente (no la apófisis xifoides). La presión se aplica durante un máximo de 30 segundos y debe tenerse precaución en pacientes con cirugía cardiaca previa o signos de lesión en el esternón.
- •
- 11.
Continuar con el examen neurológico convencional45. Prestar atención a los signos de probable contenido de conciencia no tradicionales o sugestivos de cognición encubierta (si bien no indican que el paciente tiene contenido de conciencia, pueden ser indicios y deben ser registrados)46.
- •
Apertura pasiva de los ojos de los pacientes que no presentan apertura ocular espontánea o desencadenada por estimulación y evaluar los movimientos oculares horizontales y verticales (los pacientes con síndrome de enclaustramiento clásico pueden tener preservados los movimientos oculares verticales)22.
- •
Resistencia a la apertura de los ojos ante el intento de apertura manual: cierre contundente de uno o ambos ojos al abrir manualmente los párpados superiores de los pacientes de forma bilateral47.
- •
Presencia de frecuencia de parpadeo espontáneo alta: no está estandarizado el número, pero en SVSR durante tres minutos el promedio fue 8± 2 y en ECM 18± 3, se fundamenta su observación y registro en que está modulado por la fatiga, la vigilancia, la demanda de tareas y la carga cognitiva48.
- •
Localización auditiva: se evalúa presentando estímulos auditivos (nombre del paciente, voz, ruido) detrás del paciente, fuera de la vista, durante cinco segundos dos veces en cada lado (derecho e izquierdo). Se considera presente cuando hay un movimiento claro de la cabeza o los ojos hacia los estímulos auditivos en ambas pruebas en al menos una dirección dentro de los 10 segundos de la presentación del estímulo. En la escala Coma Recovery Scale-Revised (CRS-R) es considerada una respuesta refleja, sin embargo, se ha visto y correlacionado con estudios funcionales en hasta el 62% de los ECM49.
- •
Habituación al reflejo de sobresalto (evaluado con aplauso): presentando un fuerte ruido de palmada directamente sobre la cabeza de los pacientes (fuera de la vista) 10 veces consecutivas (∼120 lpm), administrando cuatro pruebas. Si los pacientes tienen aleteo de párpados o parpadeo inmediatamente después del estímulo en al menos dos ensayos, esto se considera como sobresalto auditivo presente. Si los pacientes tienen aleteo de párpados o parpadeo después de cada aplauso, esto se considera un reflejo de sobresalto auditivo inextinguible; de lo contrario, se considera que los pacientes tienen habituación al reflejo de sobresalto auditivo50.
- •
Respuesta al olor irritante o desagradable: una respuesta olfativa discriminatoria se define por una respuesta conductual (cerrar los ojos, hacer muecas, evitar el movimiento de la cabeza o vocalizar) ante un olor desagradable (como el de una media sucia) y un olor irritante del trigémino (amoníaco), pero no ante un olor agradable (olor a rosa)51–54.
- •
Alimentación oral/deglución: la presencia de traqueotomía, el reflejo de la tos y la eficacia de la fase oral estaban relacionadas con la conciencia55.
- •
Cruce de piernas de manera espontánea56.
- •
Expresiones faciales a la nocicepción57,58.
- •
Seguimiento visual: utilizar un espejo para su evaluación y, si no se consigue con un espejo59, utilizar imágenes que muestren las caras u objetos personales del paciente o de sus familiares22.
- •
Comportamiento motor sutil: utilizar la escala Motor Behavioral Tool-revised (MBT-r)60,61, la cual permita detectar conductas motoras sutiles posiblemente pasadas por alto por el CRS-R. La escala incluye siete signos positivos y dos signos negativos. Se considera que los pacientes tienen cognición residual si al menos un ítem positivo está presente. Si bien no forman parte de la puntuación total, la presencia de un ítem negativo sugiere disfunción del tronco encefálico y respuestas automáticas potencialmente anormales.
- •
- 12.
Hablar con la familia para que relate si hay alguna señal de interacción y cuál es (estímulos emocionales).
- 13.
Continuar evaluando posibles confundidores y corregirlos (si es posible)34.
- 14.
Utilizar los resultados de las evaluaciones seriadas para identificar y tratar las complicaciones21.
- 15.
Recolectar las puntuaciones de las escalas estandarizadas utilizadas16,21,22,35,62 según el esquema planificado. Usar las escalas CRS-R17,63 o Simplified evaluation of CONsciousness disorders (SECONDs)64,65 para la evaluación de la conciencia en subagudos y unidades críticas22.
- 16.
Realizar el diagnóstico clínico basado en los criterios internacionales3,6,66,67, el examen neurológico, las escalas estandarizadas y métodos complementarios disponibles (neuroimágenes estructurales, estudios electrofisiológicos, potenciales evocados).
- 17.
Si la respuesta conductual es ambigua o inconsistente, considerar otras evaluaciones (otras escalas, estudios funcionales como resonancia magnética nuclear funcional, electroencefalograma funcional o tomografía por emisión de positrones con fluorodesoxiglucosa)21 o cuando se sospeche conciencia encubierta y se necesita diferenciar entre SVSR/ECM22.
- 18.
Integrar la información para comunicar el diagnóstico y planificar el tratamiento. Definir la mejor estrategia de comunicación del diagnóstico a la familia de forma precisa con lo que se encuentra positivamente y con lo que no encontramos nosotros, sin hacer inferencias. En una primera instancia no confrontar las apreciaciones subjetivas de la familia sino acompañar y educar a la familia con respecto a la situación del nivel de conciencia del paciente actual y la necesidad de seguir completando evaluaciones. Se propone la explicación del valor de indicaciones de soltar más que de apretar (manos) y del seguimiento ocular más que la fijación visual. Se instruye a prestar atención a movimientos espontáneos y a filmar movimientos nuevos o cualquier respuesta que la familia observe durante los momentos compartidos con el paciente. Estas consideraciones son importantes para establecer una alianza terapéutica con los cuidadores e implicarlos en el proceso de diagnóstico y el programa de rehabilitación68.
Además de lo mencionado, es importante enfatizar que los estados de alteración de la conciencia deben diferenciarse de la falta de respuesta por déficits sensoriales (ceguera y sordera), deficiencias sensoriomotoras y otros déficits primarios como afasia, agnosia o apraxia. Una de las ilustraciones más frecuentes de este hecho es el síndrome de enclaustramiento66,69, condición en la que los pacientes son conscientes, pero carecen de la capacidad de comunicarse por la alteración de la función motora. También el mutismo akinético70 es una entidad que, especialmente a partir de la evidencia de daño diencefálico, o frontal basal medial, debe ser sospechada en este tipo de pacientes.
Cabe destacar que, incluso las escalas de valoración neuroconductual estandarizadas tienen una capacidad limitada para diferenciar un subgrupo de pacientes que corren el riesgo de ser identificados erróneamente con trastorno crónico de conciencia debido a la presencia de factores clínicos confundidores14. La importancia de considerar posibles confundidores a la hora de valorar la respuesta neuroconductual de estos pacientes radica en la dificultad para el diagnóstico diferencial de cuadros neurológicos con mayores probabilidades de recuperación y/o que requieren abordajes terapéuticos específicos.
Investigaciones recientes han descubierto que aproximadamente entre el 15 y el 20% de las personas diagnosticadas como un trastorno crónico de conciencia presentan en realidad una disociación cognitivo-motora, una condición de conciencia encubierta caracterizada por la retención de la capacidad de pensamiento volitivo en ausencia de manifestaciones conductuales manifiestas o de producción motora19,29,30,40,71. Actualmente, la disociación cognitivo-motora solo se detecta usando tecnologías avanzadas como la resonancia magnética funcional y los electroencefalogramas asociados a implementar paradigmas activos o a la estimulación magnética transcraneal20,27,72. Se recomienda como métodos complementarios opcionales en contexto de investigación cuando se sospecha disociación cognitiva-motora.
Si bien la comprensión científica de esta entidad está evolucionando, la evidencia actual no permite establecer con claridad si la disociación cognitiva-motora forma parte del espectro clínico de los trastornos de conciencia o más bien se trate de un fenómeno distinto separado33,34, más parecido a un síndrome de «bloqueo» funcional.
Más allá de la disociación cognitiva-motora, las personas con trastornos crónicos de conciencia presentan una amplia gama de complicaciones y comorbilidades subyacentes que pueden exacerbar la complejidad del cuadro clínico, e incluso dificultar tanto su interpretación clínica como pronóstica. En consecuencia, los médicos y los profesionales de rehabilitación deben ser conscientes de tales dificultades al examinar a pacientes sin respuesta neuroconductual de función cognitiva residual.
En la tabla 2 se propone un listado de condiciones neurológicas, clínicas y ambientales que pueden ser factores de confusión y que pueden llevar a interpretar mal los resultados de la valoración neuroconductual. La sospecha de cualquiera de estos factores permitiría alertar al examinador de la necesidad de una revisión adicional, ya sea clínica o de métodos complementarios.
Confundidores posibles frecuentemente observados en pacientes con trastornos de conciencia
| Confundidores posibles neurológicos |
| AfoníaAnartriaApraxia del hablaAfasia globalAgnosia visualCeguera corticalSíndrome de TersonCompromiso nervio óptico bilateralPtosis palpebralCompromiso del III y IV par cranealSordera/sordera centralBlefarocolisisLesión concomitante de la médula espinalHemiplejía/paresiaHidrocefaliaComplicaciones intracranealesConvulsionesHiperactividad autonómica paroxísticaTrastornos del sueñoEspasticidadContracturasMiopatíasNeuropatíasTrastornos del movimientoApraxia |
| Confundidores clínicos |
| Disfunción neuroendocrinaDolorFracturasEnfermedad/infecciónEfectos secundarios de la medicación |
| Confundidores ambientales |
| Estimulación excesivaTemperaturaHora del díaPosicionamiento del pacientePresencia de restricciones y/o contencionesRuido |
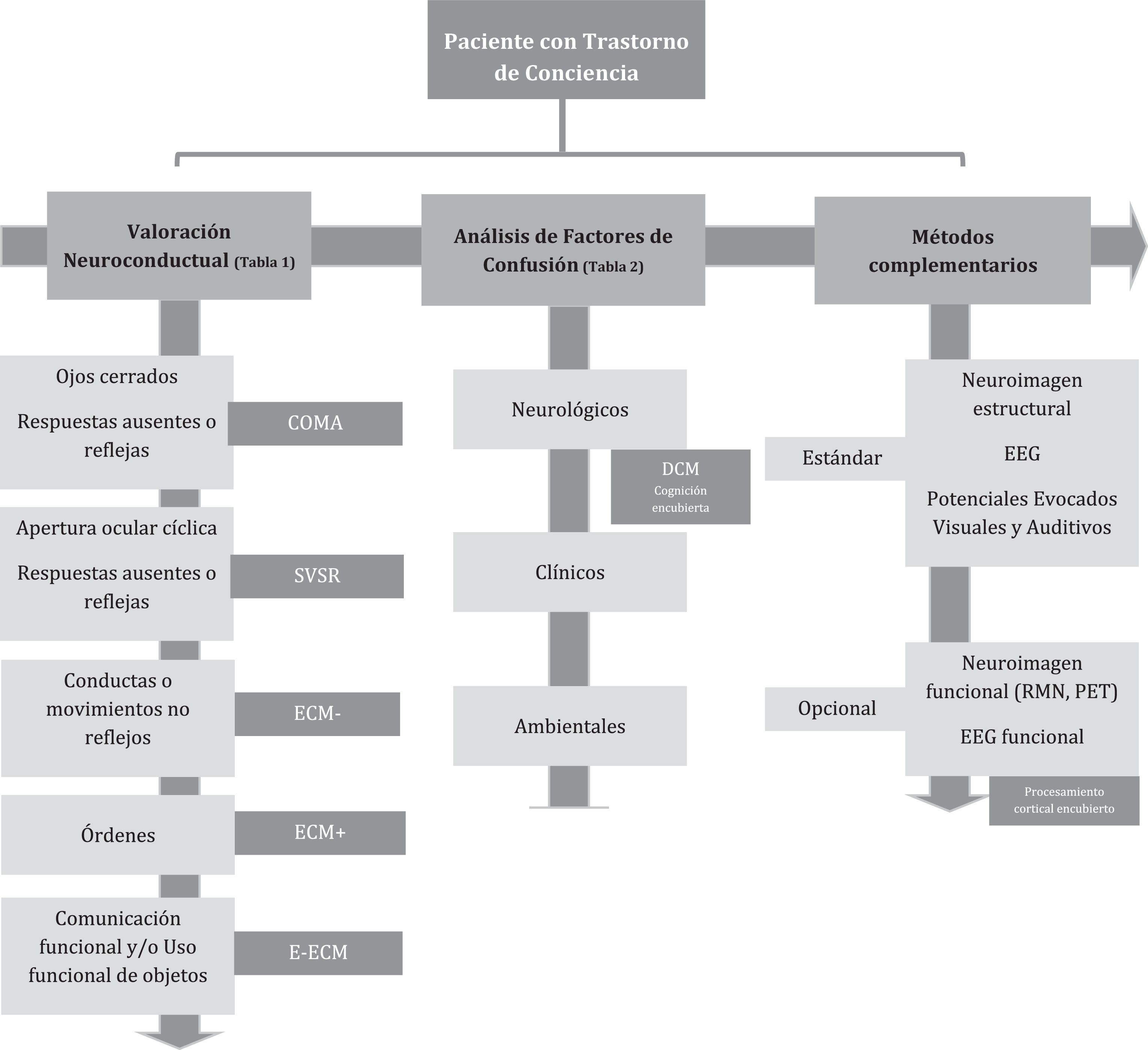
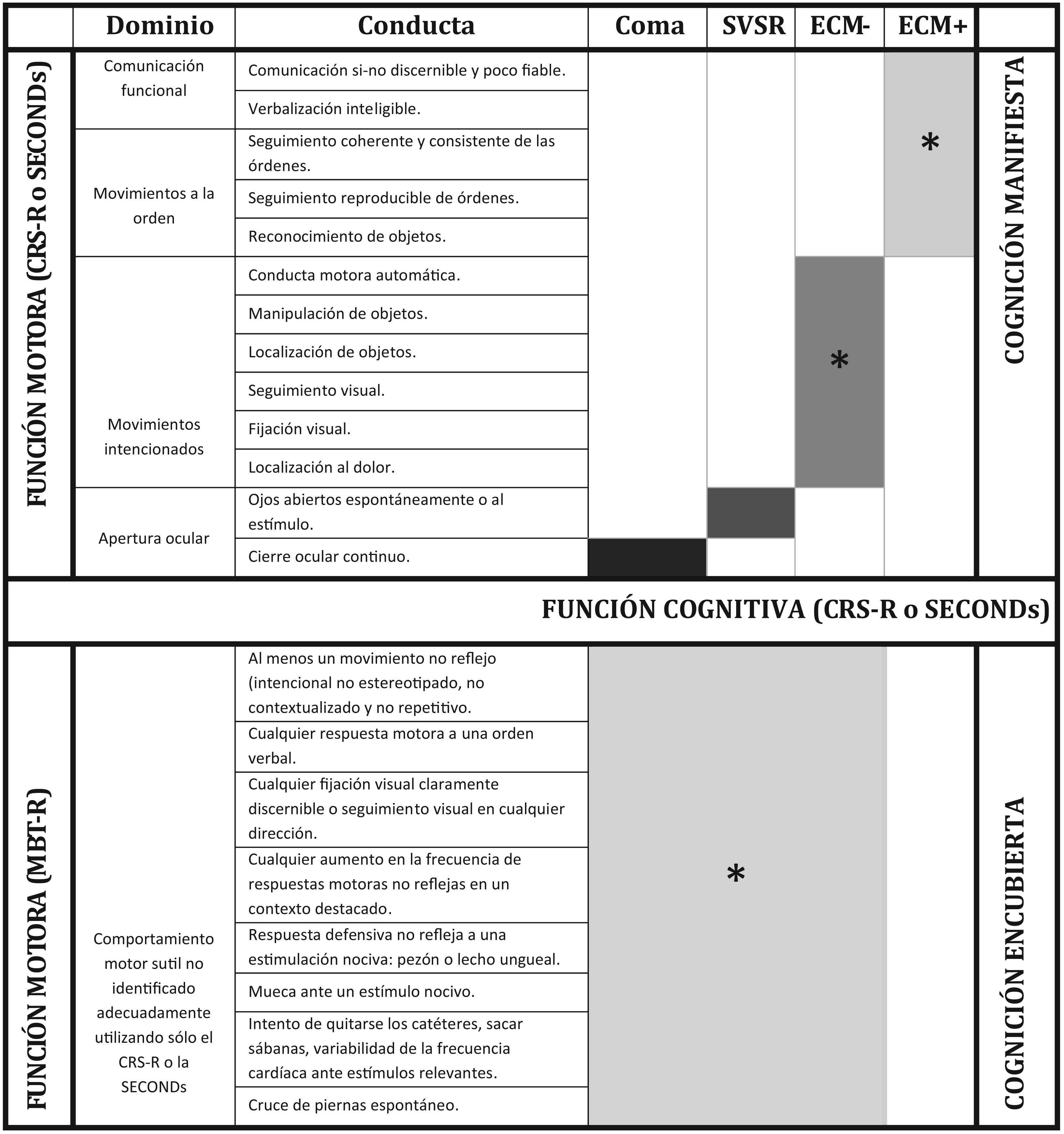
La valoración de un paciente (fig. 1) con alteración crónica de la conciencia es un tema importante en el contexto de rehabilitación, debido a que contribuye a una mejor precisión diagnóstica (fig. 2), una adecuada toma de decisiones y a una predicción pronóstica más certera. En contraste con la evaluación en un servicio de urgencias, donde ante un paciente con alteración del nivel de conciencia se debe descartar una alteración vital que requiera tratamiento inmediato; para luego evaluar el nivel de consciencia, en rehabilitación el mayor énfasis está puesto en la valoración neuroconductual del paciente.
Características clínicas distintivas para el diagnóstico de los trastornos crónicos de conciencia. Las conductas asociadas pueden conceptualizarse a lo largo de dos dimensiones: la función motora y la función cognitiva. Las regiones sombreadas de las barras indican las características distintivas de cada trastorno.CRS-R: Coma Recovery Scale-Revised; MCS: estado de consciencia mínima; MCS+: estado de consciencia mínima más («plus», en inglés); MBT-R: Motor Behavior Tool-Revised; SECONDs: Simplified Evaluation of CONsciousness Disorders.
* Al menos una característica/conducta presente.
La evaluación clínica de la conciencia (tabla 1) debe determinar el estado de alerta del paciente, según estímulos verbales y dolorosos, para establecer el grado de alteración de la conciencia y orientar el seguimiento y las intervenciones terapéuticas del paciente. Se recomienda: 1) descartar todos aquellos factores de confusión (tabla 2); 2) elegir una escala estandarizada y validada como la CRS-R17 o la SECONDs65; además de seleccionar una escala que complemente la utilidad clínica en la pesquisa de signos sutiles de conciencia encubierta61; 3) evitar hacer un diagnóstico únicamente con la primera evaluación, tratando en lo posible de planificar al menos cinco sesiones de evaluación en el término de dos semanas; 4) revisar el esquema farmacológico que permita planificar un descenso gradual y progresivo de medicamentos que alteran la neuroplasticidad y la incorporación de drogas estimulantes de la conciencia en dosis adecuadas; 5) solicitar los métodos complementarios necesarios para mejorar la precisión de la interpretación clínica y para excluir otras causas; 6) en caso de estar disponible, se pueden solicitar estudios funcionales (RMN y/o EEG) cuando exista sospecha de conciencia encubierta.
ConclusiónEn esta revisión, se expusieron estrategias semiológicas para la valoración neuroconductual pormenorizada de pacientes con trastorno crónico de conciencia debido a una lesión cerebral adquirida y los principales factores de confusión en la interpretación diagnóstica y pronóstica, haciendo hincapié en aquellas sugerencias que permiten diferenciar los estados de conciencia alterada verdaderos (SVSR o ECM) de aquellos con preservación encubierta de la misma (disociación cognitiva-motora) o con otro diagnóstico neurológico (síndrome de enclaustramiento, afasia global, mutismo akinético, etc.).
Planteamos la necesidad de ampliar el espectro de herramientas diagnósticas ante los pacientes con trastornos crónicos de conciencia que se sospeche conciencia encubierta y, en especial, en aquellos con un examen neurológico que refleje la presencia de evidentes signos sutiles de cognición pese a que el paciente no pueda evocar una respuesta motora consistente y con propósito. Una historia clínica detallada, un examen neuroconductual estandarizado y una interpretación correcta de las escalas estandarizadas y complementarias puede orientar al médico y al equipo de rehabilitación tratante para lograr un diagnóstico neurológico del trastorno de conciencia, y ante la sospecha de confundidores y/o de disociación cognitiva-motora, es necesario la derivación oportuna para realizar las pruebas diagnósticas específicas que permitan confirmarlos. Es aquí en donde los estudios complementarios funcionales (fundamentalmente resonancia magnética y/o EEG) se proponen como las mejores herramientas para ayudar a esclarecer cada caso en particular, sin embargo no podemos dejar de reconocer las dificultades que se presentan en nuestro medio para la generalización de la realización de este tipo de estudios, por lo que consideramos que la evaluación sistematizada semiológica dirigida a detectar conductas sutiles que evidencien contenido de conciencia, es una herramienta de suma utilidad práctica y de bajo costo.
FinanciaciónPara la realización del trabajo no se ha contado con ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.