Agradecemos la carta al editor de Sanchez-Larsen et al.1 en relación con nuestro artículo de revisión sobre la utilidad de acetato de eslicarbazepina (ESL) en dolor neuropático, cefaleas y neuralgias craneales2. El primer estudio que evaluó la utilidad de ESL como tratamiento de la neuralgia del trigémino (NT) en humanos merece nuestro reconocimiento y felicitaciones. Este estudio apoya la hipótesis de que ESL es un medicamento eficaz, seguro y bien tolerado para el tratamiento de la NT3.
En su carta al editor, Sanchez-Larsen et al. plantean un debate muy interesante: ¿Por qué puede resultar eficaz ESL en NT y no en otras neuropatías o condiciones de dolor neuropático?1. Nosotros nos formulamos dicha pregunta en su día de forma más genérica, y nos planteamos si lo objetivado con ESL sucedía también con los otros bloqueadores de los canales de sodio dependientes de voltaje (Nav), en concreto la subclase de las carboxamidas, que incluyen, además de ESL, la carbamazepina (CBZ) y la oxcarbazepina (OXC). Los Nav son proteínas transmembranales que permiten el paso de iones sodio a través de la membrana celular. El transporte de los iones sodio a través de estos canales es pasivo y solo depende del potencial electroquímico del ion (no requiere energía en la forma de ATP). En células excitables, tales como neuronas y cardiomiocitos, los Nav son responsables de la fase ascendente del potencial de acción (despolarización). Por tanto, son elementos que contribuyen a los síndromes de dolor mediante unas corrientes eléctricas mejoradas y una densidad mayor de Nav en las zonas lesionadas; ambos mecanismos dan lugar a una hiperexcitabilidad y una mayor transmisión del dolor4. Se han identificado nueve subtipos de Nav (Nav1.1-1.9), y se han relacionado varios Nav con la transmisión del dolor inflamatorio, nociceptivo y neuropático. Para conocer la evidencia de los bloqueadores de Nav en dolor realizamos una búsqueda bibliográfica en PubMed y Google Scholar, y tuvimos en cuenta las publicaciones más significativas utilizando los siguientes criterios de búsqueda: «carbamazepine», «oxcarbazepine» y «eslicarbazepine acetate» en combinación con «neuropathic pain», «inflammatory pain», y «chronic pain management»4.
Pese a que la NT es la única indicación real de la CBZ para el dolor según la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés- European Medicines Agency), existen algunos estudios que respaldan sus beneficios en otras indicaciones como: dolores fulgurantes tabéticos, la neuralgia postsimpatectomía, la neuropatía diabética, la neuralgia glosofaríngea y el dolor del miembro fantasma4. La OXC no tiene la indicación aprobada por la EMA para la NT. No obstante, algunas guías para la NT consideran la OXC como una opción razonable de primera línea5. También se han reconocido beneficios de la OXC para la alodinia, la neuropatía diabética, los síntomas paroxísticos en la esclerosis múltiple y la neuropatía periférica. Existen informes de casos que apoyan su uso en la neuralgia postherpética refractaria a la gabapentina, en el síndrome de dolor regional complejo refractario a gabapentina y en la radiculopatía refractaria a gabapentina4.
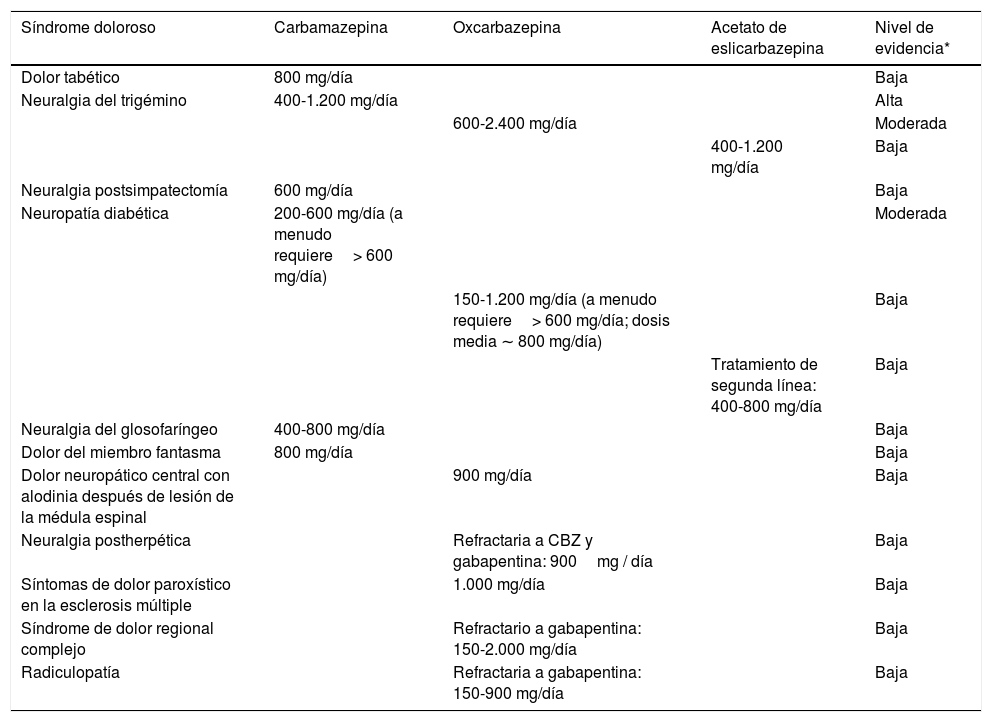
Como comentamos en nuestro artículo de revisión, se han realizado pocos estudios en dolor con ESL. No obstante, además del trabajo de Sanchez-Larsen et al. en NT, existen datos que respaldan su uso en la esclerosis múltiple con NT refractaria y en la neuropatía diabética1,2. En la tabla 1 se resume la evidencia en dolor de los bloqueadores de los Nav, subclase de las carboxamidas, comercializados actualmente en España4.
Síntesis de la evidencia en dolor de los bloqueadores de los canales de sodio
| Síndrome doloroso | Carbamazepina | Oxcarbazepina | Acetato de eslicarbazepina | Nivel de evidencia* |
|---|---|---|---|---|
| Dolor tabético | 800 mg/día | Baja | ||
| Neuralgia del trigémino | 400-1.200 mg/día | Alta | ||
| 600-2.400 mg/día | Moderada | |||
| 400-1.200 mg/día | Baja | |||
| Neuralgia postsimpatectomía | 600 mg/día | Baja | ||
| Neuropatía diabética | 200-600 mg/día (a menudo requiere> 600 mg/día) | Moderada | ||
| 150-1.200 mg/día (a menudo requiere> 600 mg/día; dosis media ∼ 800 mg/día) | Baja | |||
| Tratamiento de segunda línea: 400-800 mg/día | Baja | |||
| Neuralgia del glosofaríngeo | 400-800 mg/día | Baja | ||
| Dolor del miembro fantasma | 800 mg/día | Baja | ||
| Dolor neuropático central con alodinia después de lesión de la médula espinal | 900 mg/día | Baja | ||
| Neuralgia postherpética | Refractaria a CBZ y gabapentina: 900mg / día | Baja | ||
| Síntomas de dolor paroxístico en la esclerosis múltiple | 1.000 mg/día | Baja | ||
| Síndrome de dolor regional complejo | Refractario a gabapentina: 150-2.000 mg/día | Baja | ||
| Radiculopatía | Refractaria a gabapentina: 150-900 mg/día | Baja |
Las últimas guías de práctica clínica consultadas coinciden en señalar que los antidepresivos tricíclicos, duales (venlafaxina/duloxetina) y los antiepilépticos gabapentina/pregabalina, constituyen los fármacos de primera línea en el tratamiento del dolor neuropático; siendo los bloqueadores de los Nav una opción de segunda línea, junto con muchos otros fármacos6–7.
Aunque existe una profunda disparidad entre la cantidad y la calidad de los estudios que respaldan el uso de los fármacos de primera línea y de segunda línea para diversas afecciones de dolor, la bibliografía emergente continúa resaltando los posibles beneficios de los bloqueadores de los Nav para el tratamiento del dolor, los cuales siguen estando subestimados4.
Falta bibliografía que oriente el uso de los bloqueadores de los Nav en el dolor neuropático en comparación con los gabapentinoides, pero la mayoría de la literatura que evalúa el uso de esos fármacos para el dolor aborda los síndromes de dolor neuropático. Cabe destacar que muchos Nav se han asociado con la transmisión del dolor neuropático4, y algunos Nav se han relacionado también con el dolor inflamatorio, demostrando que las prostaglandinas incrementan la actividad de los Nav1.9 y Nav.1.74. Sin embargo, no se ha sugerido que los bloqueadores de los Nav puedan sustituir a los antiinflamatorios no esteroideos para el dolor inflamatorio. No obstante, las características farmacológicas indican que, en los pacientes que no toleran o están contraindicados los antiinflamatorios no esteroideos debido a complicaciones gastrointestinales o cardiovasculares, podría resultar eficaz un ensayo con inhibidores de los Nav. Es necesario que se realicen ensayos clínicos para evaluar y caracterizar plenamente el uso dirigido de bloqueadores de los Nav y el lugar de estos en el tratamiento del dolor inflamatorio.
Un ámbito que aún debe esclarecerse, y que podría tener un papel notable en el desarrollo de fármacos para tratar el dolor crónico, es el tratamiento dirigido a subtipos específicos de Nav. La investigación actualmente está intentando diseñar fármacos que inhiban Nav específicos de forma selectiva; no obstante, ello puede resultar complicado a causa de las similitudes estructurales entre los canales. En este sentido, el Nav1.7 es un Nav que se expresa preferentemente en neuronas periféricas, incluyendo neuronas del trigémino, y los resultados de estudios genéticos y funcionales sugieren un vínculo entre NaV1.7 y síntomas de dolor en seres humanos8. BIIB074 o vixotrigina es un bloqueador selectivo de los NaV1.7 que se encuentra en investigación para el tratamiento de la NT. Los hallazgos de los estudios electrofisiológicos han demostrado que vixotrigina inhibe preferentemente las altas frecuencias de activación en neuronas, como se esperaría encontrar en los paroxismos de dolor en la NT9. Los resultados de los ensayos clínicos fase 1 han sugerido que vixotrigina tiene una buena tolerabilidad en individuos sanos y se puede administrar en dosis terapéuticas sin una titulación prolongada. En un ensayo clínico aleatorizado de fase IIa, multicéntrico, controlado con placebo, realizado en 67 pacientes con NT clásica (de los cuales 29 se asignaron al azar al tratamiento doble ciego durante 28 días) no se encontró diferencia estadísticamente significativa (p=0,0974) entre vixotrigina (150mg tres veces al día) y placebo en el objetivo primario (medida compuesta por el fracaso del tratamiento) pero se encontraron diferencias significativas en el tiempo hasta el fracaso del tratamiento, número de paroxismos, puntuación promedio del dolor diario y evaluaciones de la función general y calidad de vida. El fármaco fue bien tolerado, siendo la cefalea y el mareo los eventos adversos más frecuentes10. Este ensayo clínico, aunque resultó negativo en el objetivo primario, sugiere claramente la posible relevancia clínica de los antagonistas de NaV1.7 en el dolor neuropático y justifica continuar con su desarrollo clínico. Por este motivo, actualmente se están llevando a cabo nuevos ensayos clínicos con vixotrigina, tanto en NT como en otros modelos de dolor neuropático (como neuropatía de fibra pequeña, eritromelalgia y radiculopatía lumbosacra)9.
En conclusión, la identificación de los subtipos de Nav relacionados con afecciones de dolor específicas y la capacidad de convertirlos en dianas farmacológicas son un atisbo del potencial de los tratamientos verdaderamente individualizados y de la transformación que hace falta en los cuidados para el dolor. Los bloqueadores de los Nav están infrautilizados según la evidencia disponible. Sin embargo, la investigación emergente ha identificado esta área como prometedora para que ensayos clínicos adicionales guíen mejor nuestra práctica clínica.