Analizar el efecto de la edad y el género sobre el dolor y los costes en pacientes con dolor neuropático periférico (DNp) crónico que inician tratamiento con gabapentina (marca) frente a gabapentina genérica (EFG).
MétodosEstudio multicéntrico-retrospectivo, realizado con registros médicos electrónicos (RME) de pacientes de ambos géneros, >18años, que iniciaron nuevo tratamiento con gabapentina de marca o genérico. Durante un año se midió la adherencia (ratio posesión medicación [RPM]) y la persistencia, la utilización de recursos sanitarios, los costes y la reducción del dolor.
ResultadosSe analizaron 1.369 RME (61,1% mujeres; edad 64,6 [15,9] años, 52,4% ≥65años); marca: 400, EFG: 969. La persistencia y la adherencia fueron mayores con marca: 7,3 vs. 6,3meses (p<0,001) y 86,5 vs. 81,3% de RPM (p<0,001). Con marca, se observaron costes sanitarios menores, tanto en <65 como en ≥65años (diferencias medias por paciente de 221€ [IC95%: 59-382] y de 217€ [51-382], respectivamente [p<0,01]), como en hombres (diferencias medias de 197€ [63-328]) o mujeres (diferencias de 239€ [96-397]), p=0,005 y p=0,004, respectivamente. Comparado con EFG, el tratamiento con marca mostró una reducción mayor del dolor: 13,5% (10,9-16,2) y 10,8% (8,2-13,5) en <65 y ≥65años, respectivamente (p<0,001), así como del 10,7% (8,2-13,2) y del 13,8% (11,0-16,5) en mujeres y hombres, respectivamente (p<0,001).
ConclusionesCon independencia del género o la edad, los pacientes que iniciaron tratamiento del DNp con gabapentina de marca vs. genérico mostraron un mayor grado de adherencia y persistencia al tratamiento, repercutiendo en unos menores costes sanitarios, a la vez que se observaron mayores reducciones del dolor.
We aimed to analyse the effects of age and sex on pain and cost for patients with chronic peripheral neuropathic pain (PNP) who have started treatment with brand name gabapentin versus generic gabapentin (EFG).
MethodsWe conducted a retrospective multicentre study using electronic medical records (EMR) for patients of both sexes, older than 18, who began treatment with brand name or generic gabapentin. Adherence (medication possession ratio [MPR]), persistence, use of healthcare resources, cost, and pain reduction were measured for one year.
ResultsWe analysed 1369 EMRs [61.1% women; mean age 64.6 (15.9), 52.4%≥65 years]; 400 used brand name drugs while 969 used generic gabapentin. Persistence and adherence were higher in patients using brand name gabapentin (7.3 vs 6.3 months, P<.001; 86.5% vs 81.3% MPR, P<.001). Lower healthcare costs were observed in patients using brand-name gabapentin in both age groups (<65 and ≥65). Mean difference in cost per patient amounted to €221 (95%CI: 59-382) and €217 (95%CI: 51-382) in the <65 and ≥65 age groups, respectively (P<.01). Mean difference in cost among men amounted to €197 (63-328), while mean difference in cost among women amounted to €239 (96-397) (P=.005 and P=.004, respectively). Compared with EFG, brand treatment showed greater pain relief: 13.5% (10.9-16.2) and 10.8% (8.2-13.5) in <65 and ≥65year patients, respectively (P<.001), and 10.7% (8.2-13.2) and 13.8% (11.0-16.5) in women and men respectively (P<.001).
ConclusionsRegardless of sex and age, patients who started PNP treatment with brand name medication showed greater persistence and adherence to treatment than those taking generic drugs. Brand name treatment also involved lower healthcare costs, and greater pain relief.
Según la Asociación Internacional para el Estudio del Dolor (International Association for the Study of Pain [IASP]), el dolor neuropático periférico (DNp) se define como un dolor iniciado o causado por una lesión primaria o disfunción del sistema nervioso, y es un síntoma común de un grupo o variedad de enfermedades1. La prevalencia estimada del DNp oscila entre el 1 y el 8% de la población adulta y supone aproximadamente el 40% de los casos de dolor crónico2.
El DNp es una enfermedad con tendencia a la cronicidad y con frecuencia con tendencia a la incapacidad, por lo que conlleva unos altos costes directos e indirectos para el conjunto de la sociedad, siendo considerado como uno de los principales problemas de salud pública3,4. Estos acontecimientos se traducen en una pérdida de la calidad de vida que afecta a su entorno familiar y sociolaboral2,5. En este aspecto, muchos pacientes no están correctamente diagnosticados, o no reciben el tratamiento farmacológico adecuado, o las dosis prescritas son inferiores a las que deberían ser pautadas1,5,6.
La terapia farmacológica constituye una de las bases fundamentales del tratamiento7. En este aspecto, la gabapentina (anticonvulsivante) es una de las opciones terapéuticas para el manejo del DNp, existiendo presentaciones de especialidades farmacéuticas de marca y genéricas (EFG)8,9. Las EFG son medicamentos con la misma eficacia, seguridad y calidad que el original, y son bioequivalentes a la marca original10. La motivación, el conocimiento por parte del médico y las políticas de intervención sanitaria sobre las EFG son algunos de los factores influyentes sobre su uso11. En nuestro país, las actuales políticas en cuanto a la restricción del precio de los medicamentos de marca frente a las EFG ya no es un argumento tan sólido para exigir su consumo en igualdad de precio (precios de referencia)12.
Revisando la literatura de algunos autores se constata que son inciertos los argumentos farmacológicos a favor y en contra a la prescripción de estos productos9,13. Otros estudios manifiestan discordancias (marca vs. EFG) por diversas circunstancias, entre ellas la adherencia al tratamiento, ocasionando generalmente una disminución de la efectividad clínica (confusión de los pacientes, mal control terapéutico, bajos resultados en salud) y un posible aumento de los costes sanitarios14,15. Recientemente hemos constatado diferencias significativas en el tratamiento del DNp crónico según que se use marca original o EFG del mismo principio activo9, pero no se había analizado el efecto de la edad o el género sobre esos resultados. Por otra parte, las evidencias disponibles acerca de la relación entre estas variables son escasas (situación de práctica clínica habitual y efecto del sexo y el género), tanto en la literatura internacional como en nuestro entorno sanitario, por lo que la realización de este estudio puede ser pertinente. Por lo tanto, el objetivo de este análisis fue analizar el efecto de la edad y el género sobre las consecuencias clínicas y económicas asociadas a pacientes con DNp crónico que inician tratamiento con gabapentina (marca original) frente a gabapentina EFG en condiciones de práctica clínica habitual.
Pacientes y métodosDiseño y población de estudioAnálisis del objetivo secundario de un estudio observacional, multicéntrico y longitudinal (de carácter retrospectivo), realizado a partir de la revisión de los registros médicos electrónicos (RME) de bases de datos informatizadas, con datos disociados, de pacientes seguidos en régimen ambulatorio y hospitalario. La población de estudio estuvo formada por pacientes pertenecientes a 6 centros de atención primaria gestionados por Badalona Serveis Assistencials S.A. La población asignada a los centros fue en su mayoría urbana, de nivel socioeconómico medio-bajo, con predominio industrial.
Criterios de inclusión y exclusiónSe incluyeron en el estudio los pacientes que demandaron atención y que iniciaron un nuevo tratamiento con gabapentina (Neurontin® o EFG) durante los años 2008 a 2012 (periodo de reclutamiento, fecha índice). Debían reunir las siguientes características: a)edad >18años; b)pacientes activos en la base de datos un mínimo de 12meses antes de iniciar el estudio; c)estar en el programa de prescripciones crónicas para la obtención de las recetas médicas (con registro constatado de la dosis diaria, el intervalo de tiempo y la duración de cada tratamiento administrado; ≥2 recetas durante el periodo de seguimiento); d)que se pudiera garantizar el seguimiento regular de los pacientes durante el periodo de estudio (≥2 registros sanitarios en el sistema informático), y e)con diagnóstico de DNp (con anterioridad o al inicio del tratamiento). Fueron excluidos: a)los sujetos trasladados a otros centros, los desplazados o fuera de zona; b)los pacientes institucionalizados permanentemente, y c)los que cambiaron de tratamiento (marca vs. EFG y viceversa). Se consideraron 4 grupos de pacientes, en función de la edad y del género: a)<65años; b)≥65años; c)hombres, y d)mujeres. El seguimiento de los pacientes a partir de la fecha índice fue de un año.
Diagnóstico y escalas utilizadasLos registros de los pacientes con DNp se obtuvieron a partir de la Clasificación Internacional de la Atención Primaria (CIAP-2)16, códigos N92-N99, y/o de la Clasificación Internacional de Enfermedades (novena edición) Modificación Clínica (CIE-9-MC; códigos 350.1, 352.9, 353.1, 353.3, 353.8, 354.0, 355.1, 355.5, 357.2, 357.4, 357.8, 357.9, 053.13). Los criterios seguidos siempre fueron a juicio del médico. Se consideró DNp como el dolor iniciado o causado por una lesión primaria o disfunción del sistema nervioso periférico, es decir, raíces nerviosas, plexos nerviosos y nervios. Como una aproximación a la efectividad clínica se obtuvo la información recogida en las historias clínicas de la escala numérica de dolor (END)17 graduada numéricamente para valoración de la intensidad del DNp en un rango de 0 (no dolor) a 10 (máximo dolor imaginable).
Variables demográficas y comorbilidadesSe recogieron el tiempo desde el diagnóstico y los antecedentes personales obtenidos a partir de la CIAP-216; hipertensión arterial (K86, K87), diabetes mellitus (T89,T90), dislipidemia (T93), obesidad (T82), tabaquismo activo (P17), alcoholismo (P15, P16), todos los tipos de fallos orgánicos (cardiaco, hepático y renal), cardiopatía isquémica (códigos: K74, K76, K75), accidente cerebrovascular (K90, K91, K93), demencias o trastornos de memoria (P70, P20), enfermedades neurológicas: enfermedad de Parkinson (N87), epilepsia (N88), esclerosis múltiple (N86) y otras enfermedades neurológicas (N99), y neoplasias malignas (todos los tipos; A79, B72-75, D74-78, F75, H75, K72, L71, L97, N74-76, T71-73, U75-79, W72-73, X75-81, Y77-79). Como variable resumen de la comorbilidad general, para cada paciente atendido se utilizó: a)el índice de comorbilidad de Charlson18 como una aproximación a la gravedad del paciente, y b)el índice de casuística individual, obtenido a partir de los Adjusted Clinical Groups (ACG), que es un sistema de clasificación de pacientes por iso-consumo de recursos19. El aplicativo ACG proporciona las bandas de utilización de recursos (BUR), con lo que cada paciente en función de su morbilidad general queda agrupado en una de las 5 categorías mutuamente excluyentes (1: usuarios sanos o de morbilidad muy baja; 2: morbilidad baja; 3: morbilidad moderada; 4: morbilidad elevada, y 5: morbilidad muy elevada).
Medicación administrada, adherencia/cumplimiento y persistencia al tratamientoGabapentina (principio activo), indicada para el tratamiento del DNp, se identificó según la clasificación Anatomical Therapeutic Chemical Classification System (ATC)20: N03AX12. La información se obtuvo de los registros procedentes de la dispensación farmacológica de medicamentos emitida por la aplicación (RCMPS) del CatSalut. La elección del medicamento de marca o EFG a un paciente en concreto fue a criterio del médico (práctica clínica). La tasa de adherencia/cumplimiento se definió según los criterios de la Sociedad Internacional de Farmacoeconomía y Resultados en Salud (ISPOR) y se calculó en función de la tasa de uso/posesión del medicamento (RPM)21. Este se evaluó desde la primera a la última prescripción y representa el número de días de medicación suministrada entre el número de días en tratamiento (a partir de la fecha índice)22. La persistencia se definió como el tiempo, medido en meses, sin abandono del tratamiento inicial o sin cambio a otra medicación al menos 30 días después de la prescripción inicial. La persistencia al tratamiento se obtuvo a los 3, 6, 9 y 12meses del seguimiento.
Uso de recursos y análisis de costesSe consideraron costes sanitarios los relacionados con la actividad asistencial (visitas médicas, días de hospitalización, urgencias hospitalarias y solicitudes diagnósticas o terapéuticas) efectuada por los profesionales. El coste fue expresado en coste medio por paciente (promedio coste/unitario). Los costes unitarios correspondientes al año 2013 se obtuvieron a partir de la contabilidad analítica de los centros, excepto la medicación. Esta última se obtuvo del Bot Plus del Consejo General de Colegios de Farmacéuticos Oficiales de España. Las prescripciones (recetas médicas) se cuantificaron según el precio de venta al público por envase en el momento de la prescripción. Para el cálculo de los costes también se incluyó la siguiente medicación concomitante: antiinflamatorios no esteroides (AINE, M01), opiáceos (N02A), analgésicos (N02B), sedantes/hipnóticos (ansiolíticos: N05C) y antidepresivos (N06A). Los costes unitarios no farmacológicos incluidos en el análisis se corresponden con visitas médicas de atención primaria (23,7€ por visita), visita médica a urgencias (119,9€), hospitalización (327,3€ por día), visita médica a especialista (68,9€), hospital de día (184,8€ por sesión), pruebas de laboratorio (22,7€ por analítica convencional), radiología convencional (18,9€) y pruebas diagnósticas (37,9€).
Aspectos éticosEl estudio siguió los principios éticos básicos contenidos en la Declaración de Helsinki para estudios en humanos. El protocolo del estudio fue clasificado por la Agencia Española de Medicamentos y Productos Sanitarios como Estudio Post-autorización-Otros diseños (EPA-OD) y fue aprobado por el Comité Ético de Investigación Clínica del Hospital Germans Trias i Pujol de Badalona (Barcelona). Este estudio no intervencionista se llevó a cabo de acuerdo con la regulación vigente sobre estudios observacionales basados en bases de datos retrospectivos. Los datos de los sujetos se sometieron a un proceso de disociación, de forma que se preservó de forma anónima la identidad del paciente, tal y como se establece en la L.O. 15/1999 de 13 de diciembre, de Protección de Datos de Carácter Personal.
Análisis estadísticoComo paso previo al análisis, y en particular a la fuente de información perteneciente a las historias clínicas informatizadas, se revisaron cuidadosamente los datos, mediante análisis exploratorio y preparación de datos para el análisis, observando sus distribuciones de frecuencia y buscando posibles errores de registro o de codificación. Se efectuó un análisis estadístico descriptivo-univariante con valores de media, mediana, desviación típica e intervalos de confianza (IC) del 95% en variables paramétricas, y mediana e intervalos intercuartílicos (percentiles 25 y 75 de la distribución) en variables no paramétricas, una vez comprobada la normalidad de la distribución con la prueba de Kolmogorov-Smirnov. La persistencia al tratamiento se calculó mediante el método de Kaplan-Meier. Para el análisis bivariante se emplearon pruebas de ANOVA y ji al cuadrado (χ2) según la distribución de los datos. La comparación de los costes sanitarios se realizó según las recomendaciones de Thompson y Barber23 mediante un modelo lineal general (análisis de la covarianza [ANCOVA]) corregido por las covariables género, edad, comorbilidad general (BUR, índice de Charlson), RPM y persistencia al tratamiento. Las comparaciones por pares se ajustaron al procedimiento de estimación de medias marginales, aplicando la corrección de Bonferroni para estimar el valor p de significación estadística. Los datos se presentaron como diferencias de medias ajustadas entre tratamientos con su correspondiente intervalo de confianza del 95% calculado con técnicas de re-muestreo (bootstraping) corregido por el sesgo, dadas las distribuciones no normales de las variables utilización de recursos y costes.
La variable clínica de intensidad de dolor en la escala numérica se analizó después de realizar una imputación simple de los valores ausentes mediante un modelo lineal general (ANCOVA) para la variación absoluta y relativa, entre inicio del tratamiento y discontinuación, de las puntuaciones de dolor, y mediante un modelo de regresión logística para la proporción de pacientes respondedores (reducción del dolor basal ≥50%) y sin dolor/dolor leve (puntuación inferior a 4 en la END). Las covariables usadas en el ANCOVA y en el modelo de regresión logística fueron la edad, el género y la puntuación en la escala al inicio del tratamiento. No respondieron la END un total del 9,7% de los pacientes, sin diferencias significativas entre la marca (8,5%) y el genérico (10,2%), p=0,382. El método de imputación de los datos faltantes fue el arrastre de la peor observación disponible, que en este caso fue la puntuación observada en la visita de inicio de tratamiento. Se compararon las puntuaciones en la visita inicial y final, la variación absoluta (puntos) y relativa (%) de la intensidad del dolor entre ambas visitas, la proporción de respondedores y la proporción de pacientes sin dolor/dolor leve.
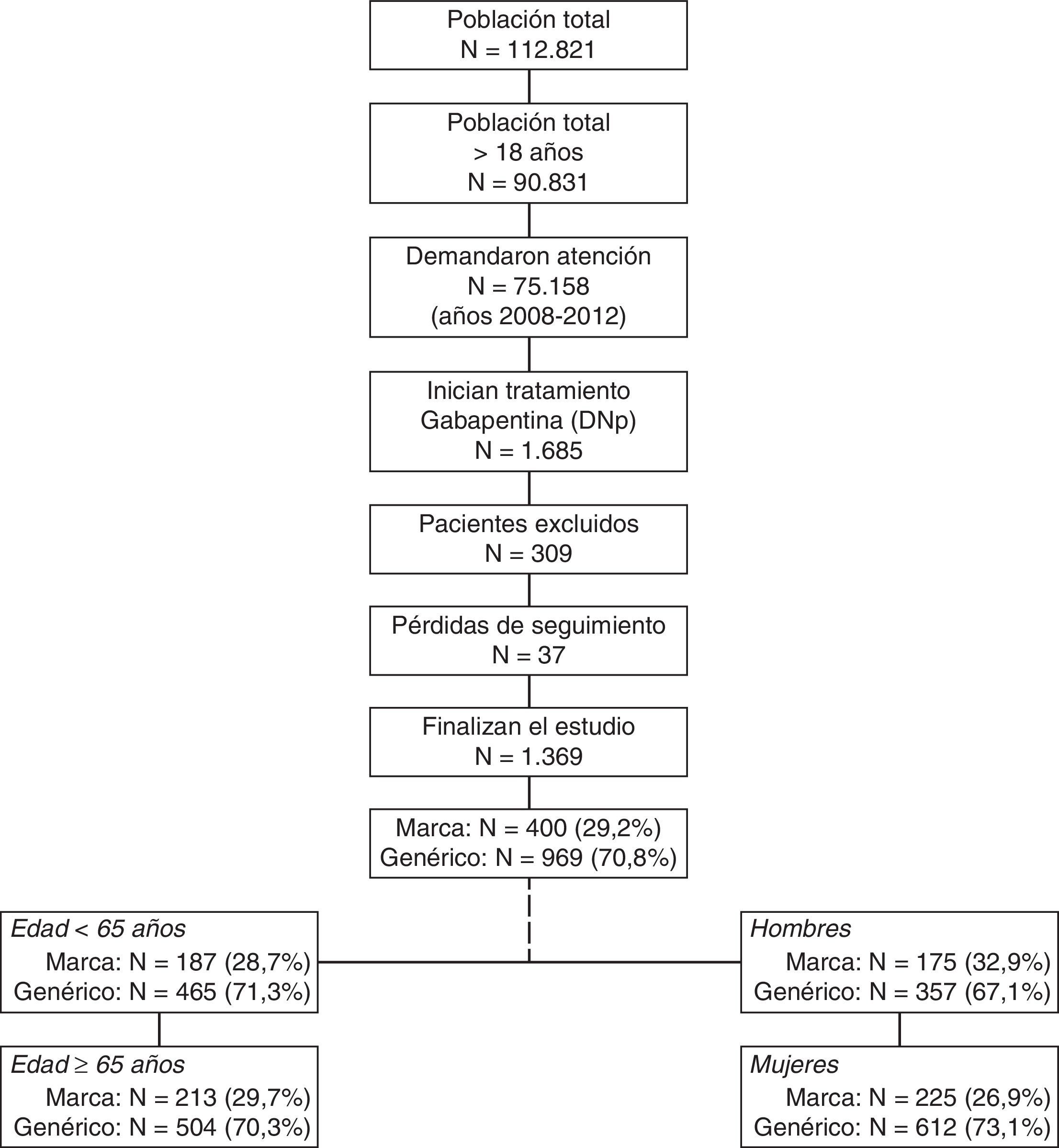
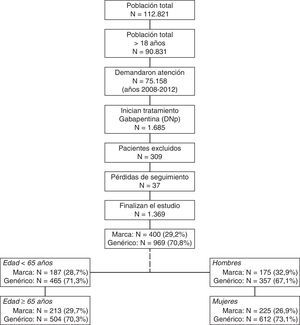
ResultadosDe una selección inicial de 90.831 sujetos mayores de 18años asignados a los centros, se reclutaron 1.369 pacientes que reunían los criterios de selección para ser incluidos en el estudio (fig. 1). En general, de los pacientes que recibieron tratamiento con gabapentina, en 400 (29,2%) fue de marca y en 969 (70,8%) de EFG; la media de edad fue de 64,6 (DE: 15,9) años, y el 61,1% fueron mujeres. Del conjunto de pacientes, el 43,0% presentaron hipertensión arterial y el 41,2% dislipidemia. Se compararon los pacientes en tratamiento de marca o EFG por los 4 grupos de estudio: a)edad <65años: marca (n=187; 28,7%) vs. EFG (n=465; 71,3%); b)edad ≥65años: marca (n=213; 29,7%) vs. EFG (n=504; 70,3%); c)hombres: marca (n=175; 32,9%) vs. EFG (n=357; 67,1%), y d)mujeres: marca (n=225; 26,9%) vs. EFG (n=612; 73,1%).
Esquema general del estudio. Se efectuó un diseño observacional de carácter retrospectivo, realizado a partir de la revisión de los registros médicos existentes (bases de datos informatizadas, con datos existentes y disociados) de pacientes seguidos en régimen ambulatorio y hospitalario que iniciaron tratamiento con gabapentina (marca vs. EFG).
EFG: especialidades farmacéuticas genéricas.
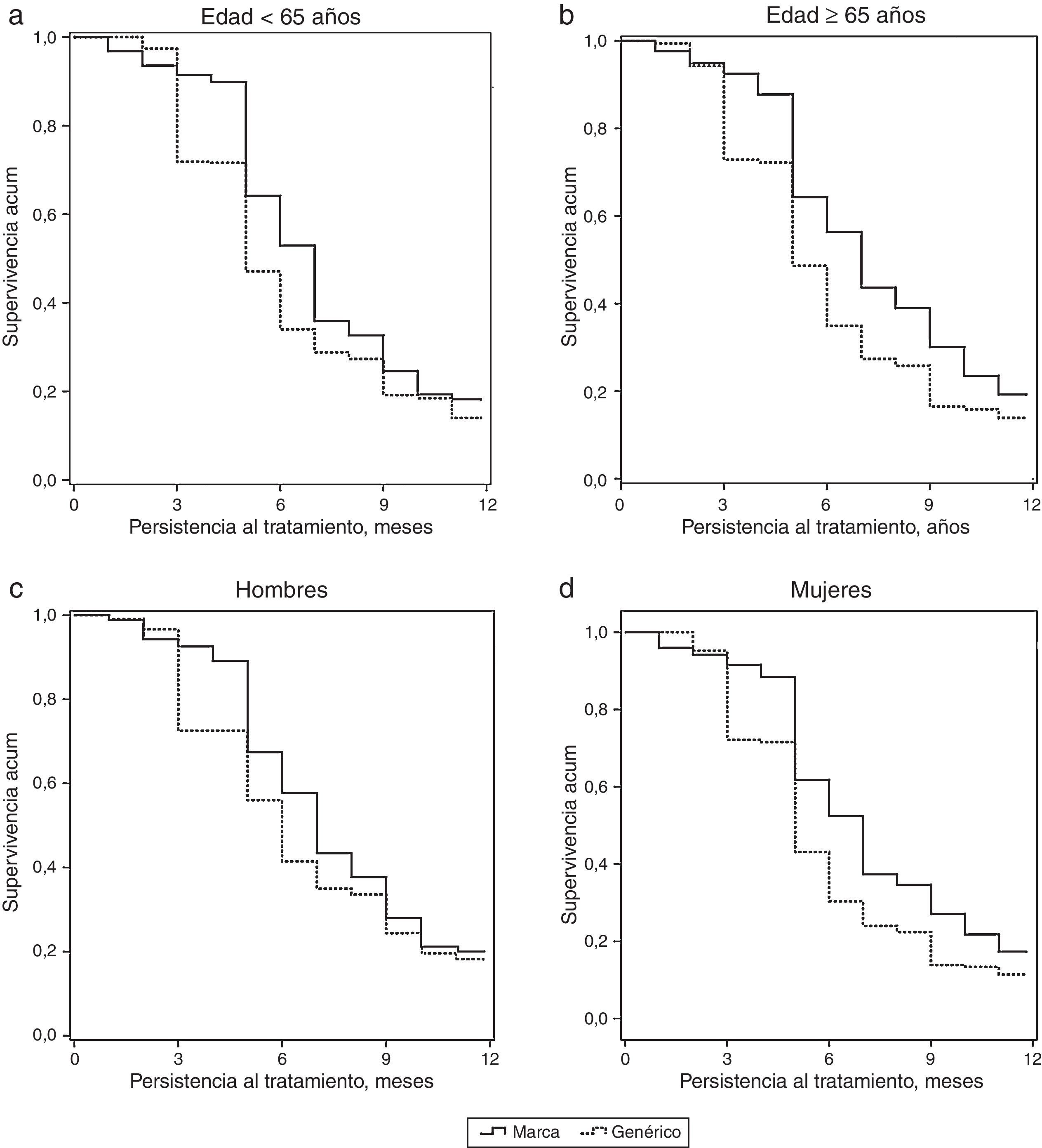
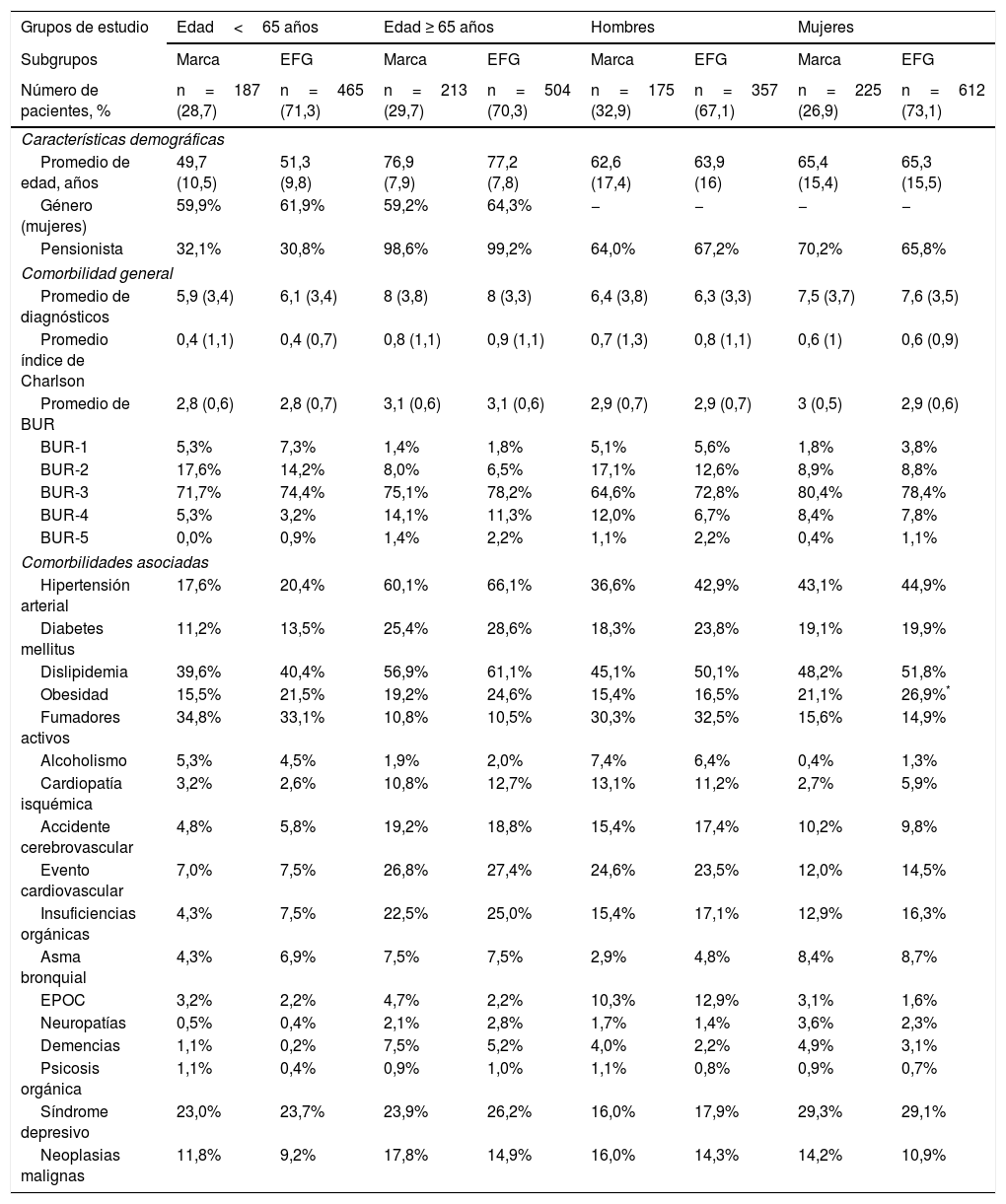
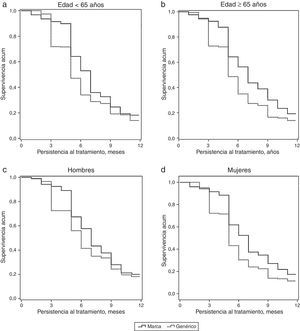
En la tabla 1 se describen las características basales y las comorbilidades asociadas a los pacientes con DNp por grupos de estudio. Los 4 grupos de estudio fueron comparables en sus características basales entre marca vs. EFG. Con gabapentina de marca, la duración media del tratamiento fue superior a la del EFG (7,3 vs. 6,3meses; p<0,001). El RPM (86,5% vs. 81,3%; p<0,001) y la media diaria de dosis de medicamento (1.322,5 vs. 1.153,5mg; p=0,008) también fueron superiores. La persistencia al tratamiento de marca vs. EFG (en todos los rangos de tiempo: 3, 6, 9 y 12meses) fue mayor. El RPM (por grupos) comparando marca vs. EFG fue el siguiente: a)en <65años, 86,3% (81,3-91,2) vs. 81,4% (77,8-84,9), diferencias no significativas; b)en ≥65años, 86,6% (82,0-91,2) vs. 81,1% (77,6-84,5), p<0,05; c)en hombres, 86,8% (81,7-91,8) vs. 83,1% (79,2-87,0), diferencias no significativas, y d)en mujeres, 86,2% (82,0-91,2) vs. 80,2% (77,0-83,4), p<0,05, respectivamente. La persistencia anual fue: a)en <65años, 19,9% vs. 14,0% (p<0,05); b)en ≥65años, 21,1% vs. 13,9% (p<0,01); c)en hombres, 20,7% vs. 15,2% (p<0,05), y d)en mujeres, 18,7% vs. 11,4% (p<0,01), respectivamente. En la figura 2 se detallan las curvas de persistencia al tratamiento.
Características basales (demográficas y comorbilidad) de la serie estudiada por grupos de estudio
| Grupos de estudio | Edad<65 años | Edad ≥ 65 años | Hombres | Mujeres | ||||
|---|---|---|---|---|---|---|---|---|
| Subgrupos | Marca | EFG | Marca | EFG | Marca | EFG | Marca | EFG |
| Número de pacientes, % | n=187 (28,7) | n=465 (71,3) | n=213 (29,7) | n=504 (70,3) | n=175 (32,9) | n=357 (67,1) | n=225 (26,9) | n=612 (73,1) |
| Características demográficas | ||||||||
| Promedio de edad, años | 49,7 (10,5) | 51,3 (9,8) | 76,9 (7,9) | 77,2 (7,8) | 62,6 (17,4) | 63,9 (16) | 65,4 (15,4) | 65,3 (15,5) |
| Género (mujeres) | 59,9% | 61,9% | 59,2% | 64,3% | − | − | − | − |
| Pensionista | 32,1% | 30,8% | 98,6% | 99,2% | 64,0% | 67,2% | 70,2% | 65,8% |
| Comorbilidad general | ||||||||
| Promedio de diagnósticos | 5,9 (3,4) | 6,1 (3,4) | 8 (3,8) | 8 (3,3) | 6,4 (3,8) | 6,3 (3,3) | 7,5 (3,7) | 7,6 (3,5) |
| Promedio índice de Charlson | 0,4 (1,1) | 0,4 (0,7) | 0,8 (1,1) | 0,9 (1,1) | 0,7 (1,3) | 0,8 (1,1) | 0,6 (1) | 0,6 (0,9) |
| Promedio de BUR | 2,8 (0,6) | 2,8 (0,7) | 3,1 (0,6) | 3,1 (0,6) | 2,9 (0,7) | 2,9 (0,7) | 3 (0,5) | 2,9 (0,6) |
| BUR-1 | 5,3% | 7,3% | 1,4% | 1,8% | 5,1% | 5,6% | 1,8% | 3,8% |
| BUR-2 | 17,6% | 14,2% | 8,0% | 6,5% | 17,1% | 12,6% | 8,9% | 8,8% |
| BUR-3 | 71,7% | 74,4% | 75,1% | 78,2% | 64,6% | 72,8% | 80,4% | 78,4% |
| BUR-4 | 5,3% | 3,2% | 14,1% | 11,3% | 12,0% | 6,7% | 8,4% | 7,8% |
| BUR-5 | 0,0% | 0,9% | 1,4% | 2,2% | 1,1% | 2,2% | 0,4% | 1,1% |
| Comorbilidades asociadas | ||||||||
| Hipertensión arterial | 17,6% | 20,4% | 60,1% | 66,1% | 36,6% | 42,9% | 43,1% | 44,9% |
| Diabetes mellitus | 11,2% | 13,5% | 25,4% | 28,6% | 18,3% | 23,8% | 19,1% | 19,9% |
| Dislipidemia | 39,6% | 40,4% | 56,9% | 61,1% | 45,1% | 50,1% | 48,2% | 51,8% |
| Obesidad | 15,5% | 21,5% | 19,2% | 24,6% | 15,4% | 16,5% | 21,1% | 26,9%* |
| Fumadores activos | 34,8% | 33,1% | 10,8% | 10,5% | 30,3% | 32,5% | 15,6% | 14,9% |
| Alcoholismo | 5,3% | 4,5% | 1,9% | 2,0% | 7,4% | 6,4% | 0,4% | 1,3% |
| Cardiopatía isquémica | 3,2% | 2,6% | 10,8% | 12,7% | 13,1% | 11,2% | 2,7% | 5,9% |
| Accidente cerebrovascular | 4,8% | 5,8% | 19,2% | 18,8% | 15,4% | 17,4% | 10,2% | 9,8% |
| Evento cardiovascular | 7,0% | 7,5% | 26,8% | 27,4% | 24,6% | 23,5% | 12,0% | 14,5% |
| Insuficiencias orgánicas | 4,3% | 7,5% | 22,5% | 25,0% | 15,4% | 17,1% | 12,9% | 16,3% |
| Asma bronquial | 4,3% | 6,9% | 7,5% | 7,5% | 2,9% | 4,8% | 8,4% | 8,7% |
| EPOC | 3,2% | 2,2% | 4,7% | 2,2% | 10,3% | 12,9% | 3,1% | 1,6% |
| Neuropatías | 0,5% | 0,4% | 2,1% | 2,8% | 1,7% | 1,4% | 3,6% | 2,3% |
| Demencias | 1,1% | 0,2% | 7,5% | 5,2% | 4,0% | 2,2% | 4,9% | 3,1% |
| Psicosis orgánica | 1,1% | 0,4% | 0,9% | 1,0% | 1,1% | 0,8% | 0,9% | 0,7% |
| Síndrome depresivo | 23,0% | 23,7% | 23,9% | 26,2% | 16,0% | 17,9% | 29,3% | 29,1% |
| Neoplasias malignas | 11,8% | 9,2% | 17,8% | 14,9% | 16,0% | 14,3% | 14,2% | 10,9% |
BUR: bandas de utilización de recursos; EFG: especialidades farmacéuticas genéricas; EPOC: enfermedad pulmonar obstructiva crónica.
Comparaciones por pares: * p<0,05.
Valores expresados en porcentaje o media (desviación estándar).
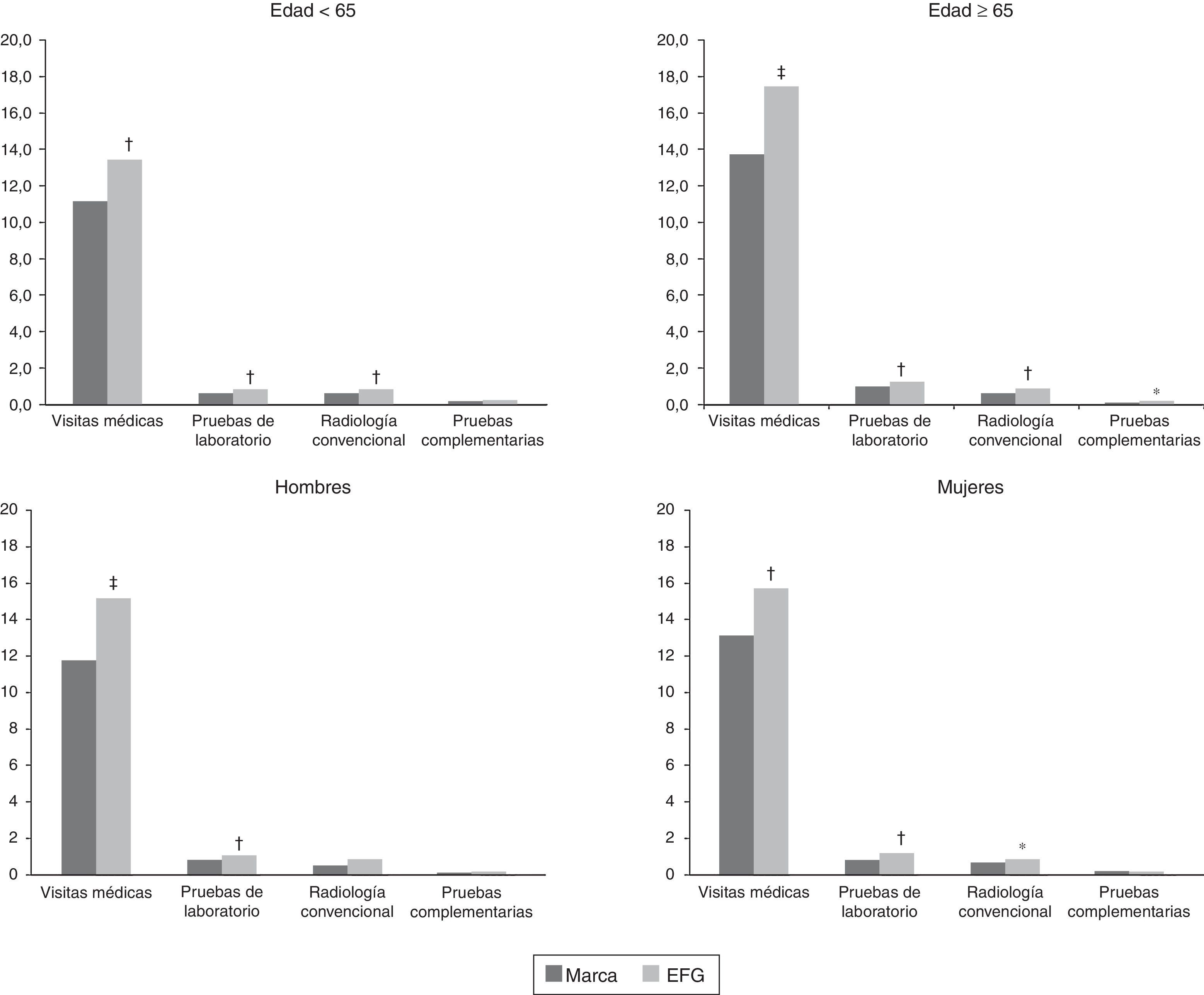
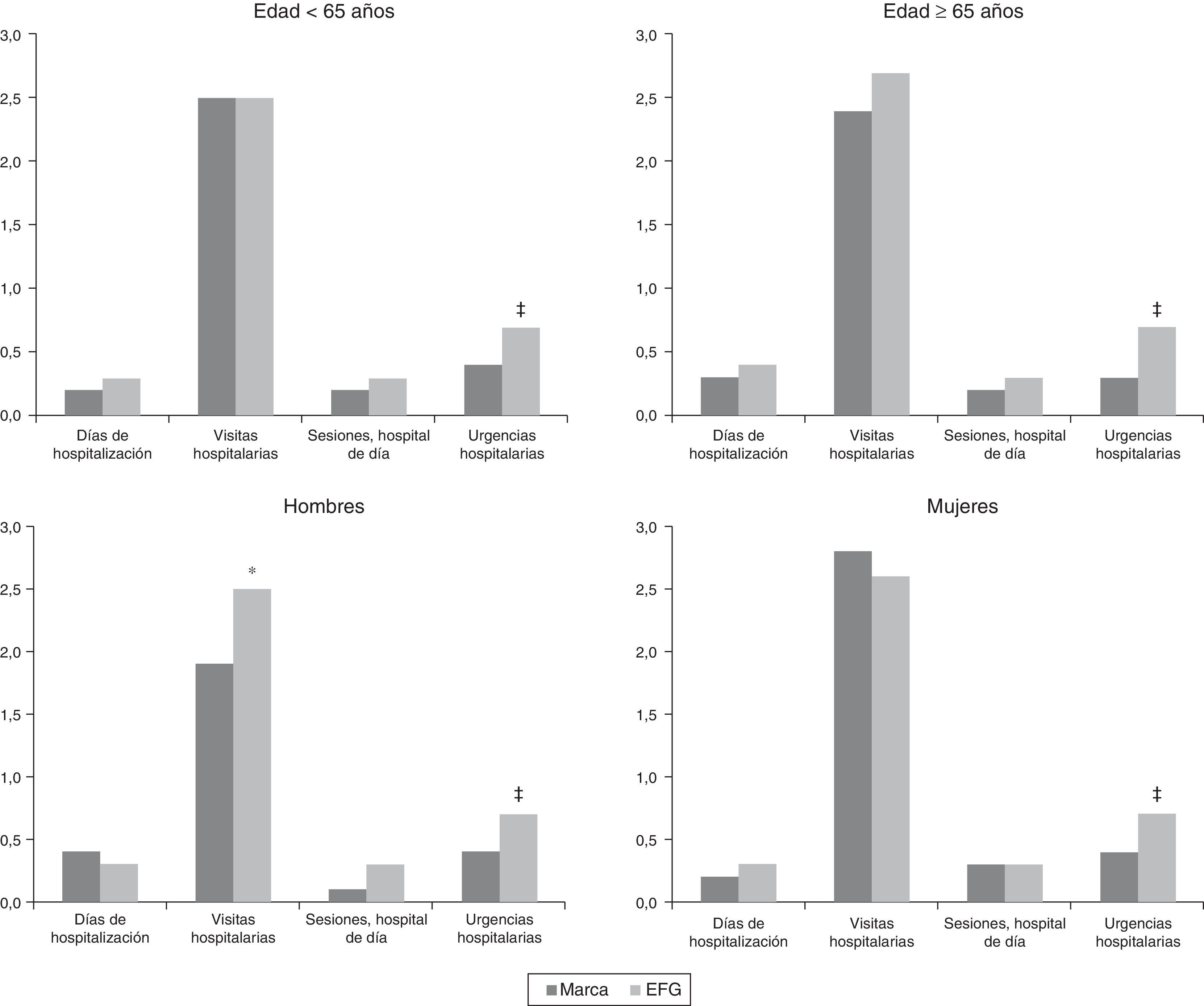
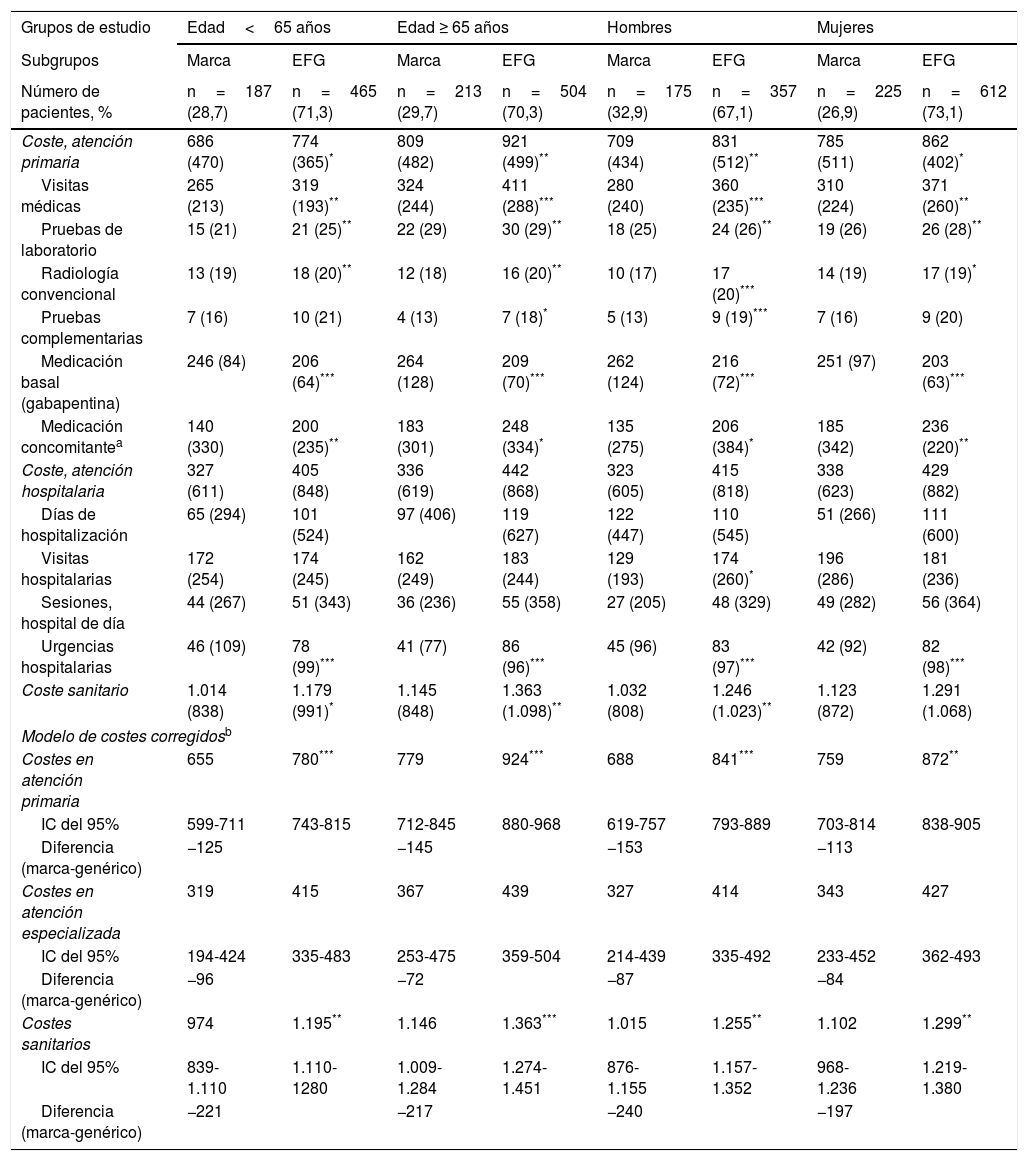
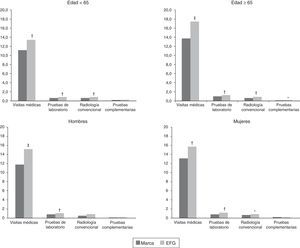
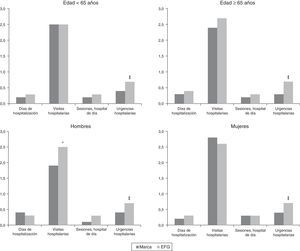
En las figuras 3 y 4 se muestra la comparación de marca vs. EFG en el uso de recursos sanitarios por los diferentes grupos de estudio. En general, los pacientes en tratamiento con gabapentina de marca utilizaron menos recursos sanitarios, especialmente en visitas médicas en atención primaria (12,5 frente a 15,5; p=0,001) y urgencias hospitalarias (0,4 frente a 0,7; p<0,001). Estas diferencias se constataron en los 4 grupos de estudio (edad y género). En la tabla 2 se detallan los diferentes componentes del coste sanitario según los grupos de estudio. El promedio/unitario del coste sanitario bruto fue mayor con la administración de EFG en comparación con la marca (1.275 vs. 1.083€; p<0,001), mientras que el coste sanitario corregido por covariables fue de 1.277 vs. 1.057€ (diferencia: 220€), respectivamente (p<0,001). Una parte de esta diferencia de costes entre marca vs EFG se observó en los costes producidos en atención primaria, puesto que las diferencias observadas en atención especializada no llegaron a ser estadísticamente significativas. Por grupos de estudio se mantuvieron estas diferencias (costes corregidos, ANOVA): en <65años, 974 vs. 1.195€ (p<0,001); b)en ≥65años, 1.146 vs. 1.363€ (p<0,001); c)en hombres, 1.015 vs. 1.255€ (p<0,001), y d)en mujeres, 1.102 vs. 1.299€ (p<0,01), respectivamente.
Costes sanitarios según los grupos de estudio
| Grupos de estudio | Edad<65 años | Edad ≥ 65 años | Hombres | Mujeres | ||||
|---|---|---|---|---|---|---|---|---|
| Subgrupos | Marca | EFG | Marca | EFG | Marca | EFG | Marca | EFG |
| Número de pacientes, % | n=187 (28,7) | n=465 (71,3) | n=213 (29,7) | n=504 (70,3) | n=175 (32,9) | n=357 (67,1) | n=225 (26,9) | n=612 (73,1) |
| Coste, atención primaria | 686 (470) | 774 (365)* | 809 (482) | 921 (499)** | 709 (434) | 831 (512)** | 785 (511) | 862 (402)* |
| Visitas médicas | 265 (213) | 319 (193)** | 324 (244) | 411 (288)*** | 280 (240) | 360 (235)*** | 310 (224) | 371 (260)** |
| Pruebas de laboratorio | 15 (21) | 21 (25)** | 22 (29) | 30 (29)** | 18 (25) | 24 (26)** | 19 (26) | 26 (28)** |
| Radiología convencional | 13 (19) | 18 (20)** | 12 (18) | 16 (20)** | 10 (17) | 17 (20)*** | 14 (19) | 17 (19)* |
| Pruebas complementarias | 7 (16) | 10 (21) | 4 (13) | 7 (18)* | 5 (13) | 9 (19)*** | 7 (16) | 9 (20) |
| Medicación basal (gabapentina) | 246 (84) | 206 (64)*** | 264 (128) | 209 (70)*** | 262 (124) | 216 (72)*** | 251 (97) | 203 (63)*** |
| Medicación concomitantea | 140 (330) | 200 (235)** | 183 (301) | 248 (334)* | 135 (275) | 206 (384)* | 185 (342) | 236 (220)** |
| Coste, atención hospitalaria | 327 (611) | 405 (848) | 336 (619) | 442 (868) | 323 (605) | 415 (818) | 338 (623) | 429 (882) |
| Días de hospitalización | 65 (294) | 101 (524) | 97 (406) | 119 (627) | 122 (447) | 110 (545) | 51 (266) | 111 (600) |
| Visitas hospitalarias | 172 (254) | 174 (245) | 162 (249) | 183 (244) | 129 (193) | 174 (260)* | 196 (286) | 181 (236) |
| Sesiones, hospital de día | 44 (267) | 51 (343) | 36 (236) | 55 (358) | 27 (205) | 48 (329) | 49 (282) | 56 (364) |
| Urgencias hospitalarias | 46 (109) | 78 (99)*** | 41 (77) | 86 (96)*** | 45 (96) | 83 (97)*** | 42 (92) | 82 (98)*** |
| Coste sanitario | 1.014 (838) | 1.179 (991)* | 1.145 (848) | 1.363 (1.098)** | 1.032 (808) | 1.246 (1.023)** | 1.123 (872) | 1.291 (1.068) |
| Modelo de costes corregidosb | ||||||||
| Costes en atención primaria | 655 | 780*** | 779 | 924*** | 688 | 841*** | 759 | 872** |
| IC del 95% | 599-711 | 743-815 | 712-845 | 880-968 | 619-757 | 793-889 | 703-814 | 838-905 |
| Diferencia (marca-genérico) | −125 | −145 | −153 | −113 | ||||
| Costes en atención especializada | 319 | 415 | 367 | 439 | 327 | 414 | 343 | 427 |
| IC del 95% | 194-424 | 335-483 | 253-475 | 359-504 | 214-439 | 335-492 | 233-452 | 362-493 |
| Diferencia (marca-genérico) | −96 | −72 | −87 | −84 | ||||
| Costes sanitarios | 974 | 1.195** | 1.146 | 1.363*** | 1.015 | 1.255** | 1.102 | 1.299** |
| IC del 95% | 839-1.110 | 1.110-1280 | 1.009-1.284 | 1.274-1.451 | 876-1.155 | 1.157-1.352 | 968-1.236 | 1.219-1.380 |
| Diferencia (marca-genérico) | −221 | −217 | −240 | −197 | ||||
EFG: especialidades farmacéuticas genéricas; IC: intervalos de confianza.
Valores expresados en media (desviación estándar) o porcentaje.
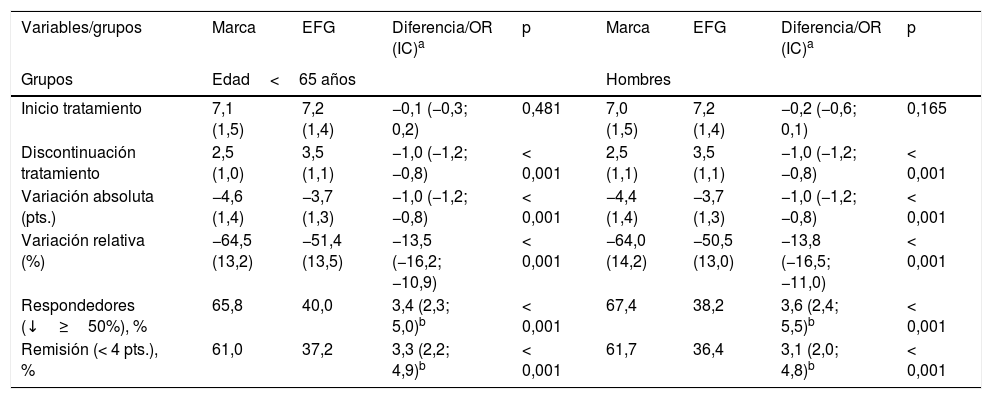
No se observaron diferencias estadísticamente significativas en las puntuaciones de las escalas de dolor al inicio del estudio. En la tabla 3 se detalla la variación de la intensidad del dolor entre inicio y discontinuación del tratamiento según grupos de estudio. Comparado con EFG, el tratamiento con marca mostró una reducción adicional del dolor basal: 13,5% (IC: 10,9-16,2) y 10,8% (IC: 8,2-13,5), en <65 y ≥65años, respectivamente (p<0,001 en ambos casos), y 10,7% (IC: 8,2-13,2) y 13,8% (IC: 11,0-16,5) en mujeres y hombres, respectivamente (p<0,001 en ambos casos).
Variación de la intensidad del dolor entre inicio y discontinuación del tratamiento según grupos de estudio
| Variables/grupos | Marca | EFG | Diferencia/OR (IC)a | p | Marca | EFG | Diferencia/OR (IC)a | p |
|---|---|---|---|---|---|---|---|---|
| Grupos | Edad<65 años | Hombres | ||||||
| Inicio tratamiento | 7,1 (1,5) | 7,2 (1,4) | −0,1 (−0,3; 0,2) | 0,481 | 7,0 (1,5) | 7,2 (1,4) | −0,2 (−0,6; 0,1) | 0,165 |
| Discontinuación tratamiento | 2,5 (1,0) | 3,5 (1,1) | −1,0 (−1,2; −0,8) | < 0,001 | 2,5 (1,1) | 3,5 (1,1) | −1,0 (−1,2; −0,8) | < 0,001 |
| Variación absoluta (pts.) | −4,6 (1,4) | −3,7 (1,3) | −1,0 (−1,2; −0,8) | < 0,001 | −4,4 (1,4) | −3,7 (1,3) | −1,0 (−1,2; −0,8) | < 0,001 |
| Variación relativa (%) | −64,5 (13,2) | −51,4 (13,5) | −13,5 (−16,2; −10,9) | < 0,001 | −64,0 (14,2) | −50,5 (13,0) | −13,8 (−16,5; −11,0) | < 0,001 |
| Respondedores (↓≥50%), % | 65,8 | 40,0 | 3,4 (2,3; 5,0)b | < 0,001 | 67,4 | 38,2 | 3,6 (2,4; 5,5)b | < 0,001 |
| Remisión (< 4 pts.), % | 61,0 | 37,2 | 3,3 (2,2; 4,9)b | < 0,001 | 61,7 | 36,4 | 3,1 (2,0; 4,8)b | < 0,001 |
| Grupos | Edad ≥ 65 años | Mujeres | ||||||
|---|---|---|---|---|---|---|---|---|
| Inicio tratamiento | 7,1 (1,5) | 7,2 (1,5) | −0,1 (−0,3; 0,2) | 0,516 | 7,2 (1,5) | 7,2 (1,5) | −0,1 (−0,2; 0,2) | 0,984 |
| Discontinuación tratamiento | 2,6 (1,1) | 3,4 (1,2) | −0,7 (−0,9; −0,5) | < 0,001 | 2,6 (1,1 | 3,4 (1,1) | −0,7 (−0,9; −0,5) | < 0,001 |
| Variación absoluta (pts.) | −4,4 (1,4) | −3,8 (1,4) | −0,7 (−0,9; −0,5) | < 0,001 | −4,5 (1,4) | −3,8 (1,5) | −0,7 (−0,9; −0,5) | < 0,001 |
| Variación relativa (%) | −62,6 (14,0) | −52,1 (14,6) | −10,8 (−13,5; −8,2) | < 0,001 | −63,0 (13,3) | −52,5 (14,7) | −10,7 (−13,2; −8,2) | < 0,001 |
| Respondedores (↓≥50%), % | 66,2 | 41,9 | 2,8 (2,0; 4,1)b | < 0,001 | 64,9 | 42,3 | 2,7 (1,9; 3,9)b | < 0,001 |
| Remisión (< 4 pts.), % | 58,7 | 39,7 | 2,3 (1,6; 3,3)b | < 0,001 | 58,2 | 39,7 | 2,4 (1,7; 3,4)b | < 0,001 |
EFG: especialidades farmacéuticas genéricas; IC: intervalo de confianza del 95%; OR: odds ratio; p: significación estadística.
Valores expresados como media (desviación típica) o porcentaje.
Mientras que en la literatura científica internacional y nacional se pueden localizar referencias al efecto diferencial de la marca original versus la EFG del mismo principio activo, y previamente hemos publicado nuestra experiencia en DNp9, sin embargo no hemos podido encontrar datos que analicen el efecto del género o de la edad sobre estos resultados, por lo que este estudio parece pertinente y oportuno. Los resultados observados ponen de manifiesto que gabapentina EFG en comparación con la marca original en pacientes con DNp se asoció a una menor persistencia del tratamiento y peores resultados clínicos (reducción del dolor), repercutiendo en un mayor uso de los recursos y costes sanitarios; y que estos hallazgos se reproducen cuando se analizan los datos por rangos de edad y género, mostrando diferencias en costes por paciente similares (en el rango de los 200€ por paciente y año de ahorro cuando se usa la marca original), a la vez que se muestran reducciones adicionales del dolor que alcanzan la significación estadística.
Es conocido que un medicamento EFG tiene la misma composición cualitativa y cuantitativa en principio activo y forma farmacéutica, con una bioequivalencia demostrada (estudios de biodisponibilidad) con el medicamento de referencia, aunque las diferencias en la composición de los excipientes y su apariencia externa son distintas, lo que puede ser responsable de problemas de bioapariencia y potencial efecto nocebo. La entrada al mercado de estos fármacos ha contribuido a una reducción en la factura farmacéutica de la sanidad pública, aunque actualmente en nuestro país medicamentos genéricos y los de marca presentan el mismo coste, por lo que a la luz de las normativas actuales no se encuentran argumentos farmacológicos que impidan indistintamente la prescripción de medicamentos de marca o EFG. Sin embargo, además de las conocidas razones de incumplimiento —que pueden ser intencionadas (factores sociodemográficos, efectos secundarios, precio de los medicamentos, falta de comprensión del tratamiento o del estado de salud, etc.) o no intencionadas (olvido de cómo tomar la medicación correctamente, etc.)—, los resultados del estudio muestran que la administración de un EFG podría considerarse un factor más a tener en cuenta; es posible que la bioapariencia o la prescripción de marcas de medicamentos EFG distintas, y no medidas en el estudio, pueda influir en nuestros resultados (falta de cumplimiento/adherencia). Entre estos factores figuran la distinta apariencia (colores, formas)24, la carencia de determinadas presentaciones (retardadas, liberación lenta o de absorción)25,26, variabilidad en cuanto a sus excipientes27, el efecto del copago28 o incluso como consecuencia del efecto nocebo29.
Sin una adecuada estandarización de las metodologías en cuanto a las características de los pacientes, así como en el número y medida de las variables estudiadas, los resultados obtenidos deben interpretarse con prudencia en su validez externa. Nuestros resultados muestran tasas de adherencia/persistencia al tratamiento de marca significativamente superiores a las del EFG. A pesar de que estos datos no están generalizados en la literatura, sí están en consonancia con diversos autores30,31. Los resultados de nuestro estudio muestran que el uso de EFG se asocia con un mayor uso de los recursos sanitarios y costes, con un grado de efectividad clínica algo inferior al medicamento de marca indistintamente del grupo de edad o género de los pacientes. La relación temporal existente entre la falta de adherencia, la menor efectividad clínica y un mayor uso de los recursos sanitarios está fuera de toda duda y es muy consistente en la bibliografía9,28-33. Estos datos son de difícil comparación por la falta de estudios publicados, como se mencionaba previamente. Tran et al.34 detallan que el uso de genéricos se asocia a una reducción de los objetivos terapéuticos de control (efectividad clínica: colesterol LDL) en el tratamiento de la dislipidemia, y Gagne et al.35, en un estudio prospectivo, observan que los pacientes que inician un tratamiento con estatinas genéricas frente a las de marca presentaban un mayor incumplimiento y mayores tasas de episodios cardiovasculares; son datos no generalizables, pero coincidentes con otros estudios publicados9,33.
Los resultados también detallan que el coste de los medicamentos de base fue mayor en los pacientes en tratamiento con gabapentina de marca, y se observó tanto en hombres como mujeres o en menores y mayores de 65años. Una posible explicación al respecto podría deberse a 3 circunstancias: a)el estudio ha tenido un periodo de inclusión de pacientes elevado (5 años), con lo que en los primeros años el precio de los medicamentos de marca era superior a los EFG (no estaban a precio de referencia); b)el cumplimiento terapéutico de estos pacientes también fue superior, y c)existe una mayor proporción de pacientes (especialmente en el grupo con gabapentina) que habían recibido dosis más altas del fármaco; aunque la explicación más plausible puede deberse a una mayor persistencia al tratamiento de marca9. No obstante, merece la pena resaltar que en los 4 grupos analizados la suma del coste de la medicación de base con la medicación concomitante para el dolor alcanzó magnitudes numéricamente inferiores (−20€, −10€, −25€ y −3€, respectivamente, en los grupos de <65años, ≥65años, hombres y mujeres, respectivamente) cuando se compara gabapentina de marca con gabapentina EFG.
Los resultados de este estudio sugieren algunas estrategias de intervención, sobre todo para los responsables políticos y de la administración sanitaria. Los cambios en la apariencia del fármaco pueden causar que los pacientes pierdan la confianza en la seguridad o eficacia de la prescripción genérica, repercutiendo en la falta de adherencia al tratamiento, especialmente en enfermedades crónicas y en pacientes polimedicados. La reducción de la variabilidad en la apariencia entre medicamentos químicamente idénticos podría ayudar a promover la adhesión13-15.
Las posibles limitaciones del estudio inciden en las propias de los estudios retrospectivos, como por ejemplo el infrarregistro de la enfermedad o la posible variabilidad de los profesionales y de los pacientes al ser un diseño observacional, o incluso al sistema de costes empleado, o a la posibilidad de la existencia de un sesgo de clasificación. En este aspecto, la posible inexactitud de la codificación diagnóstica en cuanto al diagnóstico de DNp, o bien la falta de alguna variable que pudiera influir en los resultados finales (nivel socioeconómico de los pacientes, evolución de la dosis farmacológica prescrita, cambios de forma y presentación en los EFG, etc.), deben considerarse como una limitación del estudio. Además, no se pudieron obtener los datos en todos los pacientes, como la medida de efectividad clínica, especialmente en el periodo final; no obstante, este impedimento quedó repartido de forma similar entre los subgrupos de estudio, y el hecho de que se hiciera una imputación muy conservadora (peor valor disponible) confiere cierta robustez a los resultados observados. Aunque a nuestro entender la principal objeción al estudio fueron: a)el sesgo de selección por parte del médico responsable a la hora de iniciar el tratamiento de marca o EFG, puesto que no se realizó de forma aleatoria, como es habitual en la práctica clínica diaria, y b)en la validez externa de los resultados (generalización de los datos), puesto que el estudio se ha realizado en una única entidad proveedora de servicios sanitarios, por lo que la interpretación de los resultados debe efectuarse con prudencia.
Las perspectivas futuras que nos ofrece este estudio se centran en replicarlo en otras instituciones sanitarias y en promover estrategias de intervención orientadas a fomentar la adherencia de los pacientes a los tratamientos prescritos por sus médicos. En conclusión, y teniendo en cuenta las limitaciones apuntadas, este análisis ha mostrado que los pacientes que iniciaron tratamiento con gabapentina de marca vs. genérico se asociaron a un mayor grado de adherencia al tratamiento, repercutiendo en unos menores costes sanitarios, a la vez que se observaron mejores resultados clínicos en la reducción del dolor, y que estos hallazgos fueron similares tanto en hombres como en mujeres, y tanto en <65 como en ≥65años.
AutoríaLa concepción y el diseño del estudio fueron realizados por A. Sicras y J. Rejas; la recogida de los datos y el análisis estadístico, por A. Sicras, y la interpretación de los datos, la redacción, la revisión y la aprobación del manuscrito remitido, por todos los autores.
Conflicto de interesesJ. Rejas y María Pérez son empleados de Pfizer SLU. Los demás autores declaran no tener conflictos de intereses.