La hipofosfatemia se define por una concentración de fósforo (P)1 inferior a 2,5mg/dl. Su incidencia en pacientes hospitalizados es elevada, sobre todo en pacientes sépticos, malnutridos o alcohólicos, donde se asocia a mayor morbimortalidad. Las manifestaciones clínicas aparecen cuando los niveles de P son inferiores a 1mg/dl, pero estas manifestaciones son muy diversas y nada específicas, lo que puede retrasar su diagnóstico2.
Presentamos el caso de un varón de 69 años, con trasplante renal de cadáver e insuficiencia renal, con episodios transitorios de pérdida de conciencia secundarios a hipofosfatemia grave.
Caso clínicoVarón de 69 años con antecedentes personales de exfumador, hipertensión arterial, dislipemia, cardiopatía isquémica con angioplastia coronaria transluminal percutánea (ACTP) e implantación de stent en descendente anterior, diagonal y coronaria derecha con reestenosis posterior y nueva ACTP-stent, estenosis e insuficiencia aórtica moderada, insuficiencia mitral leve, insuficiencia tricuspídea leve-moderada, miocardiopatía dilatada de origen isquémico, flutter auricular, nefrectomía por cáncer papilar, insuficiencia renal crónica estadio V-D secundaria a nefropatía isquémica en programa de hemodiálisis desde febrero 2009 con trasplante renal de cadáver en marzo 2013, diverticulosis colónica con intervención quirúrgica por perforación colónica tras colonoscopia, ulcus duodenal, necrosis avascular de rótula y cabeza de fémur, brucelosis y fiebre botonosa. Su tratamiento incluía tacrolimus, ácido micofenólico, furosemida, prednisona, acenocumarol, ramipril, lansoprazol, ácido acetilsalicílico, eplerenona, alopurinol, metoprolol, solifenacina y nitroglicerina.
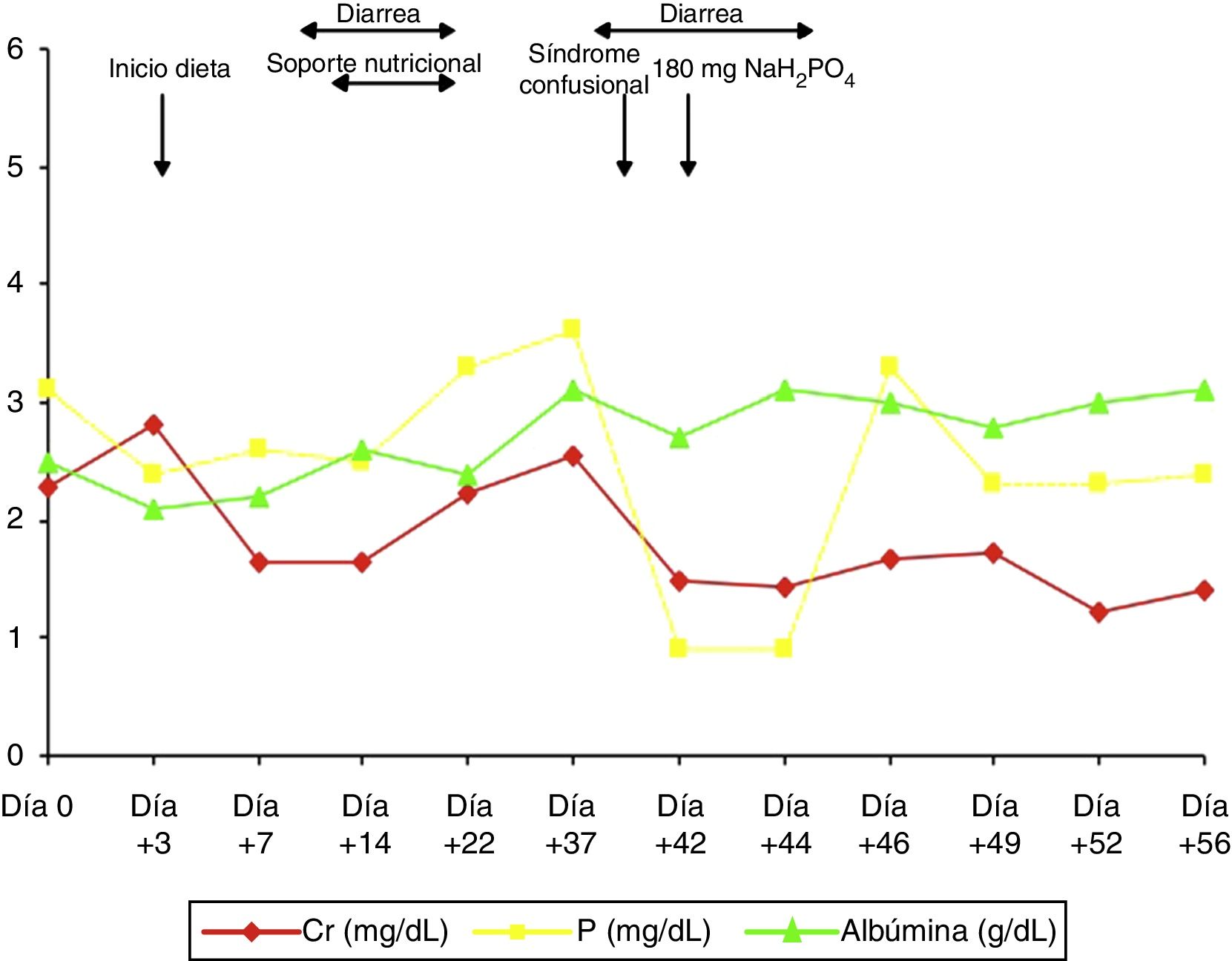
El paciente ingresa por shock séptico secundario a colecistitis aguda en la unidad de vigilancia intensiva tras realizarle colecistectomía abierta, por lo que estuvo varios días a dieta absoluta. Su evolución clínica inicial fue buena con retirada progresiva de los fármacos inotrópicos y de los esteroides, pautados a altas dosis (hidrocortisona 100mg/8h) por sospecha de insuficiencia suprarrenal relativa, pero con marcada anorexia, episodios de diarrea de repetición atribuidos al tratamiento antibiótico que provocaron reagudizaciones de la insuficiencia renal y acidosis metabólica secundaria tratada con bicarbonato y desnutrición progresiva (fig. 1). Se trasladó a cirugía general el día +21 de ingreso por evolución tórpida de la herida quirúrgica, donde continuó con tratamiento antibiótico, desbridamiento de la herida y curetaje diario. Ante la desnutrición progresiva se pautó soporte nutricional con una emulsión para perfusión de lípidos, aminoácidos y glucosa, que contenía 24mmol de fosfato (744mg), y que requería tratamiento simultáneo con insulina, pero tuvo que ser retirado por aumento de la diarrea. El día +38, el paciente presentó episodio transitorio de bajo nivel de conciencia con desorientación y desconexión del medio fluctuante, sin respuesta a estímulos verbales ni dolorosos. Dicho cuadro clínico se repitió 24h después, por lo que ante la sospecha de intoxicación por benzodiacepinas se decidió administrar ½ ampolla de flumazenilo y suspender el alprazolam, sin mejoría clínica. Nos avisan el día +45 por un nuevo evento clínico similar a los referidos previamente. A la exploración física destacaba PA 110/80mmHg, FC 90lpm y saturación de oxígeno del 98%, estaba obnubilado, con un índice de Glasgow 9/15, desorientado en tiempo y espacio, sin obedecer a órdenes sencillas y con ecolalia. La exploración de los pares craneales y reflejos era normal, el paciente movilizaba las 4 extremidades, pero con debilidad y temblor tanto en extremidades superiores como inferiores. La valoración del déficit sensitivo resultaba difícil por la poca colaboración del paciente. En el control analítico presentaba urea 51mg/dl, Cr 1,43mg/dl, Ca 10,3mg/dl, P 0,9mg/dl, Na 136mmol/l,K 3,6mmol/l, Cl 99mmol/l, con CK y CK-MB normales, gasometría venosa: pH 7,46, PCO2 43mmHg y bicarbonato real 30,6mmol/l. La TAC cerebral no mostró signos de isquemia. Ante la sospecha de deterioro neurológico secundario a hipofosfatemia grave se inició tratamiento con 180mg de fosfato monosódico a pasar en 8h, con mejoría clínica progresiva y desaparición de las manifestaciones clínicas (fig. 1), siendo dado de alta tras 56 días de ingreso.
DiscusiónLa hipofosfatemia se define por una concentración anormalmente baja de P en suero o plasma1. Si la concentración sérica está entre 1 y 2,5mg/dl se considera hipofosfatemia moderada, que normalmente no produce signos ni síntomas; estos sí aparecen en presencia de hipofosfatemia grave, con concentraciones de P inferiores a 1mg/dl2.
La incidencia de hipofosfatemia moderada en enfermos hospitalizados es del 5%, siendo menos frecuente la hipofosfatemia grave (0,1-0,2%)1,2. No obstante, en determinados grupos de riesgo como alcohólicos o sépticos, la prevalencia puede llegar al 30 e incluso al 80%, respectivamente. Su presencia se asocia a mayor mortalidad tanto en ingresados como en pacientes en diálisis.
La hipofosfatemia puede generarse por 4 mecanismos2,3: 1) Redistribución del fosfato desde el espacio extracelular al espacio intracelular, 2) Disminución en la absorción intestinal, 3) Aumento en la excreción urinaria, y 4) Disminución por terapias de reemplazo.
Las manifestaciones clínicas aparecen cuando coexisten cifras inferiores a 1-1,5mg/dl y disminución crónica del fósforo. La base etiopatogenia de dichas manifestaciones es un descenso de 2,3-DPG intraeritrocitario y del ATP intracelular. Es frecuente la aparición de hipercalciuria y osteomalacia, y puede haber descenso del gasto cardiaco que puede producir insuficiencia cardiaca congestiva y fracaso respiratorio por afectación muscular. En el músculo esquelético es frecuente la miopatía proximal, e incluso la rabdomiólisis. A nivel del sistema nervioso se ha descrito la aparición de encefalopatía metabólica, con crisis comiciales y coma, y con P inferiores a 0,5mg/dl, hemólisis1,2. En cuanto al tratamiento, la hipofosfatemia leve no requiere tratamiento. Si es moderada, además de tratar la causa, se deberían dar suplementos orales. La vía intravenosa debe utilizarse en los casos de hipofosfatemia grave con peligro de muerte, insuficiencia respiratoria, convulsiones, coma, o cuando no pueden recibir medicación oral4. Se puede comenzar la administración, dependiendo del resto de los iones, en forma de fosfato monosódico o monopotásico a dosis de 2,5-5mg/kg de peso según la gravedad5. El mejor tratamiento de la hipofosfatemia es la prevención. Los pacientes con nutrición parenteral total deben recibir un aporte de fósforo de 1.000mg/24h.
La enfermedad cardiovascular es la primera causa de muerte tras el trasplante renal. El riesgo actual de mortalidad por enfermedad cardiovascular es 50 veces superior al de la población general debido a la aglutinación de factores de riesgo cardiovasculares. Casi la mitad de las muertes de origen cardiovasculares postrasplante se deben a enfermedad cerebrovascular secundaria a ictus, siendo la ateromatosis cerebrovascular más frecuente en trasplantados renales. Sin embargo, la sintomatología sugerente de accidente cerebrovascular, puede ser secundaria a trastornos iónicos graves, lo que debe tenerse en cuenta a la hora de hacer el diagnóstico diferencial.
En nuestro caso, se trataba de un paciente trasplantado renal con numerosos factores de riesgo cardiovascular y niveles de P basales normales, que presentó hipofosfatemia grave consecuencia de la desnutrición progresiva producida por el cuadro séptico, el síndrome diarreico, el ingreso prologado con ingesta alimentaria reducida y el soporte nutricional pautado con escaso aporte de P. Además, al paciente se le prescribió tratamiento con corticoides, bicarbonato, insulina y diuréticos, todos ellos causantes de hipofosfatemia. La no inclusión de la determinación de P en los controles analíticos rutinarios, casi diarios, retrasó tanto el diagnóstico como el tratamiento.
En resumen, a pesar de que los pacientes trasplantados renales tienen elevada morbimortalidad cardiovascular, secundaria en muchas ocasiones a enfermedad cerebrovascular, trastornos iónicos como la hipofosfatemia grave, pueden simular accidentes cerebrovasculares, lo que debe tenerse en cuenta a la hora de hacer el diagnóstico diferencial. Debemos incluir la determinación de P en los controles analíticos seriados de pacientes, críticos o con ingresos prolongados, con el objetivo de establecer un diagnóstico precoz e instaurar las medidas nutricionales preventivas adecuadas.
FinanciaciónNo hemos recibido financiación para la realización de este artículo.
Conflicto de interesesLos autores de este artículo no tienen ningún conflicto de intereses que declarar.