Los neonatos a término con cardiopatía congénita (CC) tienen mayor incidencia de enterocolitis necrosante (ECN) (3-7%) que los demás neonatos a término, en lo que es rara la ECN1-3. La CC puede subyacer a entre la cuarta y la tercera parte de los casos de ECN en esta población de pacientes2,4,5.
La mala circulación sistémica, de duración prolongada o episódica, es un mecanismo que ha demostrado su contribución al desarrollo de ECN en los neonatos con 1,2,6. Es interesante que McElhinney et al1 observasen, en su gran análisis retrospectivo de ECN en neonatos con CC, que los neonatos con síndrome de hipoplasia de cavidades izquierdas, tronco arterioso y ventanaaortopulmonar tuvieran mayor riesgo de ECN. Éstas son lesiones anatómicas cardíacas que provocan, típicamente, una evidente inversión del flujo anterógrado en la aorta abdominal durante la diástole y una tensión diastólica resultante baja. Postularon que el flujo diastólico retrógrado en estas lesiones pudo desembocar en la insuficiencia de la circulación mesentérica debida a un fenómeno de “robo” diastólico.
La evaluación Doppler del flujo aórtico abdominal es un método para evaluar este fenómeno de “robo”. Investigadores anteriores han observado una disminución o inversión del flujo diastólico en la aorta descendente y en otras arterias abdominales en los neonatos prematuros con persistencia sintomática del conducto arterial7 (PCA). Sin embargo, no se ha realizado la evaluación sistemática de las características Doppler de la aorta abdominal en los neonatos a término con CC.
Supusimos que las características Doppler de la aorta abdominal pueden detectar por adelantado a un subgrupo de neonatos a término con CC que corren especial riesgo de ECN, independientemente de su tipo de lesión cardíaca. Así pues, realizamos un estudio de casos y controles igualados por edad gestacional y diagnóstico para investigar los determinantes del riesgo de ECN en neonatos a término con CC, incorporando las características Doppler del flujo abdominal.
PACIENTES Y MÉTODOSEl IRB aprobó la revisión de los datos, las imágenes y los registros médicos existentes, de acuerdo con la normativa HIPAA. La búsqueda en la base de datos de registros médicos hospitalarios identificó a 18 pacientes con CC y ECN, confirmada radiológica o quirúrgicamente, en el Cincinnati Children’s Hospital Medical Center entre 1999 y julio de 2005. Todos los datos clínicos y demográficos relevantes se extrajeron del registro médico. Para clasificar la gravedad de la ECN confirmada se utilizaron los criterios de Bell modificados8 (estadios 2a, 2b, 3a y 3b) (tabla 1).
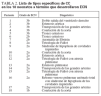
TABLA 1. Criterios de la clasificación de Bell modificada para el diagnóstico de la ECN
Los controles se seleccionaron del mismo período de tiempo. Fueron identificados inicialmente mediante el diagnóstico de la base de datos ecocardiográficos, luego se igualaron a los casos por edad gestacional y, finalmente, fueron incluidos si tenían imágenes ecocardiográficas adecuadas tomadas a una edad pos-natal similar a la de los casos. Esto consiguió la inclusión de 20 pacientes en el grupo de controles. Para la evaluación se seleccionó la ecocardiografía inmediatamente anterior al desarrollo de la ECN. En el grupo de control, las ecocardiografías se seleccionaron por su proximidad al día de vida de sus homónimos con ECN. Se seleccionó para el análisis la imagen del eje longitudinal de la aorta abdominal con subsiguiente onda Doppler pulsada. Las señales Doppler posteriores a octubre de 2003 se obtuvieron digitalmente con Vivid 7 (General Electric Corp.,
Stamford, CT) y se analizaron en un sistema Camtronics de análisis cardíaco (Hartland, WI). Antes de ese momento, las señales Doppler se registraron con una cámara Sonos 5500 (Agilent, Andover, MA) para ser luego analizadas con un sistema Digisonic de análisis cardíaco sin conexión (Houston, TX).
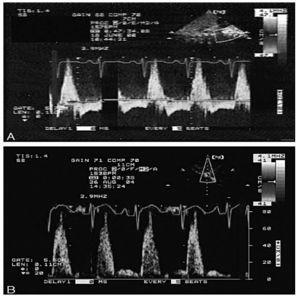
En cada paciente se midieron y promediaron al menos tres ondas Doppler respecto a las integrales de tiempo-velocidad, las velocidades máximas y el tiempo de los flujos tanto anterógrado como retrógrado en la aorta abdominal, la descendente torácica, o ambas. La proporción de inversión del flujo Doppler (proporción de IFD) se calculó dividiendo la integral de tiempo-velocidad del flujo retrógrado por la del flujo anterógrado, según el desarrollo de Rychik et al9. Las proporciones de tiempo retrógrado a anterógrado se calcularon dividiendo el tiempo transcurrido en flujo retrógrado por el transcurrido en flujo anterógrado. Se anotó la presencia o ausencia de inversión persistente del flujo diastólico Doppler (figura 1). Un solo investigador (WFC), desconocedor del estado del sujeto (caso o control), realizó todas las mediciones.
Fig. 1. Trazados Doppler del flujo, obtenidos en la imagen longitudinal abdominal en neonatos con CC. “A” muestra la inversión persistente del flujo diastólico en la aorta descendente, manifiesto por el flujo retrógrado persistente, inferior a la basal en diástole. “B” muestra un perfil Doppler normal del flujo, con una breve inversión temprana del flujo diastólico seguida de un flujo diastólico anterógrado persistente, por encima del basal.
El análisis estadístico se realizó mediante Intercooled Stata 8.2 (StataCorp, TX). Los datos continuos de distribución normalse compararon entre los grupos mediante tests t independientes, y en los datos sesgados se utilizó el test de suma de rango de Wilcoxon. Las variables categóricas fueron comparadas con el análisis χ2. Los factores independientes de predicción de la ECN se identificaron inicialmente mediante el análisis de regresión univariado. Estas variables independientes se introdujeron luego en un modelo de regresión logística múltiple anterógrado gradual, con el desarrollo de ECN como variable dependiente.
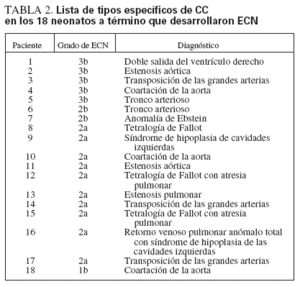
RESULTADOSSe recogieron 18 pacientes con ECN y 20 pacientes de control. La tabla 2 muestra los diagnósticos cardíacos de los pacientes con ECN. Diecisiete de los 18 pacientes con ECN correspondieron a casos de ECN según los criterios de clasificación de Bell modificados (estadio 2a en 10 pacientes, estadio 2b en 2 y estadio 3b en 5). Un paciente clasificado de estadio 1b mediante los criterios de Bell modificados fue incluido en el análisis del grupo de ECN confirmada por presentar confirmación quirúrgica en la cirugía exploradora de distensión abdominal y constricciones realizada tres semanas después, aunque la ecocardiografía analizada coincidió con el diagnóstico clínico de ECN estadio 1b. Además, dos de los pacientes en estadio 2a y todos los pacientes en estadio 3b tuvieron una ECN confirmada quirúrgicamente. Fallecieron dos de los pacientes con ECN en estadio 3b.
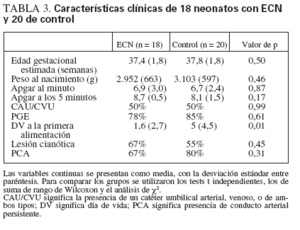
La ECN se confirmó en estos 18 neonatos a una mediana de 5 días de vida (límites 1-24 días). No hubo diferencias entre los neonatos con ECN y los de control respecto al peso al nacimiento, la edad gestacional estimada, las puntuaciones de Apgar, la presencia de CAU o CVU, el empleo de prostaglandinas o inotropos en cualquier momento antes del desarrollo de la ECN, la presión del pulso, la presencia de PCA, la función sistólica y los tipos de lesiones cardíacas (tabla 3). Los pacientes con ECN recibieron alimento significativamente antes que los controles. Cinco de los pacientes con ECN se habían sometido a cateterización cardíaca antes de desarrollar la ECN, y cuatro a cirugía cardíaca. La mediana de la edad de realización de las ecocardiografías analizadas fue 2 días de vida (límites 0-21 días) para los pacientes con ECN y 1 día de vida (límites 0-15 días) para los pacientes de control (p = 0,61). El intervalo medio entre la ecocardiografía y el diagnóstico de ECN en los neonatos afectos fue de 3 días.
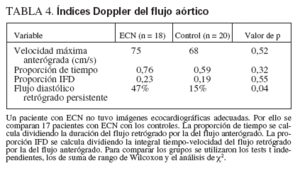
Las mediciones Doppler de las velocidades máximas, los intervalos de tiempo y las proporciones IFD no fueron significativamente distintas entre los grupos (tabla 4). Sin embargo, el 47% de los casos de ECN mostró un flujo diastólico retrógrado persistente en la aorta abdominal, frente al 15% de los controles (p = 0,04). Además, todos los pacientes con ECN estadio 2b o 3b, menos uno (86%), mostraron flujo diastólico retrógrado persistente.
TABLA 2. Lista de tipos específicos de CC en los 18 neonatos a término que desarrollaron ECN
TABLA 3. Características clínicas de 18 neonatos con ECN y 20 de control
TABLA 4. Índices Doppler del flujo aórtico
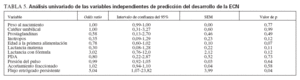
La tabla 5 presenta los resultados del análisis univariado de las variables independientes de predicción de la ECN. La presencia de flujo retrógrado persistente en la aorta abdominal fue la única variable que alcanzó la significación estadística (p = 0,04). Se observó una tendencia al aumento de la incidencia de la ECN en los pacientes que fueron alimentados precozmente o con fórmula, aunque la asociación no fue estadísticamente significativa. La presencia de catéteres umbilicales, arteriales o venosos, y el empleo de PGE no se asociaron con la probabilidad de desarrollar ECN.
TABLA 5. Análisis univariado de las variables independientes de predicción del desarrollo de la ECN
Tras el ajuste respecto al peso del neonato, la presencia de un catéter arterial umbilical, la presión del pulso, la edad a la primera alimentación y el tipo de alimentación en un modelo multivariado anterógrado gradual, el flujo diastólico retrógrado persistente fue el único factor independiente significativo de predicción de la ECN que persistió en el modelo (OR = 11,2 [1,6-78,5]).
DISCUSIÓNEste estudio de casos y controles observó que la inversión persistente del flujo diastólico en la aorta descendente se asoció con un aumento de la probabilidad de ECN en los niños a término con CC. Este aumento del riesgo persiste pese a igualar los pacientes respecto a la edad gestacional y al tipo anatómico de cardiopatía congénita.
Este estudio asocia los marcadores ecocardiográficos de la insuficiencia mesentérica con el aumento de riesgo de ECN. Coombs et al observaron menores velocidades del flujo sanguíneo en las arterias mesentéricas superiores de neonatos prematuros considerados en máximo riesgo de desarrollar ECN, aunque sólo el 11% de estos pacientes la desarrollasen10. Los estudios ecocardiográficos fetales han demostrado la ausencia o la inversión de las frecuencias telediastólicas en las arterias umbilicales11 y en la aorta12 de los fetos que luego desarrollaron ECN como neonatos prematuros. Estudios anteriores han demostrado el aumento de las velocidades del flujo en las arterias abdominales de neonatos que ya habían desarrollado ECN, aunque estos estudios no investigaron los patrones de flujo anteriores al desarrollo de la ECN13,14.
Nuestros resultados apoyan la teoría de que la insuficiencia circulatoria mesentérica secundaria al fenómeno del “robo” diastólico en los pacientes con CC puede predisponer a la ECN. Se observó flujo diastólico retrógrado persistente en los pacientes con ECN y una serie de lesiones de CC: dos con retorno venoso pulmonar anómalo total; dos con coartación de la aorta, y uno con cada una de las siguientes, estenosis aórtica, tronco arterioso y anomalía de Ebstein. Los tres pacientes de control con flujo diastólico retrógrado persistente mostraron coartación de la aorta, estenosis aórtica y tronco arterioso. Todos estos pacientes mostraban PCA, excepto los dos con tronco arterioso. Por lo tanto, todos los pacientes con flujo diastólico retrógrado persistente pudieron tener una derivación circulatoria. Sin embargo, la mayoría de los pacientes sin flujo diastólico retrógrado persistente en nuestro estudio también mostró PCA. Además, no hubo diferencia global de PCA entre los pacientes de control y los afectos de ECN. Por lo tanto, aunque la derivación circulatoria probablemente desempeñe un papel en la patogénesis de la ECN en los neonatos con CC, falta esta situación fisiológica antes de algunos episodios de ECN. Esto indica que, pese a la existencia del sustrato anatómico para el escape diastólico, no todos los pacientes lo muestran y su grado varía entre pacientes similares. Otros factores, como la resistencia vascular pulmonar, pueden ser responsables de parte de esta variación.
Una hipótesis alternativa de la fisiopatología de la ECN en estos pacientes es la presencia de episodios discretos de mala perfusión sistémica, que provocan directamente una insuficiencia mesentérica. McElhinney et al observaron que los episodios de mala perfusión periférica o shock impusieron a los neonatos con CC un riesgo adicional de ECN1. Leung et al observaron mayores tasas de apnea e hipotensión asociadas con prostaglandina en los neonatos con CC que posteriormente desarrollaron ECN2. Nuestro estudio no abordó directamente esta hipótesis. Sin embargo, no encontramos una asociación significativa entre el desarrollo de ECN y el empleo de prostaglandinas, el de inotropos, la cateterización cardíaca o la cirugía. Es probable que los neonatos con CC sean susceptibles a alguno de estos mecanismos fisiopatológicos, o a todos.
Nuestro estudio analizó otros posibles factores de riesgo de enterocolitis necrosante. Quizá por el pequeño tamaño del estudio no encontramos diferencias significativas entre los pacientes de control y los afectos de ECN respecto a la presencia de PCA, las puntuaciones de Apgar y la cateterización de los vasos umbilicales2-4,6. Además, nuestro estudio igualó a los neonatos por edad gestacional, por lo que no estuvo diseñado para encontrar diferencias de edad o peso al nacimiento, factores ambos de riesgo de ECN en los neonatos con CC1. Observamos una tendencia a la menor edad de la primera alimentación y a la alimentación con fórmula en los pacientes que desarrollaron ECN, aunque no fue estadísticamente significativa. Esto concuerda con hallazgos anteriores6, aunque el mayor de los estudios sobre neonatos con CC, de McElhinney et al, no encontró asociación entre lactancia materna o alimentación precoz y ECN1.
Las limitaciones de este estudio consisten en el variable intervalo de tiempo entre las ecocardiografías y el diagnóstico de ECN. Además, el empleo de una sola ecocardiografía, inmediatamente anterior a la detección de la ECN, podría no ser ideal porque las agresiones circulatorias pueden ser episódicas o haber ocurrido con anterioridad en el período posnatal. Finalmente, nuestro relativamente pequeño tamaño de la muestra nos impone un riesgo de error tipo II, especialmente respecto a la evaluación de otros factores independientes, posiblemente significativos, de predicción de la ECN.
CONCLUSIONESNuestra investigación de los patrones ecocardiográficos Doppler del flujo sanguíneo aórtico descendente revela que la inversión persistente del flujo diastólico se asocia con un aumento del riesgo de ECN en los niños a término con CC, independientemente de diagnóstico anatómico y la edad gestacional. Este hallazgo apoya la hipótesis de que el “robo” diastólico mesentérico desempeña un papel en la patogénesis de la ECN. La visualización rutinaria de la aorta abdominal descendente debe ser la norma de cualquier ecocardiografía, de forma que la observación de una inversión persistente del flujo diastólico pueda despertar la sospecha clínica de ECN en los neonatos con CC y síntomas clínicos compatibles.
Correspondencia: Waldemar F. Carlo, MD, Division of Cardiology, Cincinnati Children’s Hospital Medical Center, 3333 Burnet Ave, Cincinnati, OH 45229, Estados Unidos.
Correo electrónico: waldemar.carlo@cchmc. org