En Estados Unidos la otitis media aguda es la razón más frecuente para administrar tratamiento antibiótico en niños pequeños1. Los estudios observacionales sugieren que un 5-21% de los casos requieren una segunda tanda de antibióticos para obtener la resolución2-5. Las tasas nacionales del uso de antibióticos para este proceso han disminuido en los últimos años6,7. No obstante, se desconoce si, en la última década, ha cambiado la probabilidad de fracaso del tratamiento o recidiva tras una tanda inicial de antibióticos.
Las preocupaciones acerca de la resistencia antimicrobiana entre Streptococcus pneumoniae y otras bacterias causantes de OMA destacan la necesidad de disponer de información actual sobre el fracaso del tratamiento y la recidiva de la infección8. En 1999, los Centers for Disease Control and Prevention (CDC) recomendaron que en niños en riesgo alto de resistencia antibiótica la OMA se tratara con dosis altas de amoxicilina o cefuroxima9. En 2004, la American Academy of Pediatrics (AAP) amplió estas recomendaciones sugiriendo que la OMA se tratara con dosis altas de amoxicilina en todos los niños de hasta 12 años de edad1. Apenas se dispone de datos sobre hasta qué punto se ha adoptado ampliamente esta pauta de dosis altas en la práctica real y si su administración ha afectado a las tasas de fracaso del tratamiento o recidiva de la infección.
Para abordar estas lagunas en los conocimientos, condujimos un estudio de visitas para OMA en un consultorio multiespecialidad desde 1996 hasta 2004. Los objetivos del presente estudio fueron: 1) describir las tendencias en el diagnóstico inicial de la infección y fracaso del tratamiento y recidiva; 2) describir las tasas de administración de dosis altas de amoxicilina para tratar la OMA no complicada; y 3) evaluar si este tratamiento se asoció con una menor probabilidad de fracaso del tratamiento o recidiva.
MÉTODOSDiseño del estudio y recolección de datosCondujimos un estudio observacional, retrospectivo, de niños que recibían asistencia a partir de Harvard Vanguard Medical Associates (HVMA), un grupo multiespecialidad con 14 consultorios donde alrededor de 80 pediatras asisten a aproximadamente 275.000 pacientes en la mayor área de Boston. Los datos informatizados sobre visitas ambulatorias y fármacos de prescripción se obtuvieron a partir de los datos de solicitudes de la Harvard Pilgrim Health Care, una mutua sanitaria sin fines de lucro. Sólo se incluyeron los pacientes HVMA asegurados por ésta.
Población del estudioLa población del estudio incluyó a niños de 2 meses a 12 años de edad con, al menos, 90 días de cobertura por la mutua entre el 1 de enero de 1996 y el 31 de diciembre de 2004. Las visitas para otitis media aguda (OMA) no complicada se definieron como las que tenían: 1) un código de la Clasificación Internacional de las Enfermedades (CIE) 9-CM para OM [381.µ; 382.µ]; 2) una prescripción de antibiótico extendida en un plazo de 3 días de la visita, y 3) ninguna otra visita para OM tratada con antibióticos durante los 30 días previos. Excluimos las visitas para OM relacionadas con una prescripción extendida para sulfisoxazol o prescripciones de antibióticos con un suministro de más de 14 días, puesto que estos patrones sugerían que se estaban administrando antibióticos para la profilaxis de la infección. También excluimos las solicitudes para otitis media en niños hospitalizados y para visitas ambulatorias efectuadas por niños con drepanocitosis, fibrosis quística, asplenia, infección por VIH o cáncer10.
Principales variables analizadasLas dos principales variables analizadas fueron el fracaso del tratamiento de la OM y su recidiva, según lo definido por Pichichero11. Específicamente, definimos el fracaso del tratamiento como el que se produjo después de una visita para OMA no complicada si una segunda visita se asoció con una prescripción extendida de un antibiótico diferente y tuvo lugar antes de que se hubiera completado la inicial. Definimos la recidiva como la que aconteció tras una visita para OMA no complicada si la segunda visita asociada a la prescripción extendida de un antibiótico diferente tuvo lugar después de completar la prescripción índice pero en un plazo de 30 días de la visita inicial. En este análisis sólo se incluyó la primera incidencia de fracaso del tratamiento o recidiva después de cada visita para OMA no complicada.
Variables independientesDefinimos las “dosis altas de amoxicilina”, la principal variable pronóstica del presente análisis, como una dosis µ 70 mg/ kg/día y la “dosis habitual de amoxicilina” como una dosis < 70 mg/kg/día. Este umbral fue similar al mencionado en las guías de los CDC y AAP que definen las dosis altas de este antimicrobiano como 80-100 mg/kg/día. Otras variables pronósticas incluyeron la edad y sexo del paciente, año de calendario del diagnóstico de la OM índice y número de OM no complicadas que el paciente había experimentado antes del episodio que se estaba analizando. Clasificamos la edad de los pacientes en el día de la visita como 2-6 meses, 7-11 meses, 1-2 años, 3-4 años y 5-12 años. Definimos “el lugar de la asistencia” como la localización clínica donde se diagnosticó la infección. Para determinar los antecedentes de OM, calculamos el número de visitas para OMA que el paciente había efectuado entre el nacimiento y la visita para cada infección, al igual que el número efectuado en los meses previos a la visita para cada OMA.
Análisis estadísticoCalculamos las tasas de incidencia anual12 (densidad de incidencia) de la OMA no complicada, fracaso del tratamiento y recidiva dividiendo el número de acontecimientos por años-perso-na en observación durante cada año. Para cada año, se calcularon las tasas de incidencia del fracaso del tratamiento y la recidiva de la infección no complicada. Después de ponderar las categorías de edad por mes, calculamos las tasas de OMA ponderadas estratificadas por la categoría de edad. Para determinar si las tasas de incidencia de los resultados diferían por año, edad o antibiótico prescrito, al mismo tiempo que teníamos en cuenta los individuos que efectuaron múltiples visitas para OMA no complicadas, utilizamos modelos mixtos lineales generalizados bivariados que tuvieron en cuenta la no independencia de los episodios de OMA (agrupación) intraindividuo13. Para probar si las dos variables de antecedentes de otitis media se asociaban con el uso de dosis altas de amoxicilina para tratarla o la incidencia de fracaso del tratamiento o recidiva, condujimos una prueba de Wilcoxon para datos independientes.
Creamos modelos mixtos lineales generalizados multivariados13 para evaluar si las dosis altas de amoxicilina se asociaron independientemente con el fracaso del tratamiento o la recidiva después de OMA no complicada por primera vez en cada individuo. En estos modelos se efectuó un control para el año, sexo y categoría de edad del paciente, al igual que correlaciones intraconsultorio. Para reducir a un mínimo los efectos de la confusión por la indicación del tratamiento, limitamos el análisis primario a la primera OMA no complicada de cada individuo. Además, en estos análisis sólo incluimos las visitas para OM efectuadas desde el 1 de enero de 2000 hasta el 31 de diciembre de 2004, porque supusimos que, antes de 2000, la práctica clínica no habría cambiado como respuesta a las guías de los CDC para la OM publicadas en 19999. En los análisis secundarios efectuados para determinar si los antecedentes de OM habrían sido una variable de confusión en la relación entre la dosis de amoxicilina y el fracaso del tratamiento o recaída, en modelos mixtos lineales, generalizados, multivariados, en los que se efectuó un control para los antecedentes de infección, además de la dosis de amoxicilina, año, categoría de edad y sexo, agrupados por el lugar de la asistencia y el paciente, incluimos todas las visitas para OM (y no tan sólo los primeros episodios) realizadas desde el 1 de enero de 2000 hasta el 31 de diciembre de 2004.
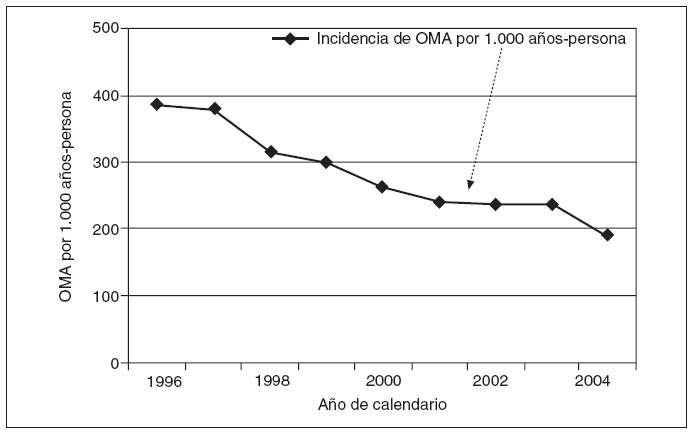
RESULTADOSOtitis media aguda no complicada (OMA)Durante el período de 9 años del estudio, identificamos 111.335 visitas para OMA no complicada. Las tasas de incidencia del proceso disminuyeron significativamente durante el período de estudio (p < 0,0001) desde 385,1 por 1.000 años-persona en 1996 hasta 188,8 por 1.000 años-persona en 2004 (fig. 1). Una mayor proporción de visitas OMA tuvieron lugar en lactantes más mayores (media ponderada = 37,1%), seguido de niños pequeños (24,4%), lactantes más pequeños (18,9%), niños en edad preescolar (14,2%) y aquellos en edad escolar (5,4%). Los niños efectuaron una media de 1,57 visitas para el proceso en los 6 meses previos a la OM índice (DE: 0,89), mientras que el número medio de visitas desde el nacimiento hasta la infección índice fue de 3,36 (DE: 3,07).
Fig. 1. Densidad de incidencia de la otitis media aguda (OMA) no complicada desde 1996 a 2004.
Antibióticos utilizados para tratar la OMA no complicadaLa proporción de infecciones tratadas con amoxicilina en dosis altas comparada con habituales cambió durante el período de 9 años del estudio (p < 0,0001), con un aumento brusco en los años 1998 a 2000 (fig. 2). Durante los 7 primeros años del estudio, la amoxicilina en dosis habituales fue el antimicrobiano más utilizado, pero, en 2003 y 2004, las dosis altas sustituyeron a las habituales y fueron utilizadas con más frecuencia para el tratamiento de niños en edad preescolar. En 2004, también se utilizaron en el tratamiento de niños de 7-12 meses de edad que representaron el 84,2% de visitas para la OMA efectuadas, comparado con el 79,2% en los de 2-6 meses de edad, 63,9% en los de 1-2 años de edad, 66,0% en los de 3-4 años y 26,0% en los de 5-12 años (p < 0,0001). Durante el estudio, también cambió la frecuencia con la que se usaron otros antibióticos en el tratamiento de esta infección, aunque los tamaños del efecto y las tasas del aumento fueron modestos comparado con amoxicilina (fig. 2). La frecuencia del uso de acitromicina aumentó significativamente durante el estudio, desde el 0% de OMA en 1996 hasta el 13,0% en 2004 (valor de p < 0,0001) (en 1995, la FDA aprobó la administración de esta última en niños con la infección)14. En comparación, durante el estudio disminuyó significativamente el uso de trimetoprim-sulfameto-xazol, desde el 13,0% de OMA en 1996 hasta el 0,3% en 2004 (valor de p = 0,0001).
Fig. 2. Uso anual de antibióticos específicos para la otitis media aguda no complicada (OMA) durante un período de 9 años.
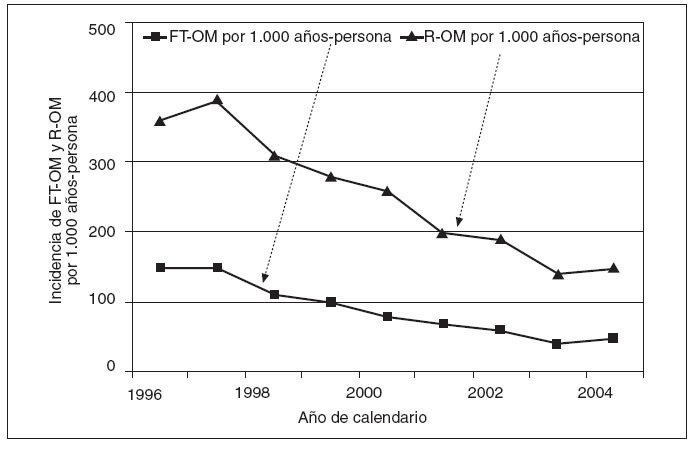
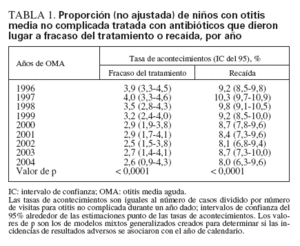
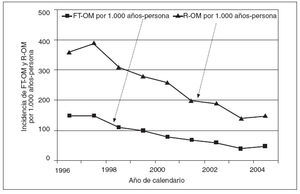
Fracaso del tratamiento y recidivaEn conjunto, durante el período de 9 años, el 3,5% de OMA no complicadas se tradujo en el fracaso del tratamiento, y el 9,3%, en recidivas. El porcentaje de las no complicadas seguido de fracaso del tratamiento disminuyó desde el 3,9% en 1996 hasta el 2,6% en 2004 (p < 0,0001). El porcentaje de las no complicadas, seguido de recidiva, disminuyó desde el 9,2% en 1996 hasta el 8,0% en 2004 (p < 0,0001) (tabla 1). Las tasas de incidencia anual de fracaso del tratamiento y recidiva también difirieron significativamente durante el período de 9 años del estudio (p < 0,0001 para ambas; fig. 3).
TABLA 1. Proporción (no ajustada) de niños con otitis media no complicada tratada con antibióticos que dieron lugar a fracaso del tratamiento o recaída, por año
Fig. 3. Densidad de incidencia del fracaso del tratamiento de otitis media aguda (FT-OM) y recidivas (R-OM) desde 1996 a 2004.
Los antibióticos más utilizados para tratar los casos de FT-OM y R-OM fueron trimetoprim-sulfametoxazol (26,0% de FT-OM; 26,6% de R-OM), eritromicina-sul-fisoxazol (21,3%; 19,7%), amoxicilina-ácido clavulánico (21,1%; 19,9%) o cefixima (11,3%; 8,6%).
Asociación de la dosis de amoxicilina con el fracaso del tratamiento y recidivasEn los análisis no ajustados, inicialmente las tasas de FT-OM y R-OM en las infecciones tratadas con dosis altas del antimicrobiano parecieron mayores que para las tratadas con la dosis habitual (p < 0,0001 para ambas comparaciones). De las infecciones tratadas con el antimicrobiano en dosis altas, el 3,4% dio lugar a FT-OM y el 10,2% a R-OM, mientras que el 3,2% de las tratadas con la dosis habitual dio lugar a FT-OM, y el 8,2%, a R-OM.
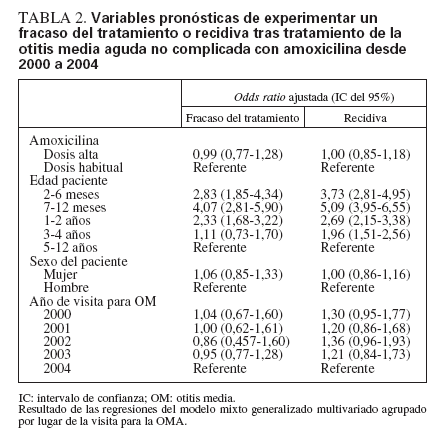
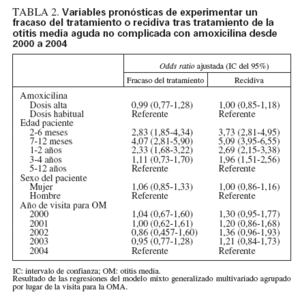
En los análisis multivariados primarios de las OMA por primera vez tratadas con amoxicilina, el uso del antimicrobiano en dosis altas no fue una variable pronóstica independiente del fracaso del tratamiento ulterior (odds ratio 0,99; IC del 95%: 0,77-1,28) o recidiva (OR: 1,00, IC del 95% 0,85-1,18), después de un ajuste para las variables asociadas con FT-OM o R-OM (edad, año de calendario y sexo) y una agrupación por el lugar de la asistencia (tabla 2). Aunque la amoxicilina en dosis altas no predijo el fracaso del tratamiento o las recidivas, la edad de los individuos predijo potentemente ambos resultados adversos. Considerando como grupo referente a niños de 5-12 años de edad, en los de 7-12 meses se identificó la mayor odds ratio ajustada de FT-OM (OR: 4,07; IC del 95%: 2,81-5,90) y R-OM (OR: 5,09; IC del 95%: 3,95-6,55).
TABLA 2. Variables pronósticas de experimentar un fracaso del tratamiento o recidiva tras tratamiento de la otitis media aguda no complicada con amoxicilina desde 2000 a 2004
En los análisis secundarios de todas las OMA tratadas con amoxicilina (no sólo las OMA tratadas por primera vez con el antimicrobiano), un número mayor de infecciones desde el nacimiento o en los 6 meses previos se asoció tanto con una mayor probabilidad de fracaso del tratamiento como de recidivas (todos los valores p < 0,0001). De forma parecida, un número mayor de OM desde el nacimiento o en los 6 meses previos se asoció con el uso de amoxicilina en dosis altas para tratar las no complicadas (todos los valores p < 0,0001). No obstante, en los análisis multivariados de todas las visitas para OMA con un control tanto para el número de infecciones desde el nacimiento como en los 6 meses previos, además de la edad, año de calendario y sexo, el uso de este antimicrobiano en dosis altas no predijo independientemente el fracaso ulterior del tratamiento (OR 0,97; IC del 95%: 0,81-1,16) o la recidiva (OR: 1,01; IC del 95%: 0,91-1,12).
DISCUSIÓNPrincipales hallazgosObservamos que las incidencias de otitis media aguda, no complicada tratada con antibióticos, el fracaso del tratamiento y las recidivas disminuyeron desde 1996 a 2004. De hecho, la otitis media aguda tratada con antibióticos fue el doble de frecuente en 1996 que en 2004. Durante este período de 9 años, aumentó el uso de amoxicilina en dosis altas para su tratamiento mientras que el uso de las dosis habituales del antimicrobiano disminuyó. Estos cambios de su utilización se iniciaron coincidiendo con la publicación de las directrices de los CDC sobre tratamiento de la OM donde se recomendaban dosis altas del antimicrobiano9. Aunque, más tarde, la AAP también las recomendó para el tratamiento de la OMA1, ambas recomendaciones se basaban tanto en datos microbiológicos que demostraban un aumento de la falta de sensibilidad a penicilina entre S. pneumoniae como en la opinión de los expertos, más que en estudios de resultados reales del tratamiento. En el contexto de estos cambios de la estrategia de tratamiento, los estudios observacionales proporcionan información importante sobre su eficacia en la práctica real.
Comparaciones con otros estudiosLos resultados del presente estudio coinciden con la investigación previa, al mismo tiempo que extienden los conocimientos epidemiológicos sobre los resultados adversos de la otitis media. El hallazgo del presente estudio de que las tasas de incidencia de otitis media aguda tratada con antibióticos disminuyeron desde mediados de 1990 hasta mediados de 2000 coincide con la investigación que reveló una disminución del uso de antibióticos para una diversidad de enfermedades en la década de los noventa6,7.
El presente estudio es exclusivo en la descripción de las tendencias en el fracaso del tratamiento de esta infección y en las incidencias de recidiva durante los 9 años extendiendo la publicación en 1999 de las directrices de los CDC para la otitis media. En otros estudios sobre administración de antibióticos se ha observado una disminución de la incidencia de esta infección antes de 2003, pero en ninguno se ha evaluado al mismo tiempo el fracaso del tratamiento o la recidiva de la otitis. Utilizando los datos de Colorado Medicaid2 y del Medical Expenditure Panel Survey3 (MEPS) encontramos tasas de fracaso y recidivas similares a las descritas en estudios previos sobre la infección, efectuados a mediados y finales de la década de los noventa. En comparación, en el presente estudio se encontraron tasas de fracasos del tratamiento y recidiva menores que las documentadas en Quebec4 y mayores que las identificadas en St Louis5 posiblemente debido a las diferencias en las definiciones de dichos acontecimientos. La amoxicilina en dosis altas se usó para tratar la OMA con más frecuencia en el ámbito de la presente investigación que en St Louis5 o Quebec4 durante años similares, rebasando la de las dosis habituales del antimicrobiano en 2003.
No detectamos que el uso de dosis altas comparado con las habituales para tratar la infección no complicada predijera independientemente el fracaso ulterior del tratamiento o las recidivas. Reconociendo que los médicos podrían haber elegido las dosis altas para los casos más graves, limitamos el análisis primario a la primera OMA no complicada en un esfuerzo por reducir a un mínimo la confusión por la indicación. Los resultados de estos análisis coincidieron con los análisis secundarios de todas las OMA no complicadas con un ajuste para los antecedentes del proceso en los pacientes, sin demostrar un efecto independiente de las dosis altas sobre el fracaso o la recidiva comparado con las dosis habituales.
InterpretaciónEl diseño del presente estudio no nos permitió identificar la razón de que la incidencia del proceso disminuyera marcadamente entre 1998 y 2004. Parece poco probable que, durante este período, cambiara la flora microbiana o la predisposición anatómica de los niños a la otitis media. Un estudio reciente efectuado en Tennessee y en Nueva York encontró que, entre 1998 y 2002, disminuyeron las tasas de otitis media y las de inserción de un tubo de timpanostomía15. Los investigadores sugirieron que esta disminución podría deberse a la introducción en 2002 de la vacuna conjugada antineumocócica en Estados Unidos, pero no pudieron incluir en el análisis el estado de dicha vacunación. Extendiendo los años estudiados por Poehling et al15 (1998-2002), la presente investigación de visitas para la OMA durante 9 años (1996-2004) observó disminuciones similares en las incidencias de otitis media no complicada, fracaso del tratamiento y recidivas. No obstante, consideramos que la introducción de la mencionada vacuna no explica los hallazgos de la presente investigación por dos razones. En primer lugar, en la población de estudio las incidencias de OMA, FT-OM y R-OM disminuyeron, como mínimo, tanto desde 1996 a 2000 como lo hicieron desde 2000 a 2004. En segundo lugar, los ensayos aleatorizados han demostrado que la vacuna conjugada antineumocócica produce un efecto modesto sobre la otitis media16,17. Consideramos que la explicación más coherente de los resultados del presente estudio es que los médicos han cambiado sustancialmente el umbral de tratamiento de esta infección, probablemente como respuesta a la presión para reducir la prescripción de antibióticos. Este cambio en el umbral diagnóstico también explicaría las disminuciones de las tasas de recidiva y fracaso, incluso durante un período en el que ha aumentado la falta de sensibilidad a los antimicrobianos más usados.
LimitacionesLos resultados de la presente investigación representan la otitis media aguda diagnosticada y tratada por alrededor de 80 médicos diferentes en un ámbito comunitario donde no están establecidos sistemáticamente umbrales estandarizados para su diagnóstico y tratamiento y que atienden a una extensa población con una diversidad relativa de razas/etnias. Sin embargo, la población del estudio procede de una sola área geográfica y la posición socioeconómica de los pacientes tiene tendencia a ser más favorecida que en la población general de Estados Unidos. Casi todos los pacientes estaban afiliados a una mutua sanitaria privada, de modo que estos resultados podrían ser menos generalizables a aquellos sin seguro.
Los hallazgos del presente estudio de que la administración de dosis altas de amoxicilina no redujo las tasas de fracaso del tratamiento o recidivas han de interpretar-se con precaución. Pudimos ajustar muchas otras variables en los análisis pero no tuvimos acceso a los datos sobre todas las posibles variables de confusión. Tratamos de controlar la confusión por indicación, pero los datos informatizados no contienen parámetros de la gravedad clínica de la OMA. Aunque no pudimos efectuar un control del estado de vacunación de los pacientes, suponemos que la recepción de la vacuna conjugada antineumocócica fue uniformemente elevada, ya que las tasas de cobertura de la vacunación entre afiliados a la HPHC son invariablemente superiores al 90%18. Identificamos la otitis media usando diagnósticos codificados y no dispusimos de datos sobre la gravedad clínica o la precisión diagnóstica. Como consecuencia, si los niños con OMA más grave tuvieron más probabilidades de ser tratados con dosis altas que habituales de amoxicilina, los hallazgos de la presente investigación de que las dosis altas no se asociaron con menos fracaso del tratamiento o recidivas revelarían que esta pauta no confiere un beneficio real. Los hallazgos no deben interpretarse como un menoscabo de las recomendaciones de usar dosis altas, porque esta pauta terapéutica podría estar justificada para prevenir la diseminación de bacterias resistentes a nivel de la población, aunque es preciso probar esta afirmación.
CONCLUSIONESDurante la última década se han diagnosticado con menor frecuencia otitis media aguda no complicada, fracasos del tratamiento y recidivas. El uso de amoxicilina en dosis altas aumentó durante este período pero no se asoció con una disminución de la probabilidad de fracaso del tratamiento o recidiva de las infecciones individuales. Muy probablemente, las tendencias observadas reflejan los cambios temporales en los umbrales del tratamiento de la infección, lo que sugiere que los médicos aplican criterios diagnósticos más estrictos. Estos cambios en la práctica clínica coinciden con las recomendaciones recientes efectuadas por los CDC9 y AAP1 y probablemente representan diversas influencias convergentes, incluidas las preocupaciones relativas al abuso de antibióticos que se han expresado en muchos foros diferentes.
Correspondencia: Colin M. Sox, MD, MS, Department of Pediatrics, Boston Medical Center, Dawling 3 South, 771 Albany St, Boston, MA 02118-2393, Estados Unidos.
Correo electrónico: colin.sox@bmc.org