El uso previo de antibióticos es un factor de riesgo para el estado de portador de S. pneumoniae resistente a los antimicrobianos y para la infección por este germen1-5. Existe un gran interés en disminuir el uso innecesario de antibióticos en pediatría, ya que los niños actúan como un importante reservorio para los gérmenes resistentes4. La otitis media aguda (OMA) es responsable del 45-62% de la prescripción de antibióticos en pediatría en Estados Unidos. La mayoría de OMA se tratan en este país con antibióticos; además, en vista de la creciente resistencia de los gérmenes, cada vez se utilizan más los antibióticos de amplio espectro. Muchos niños diagnosticados de OMA mejoran sin antibióticos; los más pequeños y más enfermos tienen menos probabilidades de mejorar sin ellos6,7.
En las normas recientes de la American Academy of Pediatrics (AAP) se define la OMA como una enfermedad aguda con inflamación de la membrana timpánica (MT) y derrame en el oído medio (DOM). La AAP basa sus recomendaciones de tratamiento antibiótico en la edad del niño, en la intensidad del proceso y en la certeza diagnóstica de OMA6 (tablas 1 y 2). Entre los criterios para definir la OMA, el DOM es el más difícil de establecer8-12; esta dificultad induce a muchos clínicos a tratar con antibióticos basándose sólo en los otros dos criterios: agudeza del proceso e inflamación13,14. Al imponer más criterios específicos para el diagnóstico y tratamiento de la OMA, las normas AAP podrían reducir el uso de antibióticos y los fenómenos medicamentosos adversos (FMA) consiguientes. Sin embargo, la compensación de una menor sensibilidad por una mayor especificidad podría prolongar los episodios de enfermedad y aumentar las complicaciones clínicas y sus costes colaterales. Alternativamente, algunos autores han recomendado una estrategia inicial de “esperar y ver”15-19 (EYV).
TABLA 1. Criterios de la AAP para el diagnóstico y el tratamiento de la OMA6
TABLA 2. Criterios de la AAP para el tratamiento de la OMA6
Nuestro objetivo consistió en llevar a cabo un análisis de decisiones para una población diana de niños que se presentaron a su médico de asistencia primaria con una posible otitis media aguda, y comparar las normas AAP con una estrategia que restrinja menos el uso de antibióticos y con otra de esperar y ver.
MÉTODOSModelo del análisis de decisionesSe utilizaron tres árboles de decisiones para valorar las tres estrategias para cada uno de los grupos de edades existentes en las normas, con un árbol de decisiones para cada grupo: niños de 2 a < 6 meses, de 6 a < 24 meses y de 2 a 12 años6. El horizonte de tiempo fue la resolución de un episodio aislado de enfermedad aguda. Los niños, independientemente, podrían padecer una verdadera OMA y presentarse con enfermedad “importante”, según se define en las normas AAP: otalgia moderada o intensa o fiebre µ 39 °C6,13. En las normas AAP, en este modelo se excluye a los niños con historia de OMA recurrente o de procesos que representan un mayor riesgo de infección bacteriana persistente o invasiva6.
Estrategias diagnósticas y terapéuticasEn la estrategia de dos criterios (2CRIT), se diagnostica la OMA si cumple dos criterios: enfermedad aguda y signos de inflamación de la MT (otalgia o eritema de la MT, criterios 1 y 2, tabla 1). Todos los niños diagnosticados de OMA se tratan con amoxicilina6; si se excluye la OMA, se controla a los niños durante 48 h sin tratamiento antibiótico.
En la estrategia AAP de tres criterios (AAP), se diagnostica la OMA si cumple los 2CRIT más el criterio de DOM. En el tratamiento antibiótico de los niños diagnosticados de OMA se siguen las normas de la AAP6 (tabla 2).
En la estrategia de esperar y ver (EYV), se controla a todos los niños durante 48 h sin tratamiento antibiótico.
Conducta clínicaEn la tabla 3 se muestran los algoritmos para la prescripción antibiótica inicial y de seguimiento, y en el Apéndice se enumeran nuestras presunciones clínicas. Los niños que no mejoran se valoran de nuevo a las 48 h, al presumir en una nueva visita que el estado verdadero de su proceso no se ha modificado entre las visitas.
TABLA 3. Estrategias de tratamiento antibiótico inicial y en la nueva visita en el análisis principal
Los niños con OMA verdadera que no mejoran pueden presentarse en la nueva visita con o sin mastoiditis, la única complicación supurada que se incluye en el modelo. Los niños con OMA que no mejoran pero no presentan mastoiditis se tratan con amoxicilina si inicialmente no habían recibido tratamiento, o con amoxicilina-clavulanato si inicialmente se habían tratado con amoxicilina. Los niños con mastoiditis se hospitalizan, reciben antibióticos de amplio espectro y se controlan luego con una visita de ORL. Los niños no tratados inicialmente y que no mejoran, sin OMA verdadera, quedan sin tratamiento en la nueva visita. Los niños con DOM que dura > 3 meses se remiten al ORL20. Hay un máximo de 1 cambio de antibióticos. Todos los casos se resuelven finalmente.
Los días de enfermedad y los días de trabajo parental perdidos se miden a partir del momento de la primera visita al consultorio; se contabilizan 0,5 días si se produce la resolución inicial. Se cuentan dos días adicionales de enfermedad y 2 días de trabajo parental perdidos si los niños necesitan una nueva visita a las 48 h, y 2 días adicionales de enfermedad y 5 o 4 días más de trabajo parental perdido si aparece una mastoiditis en niños < 2 años o de 2-12 años de edad, respectivamente21.
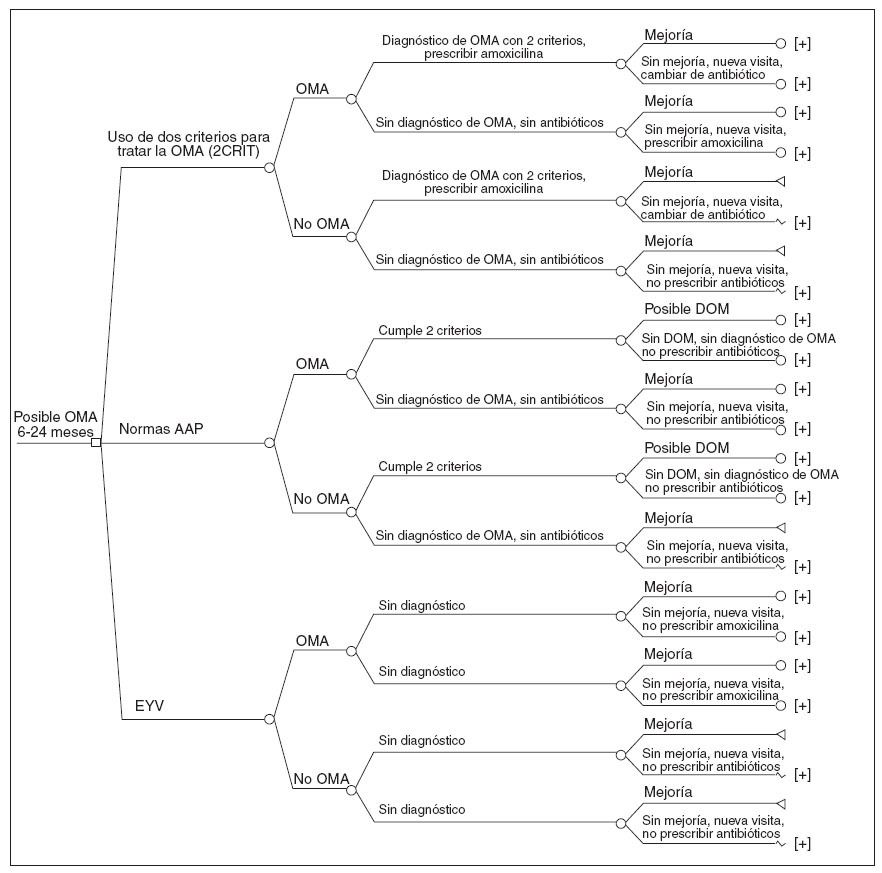
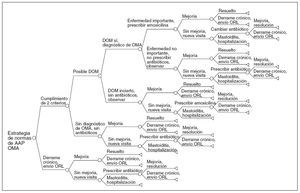
En las figuras 1 y 2 se muestran ejemplos representativos de los árboles de decisiones. Los modelos se elaboraron mediante el programa Tree Age Pro 2005, Release 0.2 (Tree Age Software, Williamstown, MA), y asumen una perspectiva societal.
Fig. 1. Comienzo del árbol de decisiones, 6-< 24 meses. 2CRIT: estrategia de 2 criterios; AAP: American Academy of Pediatrics; DOM: derrame en el oído medio; EYV: esperar y ver; OMA: otitis media aguda.
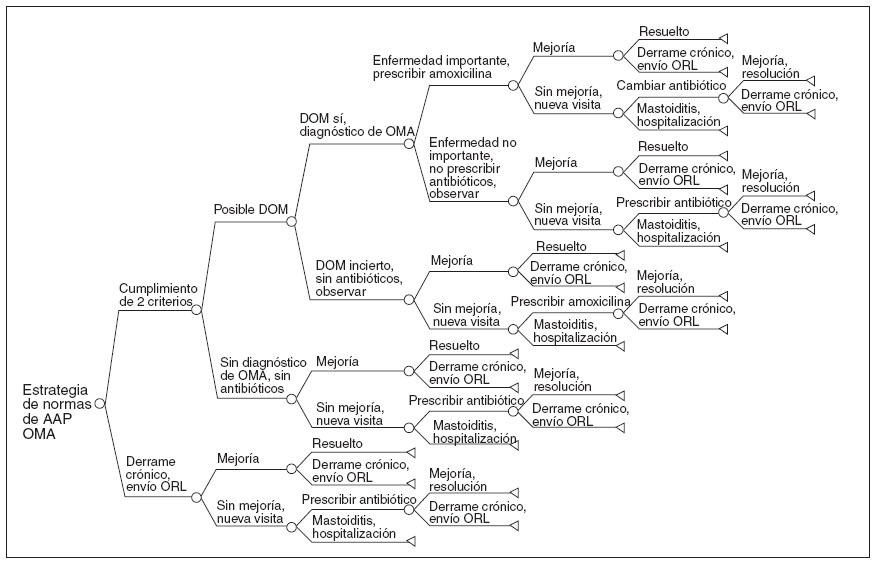
Fig. 2. Porción del final del árbol de decisiones, 2-12 años, estrategia de normas de AAP, OMA verdadera. AAP: American Academy of Pediatrics; DOM: derrame en el oído medio; OMA: otitis media agua.
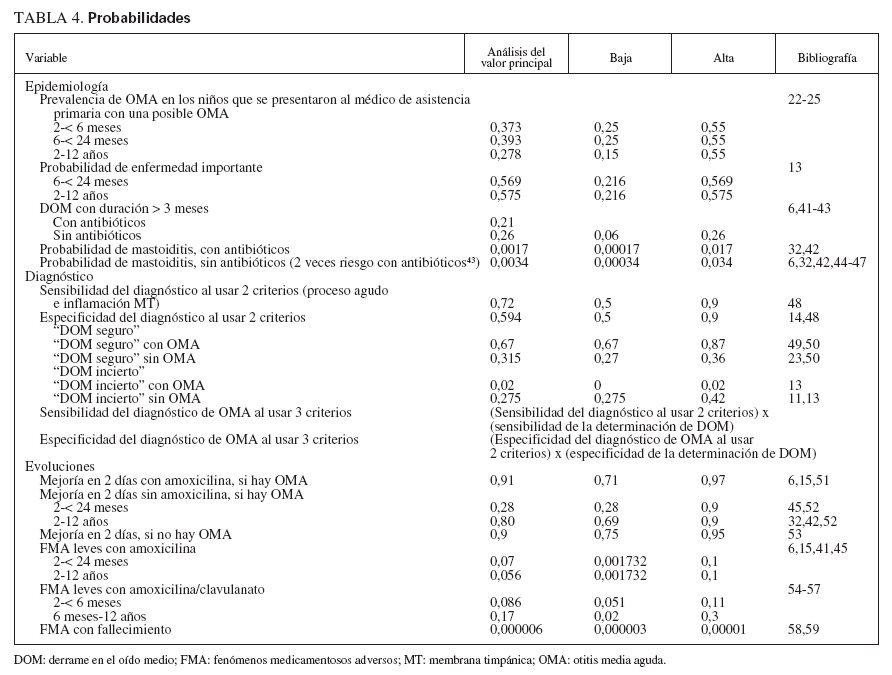
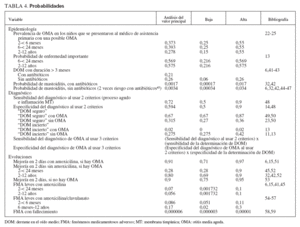
ProbabilidadesLas probabilidades y límites del modelo (tabla 4) se derivaron de estudios publicados. Cuando estuvieron disponibles, se utilizaron las probabilidades específicas para cada edad. Se emplearon los datos de la National Health Survey22 para estimar el número anual de niños valorados por una posible OMA, y la fracción de estos niños que realmente la padecía. La estimación se basó en el número anual de visitas por una posible OMA sobre el número total de visitas por “tos, resfriado, rinorrea”, “virasis”, “fiebre del heno, sinusitis” o “infección del oído medio”. Dada la tendencia a sobrediagnosticar23, se asumió que el 75% de las visitas codificadas como “infección del oído medio” representaban una verdadera OMA. El límite de probabilidades resultante concuerda con los valores publicados24,25.
TABLA 4. Probabilidades
Costes/honorariosEn la tabla 5 se presentan las estimaciones de costes, límites y datos bibliográficos para el uso de antibióticos, días de trabajo parental perdidos (incluidos los beneficios del 30%26) y hospitalizaciones. Los honorarios sirvieron para estimar los costes de las visitas en el consultorio de asistencia primaria y ORL. Cuando no se disponía directamente de los datos de 2005, se basaron en los valores de la literatura y se ajustaron para la inflación con arreglo a dólares de 2005, según las recomendaciones del US Panel on Cost-Effectiveness Research for Performing and Reporting Economic Analyses27, mediante el Consumer Price Index (CPI) general para los salarios, o los CPI específicos por categorías de precios, cuando eran aplicables28. Los costes se contrajeron durante el año de enfermedad aguda y no se descontaron.
TABLA 5. Costes
Se utilizó el Average Wholesale Price29,30 para los costes de los antibióticos. En cuanto a los costes por los días de trabajo parental perdidos, se utilizó el precio salarial medio de la hora en septiembre de 2004 en Estados Unidos, ajustado a dólares de enero de 200531. En el análisis principal se valoró equitativamente todo el tiempo de los progenitores como tiempo laboral27. Por lo que respecta a las nuevas visitas en el consultorio de asistencia primaria, se utilizaron los honorarios medios estimados a partir de los seguros privados y Medicaid32,33. En cuanto a las visitas al ORL, se empleó la tarifa para una visita de ORL inicial prolongada de nivel 333,34. Debido a que no se disponía de datos fidedignos de costes para una hospitalización por FMA (más prevalente en los niños a quienes se prescriben antibióticos), en el análisis principal no se incluyeron los relacionados con la hospitalización por mastoiditis (menos prevalente en los niños que reciben antibióticos), pero se valoró su potencial impacto con el análisis de sensibilidad. Para estimar los costes hospitalarios se ajustaron los datos de costes medios de hospitalización específicos para la edad obtenidos en la Agency for Healthcare Research and Quality’s Healthcare Cost and Utilization Project KIDS Inpatient Database21, con empleo del cociente operativo medio FY2005 cost-to-charge para los hospitales de Estados Unidos con un sistema de pagos prospectivos a corto plazo35. Se incluyeron los costes de los ingresos con un diagnóstico principal de mastoiditis36 (códigos ICD-9 383.00, 383.01, 383.02 y 383.9).
AnálisisSe compararon las evoluciones de 2CRIT, AAP y EYV. Los parámetros primarios en la evolución fueron el uso global de antibióticos, los días de enfermedad, los FMA leves y los costes totales en dólares. Los parámetros secundarios en la evolución fueron el uso de antibióticos de amplio espectro, la mastoiditis, los envíos al consultorio de ORL y los días de trabajo parental perdidos.
Se informa sobre el número necesario a tratar (NNT) con antibióticos para evitar 1 día de enfermedad. También se informa acerca del coste incremental por prescripción antibiótica evitada.
Se valoró si los umbrales clínico y económico implícitos para el uso de antibióticos, incluidos en las normas AAP, son coherentes entre los niños de los tres grupos de edades. Por coherencia entendemos que las normas impliquen que los números necesarios a tratar para evitar 1 día de enfermedad, o los cocientes de costes por prescripción antibiótica evitada, sean similares en los diferentes grupos de edades.
En cambio, puede haber falta de coherencia si el número necesario a tratar en la estrategia recomendada para un grupo de edades (p. ej., AAP para los niños de 2 a 12 años) difiere del número necesario a tratar en la misma estrategia aplicada a otro grupo de edades, y al mismo tiempo es similar al número necesario a tratar en una estrategia diferente en este mismo grupo de edades. Por ejemplo, supongamos que un análisis revela que la adopción de la AAP para los niños de 2 a < 6 meses, en vez de 2CRIT, implica que no deseamos tratar a más de 1,5 niños para evitar 1 día de enfermedad. Supongamos también que esta misma clase de análisis revela que en los niños de 2 a 12 años la adopción de AAP, en vez de EYV, implica que deseamos tratar al menos 2,4 niños para evitar 1 día de enfermedad. Estos dos resultados implicarían un umbral más estricto para el uso de antibióticos en los lactantes que en los niños de 2 a 12 años, y representaría una falta de coherencia de las normas.
Estos análisis de coherencia se complican por la incertidumbre de las estimaciones puntuales, pero el mismo razonamiento es aplicable si se comparan los límites fijados mediante intervalos de confianza, en vez de estimaciones puntuales. En estas circunstancias, para demostrar la falta de coherencia pueden emplearse intervalos de confianza que no se solapen.
Se utilizó la simulación Monte Carlo de segundo orden para derivar los errores estándar y las correlaciones y se calcularon los intervalos de confianza del 95% en torno a los NNT y los cocientes incrementales de coste-eficacia (CICE). Estos últimos intervalos se calcularon mediante el teorema de Fieller37. Se especificaron las distribuciones para las variables clave, con distribuciones normales para las variables de costes y distribuciones beta para las probabilidades38-40.
Análisis de sensibilidadSe realizaron análisis de sensibilidad para cuatro presunciones estructurales del modelo. En primer lugar, se valoró el impacto de añadir al análisis los costes de la hospitalización por mastoiditis. Si se hubieran valorado también los costes de la hospitalización por FMA, se habrían equilibrado parcialmente los costes de la hospitalización por mastoiditis.
En segundo lugar, se valoró el impacto de otras presunciones alternativas sobre el seguimiento de la prescripción de antibióticos, al modelar otras dos presunciones extremas de seguimiento: 1) los niños que no mejoraron y no presentaban una OMA verdadera recibieron tratamiento antibiótico en el seguimiento; incluso los que se trataron inicialmente con antibióticos los suspendieron, y 2) todos los niños que no mejoraron, incluso aquellos sin una OMA verdadera, recibieron antibióticos en el seguimiento.
En tercer lugar se valoró una estrategia intermedia que utilizó 2 criterios para el diagnóstico, pero basó las decisiones de tratamiento en las normas de la AAP.
En cuarto lugar, se realizó un análisis unidireccional de sensibilidad bajo la presunción de 0,5 días para la mejoría si la resolución ocurre utilizando unos límites de cero (resolución inmediata) a 1 día de enfermedad.
También se realizó un análisis unidireccional de sensibilidad para el NNT para evitar 1 día de enfermedad y el incremento de coste por la prescripción de antibióticos evitada, mediante el uso de los valores mínimo y máximo para los límites variables enumerados en las tablas 4 y 5, con exclusión en estos cocientes del coste de los días de trabajo parental perdidos.
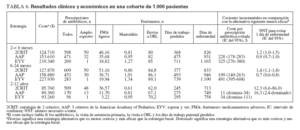
RESULTADOSUso de antibióticosEn la tabla 6 se observan las evoluciones esperadas para las cohortes de 1.000 niños al utilizar estrategias clínicas alternativas en los tres grupos de edades.
TABLA 6. Resultados clínicos y económicos en una cohorte de 1.000 pacientes
2CRIT presentó el mayor uso de antibióticos. La adopción de AAP redujo significativamente el uso de antibióticos: 21%, 26% y 67% en los niños de 2 a < 6 meses, 6 a < 24 meses y 2 a 12 años, respectivamente (en todos, p < 0,0001). Con EYV se hizo el menor uso de antibióticos, y en comparación con AAP se redujo dicho uso en 43%, 38% y 67% para estos mismos grupos de edades (en todos, p < 0,0001).
Evoluciones clínicasCon 2CRIT, y un mayor uso de antibióticos, se produjeron las cifras más elevadas de FMA. En comparación con 2CRIT, AAP redujo ligeramente los FMA en 23% (p = 0,26), 28% (p = 0,13) y 68% (p = 0,0003) en los niños de 2 a < 6 meses, 6 a < 24 meses y 2 a 12 años, respectivamente. Con EYV se redujeron los FMA en 47%, 46% y 72% en estos mismos grupos de edades, respectivamente (p = 0,02). Con 2CRIT hubo el menor número de días de enfermedad, así como de días de trabajo perdidos, mastoiditis y visitas a ORL. AAP aumentó los días de enfermedad en 13%, 14% y 4% (p < 0,0001 en las 3 comparaciones) en los niños de 2 a < 6 meses, 6 a < 24 meses y 2 a 12 años, respectivamente. Con EYV se aumentaron aún más estos porcentajes (en todos, p < 0,0001).
CostesAl incluir en el análisis el coste de los días de trabajo parental perdidos, el uso de antibióticos redujo los costes. En comparación con 2CRIT, AAP aumentó los costes globales en 23% (p = 0,01), 24% (p = 0,01) y 4% (p = 0,75) en los niños de 2 a < 6 meses, 6 a < 24 meses y 2 a 12 años, respectivamente. Con EYV se produjeron los costes más elevados en todos los grupos de edades.
Número necesario a tratar y coste por prescripción de antibióticos evitada
Como se muestra en la tabla 6, en los niños de 2 a < 6 meses, con 2CRIT hubo un NNT de 1,2 (intervalo de confianza 1,0 a 1,5) por día de enfermedad evitado, en comparación con AAP. AAP tuvo un NNT de 0,9 (0,7 a 1,0) en comparación con EYV. En los niños de 6 a < 24 meses, 2CRIT tuvo un NNT de 1,4 (1,1 a 1,8) en comparación con AAP, y AAP tuvo un NNT de 0,7 (0,6 a 0,8) en comparación con EYV. En los niños de 2 a 12 años, 2CRIT tuvo un NNT de 12,3 (6,6 a 86,0) en comparación con AAP, y AAP tuvo un NNT de 6,3 (2,4 a estar dominado) en comparación con EYV.
En los niños de 2 a < 6 meses, AAP tuvo un cociente incremental de coste-eficacia de 228 dólares (intervalo de confianza del 95%, 178 a 283 dólares) por prescripción antibiótica evitada, en comparación con 2CRIT; EYV tuvo un cociente incremental de 325 dólares (276 a 380 dólares) en comparación con AAP. En los niños de 6 a < 24 meses, AAP tuvo un cociente incremental de coste-eficacia de 199 dólares (140 a 263 dólares), en comparación con 2CRIT; EYV tuvo un cociente incremental de 491 dólares (395 a 604 dólares) en comparación con AAP. En los niños de 2 a 12 años, AAP tuvo un cociente incremental de coste-eficacia de 11 dólares (AAP domina o los costes aumentan a 34 dólares), en comparación con 2CRIT; EYV tuvo un cociente incremental de 34 dólares (EYV domina o los costes aumentan a 111 dólares) en comparación con AAP.
Grado de coherencia entre los grupos de edadesEn el grupo de 2 a 12 años, el uso de AAP en vez de EYV implica que deseamos tratar a un mínimo de 2,4 niños (mínimo del intervalo de confianza del 95% para AAP en comparación con EYV) con antibióticos para evitar un día de enfermedad. Ello se debe a que, si no lo deseamos, tendríamos una confianza del 95% de que AAP supera el número que deseamos tratar. Por otra parte, en los grupos de menos edad, la decisión de rechazar 2CRIT a favor de AAP implica que no deseamos tratar a más de 1,5 niños (límite superior de 2CRIT en comparación con AAP para los niños de 2 a < 6 meses) o a 1,8 niños (límite superior de 2CRIT en comparación con AAP para los niños de 6 a < 24 meses) para evitar 1 día de enfermedad. Ello se debe a que, si deseamos tratar al menos a 1,8 niños para evitar 1 día de enfermedad, tendríamos una confianza mayor del 95% de que deberíamos adoptar 2CRIT en vez de AAP.
La misma falta de coherencia se observó en un análisis transversal de edades basado en el coste por prescripción antibiótica evitada. En los niños de 2 a < 6 meses, la recomendación de adoptar AAP implica que el deseo de pagar para evitar una prescripción antibiótica alcanza al menos 178 dólares (el límite inferior para AAP, en comparación con 2CRIT). Ello se debe a que, si no deseamos pagar al menos 178 dólares para evitar una prescripción antibiótica, tendríamos una confianza del 95% de que AAP no representa un buen valor. De modo similar, en los niños de 6 a < 24 meses, la recomendación para adoptar AAP implica un deseo de pagar que es al menos de 140 dólares (de nuevo porque, si no lo deseamos, tendríamos una confianza del 95% de que AAP no representa un buen valor). En los niños de 2 a 12 años, por otra parte, la recomendación de adoptar AAP en vez de EYV implica un deseo de pagar que no puede superar el límite superior de confianza de 111 dólares para EYV (de otro modo tendríamos una confianza del 95% de que EYV tenía un buen valor). Así pues, el deseo de pagar para evitar una prescripción antibiótica, incorporado implícitamente en las normas AAP, es más reducido en los niños mayores (no superior a 111 dólares) que en los pequeños (al menos 178 dólares). Estos hallazgos sugieren que las normas AAP implican un mayor deseo de tratar a los niños mayores que a los pequeños.
Análisis de sensibilidadAnálisis de sensibilidad estructural
Nuestra evaluación de la presunción estructural para excluir el coste de la hospitalización por mastoiditis condujo a un aumento de 3 a 8 dólares en los CICE, según los grupos de edades. Al modelar las presunciones alternativas de tratamiento en el seguimiento, se obtuvieron unos CICE de 1 a 19 dólares más elevados que los hallados en el análisis principal. La estrategia alternativa de utilizar 2 criterios para el diagnóstico y los criterios AAP para el tratamiento presentó un cociente incremental de coste-eficacia que era mayor que con 2CRIT, la estrategia siguiente más costosa, y por lo tanto fue débilmente dominada por 2CRIT. Finalmente, al modelar la resolución alternativa, la presunción de los días de enfermedad condujo sólo a un aumento en el NNT de 0,3 con EYV, frente a AAP, para el grupo de 212 años. Estos enfoques alternativos no modificaron el hallazgo de la falta de coherencia entre los niños pequeños y mayores con respecto a los valores del deseo de pagar.
Análisis unidireccionales de sensibilidad
Los días de trabajo parental perdidos fueron el mayor componente de los costes en todas las edades. Si la proporción de progenitores que trabajan se redujera de 100% a 0% (como reflejo de una gama que va desde que uno de los progenitores perdiera tiempo laboral hasta que ninguno de los dos lo perdiera), los costes previstos por niño en la estrategia AAP se reducirían aproximadamente un 80% en los tres grupos de edades, y la estrategia EYV dominaría a AAP y 2CRIT en el grupo de 2 a 12 años.
Al variar dentro de sus límites cada una de las 17 estimaciones de costes y probabilidades, sigue observándose una falta de coherencia en el número necesario a tratar para evitar 1 día de enfermedad, y en el deseo de pagar para evitar 1 prescripción antibiótica, en los niños de 2 a < 6 meses y en los de 2 a 12 años, para todas las variables excepto 2: la probabilidad de mejoría en 2 días sin amoxicilina con OMA, y la sensibilidad de diagnosticar DOM. Siguió observándose una falta de coherencia en los niños de 6 a < 24 meses y en los de 2 a 12 años para todas las variables excepto estas 2 y otras 4 más: la probabilidad de OMA, la sensibilidad de diagnosticar OMA con 2 criterios, la probabilidad de mejoría en 2 días sin OMA, y la probabilidad de enfermedad importante.
DISCUSIÓNLas normas de la AAP se desarrollaron para afrontar el aumento de resistencia a los antibióticos, los crecientes costes de su prescripción, y la incertidumbre acerca de cuáles son los niños que deben recibir tratamiento antimicrobiano para la otitis media. Su intención era la de proporcionar a los médicos de asistencia primaria un esquema basado en la evidencia, dirigido hacia un empleo más racional de los antibióticos6. A diferencia del presente análisis, donde se han utilizado muchas de las mismas referencias consideradas por los autores de las normas, no se utilizaron modelos de decisión al desarrollarlas.
Aunque las normas tenían como objeto ayudar en las decisiones terapéuticas para la OMA infantil, hay que tener en cuenta que los clínicos pueden utilizarlas parcialmente, adaptarlas o combinarlas con otras estrategias no analizadas aquí. También hay que tener en cuenta que las tres estrategias que se comparan aquí no cubren todas las posibles permutaciones diagnósticas y terapéuticas, sino que representan una gama de los enfoques pragmáticos que pueden seguir los clínicos.
Las diversas opciones en la conducta a adoptar ante la OMA dan lugar a distintos resultados clínicos y económicos cuya importancia puede variar para los diferentes interesados. Por ejemplo, la reducción del uso de antibióticos puede ser un objetivo importante, pero también pueden serlo la reducción de los días de trabajo parental perdidos, los fenómenos medicamentosos adversos o los costes. El modo de enfocar cada una de estas estrategias depende del valor relativo que se dé a estos distintos resultados clínicos y económicos.
En el presente estudio se han obtenido los siguientes hallazgos: en primer lugar, en comparación con la estrategia de 2 criterios, menos restrictiva en el uso de anti-bióticos8,9,11, la estrategia AAP reduce su uso, pero aumenta los días de enfermedad y también los costes, especialmente los laborales de los progenitores. En los niños menores de 2 años, la estrategia AAP reduce en 21-26% el uso de antibióticos, pero aumenta los días de enfermedad en 13-14%, y los costes en 178-283 dólares por cada prescripción antibiótica evitada. En los niños mayores de 2 años, la estrategia AAP reduce el uso de antibióticos en un 67%, pero aumenta los días de enfermedad en sólo un 4% y no aumenta los costes. Este análisis apoya más los criterios AAP en los niños mayores que en los menores de 2 años.
En segundo lugar, nuestro análisis revela que en las normas AAP existe una falta de coherencia en relación con las edades, lo que puede socavar el apoyo de dichas normas en los niños menores de 2 años: los criterios AAP implican un umbral más bajo para el uso de antibióticos en los niños mayores que en los pequeños. Al considerar los resultados del NNT, si deseamos tratar con antibióticos a 2,4 niños mayores de 2 años para evitar 1 día de enfermedad, como ocurre al adoptar la estrategia AAP, para ser consecuentes debemos tener aún más deseos de tratar sólo a 1,5 a 1,8 niños menores de 2 años con antibióticos para evitar 1 día de enfermedad. Este último umbral es compatible con el uso de la estrategia 2CRIT, en vez de AAP, en los niños menores de 2 años.
¿Es problemático si las normas AAP, prácticas y fáciles de seguir, adolecen de falta de coherencia en los distintos grupos de edades? Lo es, en efecto, si creemos que debe haber el mismo umbral para tratar a los lactantes y a los niños mayores. El problema es aún mayor si, debido a la mayor vulnerabilidad de los niños pequeños, los clínicos están más deseosos de tratarlos que de tratar a los niños mayores. Si utilizamos la estrategia AAP en el grupo de más edad, por coherencia deberíamos ser más permisivos con los antibióticos en el grupo de los lactantes y adoptar para ellos la estrategia 2CRIT. Alternativamente, si deseamos mantener la estrategia AAP para los lactantes, debemos ser más estrictos con el uso de antibióticos en los niños de 2 a 12 años, y adoptar la estrategia EYV para ellos. En este contexto, no sería coherente adoptar simultáneamente la estrategia AAP para los lactantes y los niños mayores.
Al menos en 4 ensayos clínicos recientes se ha estudiado el uso de la prescripción antibiótica tardía en la visita inicial por OMA15-18, similar a nuestra estrategia EYV. Todos los autores concluyeron que sus estudios apoyaban un método de expectación armada para la OMA en la visita inicial. En 3 ensayos participaron niños a partir de 6 meses de edad y en 1 se incluyó a niños > 12 meses. En 3 estudios se excluyó a los niños con fiebre alta, y en el cuarto, aunque se excluyó a los niños sólo si presentaban un aspecto “tóxico”, participaron sólo 283 de los 776 niños que se presentaron con OMA. Además, la mayoría de los niños participantes en estos estudios tenían más de 2-3 años de edad. Por consiguiente, estos estudios no afrontan adecuadamente los resultados en los niños menores de 2 años con un proceso importante y no reflejan el espectro típico de los niños que se presentan al médico de asistencia primaria con una posible OMA.
El estudio actual presenta algunas limitaciones. En primer lugar, está limitado por el modelo de presunciones, por las probabilidades utilizadas para los fenómenos casuales y por la carencia de datos para ciertas variables. Sin embargo, por lo que respecta a las estimaciones de probabilidad, se utilizaron los mejores datos de la literatura; además, las probabilidades eran coherentes a través de las diferentes estrategias, y las preferencias relativas eran razonablemente estables frente a los cambios en las estimaciones de las variables. El valor relativo de las estrategias sólo se modificó en los extremos de las distribuciones de variables únicas, que son improbables.
En segundo lugar, un gran número de resultados clínicos y económicos son relevantes en cuanto a las decisiones sobre el tratamiento óptimo de la OMA: los costes globales, el uso de antibióticos, el evitar días de enfermedad y las complicaciones supuradas. Nosotros no tratamos de llegar a conclusiones definitivas basándonos sólo en una evolución, como el uso de antibióticos; ni proporcionamos un resumen métrico como la utilidad de haber incluido estas evoluciones en una escala única. El uso de una sola evolución habría simplificado los resultados, pero ignoraría la realidad de que los diferentes interesados podrían pensar de un modo muy diferente acerca del valor relativo de los distintos componentes de la evolución. También resulta difícil cuantificar los beneficios potenciales de reducir el uso de antibióticos sobre el retardo o la supresión del desarrollo de gérmenes resistentes a los antibióticos.
En los análisis de decisiones se pueden comparar los tratamientos de un modo que no es fácil de conseguir directamente en los ensayos clínicos. Por ejemplo, los médicos incluyen selectivamente a los pacientes en ensayos sobre otitis media realizados en el consultorio; en todos los ensayos de esperar y ver, antes descritos, se incluyó selectivamente a menos pacientes y de más edad en relación con los que se ven en el ámbito clínico con una posible OMA15-18. Además, las evoluciones raras de la OMA son difíciles de medir prospectivamente, como la hospitalización por mastoiditis y los fallecimientos por FMA.
CONCLUSIONESNuestros resultados aportan evidencia de que los criterios de AAP pueden ser más eficaces en relación con el coste en los niños mayores, en comparación con los menores de 2 años. En los niños pequeños, la estrategia AAP, con respecto a otras menos restrictivas, reduce el uso de antibióticos, pero sólo al coste clínico relativamente elevado de incrementar los días de enfermedad, y a un coste económico también relativamente elevado. La presión de los progenitores que trabajan, en el sentido de que se prescriban antibióticos a los niños menores de 2 años, puede considerarse racional en este contexto.
También hemos apreciado una falta de coherencia de las normas AAP entre las distintas edades. A menos que deseemos tolerar más días de enfermedad y unos costes económicos más elevados en los niños menores de 2 años que en los mayores, debemos ser más proclives a adoptar las normas de la AAP para la OMA en los niños pequeños, y a efectuar un seguimiento de los niños mayores sin prescribir antibióticos en la visita inicial, o adoptar las normas AAP en los niños mayores, y ser menos restrictivo con los antibióticos en los menores de 2 años.
Sospechamos que muchos clínicos ya toman en consideración las diferentes circunstancias y/o valores de cada familia al adoptar las decisiones sobre el tratamiento de la otitis media. Los resultados de este estudio deben ayudar a los clínicos a considerar más específica-mente estas compensaciones y a discutirlas más eficazmente con las familias.
APÉNDICE: PRESUNCIONESEste proyecto fue subvencionado parcialmente por un contrato cooperativo con la Agency for Healthcare Research and Quality (AHRQ) Centers for Education and Research on Therapeutic (beca #HS10399).
Agradecemos a Andrew Briggs, University of Glasgow, Reino Unido, sus valiosas sugerencias sobre las distribuciones de las variables.
Conflicto de intereses: La Dra. Meropol ha actuado como consultora de Wyeth Pharmaceuticals y recibe una ayuda parcial mediante una beca educativa no restringida de Amgen.
El trabajo se presentó parcialmente en la Pediatric Academic Societies Annual Meeting, 2 mayo de 2006, San Francisco, CA, y en la 22nd International Conference on Pharmacoepidemiology and Therapeutic Risk Management, 27 de agosto de 2006, Lisboa, Portugal.
Correspondencia: Sharon B. Meropol, MD, MSCE, Center for Clinical Epidemiology and Biostatistics, University of Pennsylvania School of Medicine, 108 Blockley Hall, 423 Guardian Dr, Filadelfia, PA 19104, Estados Unidos.
Correo electrónico: meropols@mail.med.upenn.edu