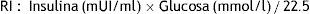La infertilidad afecta a entre el 8 y el 15% de la población en general en la etapa reproductiva. El término se refiere a la incapacidad de una pareja para lograr un embarazo posterior a un año de actividad sexual no protegida. El factor masculino es responsable de la misma en 20% y combinada con la pareja en el 30-40%.
La evaluación inicial del estado reproductivo masculino es el seminograma, considerado como herramienta fundamental de valoración.
En el hombre diversas condiciones pueden asociarse a infertilidad; entre estas se encuentran las patologías endocrinometabólicas como el hipogonadismo, la hiperprolactinemia, el distiroidismo, la dislipidemia, las alteraciones de la glucosa-insulina, la obesidad central o en los parámetros conjuntos de estas últimas llamado síndrome metabólico. La obesidad contribuye a la aparición de hipertensión arterial, dislipidemia e insulinorresistencia.
El objetivo de nuestra revisión fue documentar de la literatura médica el impacto que existe de la asociación entre circunferencia abdominal e insulinorresistencia en los parámetros seminales como posible etiología de infertilidad masculina.
La búsqueda de la información se llevó a cabo en Medline, ScienceDirect y Scopus; se tomaron como base para la revisión los términos: obesidad, circunferencia abdominal, resistencia a la insulina, infertilidad masculina, semen, parámetros seminales.
Existen estudios que documentan el efecto deletéreo tanto de la obesidad como de la resistencia a la insulina en la fertilidad femenina; algunos más realizados en varones sugieren efectos nocivos en su potencial reproductivo. Alteraciones seminales se han encontrado en varones obesos con resistencia a la insulina, pero aún se requieren de investigaciones que evalúen la asociación existente entre los mismos. La literatura reporta alteraciones seminales asociadas a la obesidad que aún están por dilucidar.
Infertility affects between 8-15% of general population of reproductive age. The term refers to the inability of couples to achieve pregnancy after one year of unprotected sexual activity. The male factor is solely responsible in 20%, and 30-40% with the couple.
The initial evaluation of the male reproductive situation is the seminogram, which is considered as a key assessment tool.
Several conditions may be associated with infertility in men, such as endocrine-metabolic diseases such as hypogonadism, hyperprolactinaemia, dysthyroidism, dyslipidaemia, alterations glucose and insulin alteration, central obesity, or to the group of parameters called metabolic syndrome (MS). Obesity contributes to development of hypertension, dyslipidaemia and insulin resistance.
The aim of our review was to find documents that showed the impact of the association between waist circumference and insulin resistance in semen parameters as a possible origin of male infertility. The search for information was conducted in Medline, ScienceDirect, and Scopus. The terms used for the basic search were: obesity, abdominal circumference, insulin resistance, male infertility, semen, semen parameters.
There are studies documenting the deleterious effect of obesity and insulin resistance in female fertility. Some performed in men suggest harmful effects on their reproductive potential.
Semen anomalies are found in obese men with insulin resistance, but still require further studied to assess the association between them. The literature reports semen anomalies associated with obesity that are still to be elucidated.
El objetivo de nuestra revisión fue documentar de la literatura médica el impacto que existe de la asociación entre circunferencia abdominal e insulinorresistencia en los parámetros seminales como posible etiología de infertilidad masculina.
MetodologíaLa búsqueda se llevó a cabo en Medline, ScienceDirect y Scopus; se tomaron como base para la revisión los términos: obesidad, circunferencia abdominal, resistencia a la insulina (RI), infertilidad masculina, semen y parámetros seminales. Se seleccionaron artículos en inglés y español que se pudiesen revisar en extenso publicados en el periodo 2004-2015. De estos artículos, la información que se buscó extraer fue la relación la de obesidad e insulinorresistencia en infertilidad masculina. El tipo de análisis de la información que se llevó a cabo fue descriptivo.
DiscusiónLa infertilidad afecta a entre el 8-15% de la población en general en etapa reproductiva. El término se refiere a la incapacidad de una pareja para lograr un embarazo posterior a un año de actividad sexual no protegida. El factor masculino es responsable de la misma en un 20% y combinada con la pareja en un 30-40%1.
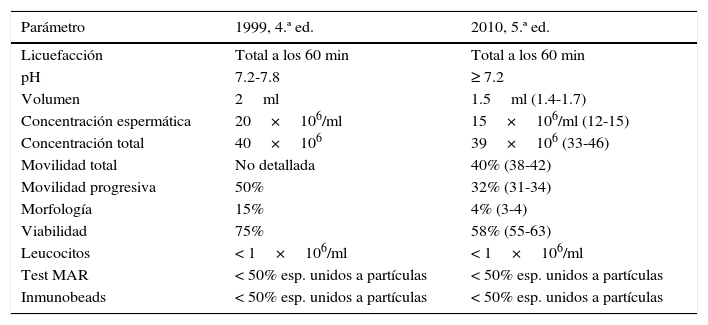
Considerado la herramienta inicial para la evaluación del factor masculino, el análisis seminal alterado por al menos 2 ocasiones identifica varones que deben ser estudiados a profundidad. Aunque no siempre será un reflejo verdadero de la fertilidad de un varón, un seminograma con parámetros alterados reconoce una disminución del potencial de fertilidad. Los valores de referencia utilizados para la interpretación del estudio seminal son los publicados por la Organización Mundial de la Salud (OMS) en 20102. Los valores reportados en esta publicación son los límites inferiores necesarios para conseguir una fertilización3,4. Se muestran en la tabla 1.
Valores de referencia del seminograma (OMS1999, 2010)4
| Parámetro | 1999, 4.ª ed. | 2010, 5.ª ed. |
|---|---|---|
| Licuefacción | Total a los 60 min | Total a los 60 min |
| pH | 7.2-7.8 | ≥ 7.2 |
| Volumen | 2ml | 1.5ml (1.4-1.7) |
| Concentración espermática | 20×106/ml | 15×106/ml (12-15) |
| Concentración total | 40×106 | 39×106 (33-46) |
| Movilidad total | No detallada | 40% (38-42) |
| Movilidad progresiva | 50% | 32% (31-34) |
| Morfología | 15% | 4% (3-4) |
| Viabilidad | 75% | 58% (55-63) |
| Leucocitos | < 1×106/ml | < 1×106/ml |
| Test MAR | < 50% esp. unidos a partículas | < 50% esp. unidos a partículas |
| Inmunobeads | < 50% esp. unidos a partículas | < 50% esp. unidos a partículas |
Valor de referencia 1999, límite inferior e intervalo de confianza del 95% entre paréntesis 2010.
La alteración seminal que con mayor frecuencia se presenta es la oligozoospermia (< 15×106/ml) y las causas que usualmente se relacionan con alteración del estudio seminal se muestran en la tabla 2, en donde la Asociación Europea de Urología no reporta alteraciones metabólicas identificadas en el estudio de 10,469 pacientes que realizó5.
Factores asociados a infertilidad masculina y porcentaje de distribución5
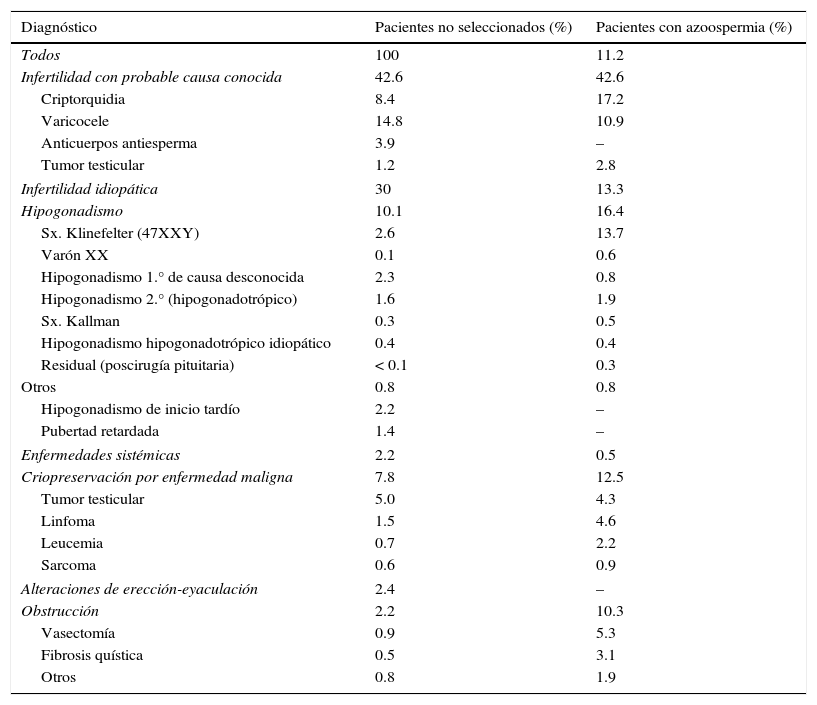
| Diagnóstico | Pacientes no seleccionados (%) | Pacientes con azoospermia (%) |
|---|---|---|
| Todos | 100 | 11.2 |
| Infertilidad con probable causa conocida | 42.6 | 42.6 |
| Criptorquidia | 8.4 | 17.2 |
| Varicocele | 14.8 | 10.9 |
| Anticuerpos antiesperma | 3.9 | – |
| Tumor testicular | 1.2 | 2.8 |
| Infertilidad idiopática | 30 | 13.3 |
| Hipogonadismo | 10.1 | 16.4 |
| Sx. Klinefelter (47XXY) | 2.6 | 13.7 |
| Varón XX | 0.1 | 0.6 |
| Hipogonadismo 1.° de causa desconocida | 2.3 | 0.8 |
| Hipogonadismo 2.° (hipogonadotrópico) | 1.6 | 1.9 |
| Sx. Kallman | 0.3 | 0.5 |
| Hipogonadismo hipogonadotrópico idiopático | 0.4 | 0.4 |
| Residual (poscirugía pituitaria) | < 0.1 | 0.3 |
| Otros | 0.8 | 0.8 |
| Hipogonadismo de inicio tardío | 2.2 | – |
| Pubertad retardada | 1.4 | – |
| Enfermedades sistémicas | 2.2 | 0.5 |
| Criopreservación por enfermedad maligna | 7.8 | 12.5 |
| Tumor testicular | 5.0 | 4.3 |
| Linfoma | 1.5 | 4.6 |
| Leucemia | 0.7 | 2.2 |
| Sarcoma | 0.6 | 0.9 |
| Alteraciones de erección-eyaculación | 2.4 | – |
| Obstrucción | 2.2 | 10.3 |
| Vasectomía | 0.9 | 5.3 |
| Fibrosis quística | 0.5 | 3.1 |
| Otros | 0.8 | 1.9 |
En el hombre diversas condiciones pueden asociarse a infertilidad; entre estas, se encuentran las patologías endocrinometabólicas6. Cuando la causa no es identificada, se determina infertilidad idiopática.
Existe un decremento en la calidad seminal desde la década de 1970, la cual se documenta en 2 metaanálisis8,17, en donde se atribuye tal efecto a factores ambientales y metodológicos, evento que también coincide con el incremento mundial de sobrepeso (IMC ≥ 25) y obesidad (IMC ≥ 30), así como las consecuencias que conllevan7.
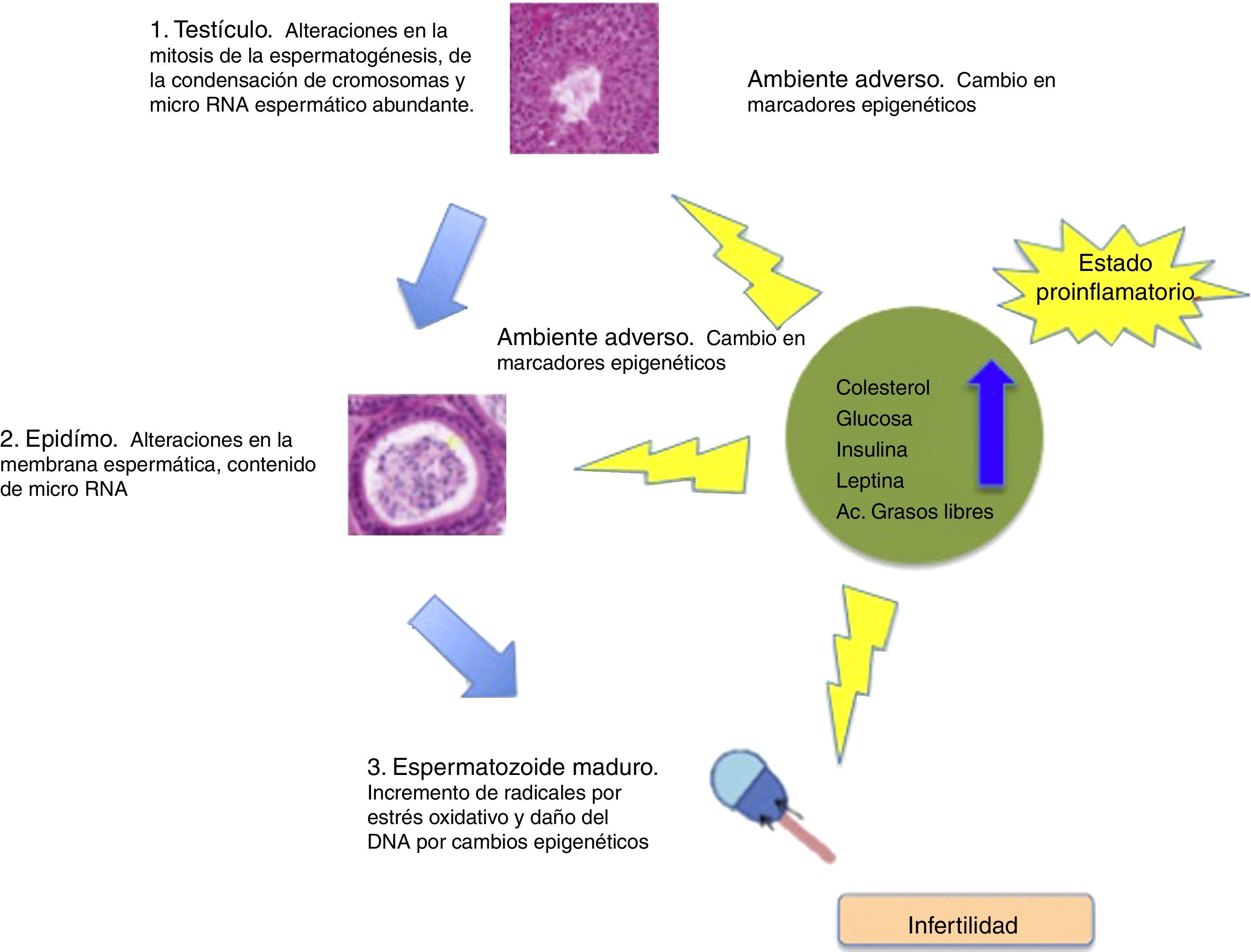
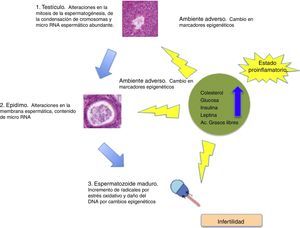
Sermondade et al. concluyen en su revisión sistemática que la obesidad en algunos hombres está asociada a incremento en oligozoospermia y astenozoospermia8. Eisenberg et al., utilizando los datos del estudio LIFE, encuentran una relación inversa de la adiposidad en varones con parámetros seminales alterados, sobre todo cuando la adiposidad es valorada por IMC y circunferencia abdominal9. La figura 1 muestra los efectos de la obesidad en la espermatogénesis.
La insulinorresistencia es la alteración metabólica más frecuentemente asociada a la obesidad. La OMS describió a la obesidad por el IMC ≥ 30 o el índice cintura-cadera > 0.9 para hombres y > 0.85 para mujeres y la insulinorresistencia como la captación de glucosa < 25% tras una prueba de pinzamiento euglucémico-hiperinsulinémico o alguna alteración en el metabolismo de la glucosa (glucosa basal alterada, diabetes mellitus o intolerancia a la glucosa).
Se define como insulinorresistencia a la elevación del índice del modelo creado para la evaluación de RI homeostasis model assessment (HOMA-IR). El índice HOMA se obtiene a través de una ecuación validada, que utiliza las concentraciones de insulina y glucosa en ayuno, permitiendo determinar la presencia de RI de manera fácil y poco invasiva, por lo que se utiliza con frecuencia10.
Es un método práctico, con adecuada correlación con el pinzamiento hiperinsulinémico euglucémico, considerado el gold estándar para determinar RI11.
Zhang et al. en su metaanálisis estudiando 29 regiones con tejido adiposo observan que la grasa visceral resultó ser la que se asocia con insulinorresistencia en mayor medida12. Así mismo la RI es el vínculo entre la obesidad y otras condiciones metabólicas que confieren riesgo de enfermedad cardiovascular y que forman parte del diagnóstico del síndrome metabólico. Como parte de los criterios diagnósticos del síndrome metabólico, ambas condiciones fueron utilizadas por la OMS en 1999.
Actualmente, la obesidad abdominal sigue formando parte de los criterios diagnósticos que se utilizan con frecuencia al igual que la glucosa en ayuno, como fueron propuestos por la Federación Internacional de Diabetes, no así la insulinorresistencia. También utiliza la circunferencia abdominal y no el IMC, ya que es el parámetro que aporta mayor información sobre los efectos negativos de la grasa visceral. La glucosa basal ≥ 100mg o el diagnóstico de diabetes mellitus tipo 2 (DM2) es otro parámetro utilizado13. La glucosa alterada permite identificar a individuos con insulinorresistencia, aunque evidentemente existirán algunos más que presenten RI y que no muestren alteraciones de la glucosa.
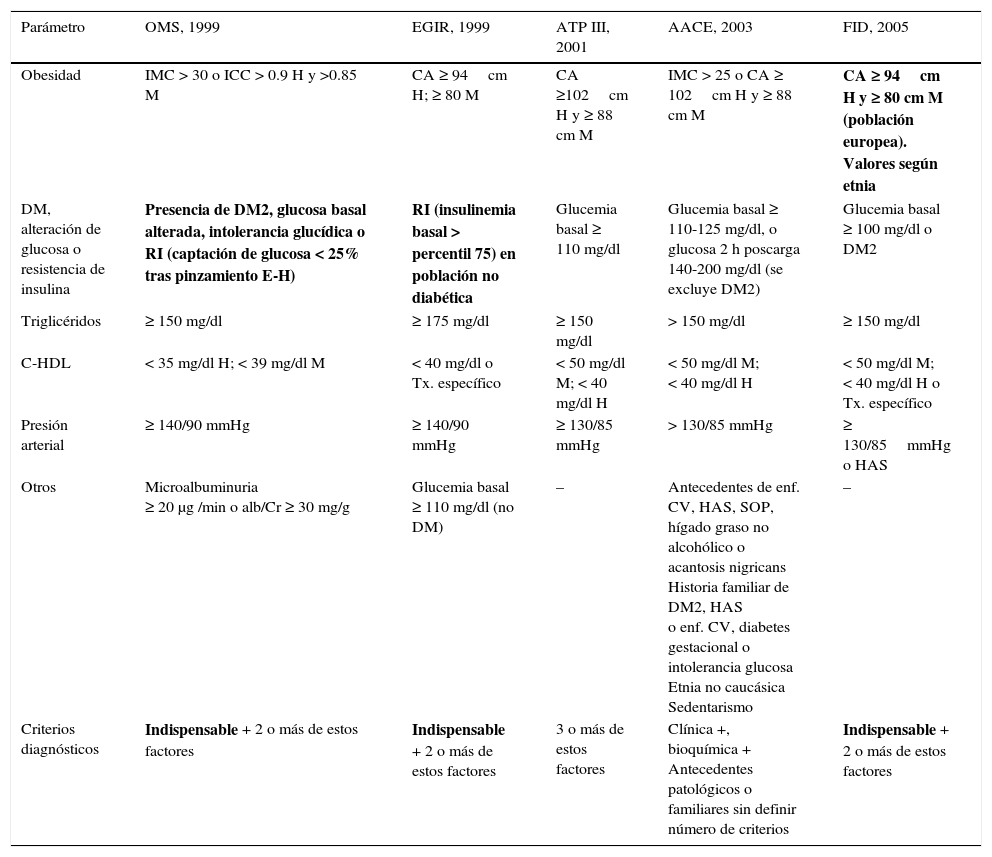
Recordemos que la RI es un estado previo a estas manifestaciones glucémicas y que gracias a la evaluación del modelo homeostático empleado para identificar la RI (HOMA-IR > 2.5) se logra conocer a adultos con dicha alteración metabólica. La tabla 3 muestra los diferentes criterios diagnósticos utilizados para el síndrome metabólico14.
Criterios diagnósticos para síndrome metabólico
| Parámetro | OMS, 1999 | EGIR, 1999 | ATP III, 2001 | AACE, 2003 | FID, 2005 |
|---|---|---|---|---|---|
| Obesidad | IMC > 30 o ICC > 0.9 H y >0.85 M | CA ≥ 94cm H; ≥ 80 M | CA ≥102cm H y ≥ 88 cm M | IMC > 25 o CA ≥ 102cm H y ≥ 88 cm M | CA ≥ 94cm H y ≥ 80 cm M (población europea). Valores según etnia |
| DM, alteración de glucosa o resistencia de insulina | Presencia de DM2, glucosa basal alterada, intolerancia glucídica o RI (captación de glucosa < 25% tras pinzamiento E-H) | RI (insulinemia basal > percentil 75) en población no diabética | Glucemia basal ≥ 110 mg/dl | Glucemia basal ≥ 110-125 mg/dl, o glucosa 2 h poscarga 140-200 mg/dl (se excluye DM2) | Glucemia basal ≥ 100 mg/dl o DM2 |
| Triglicéridos | ≥ 150 mg/dl | ≥ 175 mg/dl | ≥ 150 mg/dl | > 150 mg/dl | ≥ 150 mg/dl |
| C-HDL | < 35 mg/dl H; < 39 mg/dl M | < 40 mg/dl o Tx. específico | < 50 mg/dl M; < 40 mg/dl H | < 50 mg/dl M; < 40 mg/dl H | < 50 mg/dl M; < 40 mg/dl H o Tx. específico |
| Presión arterial | ≥ 140/90 mmHg | ≥ 140/90 mmHg | ≥ 130/85 mmHg | > 130/85 mmHg | ≥ 130/85mmHg o HAS |
| Otros | Microalbuminuria ≥ 20 μg /min o alb/Cr ≥ 30 mg/g | Glucemia basal ≥ 110 mg/dl (no DM) | – | Antecedentes de enf. CV, HAS, SOP, hígado graso no alcohólico o acantosis nigricans Historia familiar de DM2, HAS o enf. CV, diabetes gestacional o intolerancia glucosa Etnia no caucásica Sedentarismo | – |
| Criterios diagnósticos | Indispensable + 2 o más de estos factores | Indispensable + 2 o más de estos factores | 3 o más de estos factores | Clínica +, bioquímica + Antecedentes patológicos o familiares sin definir número de criterios | Indispensable + 2 o más de estos factores |
AACE: Sociedad Americana de Endocrinología Clínica; ATP III: Panel de Tratamiento del Adulto III; CA: circunferencia abdominal; EGIR: Grupo Europeo de estudio de la Resistencia a la Insulina; E-H: euglucémico-hiperinsulinémico; enf. CV: enfermedad cardiovascular; H: hombres; HAS: hipertensión arterial sistémica; ICC: índice cintura-cadera; IMC: índice de masa corporal; M: mujeres; DM2: diabetes mellitus tipo 2; OMS: Organización Mundial de la Salud; RI: resistencia a insulina; SOP: síndrome de ovario poliquístico; Tx.: tratamiento.
Tomado de referencia 13.
Negritas: criterios indispensables para diagnóstico.
En la literatura internacional existen estudios que han buscado la relación de la obesidad con infertilidad masculina, sobre todo cuando está asociada a hipogonadismo. La información que se tiene sobre el efecto de la obesidad en el estudio seminal es aún escasa.
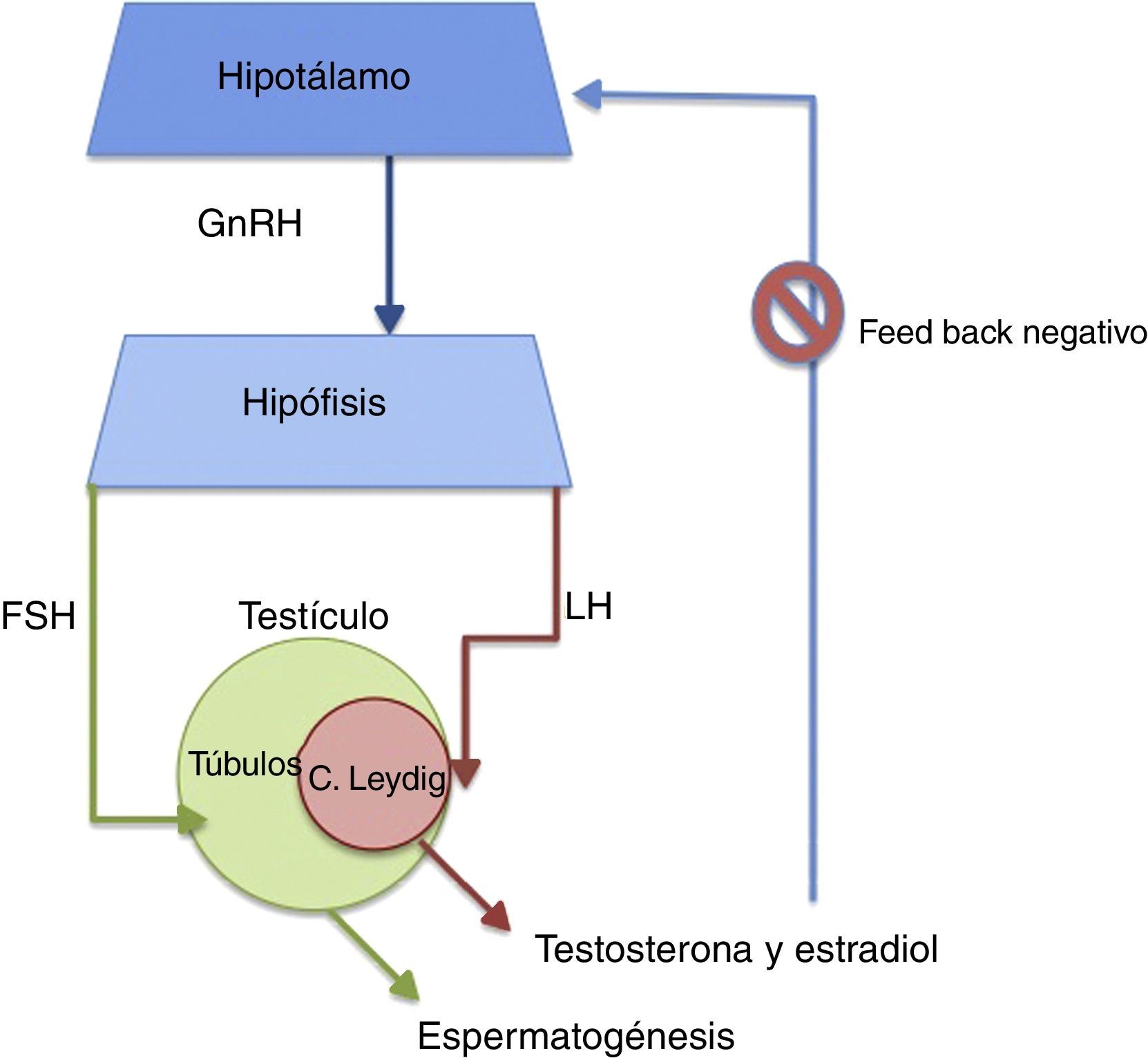
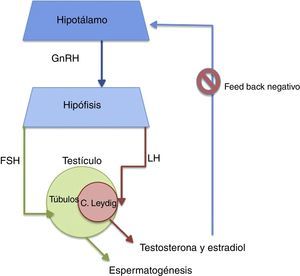
Algunos estudios han encontrado asociación entre la obesidad y cambios hormonales que finalmente tienen efecto a nivel reproductivo masculino. La probabilidad se basa en que la fisiopatología liga la obesidad con disminución de los niveles circulantes de testosterona, hormona fundamental para la espermatogénesis, por lo que en estos varones no es difícil encontrar alteraciones en el seminograma15. La figura 2 muestra la regulación hormonal de la función testicular y la producción androgénica.
El eje hipotálamo-hipófisis-testículo se ve afectado en varones con el incremento del IMC; la alteración se produce porque la globulina fijadora de hormonas sexuales se suprime por efecto de la elevación de insulina que puede existir en hombres obesos, lo que aumenta la disponibilidad de andrógenos libres biodisponibles para el tejido graso que los aromatiza aumentando así la producción de estrógenos.
La alta sensibilidad del hipotálamo a las hormonas esteroideas permite que la producción de hormona liberadora de gonadotropinas se vea disminuida por el incremento de estrógenos, es decir, se lleva a cabo una retroalimentación negativa, con lo que el eje hipotálamo-hipófisis-testículo baja la producción de testosterona16.
La disminución de testosterona total, de concentraciones de inhibina B y menor número de pulsos de hormona luteinizante, producidos por esta retroalimentación, son el resultado de falta de estímulo a la célula de Leydig, que disminuye la secreción de testosterona, y a su vez estos niveles bajos de testosterona se relacionan con alteraciones en parámetros seminales17.
Estudios epidemiológicos en humanos mencionan al hipogonadismo como factor de riesgo para desarrollo de DM2, lo que sugiere que algunos de estos sujetos cursarán con RI antes del diagnóstico de DM218.
Estados como la hiperinsulinemia y la hiperglucemia presentan un efecto inhibitorio en la cantidad y calidad seminal19, el cual parece asociarse a disfunción mitocondrial espermática secundaria al estado glucémico20.
Estudios en modelos de especies inferiores (roedores)21 establecen la relación de la obesidad con la reducción de la movilidad y morfología espermática, siendo importante mencionar que estos estudios muestran significación en el descenso de testosterona y presencia de RI22, y concluyen que la RI puede ser el agente causal del hipogonadismo que se presenta en ellos.
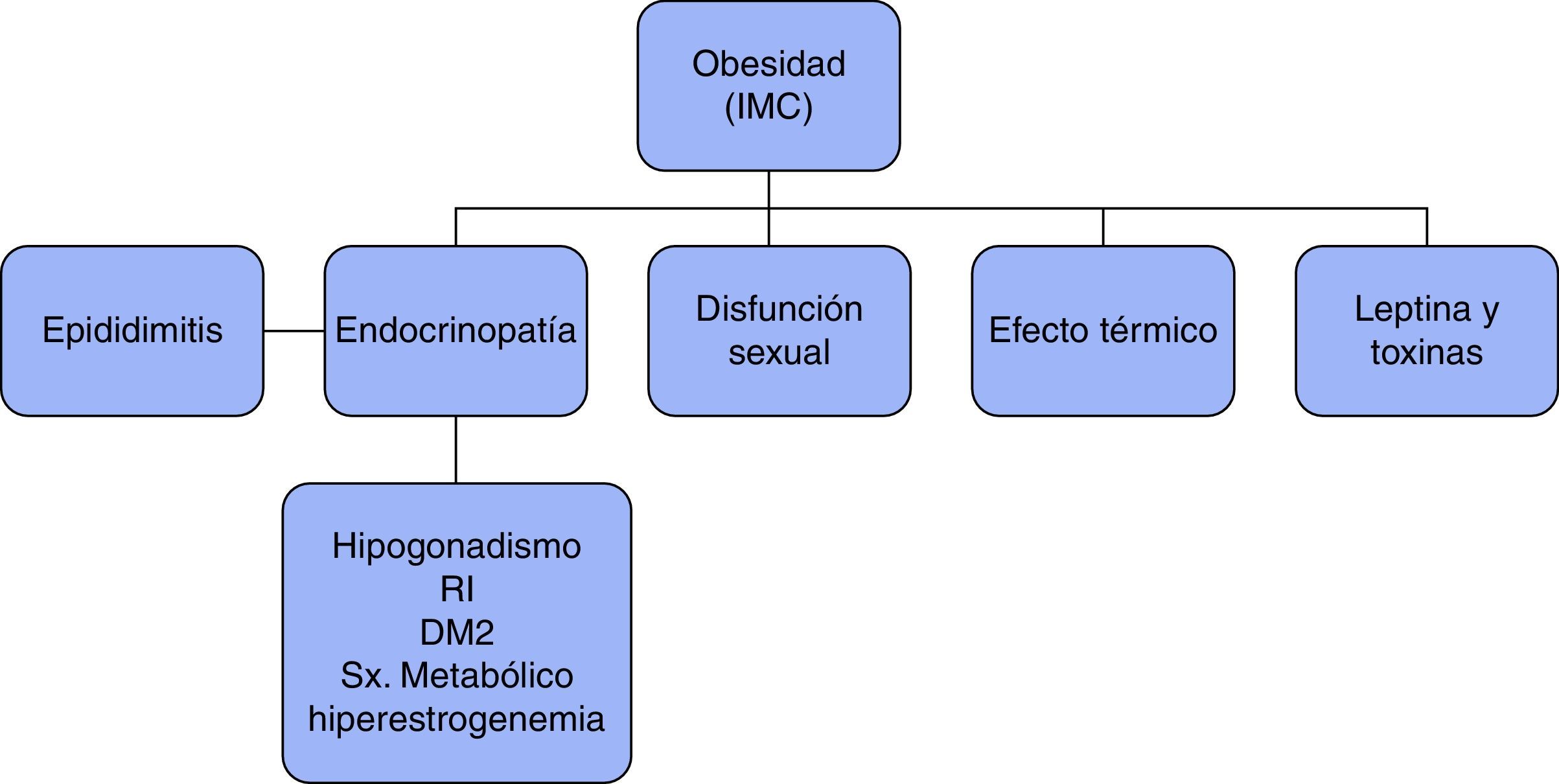
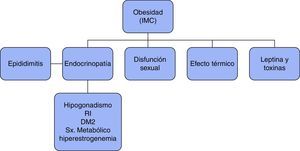
Leisegang et al. reportan niveles incrementados de insulina y leptina en el fluido seminal de hombres obesos, lo que sugiere un probable mecanismo por el que la espermatogénesis de estos varones se ve comprometida23. Otros estudios reportan concentración espermática baja en esta población con obesidad. La figura 3 muestra efectos clínicos y bioquímicos de la obesidad.
Aún queda mucho por investigar y dilucidar sobre el efecto que tiene la obesidad en la fertilidad masculina. Partiendo del hecho de que existen algunos varones obesos que logran la concepción, es trascendente conocer las condiciones que le permiten a ese espermatozoide, pese a los efectos bioquímicos a los que es sometido, lograr la fertilización y conseguir el embarazo.
Determinar con precisión la causa que les impide la concepción en este grupo de individuos permitirá comprender mejor la fisiopatología de la infertilidad masculina y buscar nuevos y oportunos manejos para favorecer su potencial de fertilización.
La fertilidad masculina tiene un campo extenso por descubrir que nos llevará a mejorar la medicina reproductiva y, con ello, la posibilidad de tener varones más sanos convertidos en padres.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.