Adalimumab (ADA) es el único tratamiento biológico aprobado por la Food and Drug Administration para el tratamiento de la hidradenitis supurativa (HS) moderada/severa. El objetivo de este estudio es evaluar la efectividad y seguridad de ADA en el tratamiento de HS en nuestra práctica clínica diaria.
MetodologíaEvaluamos retrospectivamente a los pacientes con HS atendidos en nuestro Servicio de Dermatología entre septiembre de 2015 y agosto de 2019 que fueron tratados como mínimo durante 3 meses con ADA.
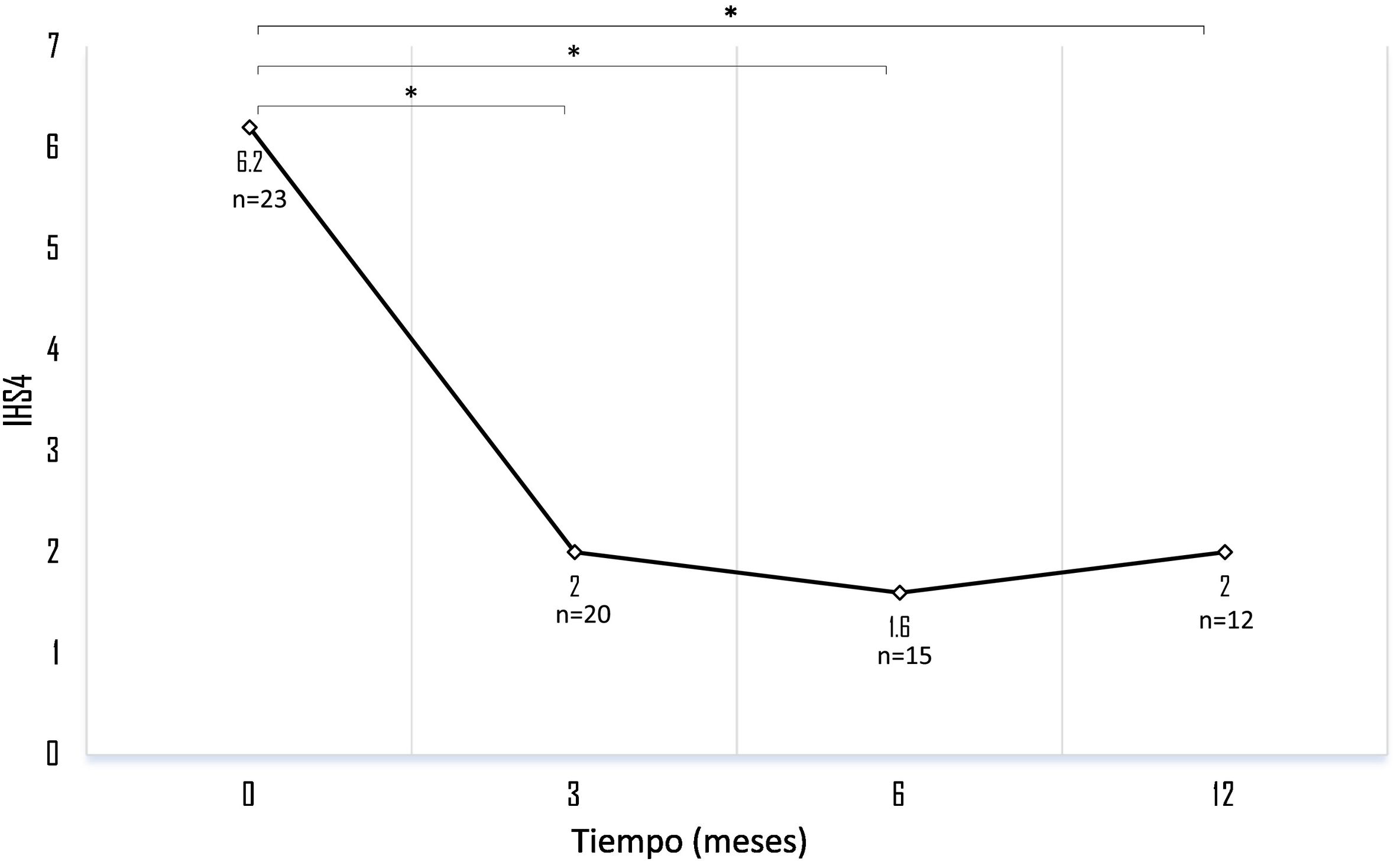
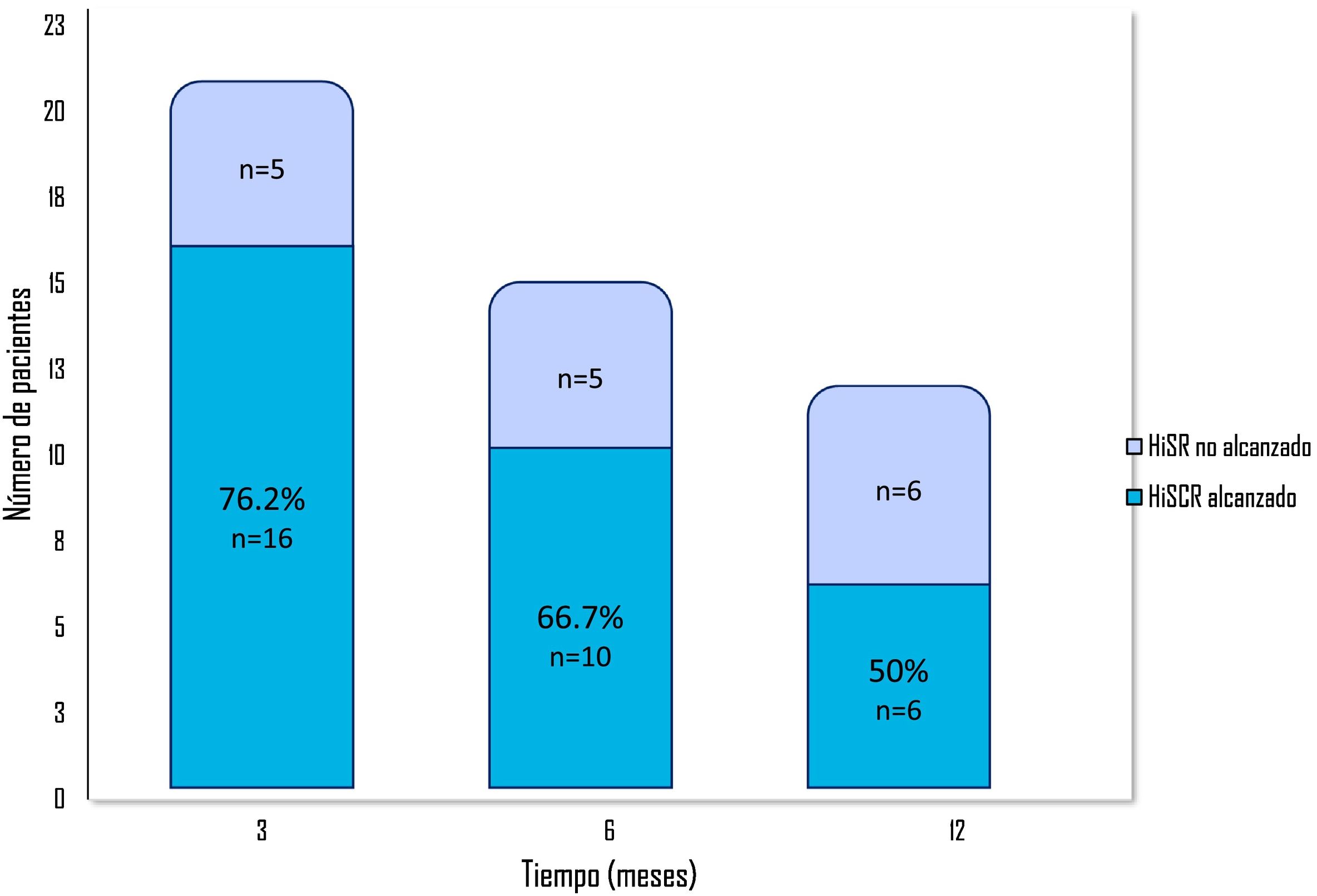
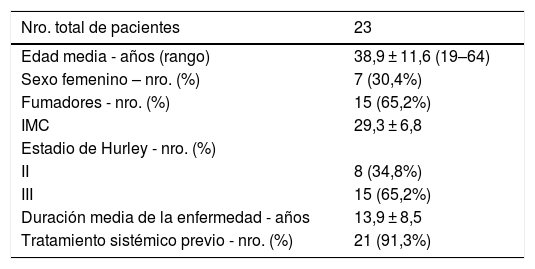
ResultadosRecolectamos 23 pacientes. La edad media de la muestra fue 38.9 ± 11.6 años. La duración media del tratamiento fue 13.3 ± 8.2 meses. El valor medio del IHS4 basal a los 3, 6 y 12 meses fue de 6.2 ± 4.8, 2 ± 4.7, 1.6 ± 3.6 y 2 ± 2.5, respectivamente. Este descenso fue estadísticamente significativo al contrastar el valor medio del Hidradenitis Suppurativa Severity Score System basal con su valor pareado correspondiente a los 3, 6 y 12 meses usando la prueba signo-rango de Wilcoxon (p < 0,05). El 76,2% de los pacientes cumplió los criterios Hidradenitis Suppurativa Clinical Response al mes 3, el 66,7%, al mes 6 y el 57%, al mes 12. Dieciséis pacientes estaban todavía en tratamiento con ADA al final del período estudiado. La causa más frecuente de suspensión del tratamiento fue el fallo secundario. El único efecto adverso que llevó a la interrupción de ADA fue la sospecha de artritis lúpica inducida por anti-TNF en un paciente.
ConclusionesADA parece ser un tratamiento efectivo y seguro en el tratamiento de la HS moderada/severa.
Adalimumab (ADA) is currently the only Food and Drug Administration-approved biologic treatment for moderate to severe Hidradenitis Suppurativa (HS). The objective of this study is to assess the effectiveness and safety of ADA in the treatment of HS in our daily practice.
MethodologyPatients with HS who visited our Dermatology Department between September 2015 and August 2019 and were treated with ADA for at least 3 months were retrospectively evaluated.
Results23 outpatients were collected. The mean age of the sample was 38.9 ± 11.6. The mean duration of treatment was 13.3 ± 8.2 months. Mean Hidradenitis Suppurativa Severity Score System (IHS4) score at baseline, 3, 6 and 12 months were 6.2 ± 4.8, 2 ± 4.7, 1.6 ± 3.6 and 2 ± 2.5, respectively. This decrease is statistically significant contrasting baseline IHS4 to their matched available values at each point of time (3, 6 and 12 months) using Wilcoxon Signed-Rank Test (p < 0,05). 76.2% of patients achieved HiSCR at month 3, 66.7% patients achieved Hidradenitis Suppurativa Clinical Response (HiSCR) at month 6 and 57% patients achieved HiSCR at month 12. Sixteen patients were still under ADA treatment at the end of the studied period of time. The main cause of withdrawal was secondary failure. The only serious adverse effect that led to ADA discontinuation was the suspicion of anti-TNF-induced lupus arthritis in one patient.
ConclusionsADA has shown to be effective and safe in patients with moderate to severe HS.
Artículo
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora