La tasa de coinfección por sífilis y virus de la inmunodeficiencia humana (VIH) varía en función de la prevalencia de cada una de estas enfermedades en la población analizada, junto con los factores de riesgo individuales. En un estudio español de 1.161 pacientes con VIH, la seroprevalencia de sífilis era del 13% y un 4% más se diagnosticó de sífilis en un período de 38 meses de seguimiento1.
Es clara la sinergia epidemiológica entre la lúes y el VIH. De hecho, Chesson et al2 han descrito que por cada 20 muertes por sida/100.000 varones adultos se reduce la incidencia de sífilis en un 7–12%. Con la introducción del tratamiento antirretroviral de alta resolución (TAR), el número de muertes por sida se ha reducido, pero se ha incrementado la incidencia de otras infecciones de transmisión sexual, entre ellas la lúes.
La infección por el VIH puede alterar la presentación clínica, la progresión y la eficacia del tratamiento de la sífilis3–5. En la actualidad, la neurosífilis es más frecuente en pacientes infectados por el VIH con formas tempranas de neurosífilis, sobre todo neurosífilis asintomática. Cuanto más alterado esté el líquido cefalorraquídeo (LCR), mayor posibilidad de desarrollar neurosífilis sintomática existirá6.
Ante el gran incremento de la incidencia de sífilis en países occidentales, incluida España1,7–12, detectado en los últimos años, y teniendo en cuenta que un alto porcentaje de los pacientes están coinfectados por el VIH, es importante establecer pautas claras de actuación para detectar los casos asintomáticos de neurosífilis en estos pacientes.
Neurosífilis e infección por el virus de la inmunodeficiencia humana: indicaciones de la punción lumbarLa neurosífilis se ha considerado incorrectamente como una manifestación tardía de la enfermedad. El término neurosífilis se refiere a la infección del sistema nervioso central (SNC) por Treponema pallidum y puede ocurrir en cualquier momento tras la infección inicial.
La clasificación tradicional de la neurosífilis se basa en el concepto de que las diferentes variantes de neurosífilis son dependientes del tiempo. En la sífilis precoz, las formas más frecuentes de neurosífilis afectan a las meninges o a la vasculatura (meningitis o enfermedad meningovascular). En fases tardías, se afectan más el parénquima cerebral y la médula espinal (paresia general y tabes dorsal). Timmermans y Carr13 refieren que la terminología hasta entonces usada en la neurosífilis carece de unas definiciones precisas y proponen una clasificación, según la naturaleza del déficit clínico predominante y los hallazgos de laboratorio, dentro de 6 categorías diagnósticas que se pueden superponer (tabla 1).
Categorías diagnósticas de la neurosífilis (Timmermans y Carr13, 2004)
| Categoría 1: desórdenes neuropsiquiátricos |
| Psicosis, delírium y demencia |
| Categoría 2: accidentes cerebrovasculares |
| Déficit neurológico, focal, agudo, compatible con ACV o evidencia radiológica de ACV |
| Categoría 3: ocular |
| Uveítis, pérdida visual o disfunción del nervio óptico |
| Categoría 4: mielopatía |
| Disfunción de la médula espinal aguda, subaguda o crónica, incluida tabes dorsal |
| Categoría 5: convulsiones |
| Crisis parciales, con generalización o no, o mioclonías |
| Categoría 6: afectación encefálica y de pares craneales |
ACV: accidente cerebrovascular.
En la era preantibiótica, la neurosífilis era más frecuente (25–35%)14. La tercera parte de estos pacientes tenía neurosífilis asintomática, otra tercera parte tenía tabes dorsal y al menos un 10% tenía paresia. La sífilis meningovascular se observaba en un 10%.
En la actualidad, las formas tardías han decaído, y las formas tempranas son las más comunes, sobre todo la neurosífilis asintomática y la meningitis sintomática. La mayoría son pacientes infectados por el VIH con sífilis precoz activa.
La T. pallidum invade el SNC en el 25% de los pacientes, independientemente de si están infectados o no por el VIH. La invasión por T. pallidum no siempre resulta en infección persistente; la resolución espontánea puede ocurrir sin respuesta inflamatoria. En otros casos, la resolución espontánea puede ocurrir tras una meningitis transitoria. Si existe un fallo en la eliminación de bacterias del LCR, T. pallidum puede persistir (meningitis asintomática) o progresar clínicamente. Los pacientes no infectados por el VIH sin tratamiento desarrollan neurosífilis entre un 4–9%9,15, pero el porcentaje de pacientes infectados por el VIH sin tratamiento que desarrollan neurosífilis es incierto. La infección por el VIH facilita la neuroinvasión por T. pallidum y viceversa, y empeora la respuesta inmunológica, por lo que es más difícil eliminar treponemas del SNC.
La T. pallidum no se puede cultivar, pero sí aislar. A principios del siglo xx se hicieron estudios que mostraron que durante la sífilis precoz hasta un 70% de los pacientes tenía alteraciones del LCR (pleocitosis, aumento de la concentración de proteínas y test de Wasserman reactivo). Hasta en un 25% se aisló T. pallidum, incluso en ausencia de alteraciones en el LCR. En las fases tardías, las alteraciones del LCR y el aislamiento de treponema son menos frecuentes16,17. La detección de T. pallidum no es más común en pacientes infectados por el VIH, no está asociada a desarrollo de neurosífilis sintomática y no predice el fallo del tratamiento. Sí se asocia con el hallazgo de pleocitosis en LCR, pero no con reactividad de Venereal Disease Research Laboratory (VDRL) ni con aumento de concentración de proteínas en el LCR.
En la era prebiótica, la existencia de alteraciones en el LCR durante cualquier fase de la enfermedad aumentaba el riesgo de neurosífilis sintomática. Actualmente, entre un 30–40% de los pacientes presentan alteraciones del LCR durante la sífilis precoz activa, que no predicen el fallo del tratamiento ni la progresión a neurosífilis16,17. En los pacientes infectados por el VIH las alteraciones del LCR son más frecuentes18.
En un estudio se demostró que los pacientes infectados por el VIH con sífilis primaria o secundaria tenían una tasa de fallo serológico mayor que los no infectados por el VIH; se entiende por fallo la falta de reducción de los títulos de Rapid Plasma Reagin (RPR) en plasma en 2 diluciones o más durante los meses posteriores al tratamiento de sífilis primaria o secundaria. Sin embargo, en ambos grupos la tasa de fallo clínico era infrecuente. La importancia clínica de esta diferencia de patrones serológicos es incierta. Podría indicar una mayor tasa de fallo del tratamiento, pero también podría ser el resultado de una respuesta inmunitaria diferente, sin estar relacionado con la eficacia del tratamiento16,19,20.
Pero está descrito que la infección por el VIH puede alterar el curso natural de la sífilis. La neurosífilis es asintomática hasta en un 60% de los casos y los restantes suelen tener afectación de pares craneales, sobre todo el facial y el auditivo21. En la literatura médica existen numerosos casos de pacientes infectados por el VIH con manifestaciones graves de sífilis, progresión acelerada a formas tardías, incluidas neurosífilis y sífilis ocular, así como recaídas con afectación neurológica, a pesar de un tratamiento penicilínico adecuado22,23.
En 1976, 2 estudios demostraron la persistencia de treponemas en el LCR después de la dosis estándar de penicilina, y no se detectó penicilina en LCR en 2 pacientes que habían recibido penicilina benzatina24,25. En 1987, también se describió la persistencia de treponemas viables en el LCR en 2 pacientes infectados por el VIH17. En un paciente infectado por el VIH, si fallase el tratamiento antirretroviral y aumentase la inmunosupresión, los treponemas persistentes en el LCR podrían reactivarse. Esto, unido a las comunicaciones de manifestaciones graves y a las recaídas con afectación neurológica, justifica la idea de algunos especialistas de realizar punción lumbar ante todo paciente coinfectado por sífilis y el VIH22. Pero no todos comparten esta actitud.
Las últimas guías de los Centers for Disease Control and Prevention (CDC)19,20 (tabla 2) no contemplan la punción lumbar en pacientes coinfectados por el VIH y sífilis precoz, y argumentan que aunque las alteraciones del LCR en estos pacientes son frecuentes, su significado clínico y pronóstico es incierto, que un VDRL reactivo durante la sífilis precoz se volverá no reactivo sin tratamiento específico para neurosífilis y que si la afectación neurológica fuese importante se habrían detectado más casos.
Indicaciones de punción lumbar (CDC 2002/CDC 2006)19,20
| Signos neurológicos/oftalmológicos/óticos |
| Sífilis terciaria activa |
| Fracaso del tratamiento |
| Paciente infectado con VIH, con sífilis latente tardía o de duración incierta |
VIH: virus de la inmunodeficiencia humana.
*En las guías CDC 2002 ya se cita la opinión de algunos especialistas de realizar punción lumbar a aquellos pacientes con una titulación RPR superior o igual a 1/32, y en las guías CDC 2006 se añade la opinión de otros de realizar punción lumbar en pacientes infectados por VIH con recuento de linfocitos CD4+ inferior o igual a 350/μl.
Hasta la fecha no hay estudios que demuestren que un VDRL reactivo en LCR sea menos indicativo de neurosífilis en un paciente con sífilis precoz que en un paciente con sífilis latente tardía o de duración incierta. Por otro lado, desconocemos la incidencia real de neurosífilis14,26.
Aunque las guías europeas para el tratamiento de sífilis (2001) coinciden con los CDC en indicar la punción lumbar cuando existe afectación del SNC y en lúes tardías, indican, además, punción lumbar 2 años más tarde a todo paciente coinfectado por VIH y sífilis precoz27.
En resumen, ante un paciente infectado por el VIH y sífilis precoz activa, algunos expertos no realizan nunca punción lumbar si no existe sospecha clínica de neurosífilis, mientras otros difieren la punción lumbar 2 años más tarde. No obstante, ambas actitudes conllevan el riesgo de pérdida de pacientes y de neurosífilis no detectadas y no tratadas. Por último, expertos más conservadores prefieren realizar punción lumbar de forma sistemática en pacientes coinfectados por VIH y sífilis antes de iniciar el tratamiento e incluso algunos recomiendan repetirla de forma periódica9,19.
Los últimos estudios han demostrado que, con independencia de la fase clínica de la infección luética o de haber recibido tratamiento previo, en el paciente coinfectado por VIH un ajuste de la dosis RPR en suero superior o igual a 1:32 incrementa 6 veces el riesgo de tener neurolúes26,28 y un recuento en sangre periférica de linfocitos CD4+ inferior o igual a 350/μl lo triplica. Ambos factores son independientes, de forma que, si coincidieran, el riesgo se incrementaría 18 veces26.
Teniendo en cuenta estos estudios, si sólo realizamos punción lumbar en aquellos pacientes infectados por VIH con sífilis latente tardía o de duración incierta, estamos ignorando a pacientes con alto riesgo de neurosífilis (pacientes con VIH y sífilis precoz con títulos de RPR en suero superiores o iguales a 1/32 o recuento de linfocitos CD4+ inferiores o iguales a 350/μl) y realizando pruebas innecesarias en pacientes con bajo riesgo (pacientes con VIH y sífilis latente tardía o de duración incierta con títulos de RPR en suero inferiores a 1/32 y recuento de linfocitos CD4+ superiores a 350/μl)28,29.
Diagnóstico y seguimiento de la neurosífilis en el paciente infectado por el virus de la inmunodeficiencia humanaEl diagnóstico de neurosífilis se basa habitualmente en la historia clínica, la exploración física y los hallazgos en el LCR.
La neurosífilis produce pleocitosis linfocitaria e hiperproteinorraquia en LCR. En el paciente no infectado por el VIH, un recuento de leucocitos superior a 5/mm3 y una concentración de proteínas superior a 45mg/dl son consistentes con el diagnóstico de neurosífilis30.
En el paciente infectado por el VIH, realizar el diagnóstico de neurosífilis es más complicado, porque estos hallazgos también podrían producirse a causa del VIH. De todas formas, la pleocitosis causada por VIH suele ser leve y se considera que una pleocitosis superior a 20/mm3 es muy indicativa de neurolúes9,17.
La realización de VDRL en LCR se considera la prueba estándar por su alta especificidad19, aunque tiene una baja sensibilidad (30%), por lo que podrían resultar falsamente negativos hasta un 70% de los pacientes con neurosífilis31. Por tanto, un valor positivo confirma el diagnóstico, pero un valor negativo no la descarta. También puede resultar falsamente positivo, si existe contaminación con sangre y si los títulos de RPR en plasma son muy altos32.
Algunos especialistas recomiendan determinar Fluorescent treponemal antibody-absorption (FTA-Abs) por su alto valor predictivo negativo, de forma que un resultado negativo excluye neurosífilis19. Los test de hemaglutinación son útiles para diagnosticar neurolúes, pero no se aconsejan en pacientes infectados por VIH, debido a los problemas de interpretación que generan9,33.
Si el paciente no tiene una historia conocida de sífilis previa, el primer paso antes de diagnosticar neurosífilis debe ser confirmar que el paciente fue infectado por T. pallidum. Los expertos consideran que, en general, las pruebas serológicas treponémicas y no treponémicas pueden interpretarse de la misma manera en pacientes infectados por el VIH que en los no infectados, pero es importante conocer que, en ocasiones, estos pacientes tienen respuestas serológicas inusuales, como títulos altos o falsos negativos por ausencia o retraso de la seroconversión34. La hipergammaglobulinemia policlonal que existe en los pacientes infectados por el VIH condiciona un exceso de anticuerpos, que impide la correcta aglutinación y visualización de los inmunocomplejos antígeno-anticuerpo (efecto prozona). El efecto prozona se corrige si se diluye la muestra35.
El éxito del tratamiento para neurosífilis se mide por la resolución o estabilización de la clínica y por la normalización de las alteraciones del LCR. Las últimas guías de los CDC20 recomiendan realizar examen del LCR 3 o 6 meses después del tratamiento y cada 6 meses hasta que el recuento de leucocitos en el LCR sea normal y el VDRL no sea reactivo, lo que indica que el recuento de leucocitos en el LCR debería reducirse 6 meses después del tratamiento (aunque no cuantifican esta reducción) y que todas las alteraciones del LCR deberían resolverse en los 2 años posteriores al tratamiento. Si estos 2 criterios no se cumplen, se debe retratar al paciente. También debe retratarse si el recuento de leucocitos en LCR aumenta o si los títulos de VDRL en el LCR se incrementan 4 veces.
Las guías europeas recomiendan realizar punción lumbar 1 o 2 años después del tratamiento para neurosífilis27.
Marra et al36 demostraron que la pleocitosis y el VDRL reactivo del LCR se normalizan, tras recibir tratamiento específico para neurosífilis, en el plazo de un año. En los pacientes infectados por el VIH es 2,5 veces menos probable que un VDRL reactivo en el LCR se normalice. Si el recuento de linfocitos CD4+ en sangre periférica es inferior o igual a 200/μl, es 3,7 veces menos probable que se normalice que si el recuento es superior a 200/μl. Estos datos indican que la respuesta inmunitaria alterada de los pacientes VIH+ contribuye a una normalización del VDRL en el LCR más lenta, pero es incierto si esto equivale a un fallo del tratamiento.
Estos autores también demostraron que los valores basales de los parámetros alterados antes del tratamiento (recuento leucocitario en LCR, títulos de VDRL en LCR, títulos de RPR en plasma) pueden modificar la posibilidad de normalización de cada uno, excepto la concentración de proteínas. Así, una pleocitosis elevada y unos títulos elevados de RPR en plasma se asociaron con una mayor probabilidad de normalización. Títulos de VDRL en LCR superiores a 1:1 tienen una posibilidad 5 veces menor de normalizarse que títulos inferiores o iguales a 1:1.
La concentración de proteínas en LCR disminuye más lentamente y de forma incompleta, de manera que cuando otros parámetros ya se han normalizado, la concentración de proteínas sigue siendo anormal; por eso, no es un buen indicador de éxito o fallo del tratamiento y no se debe retratar al paciente si es el único parámetro alterado.
En otro estudio, la normalización de los títulos de RPR en plasma en pacientes no infectados por el VIH y en pacientes infectados por el VIH con tratamiento antirretroviral predijo la normalización de alteraciones clínicas y del LCR (excepto la concentración de proteínas) en el 80% de los pacientes a los 4 meses, en más del 85% de los pacientes a los 7 meses y en más del 90% de los pacientes a los 13 meses37. Si la normalización de los títulos de RPR en plasma en estos pacientes predice el éxito del tratamiento de neurosífilis, podríamos evitar las punciones lumbares en el seguimiento, siempre que este sea exhaustivo.
Experiencia en el Servicio de Dermatología del Complejo Hospitalario Universitario de A Coruña (2003–2008)Entre enero de 2003 y mayo de 2006 (grupo 1) se realizó punción lumbar a todos los pacientes infectados por VIH y con infección sifilítica precoz activa (sífilis primaria o secundaria de curso inferior a un año), atendidos en el Servicio de Dermatología del Complejo Hospitalario Universitario de A Coruña.
Entre junio de 2006 y diciembre de 2008 (grupo 2), de acuerdo con las nuevas recomendaciones de la literatura médica, sólo se realizó punción lumbar a aquellos que tuviesen un ajuste de la dosis RPR superior o igual a 1:32 o un recuento en sangre periférica de linfocitos CD4+ inferior o igual a 350/μl o clínica neurológica, oftalmológica u ótica, o fracaso del tratamiento.
En todos los pacientes se realizó una exploración física, que incluyó una exploración neurológica. En los que tenían síntomas o signos visuales se efectuó un examen oftalmológico con lámpara de hendidura.
Los estudios analíticos y pruebas complementarias se indicaron en función de los hallazgos clínicos, incluidos, en todos los casos, hemograma, fórmula leucocitaria, VSG, bioquímica básica, proteinograma, RPR, FTA-Abs, VIH y recuento en sangre periférica de linfocitos CD4+.
El examen del LCR incluyó la determinación de glucosa, proteínas, leucocitos, eritrocitos, VDRL, FTA-Abs, tinción de Gram y cultivo microbiológico para bacterias, micobacterias y hongos.
Consideramos criterios diagnósticos de neurolúes una pleocitosis superior a 20 leucocitos/mm3 o VDRL positivo en LCR. Los datos clínicos y serológicos de ambos grupos se exponen en las tablas 3 y 4.
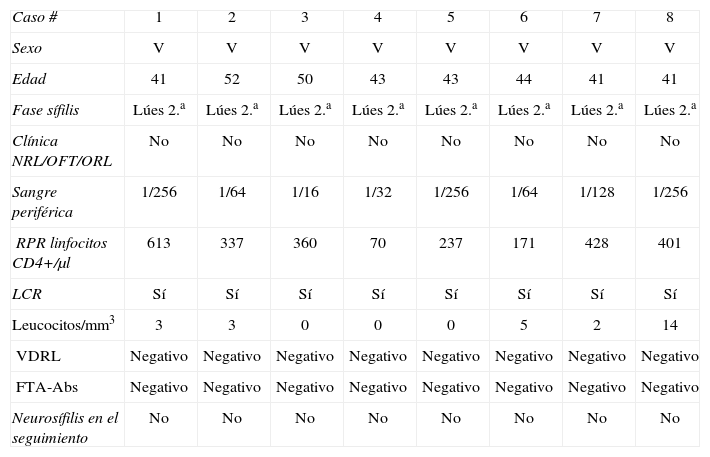
Grupo 1. Datos clínicos y de laboratorio
| Caso # | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Sexo | V | V | V | V | V | V | V | V |
| Edad | 41 | 52 | 50 | 43 | 43 | 44 | 41 | 41 |
| Fase sífilis | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a |
| Clínica NRL/OFT/ORL | No | No | No | No | No | No | No | No |
| Sangre periférica | 1/256 | 1/64 | 1/16 | 1/32 | 1/256 | 1/64 | 1/128 | 1/256 |
| RPR linfocitos CD4+/μl | 613 | 337 | 360 | 70 | 237 | 171 | 428 | 401 |
| LCR | Sí | Sí | Sí | Sí | Sí | Sí | Sí | Sí |
| Leucocitos/mm3 | 3 | 3 | 0 | 0 | 0 | 5 | 2 | 14 |
| VDRL | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo |
| FTA-Abs | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo | Negativo |
| Neurosífilis en el seguimiento | No | No | No | No | No | No | No | No |
LCR: líquido cefalorraquídeo; NRL: neurológica; OFT: oftalmológica; ORL: ótica.
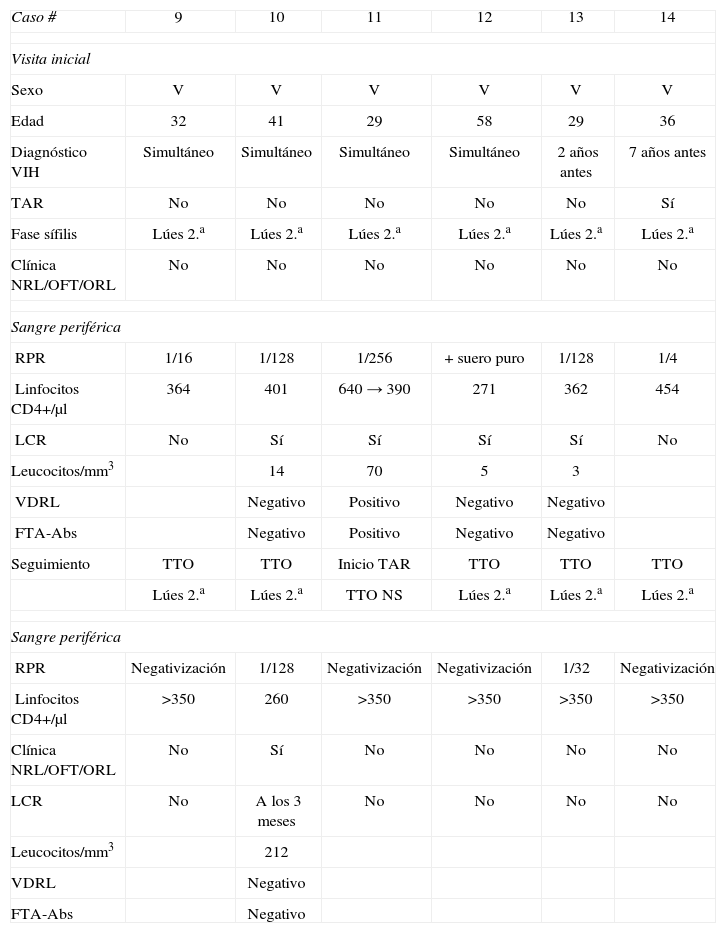
Grupo 2. Datos clínicos y de laboratorio
| Caso # | 9 | 10 | 11 | 12 | 13 | 14 |
| Visita inicial | ||||||
| Sexo | V | V | V | V | V | V |
| Edad | 32 | 41 | 29 | 58 | 29 | 36 |
| Diagnóstico VIH | Simultáneo | Simultáneo | Simultáneo | Simultáneo | 2 años antes | 7 años antes |
| TAR | No | No | No | No | No | Sí |
| Fase sífilis | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a | Lúes 2.a |
| Clínica NRL/OFT/ORL | No | No | No | No | No | No |
| Sangre periférica | ||||||
| RPR | 1/16 | 1/128 | 1/256 | + suero puro | 1/128 | 1/4 |
| Linfocitos CD4+/μl | 364 | 401 | 640 → 390 | 271 | 362 | 454 |
| LCR | No | Sí | Sí | Sí | Sí | No |
| Leucocitos/mm3 | 14 | 70 | 5 | 3 | ||
| VDRL | Negativo | Positivo | Negativo | Negativo | ||
| FTA-Abs | Negativo | Positivo | Negativo | Negativo | ||
| Seguimiento | TTO | TTO | Inicio TAR | TTO | TTO | TTO |
| Lúes 2.a | Lúes 2.a | TTO NS | Lúes 2.a | Lúes 2.a | Lúes 2.a | |
| Sangre periférica | ||||||
| RPR | Negativización | 1/128 | Negativización | Negativización | 1/32 | Negativización |
| Linfocitos CD4+/μl | >350 | 260 | >350 | >350 | >350 | >350 |
| Clínica NRL/OFT/ORL | No | Sí | No | No | No | No |
| LCR | No | A los 3 meses | No | No | No | No |
| Leucocitos/mm3 | 212 | |||||
| VDRL | Negativo | |||||
| FTA-Abs | Negativo | |||||
FTA-Abs: Fluorescent treponemal antibody-absorption; LCR: líquido cefalorraquídeo; NRL: neurológica; NS: neurosífilis; OFT: oftalmológica; ORL: ótica; TAR: tratamiento antirretroviral de alta resolución; TTO: tratamiento; VDRL: Venereal Disease Research Laboratory.
Grupo 1: entre enero de 2003 y mayo de 2006 se realizó punción lumbar a un total de 8 pacientes infectados por VIH con sífilis precoz activa (pacientes 1–8). Todos ellos tenían sífilis secundaria y la exploración neurológica fue rigurosamente normal. Ninguno tuvo síntomas o signos visuales, auditivos ni vestibulares.
En ningún caso existían criterios diagnósticos de neurosífilis, y los parámetros en el LCR entraban dentro de la normalidad o eran compatibles con infección por VIH. Tres pacientes (38%) presentaron un recuento de linfocitos CD4+ inferior o igual a 350/μl y 7 pacientes (87,5%) tenían un ajuste de la dosis en suero RPR superior o igual a 1/32 (datos publicados12).
Grupo 2: entre junio de 2003 y diciembre de 2008 se atendieron un total de 6 pacientes con sífilis precoz activa coinfectados por el VIH. Tres de los 6 pacientes (50%) tenían un ajuste de la dosis en suero RPR superior o igual a 1/32 y 2 de los 6 pacientes (33,3%) tenían un recuento de linfocitos CD4+ inferior o igual a 350/μl. Sólo 4 cumplían criterios para indicar la punción lumbar.
Se detectó un caso de neurosífilis asintomática (paciente 11), que tenía títulos altos de RPR en el suero y en las últimas semanas su función inmunitaria había decaído. Recibió la pauta de tratamiento para neurosífilis y durante 2 años de seguimiento nunca desarrolló neurosífilis sintomática. No se realizó una punción lumbar de control.
Al paciente 10 se le realizó una nueva punción lumbar a los 3 meses de seguimiento por sospecha clínica de neurosífilis sintomática, que se confirmó. Presentaba cefalea frontal y pérdida de audición temporal derecha desde hacía mes y medio, con mareos, fiebre intermitente y pérdida de atención. El ajuste de la dosis de RPR en sangre periférica no había descendido tras el tratamiento estándar para sífilis secundaria, y la función inmunitaria había decaído. Tras el tratamiento con pauta para neurosífilis, la clínica cutánea y neurológica remitió. En la punción lumbar de control, que se realizó una semana más tarde, las alteraciones del LCR habían mejorado.
Grupos 1 y 2: de un total de 14 pacientes infectados por el VIH con sífilis precoz activa, sólo 2 pacientes tenían neurosífilis. De un total de 15 indicaciones de punción lumbar (al paciente 10 se le realizaron 2 punciones lumbares), el 73% de los casos (11/15) presentaba una titulación superior o igual a 1/32 y el 42,85% (6/14) tenía un recuento de linfocitos CD4+ inferior o igual a 350/μl.
De los 11 pacientes que cumplían los criterios del grupo 2 para indicar punción lumbar, solo 2 tenían neurosífilis (18%). Además, los 2 pacientes no respondían a las pautas habituales de tratamiento de la sífilis y tenían un diagnóstico de VIH reciente, con una función inmunológica insuficiente, que podría obedecer a la primoinfección por el VIH o bien a que todavía no estaban estabilizados con tratamiento antirretroviral. Quizás en pacientes con un diagnóstico de VIH reciente se deba hacer un seguimiento más estrecho.
De los 3 que no cumplían estos criterios, ninguno tuvo neurosífilis. Si hubiésemos indicado la punción lumbar a los 14 pacientes de forma indiscriminada, habríamos indicado un procedimiento innecesario en un 22% (3/14).
Si, por el contrario, hubiésemos aplicado los criterios actuales de los CDC, que no contemplan la punción lumbar en pacientes con sífilis precoz asintomáticos, no habríamos detectado tan pronto uno de los 2 casos de neurosífilis (7,1%).
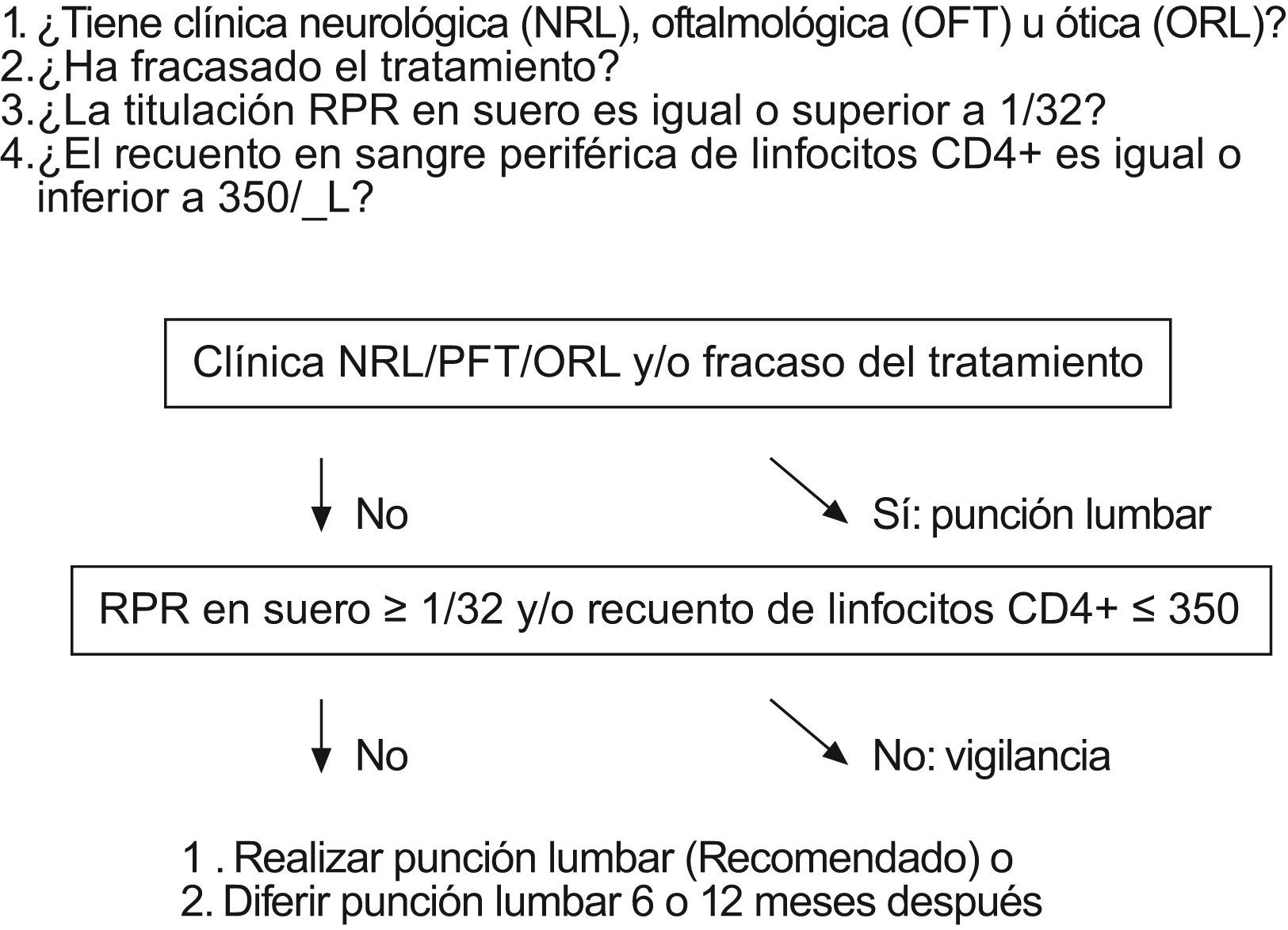
Nuestros datos apoyan la idea de que debe restringirse el uso de la punción lumbar a los casos con un riesgo relevante. Dado que el TAR ha modificado el curso de la infección por VIH y de la sífilis en estos pacientes, y teniendo en cuenta los últimos estudios, parece lógico restringir la realización de la punción lumbar a los casos con mala respuesta inmunitaria y espiroquetemia florida, y no solo sobre la base de la fase clínica o el estatus seropositivo para VIH, como se viene haciendo (fig. 1).
El número de pacientes estudiados en esta serie es demasiado pequeño para obtener datos significativos, pero un estudio publicado recientemente corrobora nuestros resultados. Este estudio se realizó en el centro Johns Hopkins Moore de Baltimore, que efectúa el seguimiento de una población de más de 4.000 infectados por el VIH. De una población de 232 pacientes infectados por el VIH con sífilis precoz activa, 202 no tenían clínica neurológica y entre ellos se detectaron 10 casos de neurosífilis asintomática. Si se hubiesen aplicado los criterios actuales de los CDC, 2/10 casos no se habrían detectado (sensibilidad del 80% [IC del 95%: 44–97%] y especificidad del 76% [IC del 95%: 60–89%]). Si, por el contrario, se hubiesen aplicado los criterios selectivos descritos recientemente, se habrían detectado todos los casos de neurosífilis asintomática y solo habría sido necesario realizar la punción lumbar en el 88% (sensibilidad del 100% [IC del 95%: 70–100%], especificidad del 87% [IC del 95%: 72–96%])38.
Sería interesante realizar estudios en una población mayor e intentar comparar el perfil de los pacientes VIH+ de larga evolución y controlados con TAR frente a pacientes VIH+ de reciente diagnóstico.