Analizar si es posible aplicar un protocolo de cribado cervical con citología y detección de VPH a partir de los 35 años con repetición cada 5 años. Estudiamos si la aplicación de este protocolo retrasa el diagnóstico de cáncer cervical.
Material y métodoDesde el año 2005 aplicamos protocolos de cribado de cáncer cervical y en el año 2010 incluimos la detección del VPH a partir de los 35 años. Realizamos un estudio retrospectivo sobre 500 mujeres que acudieron a nuestra consulta. Estudiamos si se había aplicado correctamente el protocolo y el tiempo en que se recomendaba la siguiente revisión. Analizamos los cánceres de cérvix diagnosticados en nuestras consultas desde el año 2005.
ResultadosAplicamos el protocolo de manera correcta en el 100% de las mujeres estudiadas. Realizamos citología y determinación del VPH al 45,6%, solo citología a al 23,2% y no realizamos toma de cribado al 31,2%. Al 26% de nuestras pacientes les indicamos la siguiente revisión en 5 años. La aplicación del protocolo no retrasó el diagnóstico de cáncer. De los 27 casos diagnosticados desde 2005, solo una mujer con adenocarcinoma había realizado correctamente el cribado (antes de usar la determinación del VPH). Se diagnosticaron 4 cánceres microinfiltrantes con la aplicación del cribado.
ConclusionesEs posible la aplicación de un protocolo de cribado con doble test a partir de los 35 años con repetición cada 5 años en las consultas rutinarias de un hospital. No retrasa el diagnóstico de cáncer cervical y puede servir para optimizar los recursos al distanciar las revisiones en las mujeres sanas.
To analyze screening for cervical cancer with a combination of cytology and HPV testing in women older than 35 years every 5 years and to determine whether the application of this protocol delays diagnosis of cervical cancer.
Material and methodsCervical cancer screening strategies have been applied in our hospital since 2005. HPV testing was introduced in 2010 for women older than 35 years. We performed a retrospective study of 500 women attended in our hospital. We studied whether we had correctly applied the strategy and the recommended time interval of the next review. We analyzed cervical cancers diagnosed in our hospital since 2005.
ResultsThe strategy was correctly applied in 100% of the women. Screening was performed with both cytology and HPV testing in 45.6% and with cytology alone in 23.2%; no screening was performed in 31.2%. The recommended interval until the next review was 5 years in 26% of the patients. The implementation of the strategy did not delay the diagnosis of cancer. Cervical cancer was diagnosed in 27 women since 2005. Only one woman with adenocarcinoma had been correctly screened (before the introduction of HPV testing). In the last 2 years, four microinvasive carcinomas were diagnosed with this strategy.
ConclusionsA combination of cytology and HPV testing can be applied in women older than 35 years and screening intervals can be increased to 5 years in routine clinical practice. This protocol does not delay the diagnosis of cervical cancer and optimizes resources by lengthening the interval between screening tests in healthy women.
La incorporación de la detección del VPH se ha generalizado en los últimos años en las consultas de Ginecología. El uso indiscriminado de esta prueba genera muchos resultados positivos a los que se da un valor excesivo. Sin embargo, se resta importancia a las determinaciones negativas, que son las que nos permiten hacer un cribado del cáncer de cérvix más racional y eficaz1.
En nuestro hospital estamos realizando protocolos para el cribado del cáncer cervical desde el año 2005. En el año 2010 incluimos la detección del virus del papiloma como recomiendan la mayoría de las comunidades científicas2-5.
El objetivo de este trabajo es analizar si es posible la aplicación de un cribado cervical con citología y detección del VPH a partir de los 35 años con repetición cada 5 años en las consultas rutinarias de un hospital. Estudiamos si la ejecución de este protocolo de cribado retrasa el diagnóstico del cáncer cervical.
Material y métodoTrabajamos en un Hospital Comarcal de la red pública. Se trata de un centro concertado que atiende a una población predominantemente urbana de 65.000 habitantes. Para esta población realizamos toda la cobertura ginecológica (ginecología general, planificación familiar, oncología y control de embarazos de bajo riesgo).
Hasta el año 2004 realizábamos citologías anuales. En 2005, citologías trienales a partir de los 30 años. Posteriormente, hicimos pequeñas modificaciones según se actualizaban las recomendaciones científicas6.
Desde enero del año 2010 estamos aplicando un nuevo protocolo para el cribado del cáncer de cérvix. Se trata del cribado recomendado por la SEGO2, pero en nuestro caso demoramos la prueba VPH a los 35 años. Se basa en realizar la primera citología a los 3 años de la primera relación sexual, con repetición al cabo de un año. Con 2 citologías normales se pasa a determinaciones cada 3 años hasta los 35 años. A partir de los 35 años se añade a la citología la detección del VPH. Si la citología es normal y la detección VPH negativa, el doble test se realiza al cabo de 5 años. El cribado finaliza a los 65 años.
A todas las pacientes a las que se realiza el cribado con detección de VPH se les explica que con una citología normal y una detección negativa de VPH el riesgo de desarrollar cáncer de cérvix en los próximos años es muy bajo7.
Las citologías son informadas por los patólogos del propio hospital, con amplia experiencia en patología cervical.
La detección de VPH se realiza en el Servicio de Microbiología del hospital, utilizando la prueba de detección de ADN de VPH mediante captura de híbridos (HC2; Digene Corporation, Gaithersburg, EE. UU.).
La aplicación del protocolo fue consensuada con los servicios de Anatomía Patológica y Microbiología.
Los resultados del cribado, cuando son normales, se envían por correo al domicilio de las mujeres. En la misma carta se indica el periodo en que se recomienda la próxima revisión.
Realizamos un estudio retrospectivo sobre 500 mujeres atendidas en nuestra consulta durante los meses de mayo y junio del año 2012. Se trataba de mujeres que acudían a la consulta de Ginecología general por presentar algún problema o para revisión ginecológica rutinaria (control enfermedad benigna, control método anticonceptivo o para revisión periódica sin enfermedad). Excluimos a las mujeres histerectomizadas, las que nunca habían mantenido relaciones sexuales, las que tenían una citología realizada en nuestras consultas hacía menos de un año y a las que habían tenido alteraciones citológicas previas.
Analizamos si se había aplicado el cribado correctamente y el periodo en que habíamos indicado la próxima revisión.
Exponemos todos los casos de cáncer de cérvix diagnosticados en nuestra consulta desde la puesta en marcha de nuestro primer protocolo de cribado en 2005.
Por último, registramos la evolución en el número de citologías realizadas anualmente desde el año 2005 en que comenzamos a aplicar nuestro primer protocolo de cribado de cérvix.
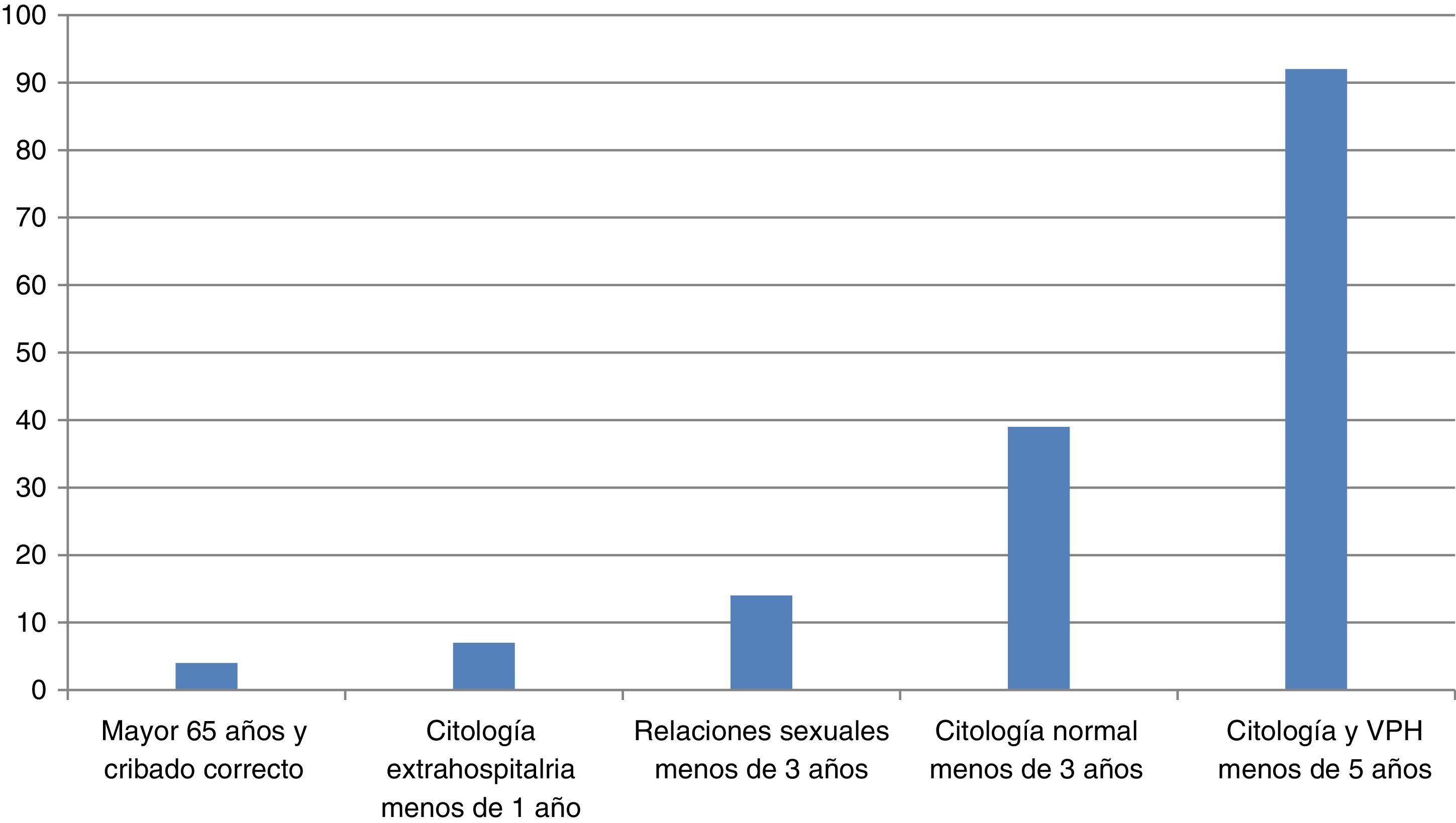
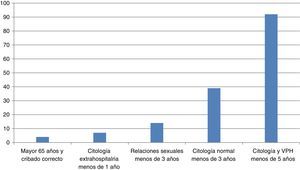
ResultadosDe las 500 mujeres estudiadas, realizamos citología y determinación de VPH a 228 (45,6%), solo citología a 116 (23,2%) y no realizamos toma de cribado en 156 casos (31,2%). En todos los casos se aplicó correctamente el protocolo de cribado. Solo se realizó una toma extra de VPH en una mujer VIH a la que debía realizarse citología anual. Las causas por las que no se realizó toma de cribado se reflejan en la figura 1.
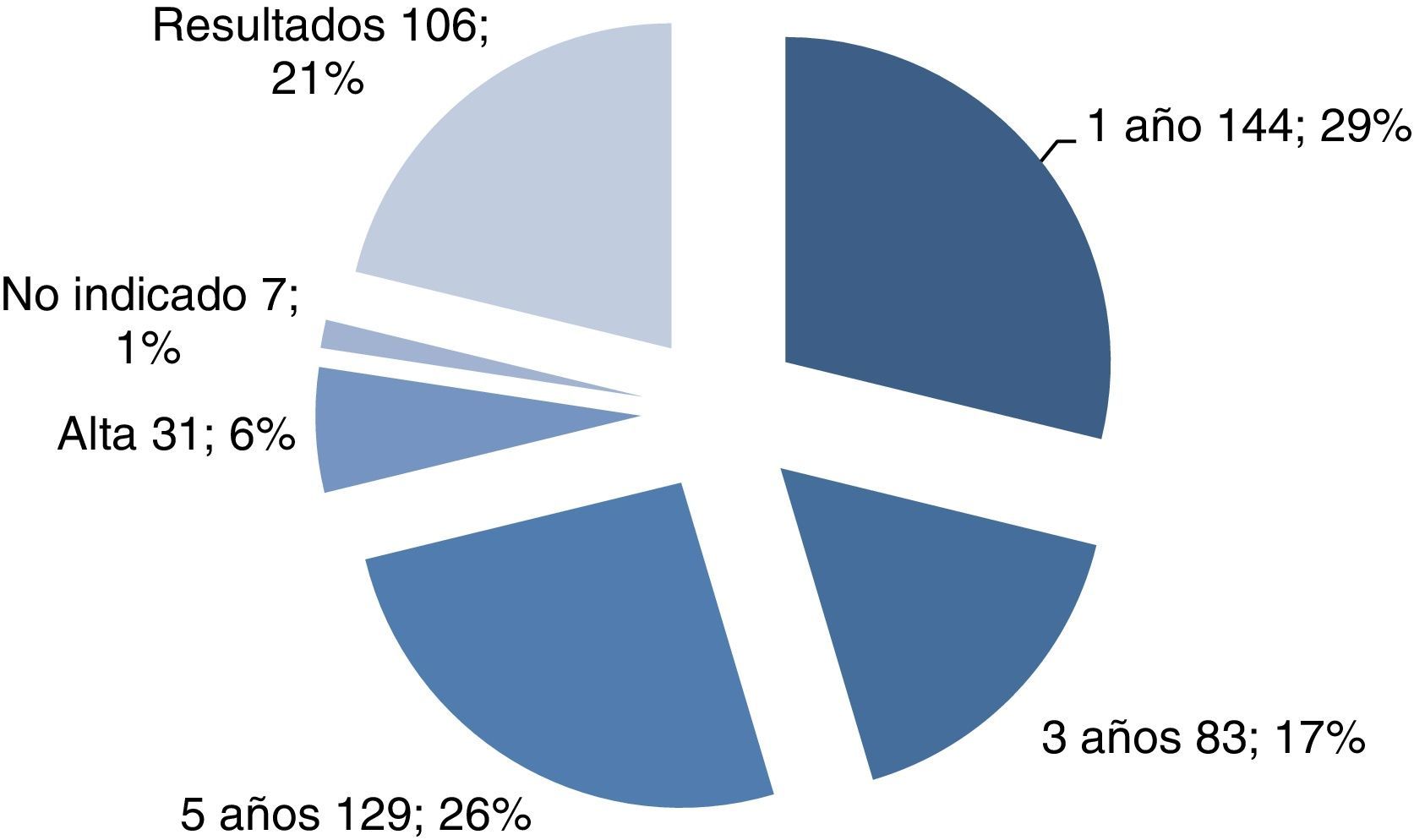
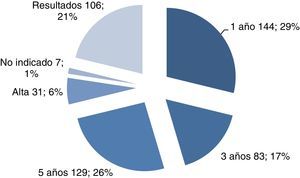
Al 26% de las mujeres se les indicó revisión en 5 años (se trataba de mujeres sin patología ginecológica ni método anticonceptivo). El resto de las indicaciones para la siguiente revisión se especifica en la figura 2.
El 6% son mujeres de más de 65 años que, al tener la citología normal y el test de VPH negativo, no necesitan más controles.
Al 31% de nuestras pacientes no les realizamos prueba de cribado, aunque la mayoría tenía una citología hecha de hacía más de un año. Las mujeres acuden a consulta por otros motivos, pero no siempre necesitan una prueba de cribado, cuando ya está realizada no la repetimos.
El 13% de las pacientes estudiadas acudieron a revisión antes del tiempo indicado en la revisión anterior y sin presentar enfermedad.
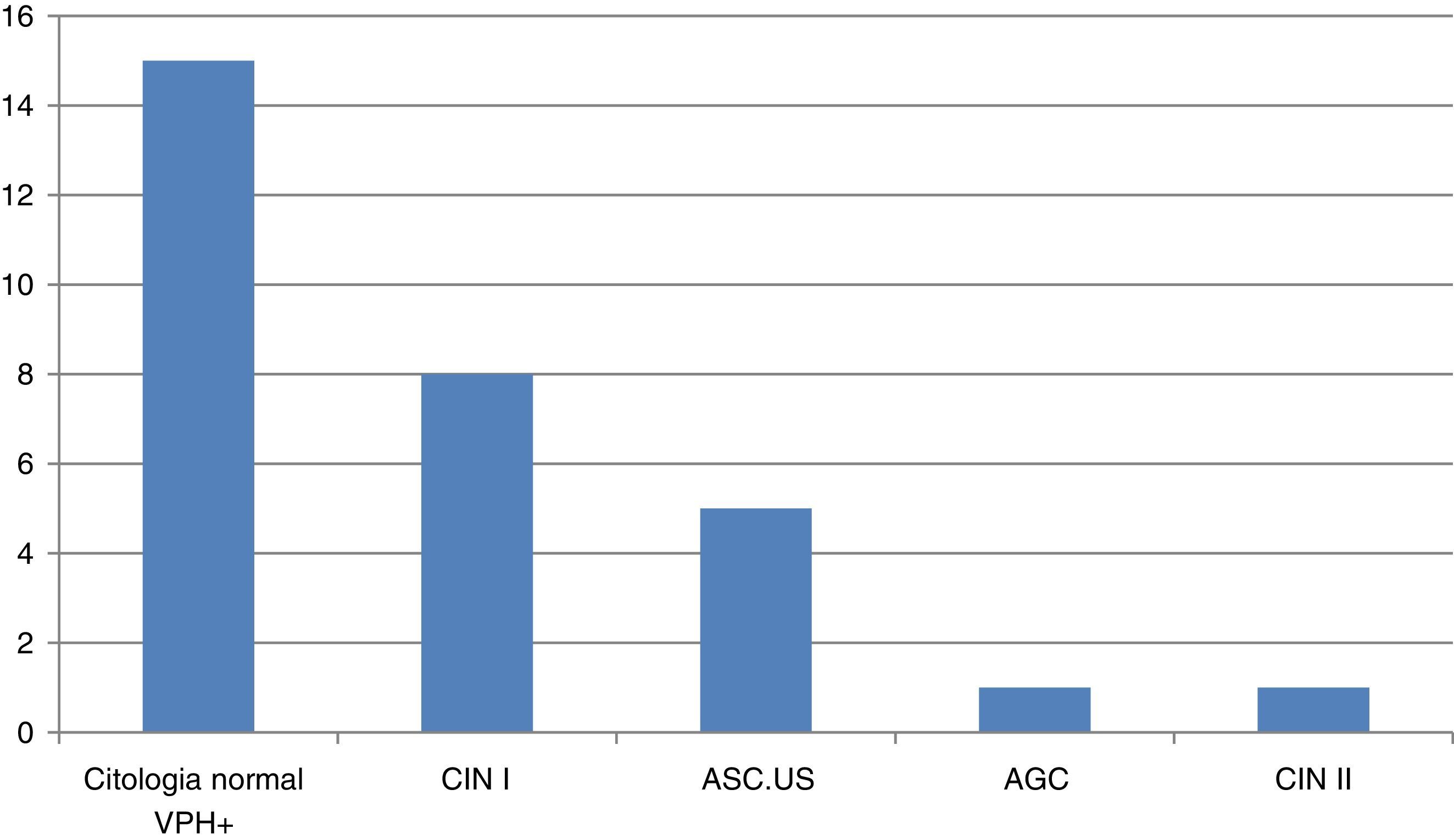
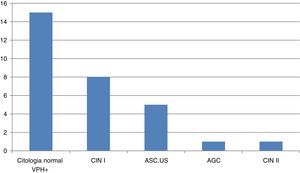
Encontramos a 30 mujeres con alteraciones en el resultado del cribado (fig. 3). El estudio de estas pacientes se realizó en la consulta de patología cervical de nuestro hospital. Solo un caso precisó conización; se trataba de una mujer de 32 años con amplia lesión de neoplasia intraepitelial grado ii. El resto de las pacientes continúan en seguimiento.
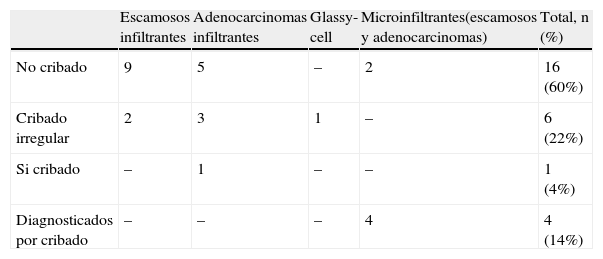
Desde el inicio de la aplicación de nuestro primer protocolo de cribado de cáncer cervical en 2005 hasta diciembre de 2013 hemos diagnosticado 27 cánceres de cérvix (tabla 1). La mayoría no había realizado cribado o había sido irregular, en algún caso extrahospitalario. Solo una mujer que presentó adenocarcinoma había realizado el cribado correctamente, pero fue antes de que utilizáramos la detección de VPH.
Veintisiete cánceres de cérvix diagnosticados desde enero 2005 hasta diciembre 2013
| Escamosos infiltrantes | Adenocarcinomas infiltrantes | Glassy-cell | Microinfiltrantes(escamosos y adenocarcinomas) | Total, n (%) | |
| No cribado | 9 | 5 | – | 2 | 16 (60%) |
| Cribado irregular | 2 | 3 | 1 | – | 6 (22%) |
| Si cribado | – | 1 | – | – | 1 (4%) |
| Diagnosticados por cribado | – | – | – | 4 | 4 (14%) |
En los 2 últimos años hemos diagnosticado con el cribado 4 carcinomas microinfiltrantes (estadio IA1) en mujeres jóvenes (29, 35, 40 y 45 años). El diagnóstico de estos tumores tan precoces y de buen pronóstico es uno de los objetivos del cribado cervical.
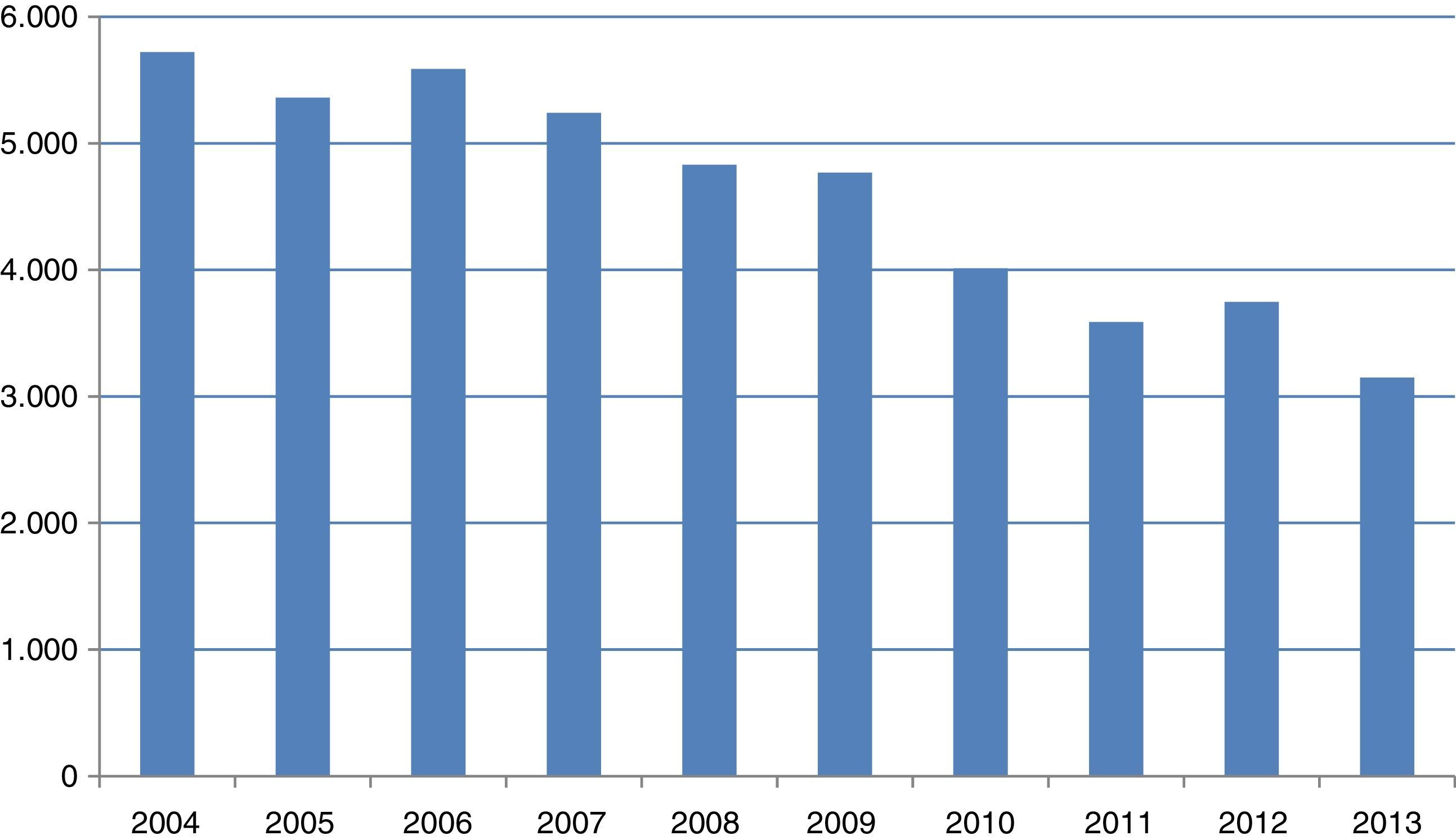
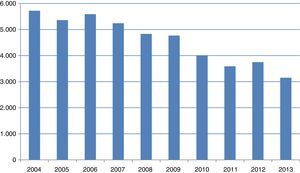
En el año 2004 se realizaron más de 5.700 citologías en todas las consultas de nuestro servicio. Desde el año 2005, cuando comenzamos con nuestro primer protocolo, el número total de citologías realizadas cada año ha ido disminuyendo progresivamente. En el año 2013 realizamos 3.150 (fig. 4).
DiscusiónHemos logrado aplicar sin dificultad el protocolo dentro de nuestro grupo. Es sencillo de recordar y conseguimos buena mecanización por parte de todos los ginecólogos en su ejecución. No se dejó de realizar el cribado en ninguna mujer que estuviera indicado.
No hemos retrasado el diagnóstico de cáncer cervical. De todos los cánceres que diagnosticamos desde el año 2005, hasta diciembre del 2013, solamente una mujer con adenocarcinoma realizó correctamente el cribado (antes del uso de VHP). Este tipo de tumores son difíciles de diagnosticar precozmente con citología8.
Confiar en el valor predictivo negativo del doble test y no repetir cribados en los siguientes 5 años nos permite distanciar las revisiones y reducir el sobrediagnóstico de pequeñas alteraciones citológicas sin repercusión clínica. De esta forma, hemos conseguido descongestionar nuestras consultas y optimizar nuestros recursos9.
Al explicar a las mujeres la base del cribado conseguimos una buena aceptación por parte de las pacientes. Solo al 13% de las mujeres que acudieron no les correspondía la revisión.
Desde el año 2005, en que comenzamos a aplicar nuestro primer protocolo, se va reduciendo progresivamente el sobreúso de la citología. En la actualidad, estamos realizando aproximadamente 2.000 citologías menos al año que cuando se hacían citologías anuales.
Sabemos que el test de VPH es muy sensible, pero a la vez poco específico para seleccionar a las mujeres que realmente pueden desarrollar enfermedad cervical importante. Nuestra mayor dificultad surgió el primer año, en que incluimos la detección del VPH. El manejo de las citologías normales con test VPH positivo generó preocupación en las pacientes y un exceso de colposcopias sin rendimiento diagnóstico. Al analizar los resultados del primer año, encontramos que habíamos indicado mayor número de colposcopias, realizado más conizaciones y no aumentamos el diagnóstico de la enfermedad cervical de alto grado. Sometimos a nuestras pacientes a una carga de ansiedad posiblemente innecesaria, al comprobar que la mayoría de los casos no había lesión o se trataba de lesiones de bajo grado. Revisamos la bibliografía al respecto y buscamos una alternativa. Controlamos a este grupo realizando a los 6 meses citología líquida. Solo remitimos para colposcopia a las mujeres que tienen la tinción dual p16 y ki-67 positiva10,11. Todo este grupo de mujeres con citología normal y determinación positiva de VPH forman parte de un estudio que estamos realizando.
La aplicación del cribado con doble test nos permite gestionar nuestras consultas de una manera más práctica. Hemos optimizado nuestros recursos, disminuyendo de manera importante las revisiones anuales en la mujer sana, a las que esas revisiones repetidas año tras año tampoco servían claramente para mejorar su salud. El tiempo ganado lo hemos utilizado para potenciar otros aspectos de nuestra especialidad, como la planificación familiar, y desarrollar programas de cribado activo para intentar captar a las mujeres que no acuden a las revisiones y son las que tienen más riesgo de poder desarrollar un cáncer cervical.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.