La gestación ovárica es una forma de presentación poco habitual del embarazo ectópico. El diagnóstico preoperatorio es difícil; algunos se diagnostican durante la intervención pero la mayoría necesita confirmación histopatológica. El tratamiento de elección es intentar la preservación de tejido ovárico para mantener la fertilidad mediante la enucleación del saco gestacional o la resección en cuña del ovario, preferiblemente por vía laparoscópica. En algunos casos el tratamiento con metotrexato intramuscular puede ser efectivo. Presentamos 2 casos de embarazo ectópico ovárico en nuestro hospital.
Ovarian pregnancy is an uncommon type of ectopic pregnancy. Preoperative diagnosis is difficult. Some cases are diagnosed during surgery and most need to be confirmed by histopathological study. The treatment of choice is conservative ovarian surgery to preserve fertility such as enucleation of the gestational sac or wedge resection of the ovary, preferably by laparoscopy. In some cases intramuscular methotrexate could be effective. We report two cases of ectopic ovarian pregnancy in our hospital.
El embarazo ectópico (EE) es una gestación que se produce fuera de la cavidad abdominal. El 95% de los EE se localizan en la trompa de Falopio y con mayor frecuencia en la porción ampular1. Existen formas no tubáricas, como los embarazos cornuales (3%), abdominales (1,3%), ováricos (0,5%), intraligamentarios (0,1%) y cervicales (0,1%)2.
La localización ovárica es una forma de presentación poco habitual del EE. El primer caso fue descrito por San Maurice en Francia en el año 16823. Tiene una incidencia de 1:7.000-40.000 recién nacidos vivos, pero en la literatura solo existen entre 300-400 casos descritos hasta la fecha4-6. Al igual que en los EE de otra localización, los síntomas son amenorrea, dolor abdominal y sangrado genital en una paciente con historia de amenorrea y test de embarazo positivo. Cursan con frecuencia con rotura y hemoperitoneo, puesto que es una zona muy vascularizada. El diagnóstico preoperatorio de EE ovárico es difícil. El tratamiento de elección es la enucleación del saco gestacional o la resección en cuña del ovario, preferiblemente por vía laparoscópica5,7-10.
Presentamos 2 casos de EE ovárico que comenzaron con dolor abdominal intenso y hemoperitoneo.
Casos clínicosCaso clínico 1Mujer de 18 años que acude al Servicio de Urgencias de Ginecología por dolor abdominal intenso de inicio brusco que comienza después de coito, acompañado de palidez y mareo. Presenta una presión arterial (PA) de 109/62 mmHg.
No refiere antecedentes patológicos de interés. Como antecedentes ginecoobstétricos presenta menarquia a los 12 años, sangrado genital hace 25 días que interpretó como sangrado menstrual, tipo menstrual (TM) de 4/28 días y una gestación con una cesárea. No utiliza ningún método anticonceptivo.
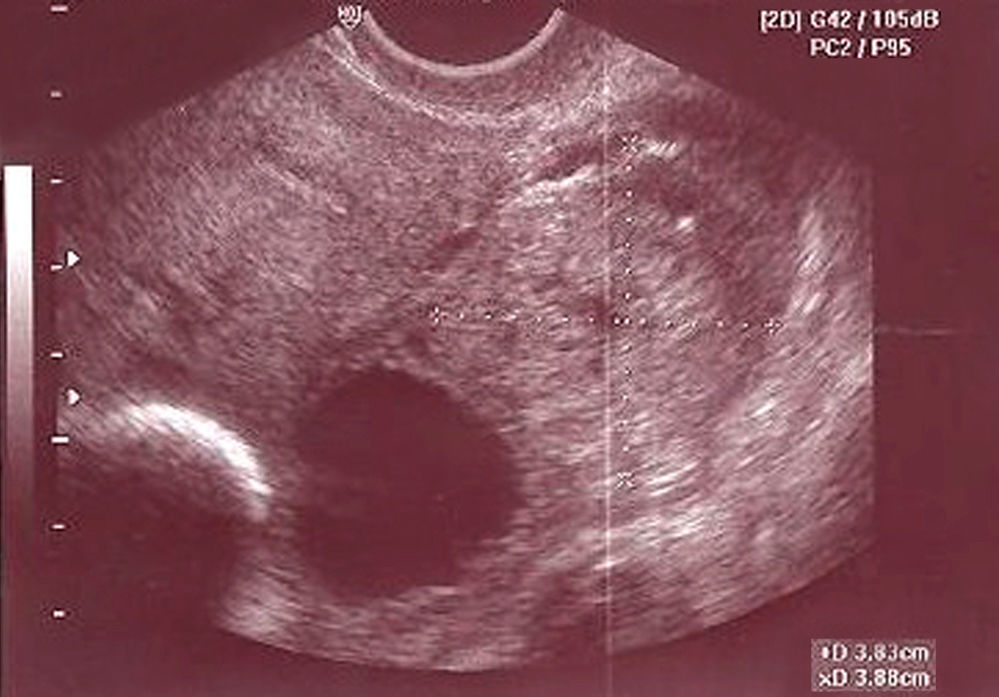
A la exploración física destaca un abdomen muy doloroso a la palpación, con defensa y molestia importante con la especuloscopia y con el tacto vaginal. Se realiza un test de gestación, con resultado positivo. En la ecografía transvaginal se visualiza un útero en anteversión, con una línea endometrial de 7mm de grosor, sin evidenciarse saco gestacional en su interior. El anejo derecho es normal y el izquierdo presenta una formación anecoica de 31×31mm, con imagen paraovárica heteroecoica de 38×38mm. Escasa cantidad de líquido libre en Douglas (fig. 1). Se solicita analítica, donde destaca una hemoglobina (Hb) de 11,6g/dl, hematocrito (Htco) del 35,3% y una β-HCG de 4.894 mU/ml.
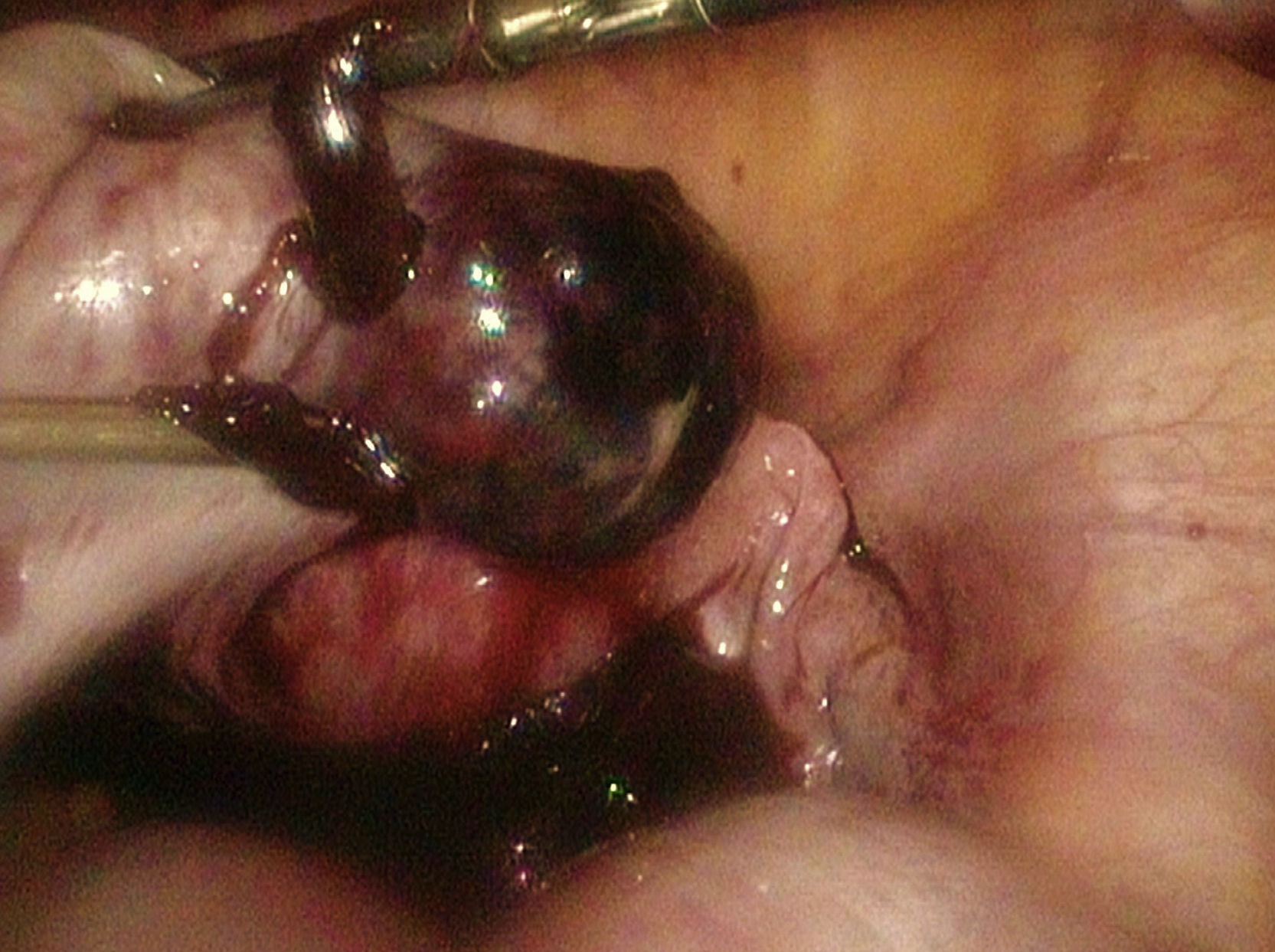
Ante la sospecha de gestación ectópica tubárica izquierda rota, se decide realizar una laparoscopia quirúrgica, objetivando la existencia de hemoperitoneo escaso, con coágulos organizados en Douglas. Útero, ambas trompas y ovario derecho, normales. En el ovario izquierdo se visualiza una formación de contenido líquido de aspecto funcional en el polo inferior y una formación hemorrágica de aproximadamente 3cm, friable y con sangrado activo en el polo inferior, sugestivo de gestación ectópica ovárica izquierda (fig. 2). Se realiza enucleación de la formación hemorrágica. El resultado de anatomía patológica viene informado como material hemático, fragmentos deciduales y vellosidades coriales compatible con EE ovárico. La paciente es dada de alta a las 48 h. Durante el postoperatorio se realiza el seguimiento de la β-HCG, que se negativiza en 15 días.
Caso clínico 2Paciente de 42 años que acude a urgencias por dolor abdominal intenso de inicio brusco, de 2 h de evolución, con sensación nauseosa y sudoración. Presenta una PA de 80/50 mmHg.
No refiere antecedentes patológicos de interés. Como antecedentes ginecoobstétricos refiere menarquia a los 12 años, relata un sangrado compatible con menstruación hace 20 días, una TM de 4/28 y 3 gestaciones espontáneas, con un embarazo a término que finalizó en una cesárea y 2 abortos espontáneos. Estuvo en estudio por una esterilidad secundaria, realizándose 3 ciclos de inseminación artificial conyugal sin conseguir embarazo.
A la exploración presenta dolor a la palpación abdominal, con defensa y un útero doloroso al tacto vaginal. Se realiza un test de embarazo, con resultado positivo. En la ecografía transvaginal se observa un útero en anteversión, con una LE de 10mm sin visualizarse el saco gestacional intraútero. No se pueden identificar estructuras anexiales por la presencia de material heteroecoico compatible con coágulos que ocupan el fondo del saco de Douglas e importante cantidad de líquido libre en la cavidad abdominal. En la analítica presenta una Hb de 10,5g/dl y un Htco del 31,1%.
Con la sospecha de EE tubárico roto, se decide intervención por vía laparotómica por la presencia de hemoperitoneo. A la exploración se visualizan un hemoperitoneo severo y gran cantidad de coágulos que ocupan la pelvis. Tras la limpieza de la cavidad abdominal se objetiva sangrado activo procedente de la superficie del ovario derecho. Se realiza una ooforectomía derecha por afectación importante del tejido ovárico circundante. La anatomía patológica se informa como ovario con cuerpo lúteo y lecho de implantación con vellosidades coriales en la superficie ovárica rota compatible con gestación ectópica. Es dada de alta a los 4 días poscirugía.
DiscusiónEl EE ovárico es muy poco frecuente y según la literatura representa el 0,5-3% de todos los EE4,11. Los factores de riesgo asociados son el uso de dispositivo intrauterino (DIU), cirugía pélvica laparoscópica o laparotómica, endometriosis, síndrome de ovario poliquístico, historia de esterilidad, uso de técnicas de reproducción asistida y malformaciones uterinas4,7,12.
En un estudio, en el que se incluyó a 1.800 pacientes con EE, el DIU es el único factor de riesgo que se correlacionó con los EE distales y ováricos13. Esto es debido a que el DIU reduce la implantación intrauterina y tubárica en un 99,5 y un 95%, respectivamente, pero no ofrece protección frente a los EE ováricos14. En las diferentes series de EE ovárico publicados en la literatura, las usuarias de DIU variaban entre un 16-90%, lo que hace pensar que deben de estar implicados otros elementos en su etiopatogenia5,15. Nuestras pacientes presentaban como factores de riesgo un antecedente de cesárea y una de ellas una historia de esterilidad secundaria.
La localización del EE ovárico puede ser superficial o intrafolicular. Las formas superficiales se producen sobre todo en pacientes con endometriosis. La fecundación se produce fuera del ovario y las células granulosas del cigoto se vuelven a adherir al folículo roto. Las formas intrafoliculares, a su vez, se pueden subdividir en corticales, cuando la fecundación se produce en un folículo no roto, o yuxtafoliculares, en aquellos casos en que después de la fecundación migra a partes más profundas del ovario16-18.
De los casos descritos en la literatura, aproximadamente el 75% se diagnostica en el primer trimestre, el 12,5% en el segundo y un 12,5% llega a término. Hay 5 casos documentados de recién nacidos vivos19. Otras formas de presentación raras son los embarazos heterotópicos20, formas bilaterales18, concomitancia con un teratoma maduro21 y retención de un feto muerto a nivel ovárico durante más de un año22.
Las pacientes cursan con dolor abdominal en un 89% de los casos, sangrado genital en un 74% y hemoperitoneo en un 21% por aumento de la vascularización ovárica y rotura posterior si existe retraso en el diagnóstico7. Los síntomas se asocian a una historia de amenorrea, niveles de β-HCG elevados (superiores a 1.000-1.500 U/l) y la ausencia de saco gestacional intraútero por ecografía23.
Ecográficamente se puede identificar dentro o adyacente al ovario un anillo hiperecogénico con un área hipoecoica en su interior que se correspondería a un saco. El diagnóstico preoperatorio del EE ovárico por imagen es difícil, ya que no se puede excluir un cuerpo lúteo hemorrágico en una gestación incipiente o una implantación tubárica24-26. El Doppler color no aporta información adicional27. En ocasiones, se puede visualizar un embrión con actividad cardíaca o partes fetales en el ovario, lo que nos confirmaría el diagnóstico de EE.
Actualmente, el diagnóstico definitivo de EE ovárico sigue siendo quirúrgico y se basa en criterios anatómicos e histológicos descritos por Spiegelberg en 18787,8,27-32: las trompas están intactas y separadas del ovario, la gestación ocupa la posición normal del ovario, la gestación está conectada al útero a través del ligamento uteroovárico y el tejido ovárico está presente adyacente al saco gestacional en la muestra tisular enviada para estudio anatomopatológico.
Por la dificultad de realizar un diagnóstico preoperatorio, su incidencia real se cree que está infraestimada. Existen casos diagnosticados como tubáricos pero que realmente están localizados en el ovario que recibieron tratamiento médico o se resolvieron de manera espontánea sin precisar cirugía29.
Durante la intervención, poder realizar el diagnóstico diferencial con un cuerpo lúteo o quiste hemorrágico en una paciente con una gestación intrauterina incipiente es difícil33. En ocasiones se puede realizar el diagnóstico de forma intraoperatoria si se visualizan el saco gestacional o las partes fetales24,32. La mayoría de las veces es necesario el estudio histológico de la pieza quirúrgica para confirmar la presencia de vellosidades coriales27.
En nuestras pacientes se sospechaba un EE tubárico roto antes de la cirugía por la clínica y por los niveles elevados de β-HCG. El diagnóstico de sospecha se realizó durante la intervención y se confirmó con el estudio anatomopatológico de la muestra.
Una paciente que durante la cirugía presenta una masa ovárica hemorrágica con trompas normales y β-HCG superior a 1.000 U/l con ausencia de saco gestacional intraútero nos debe orientar a un EE ovárico23.
El tratamiento de elección es quirúrgico. Se prefiere el acceso por vía laparoscópica, ya que ofrece la ventaja de ser una cirugía mínimamente invasiva, con una recuperación más rápida y una menor estancia hospitalaria. Clásicamente, la laparotomía se indicaba en aquellas situaciones con hemoperitoneo importante, aunque hoy en día esto ya no es contraindicación absoluta para realizar un acceso laparoscópico en manos de un cirujano experto.
La intención es ser lo más conservador posible, dejando tejido ovárico sano para poder preservar la fertilidad de la paciente. Se realiza una enucleación del saco gestacional y si no es posible una resección en cuña del ovario5,7,8,10,15. La ooferectomía o anexectomía se reserva para aquellas situaciones en las que el ovario y la trompa están muy dañados por el sangrado. En los casos de despegamiento del saco ovular, es necesario realizar un seguimiento posquirúrgico de los niveles de β-HCG por si quedan restos de tejido trofoblástico, que se podría manejar con tratamiento médico31,34.
En el caso 1 se hicieron una enucleación del saco gestacional por vía laparoscópica y un seguimiento posterior de los niveles de β-HCG, que se negativizaron en 15 días. En el caso 2 fue necesario realizar una ooforectomía por la afectación del tejido ovárico por el sangrado. Los cirujanos prefirieron hacer una laparotomía por la presencia de un hemoperitoneo severo, a pesar de que actualmente no constituye una contraindicación absoluta para la laparoscopia.
Existe algún caso descrito de EE ovárico que se trató con metotrexato por vía intramuscular (IM) o intrasacular35,36. Lo ideal sería ofrecérselo a aquellas pacientes a las que se realiza un diagnóstico precoz por ecografía. Tiene la ventaja de que es más conservador que el quirúrgico, pero normalmente suelen ir precedidos de laparoscopias diagnósticas y se ofrece a mujeres que están estables hemodinámicamente. Muchos autores defienden que la laparoscopia diagnóstica debe de ir seguida de tratamiento quirúrgico por el riesgo de sangrado que tienen estas gestaciones, puesto que es una cirugía mínimamente invasiva y de rápida recuperación10,31.
La localización ovárica del EE es muy infrecuente. Hoy en día la cirugía es el tratamiento gold standard, además de servir como diagnóstico, ya que se basa en los criterios anatómicos e histológicos descritos por Spiegelberg. Estos criterios deberían de actualizarse, puesto que en la enucleación del saco gestacional no se incluye tejido ovárico adyacente en la muestra extraída ni se tiene en cuenta la monitorización de la β-HCG poscirugía.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.