Evaluar la eficacia y la seguridad de 400 μg de misoprostol por vía sublingual y 200 μg rectal más manejo activo de la tercera fase del parto frente a manejo activo para prevenir la hemorragia posparto.
Sujetos y métodosSe sometió a 1.400 mujeres a recibir el misoprostol más manejo activo (grupo I) o manejo activo (grupo II). Las variables medidas fueron la incidencia de hemorragia posparto, el volumen de sangre perdido y el uso de uterotónicos adicionales.
ResultadosEn el grupo I hubo 28/702 (4,0%) hemorragias y en el grupo II 50/698 (7,2%), p = 0,005; riesgo relativo (RR) = 0,538; intervalo de confianza (IC) del 95% para RR (0,335-0,866). En mujeres con hemorragia posparto, el volumen de sangre perdida fue 981 ± 309 cc y 888 ± 326 cc, p = 0,225 en los grupos I y II, respectivamente.
Necesitaron uterotónicos adicionales 33 (4,7%) frente a 54 (7,7% mujeres, p = 0,025 en los grupos I y II, respectivamente).
ConclusionesSe podría recomendar la administración de misoprostol por vía sublingual/rectal junto al manejo activo para prevenir la hemorragia posparto.
To evaluate the efficacy and safety of 400 μg sublingual misoprostol and 200 μg rectal misoprostol plus active management of the third stage of labour versus active management only to prevent postpartum haemorrhage.
Subjects and methodsA total of 1400 women were randomly assigned to receive misoprostol plus active management (group I) or active management only (group II). The variables studied were incidence of postpartum haemorrhage, blood volume lost and need of additional uterotonics.
ResultsIn group I there were 28/702 (4.0%) haemorrhages and in group II 50/698 (7.2%), P=.005; RR =.538; 95% CI for RR (0.335-0.866). In women having postpartum haemorrhage the lost blood volume was 981 ± 309 cc and 888 ± 326 cc. P=.225 in groups I and II, respectively.
Additional uterotonics were needed in 33 women in group I (4.7%) vs. 54(7.7%) women in group II (P=.025).
ConclusionsThe use of sublingual/rectal misoprostol plus active management appears to be useful for the prevention of postpartum haemorrhage.
La Organización Mundial de la Salud estima que 529.000 mujeres murieron por causas obstétricas en el año 20001. La principal de estas causas obstétricas es la hemorragia posparto (HPP), ya que significa casi un tercio de estas muertes, que ocurren en el 99% de los casos en países en vías de desarrollo, donde las embarazadas no reciben ningún tipo de profilaxis para la HPP, ya que la mayoría de los casos acontece en áreas rurales sin ningún tipo de infraestructura sanitaria2. Además, muchas de estas mujeres suelen estar anémicas; la mortalidad por HPP es entonces aun mayor3,4.
La causa más común de HPP es la atonía uterina, que habitualmente se trata con los uterotónicos convencionales. Ellos requieren administración parenteral y, por tanto, agujas y jeringas estériles; además, la ergometrina necesita refrigeración y la oxitocina puede inactivarse por la luz y altas temperaturas ambiente.
El misoprostol es fácil de administrar, económico y estable a temperatura ambiente. Estas razones han hecho que se preste una gran atención a este fármaco en la prevención de la HPP5.
Tanto es así que la Organización Mundial de la Salud —en una guía reciente para la prevención de la HPP— recomendó el uso de 600μg de misoprostol oral en lugares donde no se efectúa el manejo activo de la tercera fase del parto6.
La vía sublingual presenta picos plasmáticos de ácido misoprostólico más altos que las vías oral y bucal, y estas a su vez presentan picos superiores que las vías rectal y vaginal7.
La vía sublingual presenta una buena área bajo la curva de tiempo y además una rápida absorción, lo que es muy importante en la prevención de una afección como la HPP que es, por definición, en la mayoría de casos, aguda. Los principales efectos secundarios del misoprostol son los escalofríos y la hiperpirexia, y son dependientes de la dosis y la vía. La vía rectal ha demostrado cierta eficacia en la prevención de la HPP, con concentraciones séricas de misoprostol relativamente bajas, pero mantenidas durante varias horas8,9.
Una revisión sistemática de la literatura científica sobre este tema concluyó que la combinación de diferentes vías de administración del misoprostol puede ser beneficiosa10.
El objetivo de este estudio fue estudiar la eficacia y la seguridad de 400μg de misoprostol por vía sublingual y 200μg rectal más manejo activo de la tercera fase del parto frente al manejo activo de la tercera fase del parto solamente.
SUJETOS Y MÉTODOSEste estudio clínico aleatorizado se llevó a cabo según el contenido de las Declaraciones de las Asambleas Médicas Mundiales de Helsinki (1964), Hong-Kong (1989) y Tokio (2004), y según las leyes vigentes en la República de Cuba, tomando las medidas preventivas requeridas para proteger a las participantes y sus productos de la concepción. Este estudio fue aprobado por los comités Científico y de Ética del Hospital Eusebio Hernández (Maternidad Obrera), Ciudad Habana, dentro del acuerdo de colaboración científica firmado con la Clínica Mediterránea Médica, Valencia, España.
Entre abril de 2007 y octubre de 2008 se incluyó a 1.400 mujeres que tuvieron parto vaginal en el hospital Eusebio Hernández.
Los criterios de inclusión fueron: a) edad > 18 años, b) embarazo simple, y c) parto vaginal eutócico. Los criterios de exclusión fueron: a) parto vaginal distócico (instrumentado) u operación cesárea, b) edad gestacional < 32 semanas, c) trastornos de la coagulación, d) hemoglobina preparto < 8g/dl, e) disfunción hepática o renal, f) paridad > 5, g) hipersensibilidad o cualquier contraindicación para el uso de prostaglandinas.
Información a los pacientes y obtención de su aprobaciónCuando la mujer ingresó a la sala de prepartos, se realizó la evaluación médica de ella para estimar la certeza del parto vaginal y que cumpliera los criterios de inclusión y ninguno de exclusión. Las pacientes fueron informadas que serían asignadas al azar a uno u otro tratamiento para la prevención de la HPP y que esa asignación se efectuaría cuando fuera inminente la ocurrencia del parto vaginal. Después de facilitar la información descrita se obtuvo el consentimiento informado debidamente firmado de las que decidieron participar en el estudio.
Justificación de las dosis de misoprostolSe propuso el uso de dosis de 400pg de misoprostol por vía sublingual como dosis preventiva de ataque dadas su rápida absorción y acción, y una dosis de 200 rectal para mantener en el tiempo cierta acción acorde con el perfil farmacocinético de la vía rectal11. Se utilizaron tabletas de 200pg de misoprostol (Cytotec, Laboratorios Pfizer, Alcobendas, Madrid).
Criterios y definicionesHemorragia pospartoPérdida sanguínea ≥ 500cc. Hemorragia posparto grave: pérdida sanguínea ≥ 1.000cc. Forma en que se midió la cantidad de sangre perdida: después de la salida del feto, debajo de los glúteos de la mujer, se colocó un extremo de un paño impermeable y estéril para permitir que la sangre corriera hacia un frasco milimetrado con capacidad de 2l; la lectura del volumen de sangre acopiada se hizo una vez finalizada la tercera fase del parto. El procedimiento establecido en la institución para prevenir la HPP es el manejo activo del alumbramiento o tercera fase del parto y se realiza como se describe a continuación: después que se ha producido la expulsión completa del feto, se administran 10 U de oxitocina por vía intramuscular. Se pinza y se secciona el cordón umbilical cuando este ha dejado de latir. Después se realiza la tracción mantenida del cordón con contratracción, haciendo presión con la otra mano en el pubis para evitar complicaciones como la inversión uterina. Después de la salida de la placenta se aplica masaje del fondo del útero cada 15min en las primeras 2h del puerperio y cada 30min en las otras 2h, es decir, hasta 4h después del parto.
Tratamientos- 1.
Grupo I (manejo activo + misoprostol): una vez expulsado el feto, se le administró a la paciente 400pg de misoprostol por vía sublingual y 200pg por vía rectal y se comenzó el manejo activo de la tercera fase del parto.
- 2.
Grupo II se realizó el manejo activo: se utilizaron uterotónicos adicionales (oxitocina, ergonovina o ambos), según el protocolo de atención a la HPP, si después del alumbramiento el sangrado vaginal excedió los 500ml.
Después de terminado el parto, a todas las mujeres se les midieron la presión arterial, la frecuencia cardíaca, el estado de la contractilidad uterina y el sangramiento vaginal cada 15min durante las 4 primeras horas posteriores a este, y el período de vigilancia para la HPP se extendió a las primeras 12h después del parto. Se tomó una muestra de sangre para evaluar el hematocrito después de 12h posparto, excepto que el médico ordenase la realización del mismo antes de ese tiempo.
Variables estudiadasLas variables utilizadas para la evaluación de la eficacia fueron: a) incidencia de HPP en cada grupo de tratamiento, b) volumen de sangre perdido por cada paciente medido en cc, y c) uso de uterotónicos adicionales para tratar el sangramiento. Otras variables fueron: a) descenso de los valores de hematocrito, b) necesidad de legrar la cavidad uterina, c) necesidad de transfusión de sangre o glóbulos, d) extracción manual de la placenta, e) tiempo para el alumbramiento, y f) eventos adversos del misoprostol, como son náuseas, vómitos, escalofríos, diarrea, hipertermia ≥ 38°C.
Asignación a los grupos de tratamientoLas mujeres fueron asignadas a uno u otro grupo de tratamiento según una lista aleatoria generada por una computadora. Personal ajeno al estudio preparó sobres opacos sellados con un número de serie cada uno. Cada sobre contenía una tarjeta que indicaba el grupo de tratamiento al que se asignaría la paciente, «misoprostol + manejo activo» o «manejo activo solamente» y este proceso fue supervisado por un estadístico. Los sobres sellados fueron entregados cada mañana a la secretaria de la sala prepartos y esto fue controlado por el monitor del estudio. La asignación se realizó como sigue: cuando el parto vaginal era inminente, se abrió el sobre correspondiente al número de orden de entrada de la paciente en el estudio y se aplicó el tratamiento indicado en la tarjeta contenida en el sobre.
Predeterminación del tamaño de la muestraLa incidencia de HPP fue la variable utilizada para calcular el número de sujetos que se debía incluir en el estudio. Según las estadísticas del hospital, la incidencia de la hemorragia posparto oscila entre el 7 y el 8% cuando se emplea el manejo activo de la tercera fase del parto. El tamaño de la muestra se calculó según la hipótesis nula de que la tasa de hemorragia posparto, utilizando el manejo activo más misoprostol en la tercera fase del parto, se reduciría en un 50% (3,5%-4,0%). Un análisis de la potencia indicó que con 600 mujeres en cada grupo de tratamiento sería posible detectar esa reducción con un error de tipo I = 5% y con una potencia del 85% para una prueba de dos colas12. El número de sujetos se incrementó a 705 pacientes en cada grupo (1.410 en total), para prevenir pérdidas de pacientes durante el curso del tratamiento o por posibles incumplimientos del protocolo.
EstadísticaLos resultados se presentan en porcentajes, medias ± desviaciones estándar, riesgos relativos (RR) e intervalos de confianza (IC) para los RR. Se utilizó la prueba de la %2 de Pearson, la probabilidad exacta de Fisher y la prueba de la t de Student para evaluar la homogeneidad de los 2 grupos de tratamiento y para la comparación de las variables de evaluación de la eficacia entre los 2 grupos de tratamiento. En todos estos casos, se consideró significativo un valor de p < 0,05 y todas las pruebas estadísticas fueron de dos colas. Los datos fueron almacenados con el Sistema Visual FoxPro 8,0 sobre Windows XP (Microsoft, Redmond, EE. UU.) y la información fue procesada con el SPSS 11,5 (SPSS, Chicago, EE. UU.) en Windows XP (Microsoft, Redmond, EE. UU.).
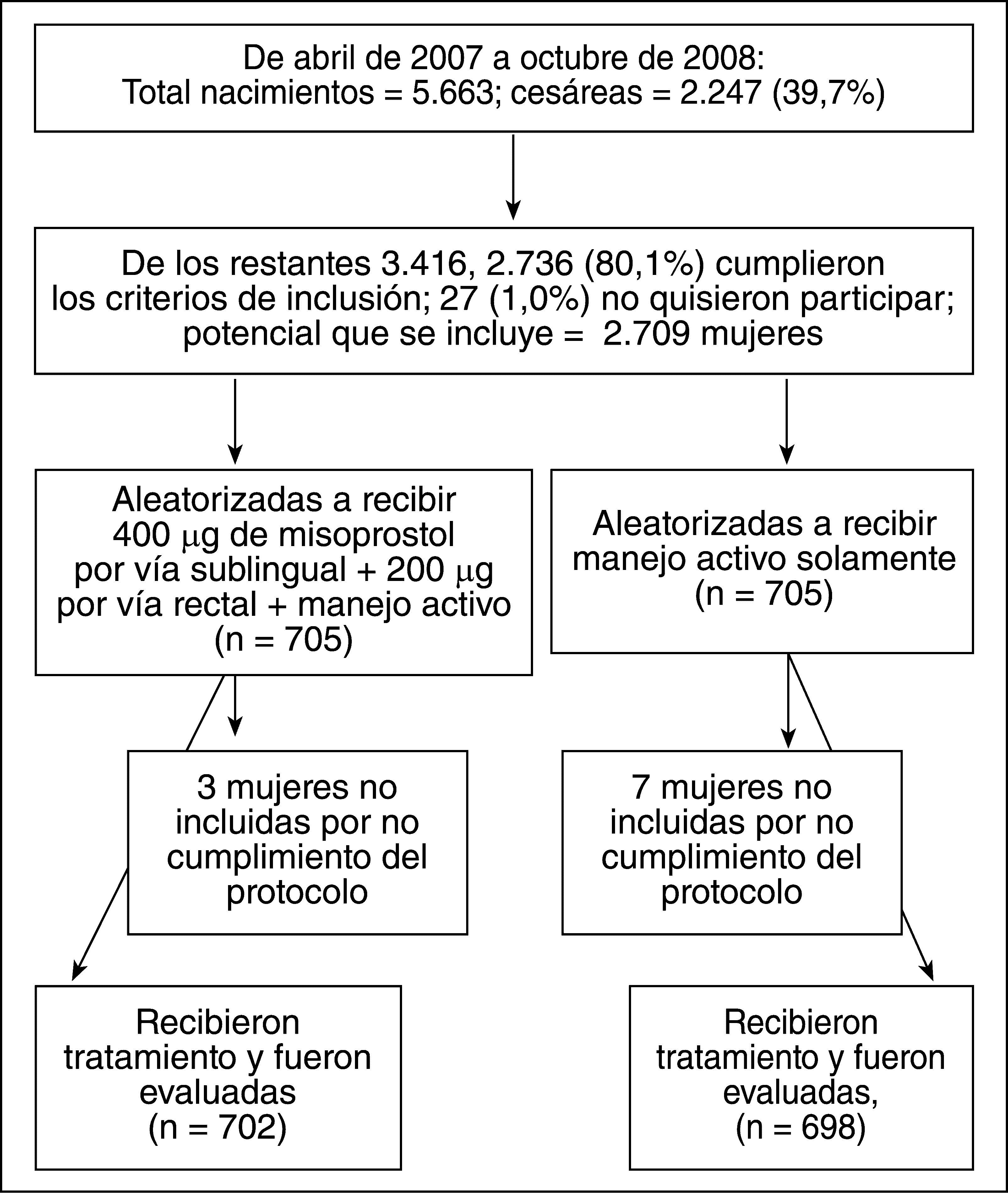
RESULTADOSEl estudio comenzó en abril de 2007 y finalizó en octubre de 2008; participaron 3 de los 6 equipos de guardia del hospital y el equipo diurno del salón de partos. En ese período ocurrieron 5.663 nacimientos y 2.247 (39,7%) fueron por cesárea. De los 3.416 nacimientos restantes, 2.736 (80,1%) cumplieron con los criterios de entrada al estudio y no aceptaron participar 27/2.736 (1,0%) mujeres.
Se aleatorizó a 1.410/2.709 (52,0%) mujeres y se incluyeron finalmente 1.400, 702 en el grupo de misoprostol + manejo activo (grupo I) y 698 en el grupo de manejo activo solamente (grupo II). Tres y 7 de las mujeres aleatorizadas a los grupos I y II, respectivamente, no recibieron ningún tratamiento por incumplimiento del protocolo y, como la información correspondiente a ellas no fue registrada en ningún momento, no forman parte de este informe (fig. 1).
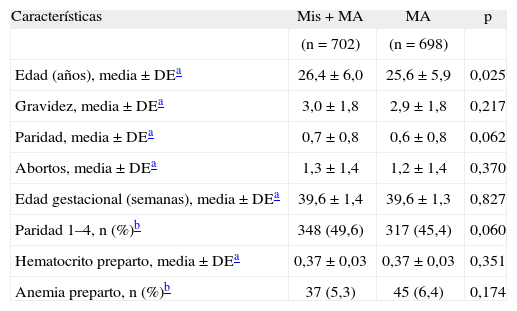
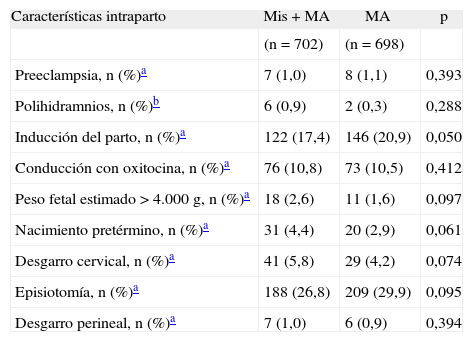
En la tabla 1 se muestran las características generales de las mujeres incluidas en el estudio. Con excepción de la edad, no hubo diferencias significativas entre los grupos; 6 mujeres tenían paridad 4 y no hubo ninguna con paridad ≥ 5. La tabla 2 muestra la comparación de las características intraparto entre los grupos de tratamiento; ambos grupos fueron comparables con respecto a las variables intraparto estudiadas.
Características de las mujeres incluidas en el estudio según grupos de tratamiento
| Características | Mis + MA | MA | p |
| (n =702) | (n = 698) | ||
| Edad (años), media ± DEa | 26,4 ± 6,0 | 25,6 ± 5,9 | 0,025 |
| Gravidez, media ± DEa | 3,0 ± 1,8 | 2,9 ± 1,8 | 0,217 |
| Paridad, media ± DEa | 0,7 ± 0,8 | 0,6 ± 0,8 | 0,062 |
| Abortos, media ± DEa | 1,3 ± 1,4 | 1,2 ± 1,4 | 0,370 |
| Edad gestacional (semanas), media ± DEa | 39,6 ± 1,4 | 39,6 ± 1,3 | 0,827 |
| Paridad 1–4, n (%)b | 348 (49,6) | 317 (45,4) | 0,060 |
| Hematocrito preparto, media ± DEa | 0,37 ± 0,03 | 0,37 ± 0,03 | 0,351 |
| Anemia preparto, n (%)b | 37 (5,3) | 45 (6,4) | 0,174 |
DE: desviación estándar; Mis: misoprostol; MA: manejo activo.
Comparación de las características intraparto entre los grupos de tratamiento
| Características intraparto | Mis + MA | MA | p |
| (n = 702) | (n = 698) | ||
| Preeclampsia, n (%)a | 7 (1,0) | 8 (1,1) | 0,393 |
| Polihidramnios, n (%)b | 6 (0,9) | 2 (0,3) | 0,288 |
| Inducción del parto, n (%)a | 122 (17,4) | 146 (20,9) | 0,050 |
| Conducción con oxitocina, n (%)a | 76 (10,8) | 73 (10,5) | 0,412 |
| Peso fetal estimado > 4.000g, n (%)a | 18 (2,6) | 11 (1,6) | 0,097 |
| Nacimiento pretérmino, n (%)a | 31 (4,4) | 20 (2,9) | 0,061 |
| Desgarro cervical, n (%)a | 41 (5,8) | 29 (4,2) | 0,074 |
| Episiotomía, n (%)a | 188 (26,8) | 209 (29,9) | 0,095 |
| Desgarro perineal, n (%)a | 7 (1,0) | 6 (0,9) | 0,394 |
Mis: misoprostol; MA: manejo activo.
En el grupo I hubo 28/702 (4,0%) hemorragias posparto y en el grupo II ocurrieron 50/698 (7,2%) hemorragias; esta diferencia fue significativa (p = 0,005 y RR = 0,538; IC del 95%, para RR = 0,335, –0,866). En total, hubo 78/1.400 (5,6%) hemorragias posparto en el estudio.
El tiempo promedio de trabajo de parto en el grupo I fue 6,0 ± 1,5h y en el grupo II fue 6,1 ± 1,5h, y esta diferencia no fue significativa (p = 0,181). El tiempo promedio para el alumbramiento fue 6,6 ± 4,4min en el grupo I y 6,7 ± 4,3min en el grupo II (p = 0,629).
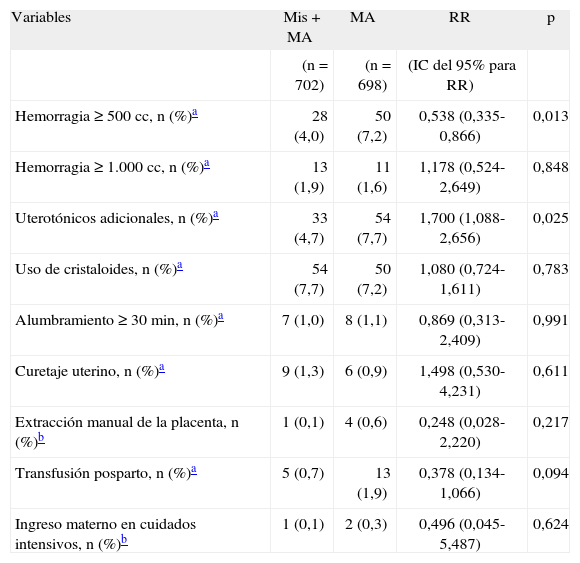
En la tabla 3 se presentan los resultados de las variables posparto estudiadas.
Variables posparto
| Variables | Mis + MA | MA | RR | p |
| (n = 702) | (n = 698) | (IC del 95% para RR) | ||
| Hemorragia ≥ 500cc, n (%)a | 28 (4,0) | 50 (7,2) | 0,538 (0,335-0,866) | 0,013 |
| Hemorragia ≥ 1.000cc, n (%)a | 13 (1,9) | 11 (1,6) | 1,178 (0,524-2,649) | 0,848 |
| Uterotónicos adicionales, n (%)a | 33 (4,7) | 54 (7,7) | 1,700 (1,088-2,656) | 0,025 |
| Uso de cristaloides, n (%)a | 54 (7,7) | 50 (7,2) | 1,080 (0,724-1,611) | 0,783 |
| Alumbramiento ≥ 30min, n (%)a | 7 (1,0) | 8 (1,1) | 0,869 (0,313-2,409) | 0,991 |
| Curetaje uterino, n (%)a | 9 (1,3) | 6 (0,9) | 1,498 (0,530-4,231) | 0,611 |
| Extracción manual de la placenta, n (%)b | 1 (0,1) | 4 (0,6) | 0,248 (0,028-2,220) | 0,217 |
| Transfusión posparto, n (%)a | 5 (0,7) | 13 (1,9) | 0,378 (0,134-1,066) | 0,094 |
| Ingreso materno en cuidados intensivos, n (%)b | 1 (0,1) | 2 (0,3) | 0,496 (0,045-5,487) | 0,624 |
Mis: misoprostol; MA: manejo activo.
En las mujeres del grupo I que tuvieron HPP el volumen promedio de sangre perdida fue 981 ± 309cc y en el grupo II fue 888 ± 326cc. Esta diferencia no fue significativa (p = 0,225). En las mujeres del grupo I que no tuvieron HPP, el volumen promedio de sangre perdida fue 213 ± 176cc y en el grupo II fue de 191 ± 132cc; esta diferencia fue significativa (p = 0,009).
La disminución promedio registrada en el hematocrito posparto fue 3,1 ± 2,2 (rango 0-13) en el grupo I y en el grupo II fue de 3,4 ± 2,4, (rango 0-16); la diferencia entre los grupos no fue significativa (p = 0,080).
Requirieron transfusión de sangre o glóbulos 18/78 (23,1%) de las pacientes con HPP; 5/28 (17,9%) del grupo I y 13/50 (26,0%) del grupo II (p = 0,207). En 4/13 (30,8%) pacientes del grupo II fue necesario utilizar 3 o más bolsas de sangre. No hubo ninguna histerectomía posparto ni tampoco muerte materna en ninguno de los 2 grupos.
En 268/702 (38,2%) mujeres que recibieron el misoprostol no se observó ningún efecto secundario. Los escalofríos fue el efecto secundario más frecuente y ocurrió en 390/702 (55,6%) pacientes del grupo I y en 81/698 (11,6%) del grupo II (p < 0,001; RR = 0,105; IC del 95%, 0,082-0,142). La hipertermia (≥ 38° C) se observó en 272/702 (38,7%) mujeres y en 23/698 (3,3%) de los grupos I y II, respectivamente (p < 0,001; RR = 0,053; IC del 95%, 0,034-0,082). Los vómitos, las náuseas y la diarrea ocurrieron en el 4, el 2 y el 1,5 de los sujetos del grupo I y en el 0,6, el 0,3 y el 0,3 de los del grupo II.
El peso promedio al nacer fue 3.335 ± 434g en el grupo I y 3.297 ± 424g en el grupo II; esta diferencia no fue significativa (p = 0,101). En las mujeres que tuvieron HPP ≥ 500cc, el peso promedio de sus neonatos fue de 3.504 ± 416g y en las que no tuvieron HPP el peso promedio neonatal fue de 3.304 ± 427g; esta diferencia fue significativa (p < 0,0001). Hubo 8/702 (1,1%) neonatos con una puntuación de Apgar al minuto < 7 en el grupo I y 4/698 (0,6%) en el grupo II (p = 0,390). A los 5min hubo 1/702 (0,1%) neonato con una puntuación de Apgar de 6 en el grupo I y 1/698 (0,1%) neonato con una puntuación en la prueba de Apgar de 6 en el grupo II (p = 1,000).
Fueron ingresados en cuidados intensivos 12/702 (1,7%) y 9/698 (1,3%) neonatos de los grupos I y II, respectivamente (p = 0,670). Las causas de los ingresos en cuidados intensivos de neonatos del grupo I fueron: 2 (0,3%) por bajo peso, 4 (0,6%) por peso ≥ 4.200g, 5 (0,7%) para observación por ser hijos de madres diabéticas y 1 (0,1%) por malformación congénita. En los neonatos del grupo II ingresados en cuidados intensivos las causas fueron: 3 (0,4%) por bajo peso, 1 (0,1%) por peso ≥ 4.200g, 3 (0,4%) para observación por ser hijos de madres diabéticas y 2 (0,3%) por asfixia ligera intraparto.
DISCUSIÓNLa diferencia obtenida entre los porcentajes de HPP en el grupo I, 28/702 (4%), y en el grupo II, 50/698 (7,2%), es significativa (p = 0,013), con un 44% menos de HPP en el grupo I debido, hipotéticamente, al efecto añadido del misoprostol. Aunque los resultados que se obtienen con el uso del manejo activo de la tercera fase del parto son bastante satisfactorios, no habría que desdeñar mejorar esos resultados con la adición sistemática de una dosis de misoprostol que reduce en casi un 50% el porcentaje de hemorragias que se producen con la aplicación del manejo activo.
Este es uno de los pocos estudios que se han realizado añadiendo misoprostol al protocolo de manejo activo de la tercera fase del parto y el primero en el que el misoprostol se administra por vías sublingual y rectal, ya que en la mayoría de los estudios publicados se sustituye la oxitocina o la metilergonovina por el misoprostol, comparando la eficacia de este último con la que se obtiene con los uterotónicos estándar o con grupos placebo6,8,13-21.
En nuestra opinión, en los países donde se aplica el manejo activo, no se trata de sustituir la oxitocina o la metilergonovina por el misoprostol u otro fármaco, sino de valorar qué beneficios aportaría su uso sistemático junto con el manejo activo, ya que está bien demostrado que el misoprostol no es más eficaz que los uterotónicos estándar, sino que tiene una eficacia similar o ligeramente inferior según sean los estudios6,8,13-21.
Este menor porcentaje de hemorragias en el grupo con misoprostol añadido podría estar ligeramente sesgado por el mayor número de inducciones del parto que se dieron en el grupo sin misoprostol 122 (17,4%) frente a 146 (20,9%), con un valor de p en el limite de la significación (p = 0,05).
Hay que resaltar que añadir misoprostol al manejo activo no disminuyó el porcentaje de hemorragias graves (≥ de 1.000cc) contra lo que hubiera podido esperarse. Es decir, el misoprostol disminuyó la incidencia de hemorragias de forma significativa pero no su gravedad. Por el contrario, sí disminuyó la necesidad de uterotónicos adicionales (el 4,7 frente al 7,7%); esta diferencia fue significativa (p = 0,025). También hubo una tendencia a un menor número de transfusiones sanguíneas en el grupo con misoprostol añadido: 5 (0,7%) frente a 13 (1,9%), aunque sin significación estadística (p = 0,094). Probablemente esta diferencia sería significativa en una muestra de mayor tamaño.
Hay que destacar que no hubo diferencias significativas en el resto de variables estudiadas: a) uso de cristaloides, b) duración del alumbramiento, c) número de legrados uterinos, d) número de extracciones manuales de placenta, y e) número de neonatos ingresados en cuidados intensivos.
Es conveniente explicar que de las 2.736 pacientes que cumplieron los criterios de entrada al estudio, sólo 1.410 entraron a este debido a que de los 7 equipos de guardia del hospital, sólo 3 estaban autorizados a participar en este estudio.
Es llamativo el hecho de que las pacientes que tuvieron HPP en ambos grupos dieron a luz neonatos de mayor peso (3.504 ± 416g) que las que no tuvieron HPP (3.304 ± 427g) (p ≤ 0,0001). En nuestra opinión, esta diferencia de 200g, a pesar de ser muy significativa, no debió de desempeñar una gran influencia en el desencadenamiento o no de las hemorragias.
Es llamativo el alto porcentaje de escalofríos (55,6%) obtenido en el grupo I; probablemente el porcentaje de escalofríos debido al efecto del misoprostol sea menor, ya que en el grupo II hubo un 11,6% de escalofríos a pesar de que no recibieron misoprostol.
Los porcentajes de escalofríos e hiperpirexia en este estudio fueron similares a los obtenidos por Hoj et al16 (57%), que utilizaron 600μg por vía sublingual, y superiores a los obtenidos en otros estudios realizados con 100, 200 o 400μg por vía sublingual también15,17 y, lógicamente, también superiores a los obtenidos en otros estudios en los que se utilizó la vía oral o rectal8,13. Hay que señalar que, en este trabajo, no se estudió la intensidad de los escalofríos, pero al igual que Caliskan et al13, pensamos que estos, en la gran mayoría de los casos, fueron bien tolerados por la mujer. No obstante, es conveniente que las salas de partos estén a la temperatura adecuada y que cuenten con mantas o coberturas para la paciente.
Los dos únicos estudios publicados con los que se pudieran contrastar nuestros resultados son los realizados por Caliskan et al8,13, ya que en uno de los brazos de estudio se administró misoprostol más oxitocina y manejo activo como en este trabajo. En el estudio con misoprostol por vía oral el porcentaje de HPP que obtiene es similar al nuestro (el 3,2 frente al 4%), es decir, también obtuvieron una significativa disminución del porcentaje de hemorragias cuando se añadió misoprostol al manejo activo13. Nuestro porcentaje de hemorragias es menor que en el otro estudio de Caliskan et al8, probablemente debido al uso del misoprostol por vía rectal en este estudio.
Sería deseable que existiese una presentación flash del misoprostol, ya que probablemente su absorción sea más rápida y, por tanto, su acción clínica antihemorrágica también. Es posible que en una presentación flash aumenten los efectos secundarios ligeramente, aunque probablemente su aceptabilidad sea mayor ya que se evitará la incomodidad que representa tener unas pastillas debajo de la lengua, que tardan de a 30min en disolverse, lo que, en ocasiones, provocan una sensación no placentera.
A modo de conclusión, podríamos afirmar que, dado el bajo coste, la facilidad de administración y que se produce una disminución del porcentaje de hemorragias superior al 40% respecto del grupo que no lleva misoprostol, se podría plantear la administración por vía sublingual junto al manejo activo, si no de forma sistemática, si al menos en los casos que tuvieran factores de riesgo para HPP.
Sería conveniente realizar más estudios con la vía sublingual y quizás con dosis superiores, que incluyeran también la aceptabilidad por parte de la mujer.
Queremos agradecer la invalorable colaboración de Iris Villa Gener.