El pronóstico de los sarcomas musculoesqueléticos se relaciona con su adecuado manejo en el seno de los equipos multidisciplinarios con formación específica. El radiólogo musculoesquelético es el responsable de la biopsia percutánea con control de imagen de estos tumores, que se ha impuesto a la quirúrgica en la mayoría de los casos, con una fiabilidad diagnóstica de al menos el 80%. Debe conocer: a) sus limitaciones respecto de la biopsia quirúrgica; b) qué se debe y no se debe biopsiar; c) la adecuada planificación de la biopsia percutánea, con especial atención a la vía de abordaje, teniendo en cuenta la anatomía compartimental y la vía de abordaje del posterior tratamiento quirúrgico; y d) aspectos técnicos del procedimiento, tales como la zona de la tumoración a biopsiar, calibre de la aguja, número y longitud de las muestras obtenidas para optimización del rendimiento diagnóstico, y técnicas en función de la modalidad de imagen y penetración ósea.
The prognosis of musculoskeletal sarcomas is related to appropriate management by specifically trained multidisciplinary teams. Musculoskeletal radiologists are responsible for the image-guided percutaneous biopsy of these tumors, which has a diagnostic accuracy of at least 80%. It is essential for radiologists to know: a) the limitations of percutaneous biopsy with respect to surgical biopsy; b) what should and should not be biopsied; c) how to appropriately plan percutaneous biopsy, with special attention to the route of approach, taking into account the compartmental anatomy and the route of approach after surgical treatment; and d) technical aspects of the procedure, like the area of the tumor to biopsy, the caliber of the needle, the number and length of the specimens to obtain to ensure optimal pathological diagnosis, and techniques in function of the imaging modality and bone penetration.
La incidencia de sarcomas óseos en España se ha establecido en 1/100.000 habitantes y la de sarcomas de partes blandas de extremidades, en 3-4/100.000 habitantes (una incidencia aproximada 3 veces superior a los óseos) lo cual suma un total de unos 2.000 casos nuevos/año de tumores musculoesqueléticos en España. Estos datos son consistentes con los publicados en los registros internacionales1.
Se ha demostrado que el pronóstico de los pacientes no tratados en unidades multidisciplinarias con formación específica se ve seriamente afectado por la realización de biopsias o tratamientos inadecuados2, por lo que es fundamental planificar de forma correcta la biopsia percutánea de la lesión, que presenta ventajas e inconvenientes respecto de la biopsia quirúrgica (tabla 1).
Ventajas e inconvenientes de la biopsia percutánea
| Ventajas | Inconvenientes |
| Más económica | Menor disponibilidad |
| No necesidad de quirófano | Sobre todo para la biopsia ósea |
| Hospital de día | Necesidad de radiólogo intervencionista |
| Menos traumática | Mayor coordinación multidisciplinaria |
| Incisión cutánea de un par de milímetros | Menos obtención de muestra |
| No disección de planos-tejidos | Requiere biopsia múltiple o un muestreo representativo por: |
| Recuperación inmediata | • posible necrosis |
| Menos contaminación tumoral | • sangrado |
| Por menos traumática | • tumor de composición variegata |
| Menos sangrado | Mayor dificultad en el diagnóstico histológico |
| Menos riesgo de: | |
| Infección | |
| Hemorragia |
Veremos a continuación aspectos fundamentales a considerar en esta tarea, que responde a las siguientes preguntas:
¿Qué no se debe biopsiar?El radiólogo debe conocer aquellas lesiones óseas y de partes blandas que son características y benignas por imagen (tabla 2), sin riesgo de que pueda tratarse de una lesión maligna. En general, las lesiones óseas de tipo geográfico I a (aquellas bien definidas con un halo escleroso en la radiología convencional), no suelen requerir biopsia y solo podría estar justificada en algún caso de displasia osteofibrosa, cuando pudiera considerarse la posibilidad de adamantinoma, o en algunos casos de sospecha de osteomielitis, para identificación del germen. En las lesiones lipomatosas de partes blandas, deben biopsiarse aquellas lesiones con algún componente de tejido con señal o atenuación diferente de la grasa madura.
Lesiones de «no biopsiar»
| Lesión ósea | Lesión de partes blandas |
| Lesión geográfica I a | Lesión benigna de aspecto característico por imagen |
| Fibroma no osificante | Lipoma |
| Quiste simple | MAV-hemangioma |
| Quiste óseo aneurismático 1° | Ganglión-quiste sinovial |
| Encondroma pequeño (falange) | Sinovitis villonodular |
| Displasia fibrosa | TCG-VT |
| Osteomielitis con hemocultivo + | Angiomioma |
| Osteocondroma típico | Miositis osificante |
| Hemangioma vertebral típico | Adenopatía con serología específica positiva |
| Avulsión osteotendinosa | |
| Fractura de estrés |
MAV: malformación arteriovenosa; TCG-VT: tumor de células gigantes de la vaina tendinosa.
Para las otras lesiones, si son típicas, la biopsia en el mejor de los casos solo añade morbilidad. Podría incluso equivocar a un patólogo no experto. Así por ejemplo, podría confundirse una miositis osificante en su fase aguda-subaguda, o una avulsión osteotendinosa en fase de reparación y calcificación, con un osteosarcoma, con la morbilidad que esto implicaría para el paciente.
Por el contrario, no debe asumirse la inocencia de una lesión simplemente porque es pequeña, indolora, subcutánea y no infiltrativa, porque podría tratarse de un leiomiosarcoma o de un fibrosarcoma subcutáneo, por ejemplo. Deberíamos desconfiar también de la fascitis nodular, aunque parezca típica, y estar muy atentos a lo que parece un «hematoma espontáneo» en un paciente sin problemas de coagulación3.
¿Por dónde hacer la biopsia? Planificación de la biopsia y vía de abordajeUn primer aspecto fundamental para el radiólogo musculoesquelético es conocer la anatomía compartimental (tabla 3), de manera que la regla de oro a la hora de planificar la biopsia percutánea es respetar el compartimento anatómico en cuestión4. Si el trayecto de biopsia contamina otro compartimento5, la convierte en extracompartimental y podría comprometer una cirugía conservadora del miembro (CCM).
Compartimentos anatómicos
| Espacios extracompartimentales | General | Miembro superior | Miembro inferior | Pelvis | |
| Cebeza | T. periclavicular | Hueso | T. periescapular | Muslo | Cada músculo |
| Cuello | Fosa antecubital | T. paraóseo | Brazo | Anterior | Cada hueso |
| Axila | Fosa poplítea | Articulación | Anterior | Posterior | individual |
| Muñeca | Dorso mano | Piel y T. celular subcutáneo | Posterior | Medial | |
| Ingle | Dorso pie | Antebrazo | Pierna | ||
| Tobillo | Volar | Anterior | |||
| T. paraespinal | Dorsal | Posterior | |||
| Palma mano | Post profundo | ||||
| Lateral | |||||
| Pie | |||||
| Medial | |||||
| Central | |||||
| Lateral | |||||
Fuente: basado en Anderson et al.4.
T: tejido.
Por tanto, una correcta biopsia de un tumor musculoesquelético comienza por una detallada descripción de su extensión locorregional en el estudio de resonancia magnética (RM), bajo el concepto de esta anatomía compartimental (fig. 1). La norma general para la planificación del punto de abordaje y trayecto de la biopsia es el camino más directo a la lesión, siempre que cumpla 2 requisitos fundamentales: 1) no atravesar otro compartimento anatómico, y 2) que coincida con la vía de abordaje quirúrgico definitiva6. Junto a estos 2 principios básicos, se debe evitar contaminar el eje vasculonervioso y las articulaciones.
Descripción de la extensión locorregional de la tumoración en el seno de la anatomía compartimental. Histiocitoma fibroso maligno (flechas negras) en el compartimento volar del antebrazo (rojo). Imagen RM axial SE T1. Huesos: C cubito, R radio. Músculos: Br brachioradialis, Pt pronator teres, FCR flexor carpi radialis, FDS flexor digitorum superficialis, FCU flexor carpi ulnaris, FDP flexor digitorum profundus, APL abductor pollicis longus, ECU exensor carpi ulnaris, EDM extensor digiti minimi, ED extensor digitorum, S supinador, ECRB-L extensor carpi radialis brevis y longus. Ejes neurovasculres: 1: nervio radial; 2: nervio mediano; 3: nervio interóseo anterior; 4: nervio interóseo posterior; 5: nervio cubital. Observe la hiperintensidad de señal en la imagen T1 sin gadolinio, debido a sangrado (metahemoglobina).
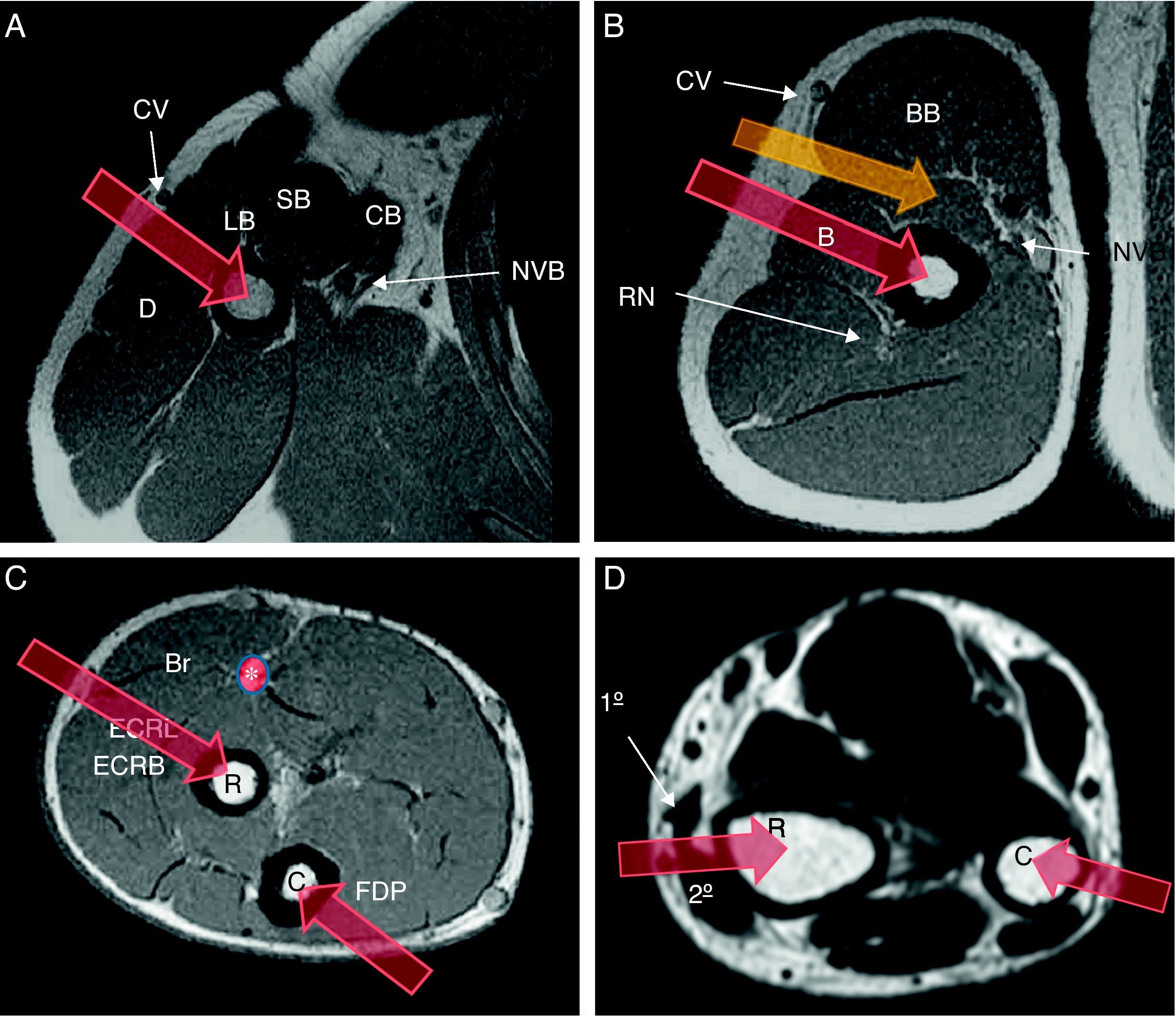
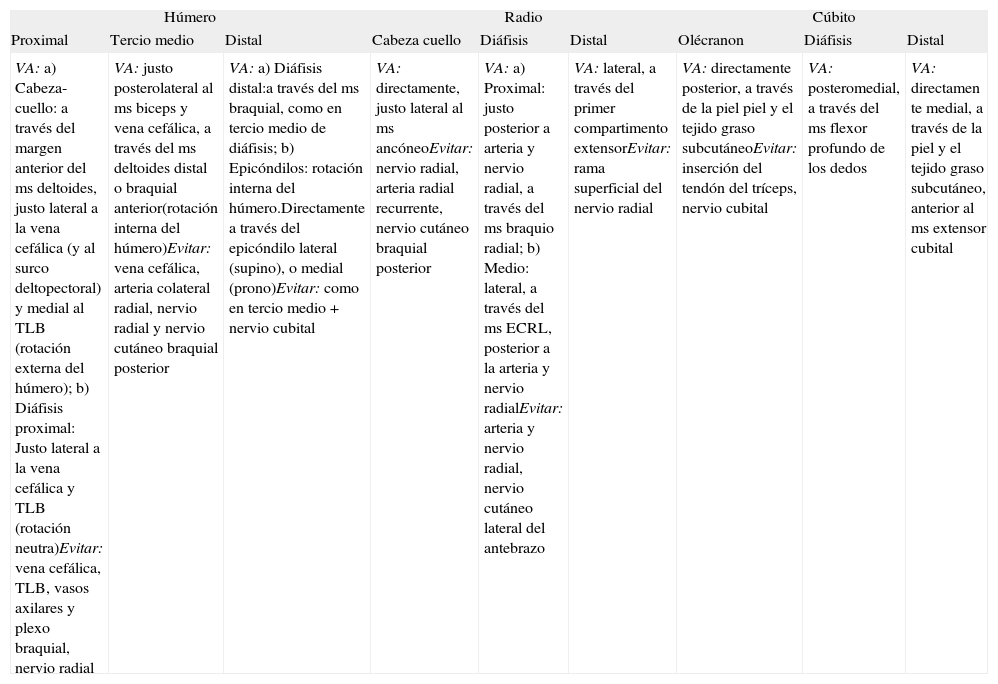
Aunque no se pueden dar pautas universales, sí se deben considerar unas recomendaciones generales, que deben adaptarse a cada caso en el seno del equipo multidisciplinario7. En la tabla 4 se expone la vía de abordaje de biopsia recomendada para cada uno de los huesos del miembro superior, en función de una localización proximal, diafisaria o distal (figs. 2 y 3). Se especifican para cada apartado las estructuras que deben evitarse. El abordaje de la escápula debe hacerse medialmente, por ser este el abordaje quirúrgico estándar.
Vía de abordaje de biopsia del miembro superior (figs. 2 y 3)
| Húmero | Radio | Cúbito | ||||||
| Proximal | Tercio medio | Distal | Cabeza cuello | Diáfisis | Distal | Olécranon | Diáfisis | Distal |
| VA: a) Cabeza-cuello: a través del margen anterior del ms deltoides, justo lateral a la vena cefálica (y al surco deltopectoral) y medial al TLB (rotación externa del húmero); b) Diáfisis proximal: Justo lateral a la vena cefálica y TLB (rotación neutra)Evitar: vena cefálica, TLB, vasos axilares y plexo braquial, nervio radial | VA: justo posterolateral al ms biceps y vena cefálica, a través del ms deltoides distal o braquial anterior(rotación interna del húmero)Evitar: vena cefálica, arteria colateral radial, nervio radial y nervio cutáneo braquial posterior | VA: a) Diáfisis distal:a través del ms braquial, como en tercio medio de diáfisis; b) Epicóndilos: rotación interna del húmero.Directamente a través del epicóndilo lateral (supino), o medial (prono)Evitar: como en tercio medio + nervio cubital | VA: directamente, justo lateral al ms ancóneoEvitar: nervio radial, arteria radial recurrente, nervio cutáneo braquial posterior | VA: a) Proximal: justo posterior a arteria y nervio radial, a través del ms braquio radial; b) Medio: lateral, a través del ms ECRL, posterior a la arteria y nervio radialEvitar: arteria y nervio radial, nervio cutáneo lateral del antebrazo | VA: lateral, a través del primer compartimento extensorEvitar: rama superficial del nervio radial | VA: directamente posterior, a través de la piel piel y el tejido graso subcutáneoEvitar: inserción del tendón del tríceps, nervio cubital | VA: posteromedial, a través del ms flexor profundo de los dedos | VA: directamen te medial, a través de la piel y el tejido graso subcutáneo, anterior al ms extensor cubital |
ECRL: tendón o músculo extensor largo radial del carpo; TLB: tendón largo del bíceps; VA: vía de abordaje recomendado.
Fuente: basado en Liu et al.7.
Vía de abordaje de biopsia en el brazo y el antebrazo (flechas rojas). A) Diáfisis proximal del húmero, por el margen inferior del deltoides (D), justo por detrás de la vena cefálica (CV). LB, SB cabeza larga y corta del ms biceps. CB ms coracobraquial. NVB paquete neurovascular axilar. B) Tercio medio de diáfisis humeral, a través del ms braquial. Vía de abordaje recomendada para TPB localizado en la profundidad del compartimento anterior (flecha amarilla). RN nervio radial. BB ms biceps braquial. C) Diáfisis radial, por el margen posterior del ms extensor largo radial del carpo (ECRL), posterior a la arteria radial y rama superficial del nervio radial (*). Br ms braquiorradial. Diáfisis cubital, por el margen posterior del flexor profundo de los dedos (FDP). D) Cúbito distal, directamente a través de la piel y el tejido graso subcutáneo. En el radio distal, entre el primero y segundo compartimentos extensores (1°, 2°). R radio, C cúbito.
La tabla 5 expone la vía de abordaje de biopsia recomendada para cada uno de los huesos del miembro inferior, según un esquema semejante al miembro superior (fig. 4). Cabe resaltar también algunas consideraciones. Debe evitarse, en la medida de lo posible, atravesar el músculo sartorio y el gracilis ya que suelen utilizarse como autoinjertos. Debe evitarse también atravesar la musculatura glútea, el músculo recto anterior, el vasto intermedio, el tendón del cuádriceps o el rotuliano, por su importante repercusión funcional. En el tercio inferior del muslo debe sortearse el músculo o el tendón por su margen medial. En la pelvis es recomendable acceder a la lesión a través de las espinas ilíacas anteriores o posterosuperior. Después de un punto y aparte:
Vía de abordaje de biopsia del miembro inferior (fig. 4)
| Fémur | Tibia | Peroné | |||
| Cabeza y cuello | Diáfisis | Distal | Proximal y distal | Diáfisis | |
| VA: subtrocantéreo lateral, angulado cranealmenteEvitar: bursas peritrocantéreas, articulación de la cadera, rama transversa de la arteria circunfleja femoral lateral | VA: lateral, justo anterior al LIS, a través del margen posterior del vasto lateralEvitar: ms recto femoral y vasto intermedio, nervio ciático y vasos femorales profundos | VA: a) Medial: margen posterior del vasto medial. Lateral: como en diáfisis; b) Directamente en cóndilos lateral o medial, posterior a inserción de retináculosEvitar: arteria geniculares superiores, articulación de la rodilla, nervio y vasos poplíteos | VA: directamente anteromedial, a través de la piel y el tejido graso subcutáneoEvitar: a) Extremo proximal: tubérculo tibial (inserción del tendón patelar), pata de ganso; b) Extremo distal: vena safena mayor, nervio safeno | VA: directamente lateral, a través de la piel y el tejido graso subcutáneoEvitar: a) Extremo proximal: nervio peroneo común, inserción del ms bíceps femoralb) Extremo distal: nervio cutáneo dorsal lateral, tendones peroneos | VA: justo anterior al PIS, a través del margen posterior del ms peroneo largoEvitar: nervios peroneos superficial y profundo |
LIS: septo intermuscular lateral; PIS: septo intermuscular posterior; VA: vía de abordaje recomendada.
Vía de abordaje de biopsia en el muslo y la pierna (flechas rojas). A) Diáfisis proximal del fémur, justo anterior al septo intermuscular lateral (LIS) (azul). Evitar el abordaje anterior que fue realizado, a través del ms recto anterior y vasto intermedio (afortunadamente se trató de un linfoma folicular de bajo grado). Vía de abordaje recomendada (flecha amarilla) para un TPB que se localizara en el compartimento medial, posterior al paquete vasculonervioso. B) Fémur distal, directamente en el cóndilo afectado, por detrás del retináculo patelofemoral. Si se localiza ligeramente proximal, se realiza a través del margen posterior del vasto lateral o medial. Histiocitoma fibroso maligno. C) En la pierna, el abordaje se realiza directamente a través de la piel y el tejido graso subcutáneo en el extremo distal de la tibia y el peroné. Tumor de células gigantes. En la diáfisis peronea, se realiza justo anterior al septo intermuscular posterior (PIS) (azul), a través del ms peroneo largo.
Se hacen también algunas recomendaciones puntuales para el abordaje de un tumor de partes blandas (TPB) de localización profunda (figs. 3 y 4).
¿Qué parte de la lesión debe biopsiarse?Deben evitarse las áreas de necrosis o hemorragia: en general es mejor obtener muestra de la periferia de una tumoración y del componente de partes blandas de una tumoración ósea. Es también preferible la zona con mayor actividad metabólica de una lesión (gammagrafía ósea con SPECT o PET-TC), incluso para poder detectarla en un procedimiento TC dirigido (fig. 5).
A) PET-TC de la pelvis muestra un claro aumento del metabolismo de la glucosa en el ilíaco derecho, próximo a la espina ilíaca anterosuperior (EIAS), sin alteraciones en la atenuación ósea de la imagen TC. B) Biopsia a través de la EIAS con dirección ligeramente ascendente, guiados por la imagen PET-TC. Metástasis de Ca de pulmón.
Si bien una punción aspiración con aguja fina (PAAF), puede ser efectiva en afecciones como metástasis o mieloma, en general debe realizarse biopsia con aguja gruesa por su mayor fiabilidad. La rentabilidad diagnóstica de la biopsia percutánea se ha relacionado con la longitud del cilindro de tejido de la muestra obtenida, prácticamente el doble en cilindros de más de 10mm (82%) respecto de aquellos de menos de 5mm (42%), con un rendimiento diagnóstico óptimo con la obtención de 4 muestras (cilindros de tejido) para TPB, y de 3 muestras para lesiones óseas8. Sin embargo, estos autores establecieron un rendimiento semejante utilizando agujas de 14 o 18G. En nuestra experiencia es preferible agujas de 11-13G para el hueso y de al menos 16G para TPB, con cilindros de 10-20mm. Son necesarios previo a la biopsia: el estudio locorregional detallado con RM (ya comentado), el consentimiento informado del paciente y el estudio de coagulación. No olvidar prever la interrupción de un tratamiento antiagregante y el cambio oportuno de anticoagulante oral a heparina. Es suficiente una buena anestesia local para los TPB. Se puede acompañar de la administración previa de un ansiolítico de rápido efecto (alprazolam). En tumoraciones óseas es preferible además el apoyo del anestesista (sedación profunda con monitorización del paciente).
Guía de imagen- a)
La guía fluoroscópica prácticamente se utiliza solo en algún caso de biopsia transcervical de cabeza femoral.
- b)
Biopsia eco-dirigida.
Lo más frecuente para una TPB es la biopsia eco-dirigida. Planificada la biopsia, se marca en la piel el punto de incisión con visualización ecográfica en tiempo real de la tumoración. El seguimiento ecográfico de la aguja (con un plano paralelo al haz de ultrasonidos), requiere un trayecto menos vertical que con TC (fig. 6). La muestra se envía en formol para estudio histológico. Si el trayecto es profundo y complicado, es recomendable la colocación inicial eco-dirigida de una aguja introductora 15G, dejando el extremo inmediatamente superficial a la tumoración. A continuación se pueden dar los pases necesarios con aguja de disparo automático 16G, coaxial a la aguja introductora, y con visualización ecográfica en tiempo real. Podría ser preferible realizar esta técnica con control TC cuando la visualización ecográfica no es óptima (fig. 7).
Figura 6.Biopsia eco-dirigida de tumoración de partes blandas. A) Sistema de disparo automático con aguja trucut de 14-16G, y recorrido de 15 o 22mm. B) Visualización en tiempo real del trayecto de la aguja hacia la lesión, patralela al haz de ultrasonidos. Observe en el ángulo inferior izquierdo la aguja con la muestra en su interior.
(0.33MB).Figura 7.Biopsia TC-dirigida de tumoración de partes blandas. 1: Se inserta una aguja Chiba de 19-22G, tras planificación y marcaje de la vía de abordaje de la biopsia, para infiltración del anestésico local y señalización segura del trayecto de biopsia, entre el conducto inguinal y el paquete vasculonervioso femoral (flechas blancas); 2: Después de romper la cabeza de la aguja Chiba, introducción coaxial a la Chiba de una segunda aguja (que podría ser en este caso una aguja introductora 15G); 3: Previa retirada de la aguja Chiba, introducción coaxial de una aguja 16G de disparo automático y muestreo con 4 pases y pequeñas angulaciones de la aguja introductora. Condroma perióstico (flechas rojas).
(0.39MB). - c)
Biopsia tomografía computarizada-dirigida
Lo habitual para una tumoración ósea es la biopsia TC-dirigida, salvo si existe aumento de partes blandas accesible con ecografía. La infiltración profunda y la dirección segura del tracto pueden realizarse con aguja Chiba de 20-22G y al menos 16cm de longitud, como en la figura 7. La aguja de biopsia ósea se introduce coaxial por la aguja Chiba hasta la cortical ósea. Se pueden utilizar distintas estrategias para atravesar la cortical en función de su dureza, desde giro-presión, con o sin efecto berbiquí, hasta taladro automático con aguja Kischner o broca, pasando por percusión con martillo. Para ello existen distintas agujas y sets de biopsia ósea en el mercado (fig. 8). La toma de biopsia múltiple (siempre aconsejable) puede realizarse con una cánula coaxial de mayor longitud y menor calibre, con distintas angulaciones o recolocación de la aguja de biopsia. La obtención de la última muestra (de mayor grosor) se realiza con la propia aguja de la biopsia.
Biopsia TC-dirigida de tumoración ósea con cortical dura. 1: Tras planificación y marcaje, infiltración del trayecto de biopsia hasta el periostio; 2: Introducción del estilete paralelo a la anterior, hasta clavarlo en la superficie de la cortical; 3: Introducción coaxial al estilete de la cánula introductora; 4: Retirada del estilete e introducción coaxial de la aguja berbiquí. Presión y rotación penetrando la cortical ósea; 5: Retirada del berbiquí e introducción de la cánula de biopsia; 6: Eyección de la muestra con el eyector mediante la cánula de biopsia. Osteoma osteoide.
En la biopsia de algunas lesiones óseas se obtiene un aspirado hemático cuyo procesamiento histológico es con frecuencia valorable. Es recomendable separar en distintas muestras en formol, bien rotuladas, la muestra de aspirado hemático de la muestra de cilindro de tejido óseo, así como el envío de una muestra en recipiente estéril para estudio microbiológico.
En la columna vertebral el acceso al cuerpo vertebral puede ser paravertebral, costovertebral o transpedicular, según el caso. Incluso puede ser necesario un abordaje transoral en la columna cervical alta9 (fig. 9).
ConclusiónLa biopsia percutánea ha demostrado su utilidad en el diagnóstico de la patología tumoral musculoesquelética, aunque se ha publicado un rendimiento diagnóstico menor para las lesiones óseas esclerosas (57%) respecto de las líticas (87%), para las lesiones pequeñas, sobre todo inferiores a 2cm, y para las lesiones benignas8. La literatura y nuestra experiencia establecen una fiabilidad para diferenciar lesión benigna de maligna de al menos el 80% con un rendimiento diagnóstico para malignidad del 81,4-98%; y para las lesiones benignas del 78-92,85%10–12, con un valor predictivo positivo del 98,9% para la lesión maligna y del 90,2% para la lesión benigna10.
Esta técnica es, además, mínimamente invasiva, y no presenta complicaciones importantes10–12 si se realiza en el seno de equipos multidisciplinarios con experiencia. El radiólogo musculoesquelético debe conocer y dominar los aspectos de la biopsia percutánea, cuyos fundamentos se han desarrollado en este capítulo.
Autorías- 1.
Responsable de la integridad del estudio: ABH y JMV.
- 2.
Concepción del estudio: ABH y JMV.
- 3.
Diseño del estudio: ABH y JMV.
- 4.
Obtención de los datos: ABH y JMV.
- 5.
Análisis e interpretación de los datos: ABH y JMV.
- 6.
Tratamiento estadístico: No procede.
- 7.
Búsqueda bibliográfica: JMV.
- 8.
Redacción del trabajo: ABH.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: JMV.
- 10.
Aprobación de la versión final: ABH y JMV.
Los autores declaran no tener ningún conflicto de intereses.