El cáncer de mama sigue siendo el tumor maligno más frecuente entre las mujeres occidentales. La mamografía es, hoy por hoy, la técnica de elección para el cribado poblacional. Aunque es una técnica ampliamente validada, tiene limitaciones, especialmente en las mamas densas. La tomosíntesis de mama ha supuesto una revolución en el diagnóstico de cáncer de mama. Permite definir lesiones ocultas en el interior del tejido glandular y, por tanto, detectar tumores de mama no visibles mediante estudios mamográficos convencionales.
Para considerar el uso combinado de ambas técnicas, hay que tener en cuenta muchos factores aparte de la detección de cáncer, como la radiación adicional, la tasa de rellamadas, y el tiempo de realización y lectura de ambas pruebas.
En este artículo revisamos los principios técnicos de la tomosíntesis, sus principales utilidades y las perspectivas de futuro de esta técnica de imagen.
Breast cancer continues to be the most common malignant tumor in women in occidental countries. Mammography is currently the technique of choice for screening programs; however, although it has been widely validated, mammography has its limitations, especially in dense breasts. Breast tomosynthesis is a revolutionary advance in the diagnosis of breast cancer. It makes it possible to define lesions that are occult in the glandular tissue and therefore to detect breast tumors that are impossible to see on conventional mammograms.
In considering the combined use of mammography and tomosynthesis, many factors must be taken into account apart from cancer detection; these include additional radiation, the recall rate, and the time necessary to carry out and interpret the two tests.
In this article, we review the technical principles of tomosynthesis, it main uses, and the future perspective for this imaging technique.
El cáncer de mama es la neoplasia más frecuente y la principal causa de muerte por cáncer entre las mujeres1. La mamografía es la técnica de elección para el cribado poblacional, la única que ha demostrado una disminución a largo plazo de la mortalidad2,3. Aunque se trata de una técnica muy útil, hasta un 20-30% de los cánceres de mama pueden no detectarse en el cribado mamográfico4,5.
Son muchos los factores que influyen en la precisión diagnóstica de la mamografía4,5; el patrón de densidad mamaria es uno de los más relevantes. La sensibilidad de la mamografía oscila entre un 98% en las mamas de predominio graso y un 40% en las densas6. Con el desarrollo de la mamografía digital (MD) se ha conseguido mejorar levemente la sensibilidad de la técnica en subgrupos poblacionales como las mujeres menores de 50 años y aquellas con mamas densas, aunque, en este último grupo, sigue estando alrededor del 60%4. Además, ha permitido detectar mejor las microcalcificaciones y los carcinomas intraductales7. La menor sensibilidad de la mamografía en las mamas densas está relacionada con las características de la técnica. Al tratarse de una imagen bidimensional, en las mamas densas la cantidad de tejidos superpuestos hace más difícil detectar lesiones sospechosas de malignidad o crea imágenes falsamente sospechosas. Este hecho, además de retrasar el diagnóstico, puede aumentar las rellamadas y las biopsias innecesarias.
La tomosíntesis es una técnica novedosa que permite disminuir la superposición de los tejidos al adquirir secuencialmente imágenes consecutivas de baja dosis de radiación. Esta cualidad permite mejorar la precisión diagnóstica de la mamografía en las mamas densas8 y disminuir el número de rellamadas innecesarias9.
En este artículo describimos la técnica de la tomosíntesis, sus principales indicaciones clínicas y las perspectivas de futuro.
Técnica de imagenGeneración de la imagenEn la MD la dosis de radiación se emite en una dirección predeterminada desde un tubo de rayos X que permanece estático. Esa dosis de radiación atraviesa la mama, comprimida con el propósito de disminuir la dosis de radiación y dispersar el tejido mamario, para apreciar mejor las lesiones mamarias. Finalmente, la radiación es recogida por un detector que la codifica en una señal eléctrica que forma la imagen.
En los estudios de tomosíntesis, el tubo de rayos X se mueve realizando un arco de amplitud variable (dependiendo del fabricante puede ir desde los 11 a los 60°) mientras emite pulsos de radiación de baja dosis. Estos pulsos se emiten de manera regular cada 1 o 2°, atraviesan la mama comprimida y son recogidos por el detector generando de esta manera los datos brutos. La información es procesada y reconstruida en planos paralelos al detector, normalmente de 1mm de grosor. Así obtenemos las imágenes consecutivas que conforman la tomosíntesis de mama.
Dosis de radiaciónPor consenso, la dosis máxima de la tomosíntesis de mama es, en conjunto, menor de 300mrad10 para una mama de espesor medio de unos 5cm tras comprimirla. Por tanto, la dosis media glandular es similar a la de una MD (250mrad)11–13. En la dosis influyen múltiples factores, como la densidad y el grosor de la mama, que hacen que aumente de manera significativa la dosis de radiación necesaria para la tomosíntesis13. Esta dosis, no obstante, está siempre dentro de los límites permitidos por la FDA para los estudios de imagen de la mama14.
La forma más extendida de trabajar con MD y tomosíntesis es combinando ambas técnicas. Existen diferentes secuencias de adquisición. Algunos fabricantes hacen las 2 pruebas con múltiples emisiones consecutivas de rayos X con una sola compresión (modo COMBO). Otros sistemas las hacen por separado. Por supuesto, también puede emplearse la tomosíntesis como técnica complementaria para resolver dudas generadas en la MD.
Papel de la tomosíntesisLa tomosíntesis es una técnica de imagen desarrollada a partir de la MD. Desde un principio, se han investigado los puntos fuertes de la tomosíntesis con el objetivo de establecer cuál puede ser su papel en la práctica clínica diaria o incluso su posible utilidad en un futuro escenario de cribado poblacional15. A continuación trataremos las cuestiones más relevantes de la tomosíntesis en la enfermedad mamaria.
Aumento en la tasa de detección de cáncer de mamaEl uso combinado de la MD y la tomosíntesis mejora mucho la detección del cáncer de mama16–18. Al mostrar la glándula mamaria en cortes finos, la tomosíntesis detecta cánceres ocultos dentro del parénquima mamario.
Rafferty et al.8 publicaron los resultados de un estudio retrospectivo multicéntrico en el que se evaluó la tomosíntesis combinada con la MD en 2 cohortes de más de 300 pacientes. Todos los radiólogos mejoraron significativamente su precisión diagnóstica para el cáncer de mama usando ambas técnicas. Este trabajo apoya los resultados de trabajos previos como el de Michell et al.16, en el que se demostró que combinar tomosíntesis y MD aumentaba la sensibilidad y especificidad frente al uso combinado de MD en distintas modalidades. Svahn et al.19 analizaron de manera retrospectiva a un grupo 50 pacientes con alteraciones mamográficas a las que además se les realizó una tomosíntesis. Con las 2 técnicas la precisión diagnóstica fue mayor que con 2 proyecciones mamográficas complementarias.
Estos trabajos difieren de algunos que matizan que los beneficios de la tomosíntesis puede que no sean similares en todos los supuestos. Wallis et al.20 evaluaron de manera retrospectiva el papel de la tomosíntesis como técnica combinada con la MD en 130 pacientes. Aunque combinarlas mejoró la precisión diagnóstica, esto solo fue así para los radiólogos con menos de 10 años de experiencia. Las diferencias no fueron significativas entre los radiólogos más expertos. Por tanto, parece que la experiencia previa en la lectura de mamografías puede influir en los resultados de la tomosíntesis. Para Teertstra et al.21, la tomosíntesis tampoco fue superior a la MD. Evaluaron el papel de la tomosíntesis como técnica complementaria en 513 pacientes con alteraciones en la mamografía de cribado. De los 112 cánceres detectados, tanto la tomosíntesis como las mamografías adicionales fueron negativas en 8 pacientes, por lo que no hubo diferencias significativas entre ambas.
Características de las lesiones adicionales detectadas por tomosíntesisEn gran parte de los trabajos las lesiones adicionales detectadas con tomosíntesis se clasifican en lesiones de tejidos blandos (nódulos, distorsiones y asimetrías) y lesiones calcificadas (microcalcificaciones).
Mientras que la mayoría de los estudios coinciden en que combinar tomosíntesis y mamografía identifica más lesiones de tejidos blandos, existe cierta controversia sobre las microcalcificaciones16,22–24. La capacidad de la tomosíntesis para detectar microcalcificaciones depende de factores como la dosis de radiación, el ángulo desde el que se emite cada pulso de rayos X y el algoritmo de reconstrucción utilizado. Sin embargo, aparte de detectar microcalcificaciones, otra de las utilidades de la tomosíntesis puede ser la interpretación de lesiones de este tipo que con los estudios mamográficos convencionales no sean concluyentes20,22.
Al ser la tomosíntesis una técnica tomográfica, permite evitar la superposición del tejido adyacente a una lesión. De esta manera, establece mejor los márgenes de los nódulos y permite identificar los bordes mal definidos o espiculados (fig. 1) que en la MD pueden quedar enmascarados. Asimismo, se trata de una técnica muy sensible para detectar distorsiones estructurales (fig. 2), ya que por los mismos motivos permite diferenciar las finas espículas que componen estas lesiones25,26. De este modo es posible detectar un mayor número de cánceres infiltrantes y de lesiones esclerosantes complejas-cicatrices radiales.
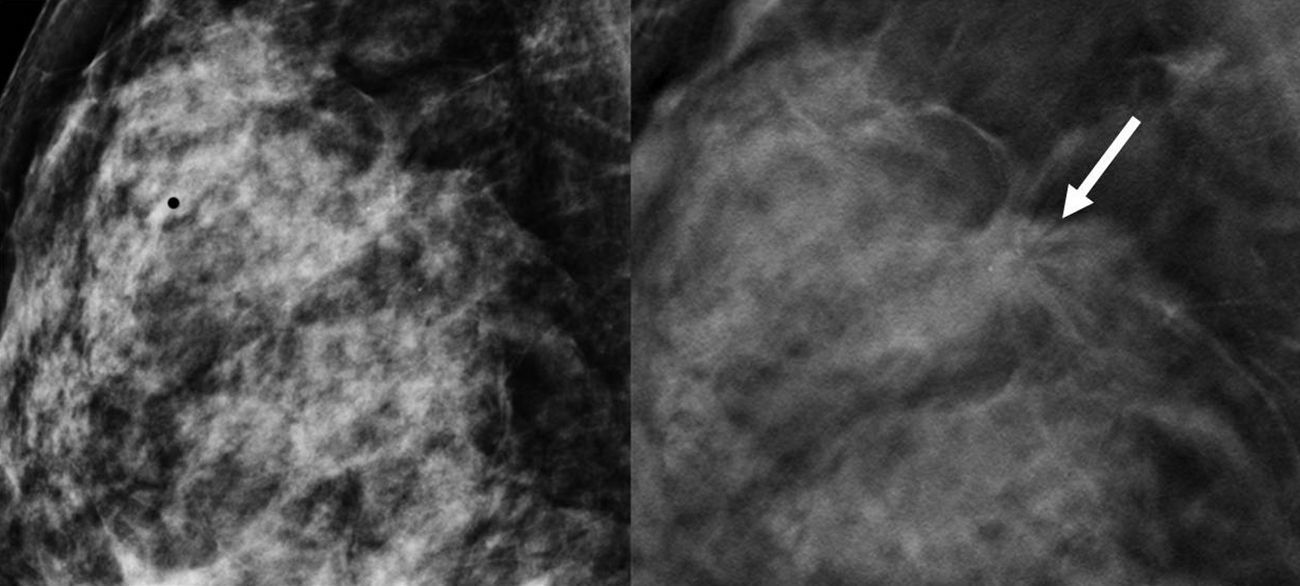
Estudio comparativo: mamografía convencional (izquierda) y tomosíntesis (derecha). Nódulo espiculado asociado a microcalcificaciones, muy sospechoso de malignidad, que no se observa en el estudio convencional de mamografía y sí en el de tomosíntesis (flecha blanca). Diagnóstico anatomopatológico: carcinoma ductal infiltrante.
Estudio comparativo: Mamografía convencional (izquierda) y tomosíntesis (derecha). Distorsión arquitectural en el cuadrante superior externo de la mama izquierda, solo identificable en tomosíntesis (flecha blanca). Diagnóstico anatomopatológico: carcinoma tubular sobre cicatriz radial.
Algunos autores han descrito una importante reducción del número de pacientes que tendrían que haber acudido nuevamente para someterse a estudios complementarios si no se hubiese usado la tomosíntesis 15. Gur et al.9 analizaron de forma retrospectiva una serie de 125 pacientes a las que se les realizaron mamografías y tomosíntesis, y demostraron una disminución de hasta el 30% en las rellamadas. Recientemente, Bernardi et al.27 realizaron un estudio prospectivo que incluyó a 158 pacientes a las que se les hizo una tomosíntesis tras ser rellamadas para realizarse estudios mamográficos de rutina. Con la ayuda de la tomosíntesis se hubiesen evitado un 74,4% de las rellamadas. Además, la tomosíntesis demostró ser más útil en pacientes con mamas densas y para estudiar correctamente lesiones no calcificadas (distorsiones, asimetrías y nódulos). Estos datos son apoyados por la mayor parte de los estudios publicados, aunque también se han descrito incrementos en la tasa de rellamadas usando ambas técnicas28.
Tomosíntesis y cribado poblacionalAl valorar la posibilidad de utilizar la tomosíntesis combinada con la mamografía para el cribado poblacional, existen muchos factores, aparte de los ya mencionados, que deben ser considerados. Son pocos los trabajos que han analizado las ventajas e inconvenientes de combinar las 2 técnicas15,27,29. Uno de los aspectos más relevantes es el aumento en el tiempo de estudio y lectura de las pruebas, porque el número de pacientes que se estudiarían diariamente es muy grande. En el estudio preliminar de Bernardi et al.29, el tiempo de la tomosíntesis y mamografía aumenta un minuto de media por paciente (un 33% más) y el de lectura el doble (unos 90s). Estos datos concuerdan con los aportados por Skaane et al.15 en el estudio prospectivo multicéntrico realizado con más de 12.000 pacientes. Sin embargo, este trabajo concluye que, combinadas, las 2 técnicas aumentan significativamente la tasa de detección de cáncer (40%), y disminuyen los falsos positivos y las rellamadas (15%). El incremento en el tiempo de realización y lectura de las pruebas debe ser valorado junto con estos beneficios. Probablemente, también se produciría una disminución de las pruebas complementarias, lo que ahorraría en recursos tanto humanos como económicos.
Limitaciones de la tomosíntesisA pesar de las ventajas descritas, la tomosíntesis no está exenta de limitaciones. En primer lugar, es esencial colocar correctamente la mama, porque, al igual que en la mamografía convencional, las lesiones no incluidas dentro del campo del detector no son visibles en el estudio. Además, para detectar la lesión, debe tener una densidad diferente a la del tejido adyacente, es decir, necesita una mínima cantidad de grasa alrededor para poder definir sus bordes. En nuestra experiencia, las lesiones rodeadas completamente por tejido glandular pueden no detectarse con tomosíntesis y sí, por ejemplo, mediante otras técnicas como la ecografía. Otro factor a tener en cuenta es que en las mamas muy densas aumenta significativamente la dosis de radiación13.
A pesar de ser una técnica de imagen sencilla de interpretar para los radiólogos de la mama, como todas las técnicas de imagen requiere una pequeña curva de aprendizaje. La fase de entrenamiento puede ser de unos 100-150 casos8,15. Sin embargo, el incremento en la precisión diagnóstica de la tomosíntesis puede ser menor en los radiólogos con mayor experiencia en la lectura de mamográfías que en los radiólogos menos expertos, lo que también debe tenerse en cuenta.
Recientemente algún estudio ha mostrado datos contradictorios sobre la tasa de rellamadas con el uso conjunto de ambas técnicas28. Esto debe analizarse cuidadosamente, teniendo en cuenta las características de las pacientes incluidas (lesiones benignas, densidad mamaria) y la experiencia en la lectura de tomosíntesis de los radiólogos participantes.
Por último, el tiempo de lectura combinando ambas técnicas es significativamente mayor que el de la mamografía aislada15,29, lo que debe ser considerado cuando se valore su implantación en los programas de cribado poblacional.
Perspectivas de futuroHasta ahora, la tomosíntesis ha sido una técnica complementaria a la mamografía a la cual no ha sustituido. Ello se debe a que la mamografía está ampliamente validada como técnica de detección precoz del cáncer de mama. Además, la mamografía convencional sigue siendo indispensable para comparar los hallazgos de una exploración con estudios previos. Sin embargo, recientemente se ha introducido un nuevo concepto como es la imagen sintetizada. Consiste en obtener la imagen de mamografía convencional sumando los datos de los diferentes cortes de tomosíntesis, conformando así una imagen 2D similar a una MD. La principal ventaja de este nuevo sistema es que reduce la dosis de radiación, porque no hacen falta las MD convencionales.
No obstante, esta prometedora técnica está aún en estudio, porque debe analizarse si la calidad de la reconstrucción bidimensional es similar a la de la MD convencional30.
También se están desarrollando sistemas que permiten adquirir MD en 2D con una dosis de radiación mucho menor a la actual que permita combinarla con la tomosíntesis con una dosis total menor. Estos equipos de nueva generación prescinden de la parrilla antidifusora y corrigen el ruido inducido por la radiación dispersa, por lo que la calidad de imagen es la misma con menor dosis.
ConclusiónEn nuestra opinión, la tomosíntesis es ya una técnica muy útil combinada con la MD. Actualmente, los esfuerzos se están centrando en disminuir la dosis de radiación utilizada en ambas técnicas. En este caso, puede tener un papel importante en el cribado poblacional, sobre todo en pacientes con mamas más densas o que presenten otros factores de riesgo.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Autoría- 1.
Responsable de la integridad del estudio: PMM, JE
- 2.
Concepción del estudio: PMM, JE
- 3.
Diseño del estudio: PMM, JE
- 4.
Obtención de los datos: PMM, JE
- 5.
Análisis e interpretación de los datos: PMM, JE
- 6.
Tratamiento estadístico: no procede
- 7.
Búsqueda bibliográfica: PMM, JE
- 8.
Redacción del trabajo: PMM, JE
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: PMM, JE
- 10.
Aprobación de la versión final: PMM, JE
Los autores declaran no tener ningún conflicto de intereses.