INTRODUCCIÓN
La hipercalcemia es un trastorno metabólico cuya prevalencia en el ámbito extrahospitalario se cifra en el 1% aproximadamente, mientras que alcanza hasta el 5% de los pacientes hospitalizados1. En éstos, las neoplasias malignas representan su origen más frecuente. Hasta el 20-30% de los pacientes oncológicos presenta en algún momento de la enfermedad una situación de hipercalcemia, siendo más frecuente en estadios avanzados2,3.
Dependiendo de los niveles de calcemia y de la velocidad de su instauración, se presenta como una entidad de tratamiento urgente, dado que llega a comprometer la vida del enfermo4. Así, las alteraciones neurológicas, cardiovasculares y renales resultantes del aumento brusco de los niveles de calcio en sangre determinan la gravedad de este cuadro. La hipercalcemia de instauración lenta o con cifras más cercanas al límite superior de la normalidad puede no detectarse por ausencia de síntomas o se manifestará a través de un patrón clínico inespecífico, no siempre fácil de reconocer, pero que afecta a múltiples órganos5,6.
El 90% de los enfermos con hipercalcemia presenta una enfermedad oncológica o un hiperparatiroidismo. La detección de esta alteración metabólica en un paciente con cáncer conlleva un mal pronóstico, hasta el punto de que la mitad de ellos fallecen en los siguientes 30 días2,6.
CONCEPTO
Definiremos hipercalcemia como el aumento de los niveles de calcio en sangre por encima de 10,5 mg/dl (rango normal entre 8,5-10,5)7. Solo el 45% del calcio sérico se encuentra en forma iónica o activa (calcio iónico), mientras que el 55% restante se presenta unido a otras sustancias, fundamentalmente proteínas y en menor medida fosfato. De esta manera, cualquier alteración en la concentración de las proteínas plasmáticas puede condicionar una cifra inexacta de calcio. Para evitar esto, conviene aplicar la siguiente fórmula:
Ca corregido = Ca sérico + 0,8 (4 - albúmina en sangre)7
Si existe la posibilidad de la determinación de calcio iónico, se definirá hipercalcemia como aquellos valores por encima de 1,35 mmol/l. La hipercalcemia per se puede cursar de manera asintomática cuando las cifras no sobrepasen los 13 mg/dl, o cuando su velocidad de instauración sea lenta. Por este motivo, y con una finalidad práctica, haremos la distinción entre hipercalcemia leve (10,5-12,5 mg/dl), moderada (12,5-14,5 mg/dl) y grave (> 14,5 mg/dl)7.
En los casos de hipercalcemia grave algunos autores hablan de crisis hipercalcémica, siendo sintomáticas y representando una urgencia médica4. Esta situación es frecuentemente la forma de presentación de la hipercalcemia asociada a neoplasia maligna, mientras que el hiperparatiroidismo se caracteriza por cifras menos elevadas de calcemia y de instauración más lenta6,7.
ETIOLOGÍA
Como se expuso previamente, el 90% de los casos de hipercalcemia tiene su origen en el cáncer y en el hiperparatiroidismo. En el primer caso, el mecanismo mediador es independiente de la hormona paratiroidea (PTH), mientras que en el segundo la calcemia sigue un estímulo directo de la PTH8.
Dentro de las neoplasias malignas, el cáncer de pulmón, el de mama y el mieloma múltiple son las causas más frecuentes de hipercalcemia tumoral. Otras causas de hipercalcemia maligna son los linfomas y las leucemias, aunque con menor frecuencia que los previamente descritos. Tan sólo en el 4% de las hipercalcemias asociadas a malignidad el tumor es de origen desconocido9.
El resto de causas de hipercalcemia se describe detalladamente en la tabla 1.
MECANISMOS FISIOPATOLÓGICOS DE LA HIPERCALCEMIA TUMORAL
1. Hipercalcemia por osteolisis. Representa el 20% de los casos. La invasión del hueso por las células tumorales activa un proceso de osteolisis mediado por sustancias como las citoquinas, el factor de necrosis tumoral (TNF) y la proteína relacionada con la parathormona (PTH-rP). Este mecanismo mediado por esta proteína parece el factor predominante en las metástasis óseas del cáncer de mama8,10,11. Dentro de este subgrupo, pero a través de un complejo sistema regulador de los osteoclastos, denominado osteoprotegerina-ligando del receptor activador del factor nuclear kB (RANKL), se explica el fenómeno de la hipercalcemia en el mieloma múltiple11,12.
2. Hipercalcemia humoral. Es el mecanismo más frecuente de la hipercalcemia asociada a neoplasia (80%). La secreción de PTH-rP, citada con anterioridad, se describe como la razón fundamental por la que tumores como el cáncer de esófago, el cáncer epidermoide pulmonar, el hipernefroma y el linfoma no-Hodgkin presentan hipercalcemia. En estos tumores el fenómeno osteolítico es raro, y, por tanto, las metástasis óseas. Los pacientes con hipercalcemia mediada por la PTH-rP suelen presentar una enfermedad más avanzada y consecuentemente peor pronóstico8. La medición de esta proteína es de utilidad no sólo en su diagnóstico, sino como marcador de respuesta terapéutica al tratamiento oncológico y al tratamiento hipocalcemiante con bifosfonatos.
3. Hipercalcemia por secreción de calcitriol (1,25 dihidroxivitamina D). Es un mecanismo menos frecuente (< 1%), pero explica la hipercalcemia asociada a la mayoría de los linfomas. También se relaciona con el fenómeno asociado a ciertas granulomatosis como la sarcoidosis8,13,14. Desde un punto de vista terapéutico, la hipercalcemia mediada por calcitriol es más sensible al tratamiento con glucocorticoides.
4. Hipercalcemia por secreción ectópica de PTH. También rara; se relaciona con tumores ováricos, algunos subtipos pulmonares, rabdomiosarcomas y neoplasias pancreáticas8.
Existe una relación recíproca entre el hiperparatiroidismo primario y el cáncer, por lo que la determinación de PTH y PTH-rP puede contribuir al diagnóstico de una u otra causa de hipercalcemia, o a la coexistencia de ambas8.
PRESENTACIÓN CLÍNICA DE LA HIPERCALCEMIA COMO URGENCIA
Como se ha descrito anteriormente, las manifestaciones clínicas de la hipercalcemia van a depender de los niveles de calcio en sangre y de la rapidez de su ascenso1,15. Así, en el caso del hiperparatiroidismo donde se produce un incremento de calcio durante un largo período y, generalmente, sin alcanzar cifras mayores de 13 mg/dl, los pacientes pueden presentarse de manera asintomática o mostrar alteraciones leves o inespecíficas como náuseas, falta de concentración, poliuria-polidipsia y cierto grado de astenia. En el caso del hiperparatiroidismo se encontrarán nefrocalcinosis y osteítis fibrosa quística como datos sugerentes para su diagnóstico.
Pero en el caso de la hipercalcemia grave (> 14,5 mg/dl), la disfunción del sistema nervioso central o las alteraciones cardiovasculares se manifiestan de tal forma que son, junto con el fracaso renal, las principales causas de mortalidad en estos pacientes. En estas situaciones, la hipercalcemia representa una verdadera urgencia médica, obligando a la instauración de medidas correctoras inmediatas para la restauración de la homeostasis y, así, el correcto funcionamiento de estos órganos.
El paciente con una crisis hipercalcémica, que como se ha ido desarrollando suele corresponder a un enfermo oncológico, es un paciente deshidratado por definición. Presenta un deterioro más o menos brusco del nivel de conciencia, pudiendo desarrollar un cuadro de coma en un breve plazo de tiempo. Desde un punto de vista cardiovascular, las alteraciones más comunes son la elevación de las cifras de presión arterial y un característico acortamiento del intervalo QT en el registro electrocardiográfico16. Se ha descrito la aparición de la onda J, no patognomónica, puesto que se relaciona también con la hipotermia (onda J de Osborn)17. Estas alteraciones pueden desembocar en taquiarritmias y parada cardíaca. Debemos resaltar que en situaciones de hipercalcemia, los pacientes en tratamiento con digoxina pueden ver incrementados sus niveles en sangre y contribuir a la sintomatología gastrointestinal y cardiovascular16.
Finalmente, la depleción de volumen y la insuficiencia renal aguda se presentan como parte de este síndrome hipercalcémico, cuyas consecuencias sobre la homeostasis iónica y el equilibrio ácido-base pueden complicar aún más el cuadro (hiperpotasemia, acidosis metabólica).
MEDIDAS TERAPÉUTICAS DE APLICACIÓN URGENTE
FLUIDOTERAPIA
La deshidratación presente en el enfermo con hipercalcemia aguda obliga a una restauración hídrica intensiva y precoz con el fin de aumentar el volumen de filtrado glomerular e inducir la excreción de calcio o calciuresis. La resucitación volumétrica en estos pacientes se ha de realizar con suero salino isotónico (0,9%), a un ritmo de perfusión entre 200-500 ml/h, siempre atendiendo a la tolerabilidad hemodinámica del individuo18. En definitiva, el objetivo es administrar entre 4.000-5.000 cc de suero salino en las primeras 24 h y conseguir un ritmo de diuresis en torno a 100 ml/h18-20.
DIURÉTICOS DE ASA (FUROSEMIDA)
La utilización de diuréticos antes de conseguir el pleno restablecimiento del filtrado glomerular puede incrementar la depleción de volumen, aumentar la reabsorción de calcio a nivel renal y perpetuar la situación de hipercalcemia. Por este motivo existe controversia sobre la utilización de furosemida a dosis bajas (10-20 mg por vía intravenosa) como inductor de calciuresis. Algunos autores proponen reservar su uso a situaciones en las que la expansión de volumen haya sobrepasado la tolerancia hemodinámica del enfermo y exista, por tanto, una sobrecarga hídrica19,20.
GLUCOCORTICOIDES
La utilización de prednisona e hidrocortisona en el síndrome hipercalcémico debe formar parte de la terapia en situaciones muy concretas7,9,21. Se emplean con cierta eficacia en las hipercalcemias inducidas por calcitriol, como las asociadas a linfomas. También tienen un papel terapéutico en la hipercalcemia asociada a la sarcoidosis13,14. No se consideran de acción hipocalcemiante rápida, y en los casos en que se emplee calcitonina en el tratamiento pueden ayudar a retrasar la taquifilaxia asociada a ésta.
BIFOSFONATOS
En la actualidad son considerados como los agentes terapéuticos más rápidos y seguros en el tratamiento de la hipercalcemia grave, particularmente en la inducida por PTH-rP22,23. Actúan como potentes inhibidores de la resorción ósea, impidiendo así la liberación de calcio desde el hueso. Pueden llegar a conseguir niveles normales de calcio en las primeras 48 h mediante la administración intravenosa. Pueden, incluso, tener beneficios sobre la recidiva de crisis hipercalcémicas e interferir en la génesis de las metástasis óseas de algunos tumores20, no así sobre la supervivencia de estos pacientes. De los bifosfonatos con utilidad en el tratamiento urgente del síndrome hipercalcémico agudo destacan el pamidronato y el ácido zolendroico, por su disponibilidad por vía endovenosa y mayor experiencia en su empleo23,24. Clodronato e ibandronato tienen propiedades similares con menos análisis comparativos en cuanto a su eficacia en este contexto. Entre los resultados publicados al respecto, existe evidencia de la superioridad de zolendronato sobre pamidronato, en cuanto a la eficacia y rapidez para lograr normocalcemia y en el mantenimiento de ésta23,25.
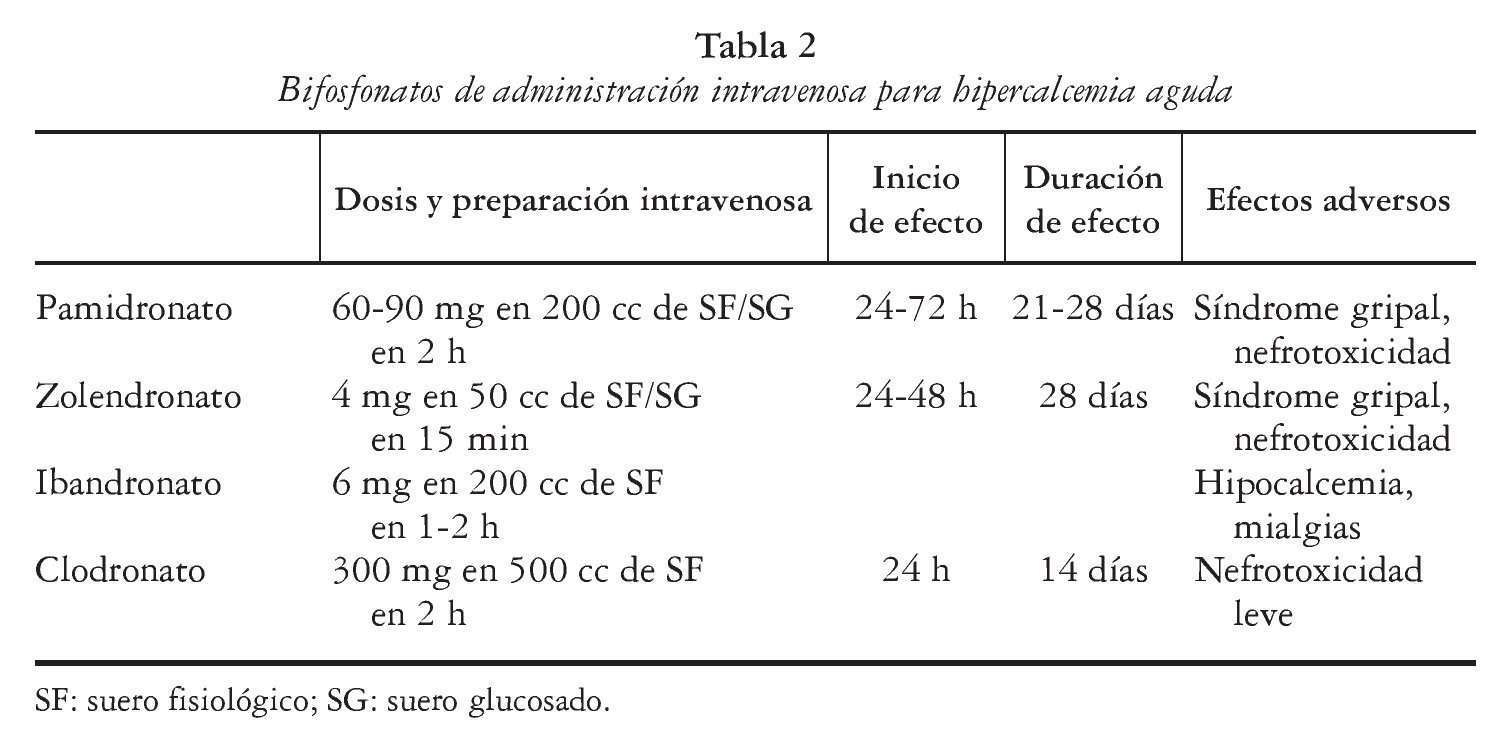
Asimismo, zolendronato se puede perfundir en 15 minutos, lo que implica una mayor agilidad terapéutica24. En los casos de insuficiencia renal con niveles de creatinina > 3 mg/dl o aclaramientos < 30 ml/min se desaconseja el uso de zolendronato26. Como alternativa, se debe intentar corregir la cifra de creatinina con una intensa reposición hídrica o disminuir la dosis a perfundir26,27. Con respecto a pamidronato, se considera seguro en los pacientes con fracaso renal e hipercalcemia como puente a la diálisis23. Ibandronato no se ha estudiado suficientemente en el tratamiento de crisis hipercalcémicas y deterioro de la función renal, aunque algunos trabajos lo presentan con una nefrotoxicidad similar a placebo27. Las dosis y la posología de los bifosfonatos utilizados por vía intravenosa se exponen en la tabla 2.
Sus principales efectos adversos son la nefrotoxicidad y la osteonecrosis mandibular. Pueden agravar la insuficiencia renal, sobre todo en tratamientos repetidos en un corto plazo de tiempo, en pacientes con tratamientos citostáticos que contribuyen al deterioro renal y en pacientes de edad avanzada27. La mayoría de los pacientes a los que se les administra tratamiento con bifosfonatos puede exhibir un cuadro pseudogripal en las horas posteriores a su administración, de fácil control con paracetamol27.
NITRATO DE GALIO
Actualmente no es una terapia cotidiana en el tratamiento de este síndrome, pero existen ensayos que han demostrado mayor eficacia que la calcitonina y que el etidronato26,28. Se ha utilizado sobre todo en hipercalcemias asociadas a tumores de estirpe epidermoide. Dosis: 200 mg/m2/día, infusión intravenosa durante 5 días29.
DIÁLISIS
Debe plantearse como tratamiento urgente en hipercalcemias > 18 mg/dl, en aquellas cuya función renal contraindique el uso de bifosfonatos, o en pacientes con sobrecarga hemodinámica en los que no se pueda realizar la reposición de fluidos necesaria o exista oligoanuria refractaria20,23.
CALCITONINA
Acción menos potente que los bifosfonatos, aunque tiene su utilidad al inicio del tratamiento hasta conseguir el efecto de éstos. Su acción es breve debido a taquifilaxia9,23. Este efecto puede disminuirse con el uso concomitante de glucocorticoides. Dosis: 4-8 UI/kg/6-12 h por vía intramuscular o subcutánea.
MITRAMICINA
Se considera en desuso por su elevado número de efectos indeseables7.
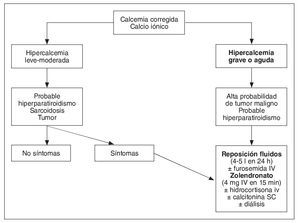
En el paciente con hipercalcemia grave y/o aguda, estos son los tratamientos de aplicación precoz para minimizar los riesgos que conlleva este desorden iónico. El flujo de actuación se detalla a modo de algoritmo en la figura 1.
Fig. 1. Algoritmo diagnóstico-terapéutico de la hipercalcemia. SC: por vía subcutánea; IV: por vía intravenosa.
Los pacientes con neoplasia maligna subyacente precisan de un tratamiento dirigido a su tumor que contribuya a disminuir las posibilidades de desarrollar una hipercalcemia durante su enfermedad. De la misma forma, la paratiroidectomía será el tratamiento principal cuando la etiología sea la hiperproducción de PTH.
Próximamente se conocerán nuevas moléculas que interfieran en los mecanismos fisiopatológicos descritos con anterioridad, dirigidas a bloquear la acción osteoclástica de citoquinas, la osteoprotegerina-RANKL, los inhibidores de la tirosina kinasa (sunitinib)30,31, los anticuerpos monoclonales anti-PTH-rP, que permitirán tratamientos más dirigidos al biometabolismo óseo.
CONCLUSIONES
La hipercalcemia de instauración aguda o con cifras mayores de 14 mg/dl representa una situación clínica urgente por su afectación cardíaca, neurológica y renal, que puede llevar a la muerte del paciente. Se reconoce con dificultad a tenor de la sintomatología inespecífica que generalmente presenta, pero el diagnóstico se establece fácilmente con la determinación en sangre del calcio y las proteínas, o bien el calcio iónico. La intensiva fluidoterapia y los bifosfonatos forman los pilares básicos de su tratamiento, consiguiendo restaurar la homeostasis iónica precozmente y yugulando las complicaciones fatales. El conocimiento de los mecanismos que alteran el metabolismo del calcio es básico para utilizar las distintas herramientas terapéuticas actualmente disponibles.
Los continuos avances en la investigación sobre la biología del osteoclasto y su implicación clínica permitirán, en un corto plazo de tiempo, nuevas terapias que impidan no sólo la aparición de esta alteración metabólica, sino la invasión ósea relacionada con los tumores malignos.
Correspondencia: J.A. Nuevo-González. Servicio de Urgencias.
Hospital General Universitario Gregorio Marañón.
C/ Dr. Esquerdo, 46.
28007 Madrid. España.
Correo electrónico:
januevo.hgugm@salud.madrid.org