Introducción
La prescripción por principio activo (PPA) o prescripción por denominación oficial española (DOE) es una estrategia adoptada por los Servicios de Salud de las Comunidades Autónomas para contribuir al uso racional de los medicamentos.
Con carácter previo es preciso indicar que la PPA no conforma un fin en sí misma, sino que es un elemento más de una estrategia global sobre la prestación farmacéutica, planteada a medio y largo plazo, con la que deben ser coherentes y concordantes el resto de las iniciativas adoptadas en este ámbito de gestión.
En este sentido cabe manifestar que no se trata de una medida de implantación inmediata, sino que se adopta cuando se cumplen todos y cada uno de los requisitos que se consideran necesarios antes de iniciar el proyecto: sistema de información, prescripción informatizada y porcentaje relevante de utilización de genéricos.
Por ello, el objetivo de este artículo es proporcionar una visión general de la situación de partida y de las diferentes etapas que ha sido necesario cubrir para llegar al momento actual, en que la PPA ya está implantada y se ha podido hacer el seguimiento y evaluación de la medida.
Para hacer patentes todos estos aspectos se hará referencia a la propuesta europea, la situación en España, la estrategia de implantación en Castilla y León y finalmente algunos resultados y conclusiones de todo el proceso.
Propuesta europea
Antes de entrar en actuaciones a nivel nacional es interesante destacar una propuesta del colectivo "Europa y Medicamento", en el que participan diversas instituciones europeas, que ha sido difundida por la revista Prescrire y que puede ayudar a valorar los objetivos esenciales de esta iniciativa (tabla 1).
En cuanto a la realidad de esta iniciativa hay que indicar que se está prescribiendo por DOE en países de nuestro entorno socioeconómico como Reino Unido, Francia o Estados Unidos, sin que esta modalidad de prescripción introduzca distorsiones en el conjunto de la cadena del medicamento y de la asistencia sanitaria.
Además, unas cifras recientes publicadas por la Office of Health Economics del Reino Unido, sobre las modalidades de prescripción y dispensación y sus costes, recogían unos datos que figuran en la tabla 2, según los cuales existía una importante diferencia de coste por envase, y por tanto, en su impacto económico.
Situación de la prescripción por principio activo en el Sistema Nacional de Salud
Teniendo en cuenta que se está prescribiendo por PA en muchos de los países desarrollados, como medida para promover el uso de genéricos y ser más eficientes con respecto a la prestación farmacéutica, parece lógico que en el Sistema Nacional de Salud (SNS) de España constituya una iniciativa que tenga un amplio recorrido en aquellas Comunidades Autónomas (CCAA) en las que sea posible su implantación. A efectos informativos es obligado indicar que la prescripción de genéricos en envases en el SNS ya se encontraba en el 20,9% en enero de 2008, y cuenta con un amplio margen de mejora que podría suponer en torno a un 25% adicional.
De hecho, en Andalucía el despegue de los genéricos se ha producido desde la implantación de la PPA en septiembre de 2001,lo que ha significado una desaceleración del crecimiento del gasto farmacéutico, especialmente del gasto medio por receta, en comparación con el resto de las CCAA.
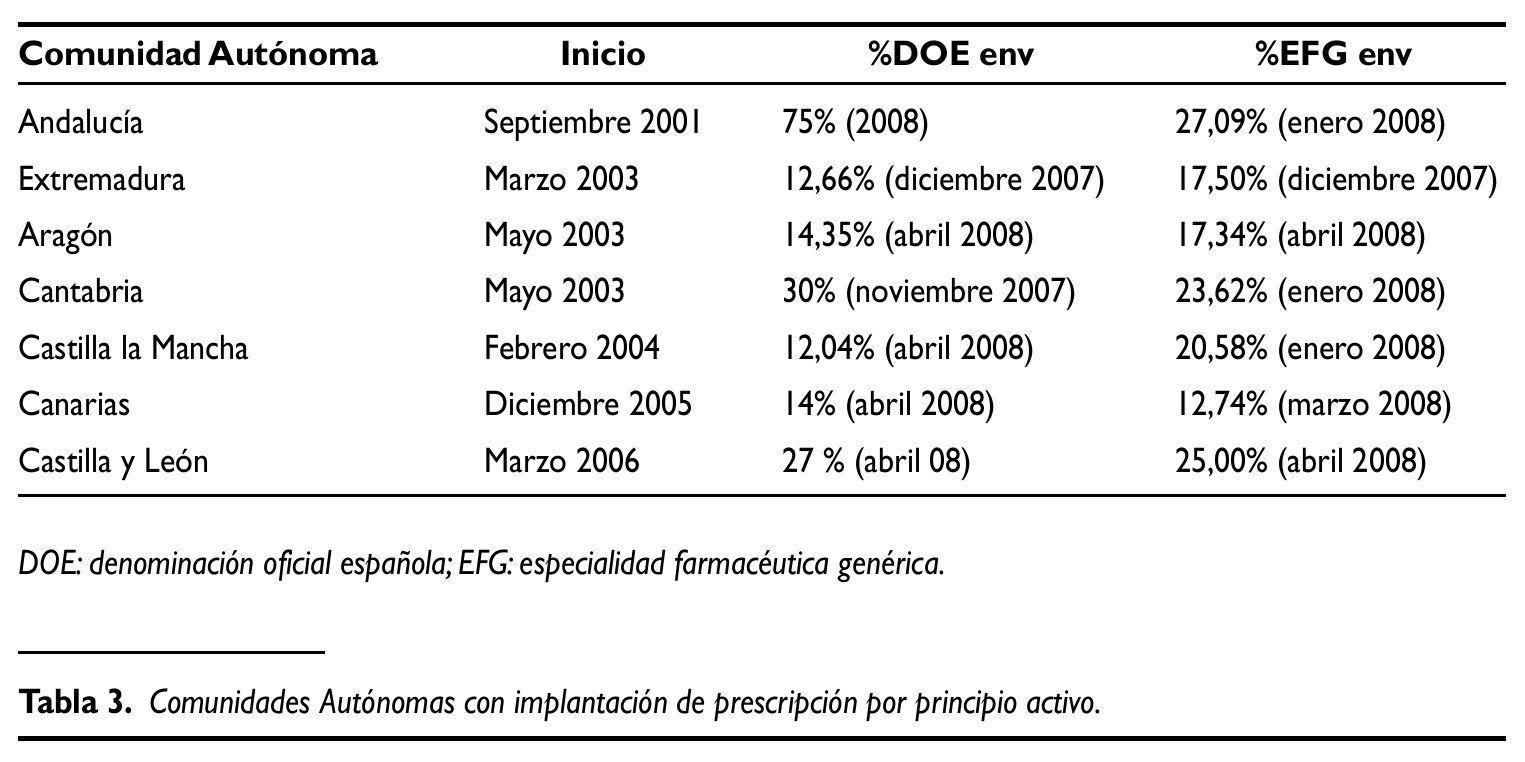
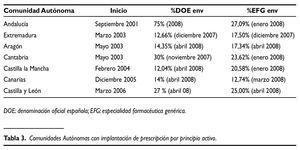
En la tabla 3 figuran las CCAA que tienen recogido en su concierto algún aspecto relacionado con la PPA y su fecha de inicio de aplicación.
De todas ellas las que más han avanzado en los mecanismos de aplicación son Andalucía, Castilla y León, Cantabria, Castilla la Mancha y Aragón. Los resultados mejor evaluados son los de Andalucía, en que la PPA supera el 75%.
Solamente indicaremos que los sistemas acordados son similares, y las diferencias más relevantes se producen con respecto a la extensión del volumen de conjuntos de productos para los que se fijan precios menores, que puede ser para la práctica totalidad de productos y presentaciones o solamente para aquellos conjuntos de productos que cuenten con genérico en el mercado.
Las ventajas de la prescripción por principio activo en el Sistema Nacional de Salud
Las ventajas más importantes detectadas,tanto desde el punto de vista de profesionales y pacientes como de la gestión son las siguientes:
1. Facilita y da homogeneidad a la búsqueda e identificación del PA elegido en los sistemas de prescripción informatizada, accediendo a todas las presentaciones y posibilidades de prescripción (dosis, forma farmacéutica, etc.), por lo que no es necesario recordar los 17 o 20 nombres comerciales existentes para algunos productos. Actualmente (mayo de 2008) existen en el mercado y financiadas 11.124 presentaciones para
1.197 PA. Incluso para omeprazol 20 mg, 28 cápsulas existen 74 presentaciones en alta.
2. Utiliza un lenguaje internacional y común en Atención Primaria (AP), Atención Especializada (AE),en la Oficina de Farmacia y con los pacientes.
3. Hace posible los acuerdos de precios menores con Colegios Oficiales de Farmacéuticos, estableciendo las condiciones de dispensación y facturación. Además, la actualización de precios menores en las órdenes ministeriales de precios de referencia proporcionan un sistema equivalente a la revisión o implantación de dichos precios para todos los productos afectados por esta modalidad de prescripción.
4. Promueve el uso de especialidades farmacéuticas genéricas (EFG) debido a la obligación de dispensar este tipo de medicamentos cuando existan en el mercado, tal como establecen los artículos 85, 86 y 93 de la Ley 29/2006, de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios.
5. Facilita el cumplimiento de objetivos de Plan Anual de Gestión o contratos de Gestión, entre los que se encuentran el porcentaje de genéricos y el cumplimiento presupuestario.
6. Mejora la eficiencia,manteniendo la calidad de la Prestación Farmacéutica, con una moderada evolución del precio medio por envase. Por tanto, reduce el gasto para ciudadanos (en el caso de que efectúen aportación económica) y CCAA, resultando una menor presión sobre el conjunto del Sistema Sanitario y liberando fondos para financiar las innovaciones.
Posición de la industria farmacéutica
La industria farmacéutica se opone a esta iniciativa, basándose en problemas relacionados con la atención al paciente debido a los posibles cambios en las dispensaciones a través del tiempo para pacientes crónicos. Sin embargo, sorprende que no se oponga a las situaciones en las que se permite de forma continuada la sustitución de los genéricos entre sí, aunque hayan sido identificados con el nombre del laboratorio titular en la prescripción.
Sin embargo, hay que precisar que en el caso de PPA no hay sustitución, sino que se elige el medicamento dispensado y se promueve la dispensación de un genérico si existe. De esta forma, el farmacéutico gestiona el 80% de su stock de genéricos con dos o tres laboratorios que mantienen un adecuado suministro, y los pacientes crónicos reciben siempre el mismo producto, garantizando la continuidad y la atención adecuada.
Por ello, ante esta aparente incoherencia, parece más probable que en la oposición a la PPA exista además un componente de estrategia de mercado en dos sentidos: a) el primero de ellos sería la protección de las marcas y de la promoción que se realiza de las mismas a través de la visita médica. Ante ello, habría laboratorios que tendrían que plantearse cambiar su estrategia comercial, frente a lo que ofrecen ciertas resistencias; b) el segundo de los motivos se podría encontrar en el papel de las licencias concedidas por los laboratorios innovadores a aquellos que aportan su capacidad de introducción de nuevos medicamentos mediante sus fuerzas de ventas. Pero con la PPA no es posible valorar la proporción de la dispensación que corresponde a la actividad promocional de cada una de las compañías farmacéuticas, ni las cuantías que debe abonar el laboratorio que obtiene la licencia al innovador. Por tanto, en cierta medida se limita este tipo de estrategia, ventajosa para ambas partes.
Sin embargo, también hay que considerar que esta última situación se plantea cuando la PPA se realiza en una elevada proporción de productos para los que no hay genérico en el mercado, pero se minimiza cuando se centra en el mercado de genéricos.
Por otra parte, el editor de la revista Prescribe contesta en cierta medida a estas críticas, afirmando que los límites a la utilización de la DCI o DOE son raros, y los problemas en general son falsos problemas y están ligados a malas voluntades.
En estas circunstancias se considera que la mejor forma de avanzar en el ámbito de la prestación farmacéutica es el respeto mutuo hacia las nuevas iniciativas, y pensar que se trata de un entorno globalizado en el que hay que aprender de las tendencias y resultados internacionales, y tomar medidas que permitan avanzar en la utilización racional de los recursos y en la sostenibilidad de los sistemas sanitarios.
Estrategia y desarrollos en Castilla y León
Como se ha indicado anteriormente la adopción efectiva de este tipo de medidas sólo se puede realizar si se cumplen determinadas condiciones y se cuenta con el desarrollo de unos recursos que son imprescindibles para su implantación, seguimiento y evaluación en los diferentes niveles de la organización. Entre los recursos y condiciones necesarias se encuentran los siguientes:
Sistema de información
Es un sistema que consta de varios módulos integrados e interrelacionados entre sí, lo que permite una mejor explotación de todas las utilidades que presenta, destacando las siguientes:
1. Establecer estrategias que orientan la mejora de la prescripción: las actuaciones sobre la base de datos de medicamentos que posteriormente se detallan permiten la organización de los productos para facilitar su prescripción, así como el seguimiento y explotación de consumo, facturación y sistemas de evaluación.
2. Estudiar modelos de impacto para unos determinados objetivos y resultados: se puede hacer estudios sobre el impacto previsto de las reducciones de precios en las CCAA, sistema de precios de referencia, cambio de márgenes o la consecución de determinados objetivos.
3. Efectuar el seguimiento y evaluación de los objetivos establecidos en los Planes Anuales de Gestión, como la PPA, así como valorar el nivel de implantación en cada ámbito de gestión.
Base de datos de medicamentos
Para el desarrollo de la PPA el elemento esencial es la organización y estructura de la base de datos de productos farmacéuticos.
Esta base de datos se obtiene a partir de varios ficheros, no homogéneos, que envía mensualmente el Ministerio de Sanidad y Consumo y que se someten a un proceso mediante el cual se completan y homogeneizan los contenidos. Esta información se agrega en un fichero único y se incorporan datos como las dosis diarias definidas (DDD), necesidad de visado, el número máximo de envases que se pueden prescribir o la posibilidad o no de sustitución. Pero para implantar la prescripción DOE se requiere:
1. La creación de los "conjuntos de PA" que comprenden los medicamentos con igual composición, dosis, forma farmacéutica, vía de administración y número de unidades de dosificación, con el fin de agrupar y ordenar la búsqueda y selección para la prescripción y establecer precios menores para cada conjunto.
2. La codificación de cada conjunto de PA, asignando un código de 6 dígitos que se incorpora a la receta y se imprime en formato PDF, lo que permite su captación por métodos ópticos en el proceso de facturación. De esta forma se puede comprobar automatizadamente que el producto dispensado se corresponde con el prescrito, evitando dispensaciones y/o sustituciones inadecuadas.
3. La codificación de los principios activos según la clasificación ATC, adaptada para un mejor manejo por el médico, para permitir otra alternativa de búsqueda y selección: subgrupo terapéutico o principio activo.
4. Identificación y diferenciación de los principios activos que presentan limitaciones para ser sustituidos, bien por estrecho rango terapéutico o por otros motivos, informando al médico de esta limitación para que elija la marca que desea prescribir. Estos principios activos están excluidos del sistema de precios menores.
5. Incorporación de un sistema para determinar de nivel de eficiencia en cada uno de los conjuntos de PA, permitiendo estimar el gasto evitable en cada nivel asistencial.
Sistema de gestión de historia clínica en Atención Primaria
Con este trabajo previo en la base de datos de productos farmacéuticos se ha desarrollado un módulo de prescripción en el nuevo sistema de gestión clínica de AP (MEDORACYL), que incorpora gran parte de las utilidades previstas y que ampliará los elementos de ayuda a la prescripción en próximas versiones, dotándolos de contenido clínico.
El objetivo esencial de este módulo es garantizar la calidad y la eficiencia de la prestación farmacéutica y sentar las bases de la receta electrónica.
Para ello se proporcionan herramientas de ayuda a la búsqueda y selección de medicamentos, productos sanitarios y dietoterápicos, con la finalidad esencial de que el médico cuente con un elemento de apoyo que agilice el procedimiento de prescripción, tanto en procesos agudos como crónicos.
Acuerdo de precios menores
A pesar de que la promoción de la PPA era una demanda reiterada por parte de médicos y farmacéuticos, se consideró que se debía asociar a la disponibilidad de un sistema de información que permitiera generar y mantener de forma automatizada los diferentes procesos que se requieren, alcanzar un nivel de prescripción de genéricos relevante y contar con un módulo de prescripción asistida por ordenador que facilitase la selección del PA. Por ello, una vez cumplidas estas condiciones se inició el trabajo para acordar un sistema de precios menores, cuyos aspectos más importantes son los referidos a condiciones de dispensación, facturación y estrategias de implantación.
Para esta tarea se ha contado con la experiencia y ayuda del resto de las CCAA que ya lo habían implantado, lo que ha permitido trabajar con una mayor agilidad y fiabilidad en los contenidos y en los resultados.
Contenido del acuerdo y condiciones de dispensación
Tanto en el año 2007 como en 2008 se toma como referencia para establecer los precios menores el anejo 5 de las correspondientes órdenes de precios de referencia (Orden 3997/2006, de 28 de diciembre y Orden 3867/2007, de 27 de diciembre),sometiéndose posteriormente a un proceso de revisión, en el que se tiene en cuenta la disponibilidad en el mercado de las presentaciones con precio menor y la estructura y agrupación de presentaciones en conjuntos de igual dosis y forma farmacéutica.
Actualmente afecta a 744 conjuntos de PA y a 122 PA con consumo relevante, para los que existe genérico en el mercado. Afecta a 7.015 presentaciones, que representan el 63% de las financiadas en alta, y suponen el 45% del consumo en envases. Como se citó anteriormente los conjuntos corresponden a medicamentos con igual composición, dosis, forma farmacéutica, vía de administración y unidades de dosificación.
Para cada uno de los conjuntos se establece un precio menor y, con carácter general, por debajo del mismo existirá, al menos, un genérico.
A efectos de la dispensación se aplica el contenido de los artículos 85,86 y 93 de la Ley 29/2006,de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios, de forma que cuando se prescriba por PA se dispensará una EFG si existe en el mercado y, si no, una marca. No obstante, se podrán dispensar especialidades con precio inferior o superior al menor establecido, actuando en tal caso como sigue:
- En el caso de que el producto dispensado se encuentre por debajo del precio menor, al paciente se le cobrará la aportación que corresponda al precio de venta al público (PVP) y se facturará a ese precio.
- Si el PVP del producto dispensado se encuentra por encima del precio máximo se cobrará la aportación sobre el precio máximo y se facturará también a dicho precio.
Asimismo se establece la recomendación de mantener la dispensación del mismo producto en pacientes crónicos y si es preciso efectuar un cambio se informará al paciente.
Facturación
Las recetas prescritas por PA se facturarán en grupo aparte con el fin de hacer un seguimiento y valoración de las mismas.
Está prevista la evaluación mensual de incidencias, como desabastecimientos o conjuntos en que quedan menos de dos especialidades con precio igual o inferior al máximo.
Se había previsto una revisión anual, salvo el primer año que se realizó una revisión semestral, debido a la necesidad de incorporar las reducciones voluntarias de precios, aplicadas el 1 de marzo de 2006, y para efectuar aquellas correcciones o ajustes del sistema que se considerasen necesarias.
No obstante, la actualización de los Anejos 5 de las órdenes de precios de referencia son las que están estableciendo la pauta de las revisiones.
La implantación para profesionales, pacientes e industria
Para los médicos
Uno de los mensajes transmitidos a los médicos trataba de promover preferentemente la PPA en aquellos medicamentos en los que había genérico en el mercado, y se considera que lo han entendido de forma acertada. De esta manera con un único esfuerzo se valoran los objetivos doblemente: como PPA en la prescripción y como genérico en la dispensación.
Para apoyar toda la estrategia se ha informado a los profesionales a través de un boletín (Ojo de Markov), a través de los farmacéuticos de AP de cada Área, e incluso en el Boletín de Farmacovigilancia de la CA.
La PPA se recoge como una opción preferente en el módulo de prescripción informatizada.
Para los farmacéuticos
La condición de que la PPA implica la dispensación de EFG cuando existe en el mercado, conlleva que en la actualidad (mayo 2008) los mensajes y la situación sean los siguientes:
- No hay sustitución, sino elección del genérico a dispensar. Esta situación es conocida y aceptada por el médico, el paciente y el farmacéutico.
- El farmacéutico gestiona el stock del 80% de los genéricos que dispensa, puesto que esa es la proporción de EFG prescritas como PA.
- La mejora de la gestión del stock de genéricos con un número reducido de laboratorios permite fidelizar a los pacientes crónicos y mantener la dispensación del mismo medicamento a dichos pacientes.
Para los pacientes
Se ha llevado a cabo una labor de información para los pacientes acerca de esta modalidad de prescripción dentro de la Campaña de Uso Racional de los Medicamentos en noviembre de 2005,y mediante una campaña específica sobre PPA o prescripción DOE y su significado en diciembre de 2007.
Para la industria
Según los objetivos y la estrategia adoptada se promueve la PPA en los medicamentos para los que existe genérico en el mercado, se mantiene el respeto a los medicamentos prescritos por marca comercial y no se permite la sustitución, salvo situaciones de urgencia o desabastecimiento.
Por ello, este modelo de actuación no tiene impacto o es mínimo para compañías innovadoras que promueven la utilización de sus marcas, y tampoco debería afectar a los sistemas de licencias, luego no debería existir motivo de preocupación para las compañías farmacéuticas porque no se produce distorsión del mercado para las condiciones de PPA descritas en este documento.
Impacto estimado
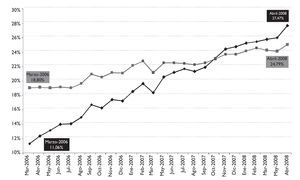
Considerando que el porcentaje de utilización de genéricos de partida (marzo 2006) era de un 18,8% en envases, esta circunstancia permitía avanzar inicialmente de forma rápida sin cambiar sustancialmente los hábitos de prescripción, solamente si se convertía la prescripción de genéricos en DOE.
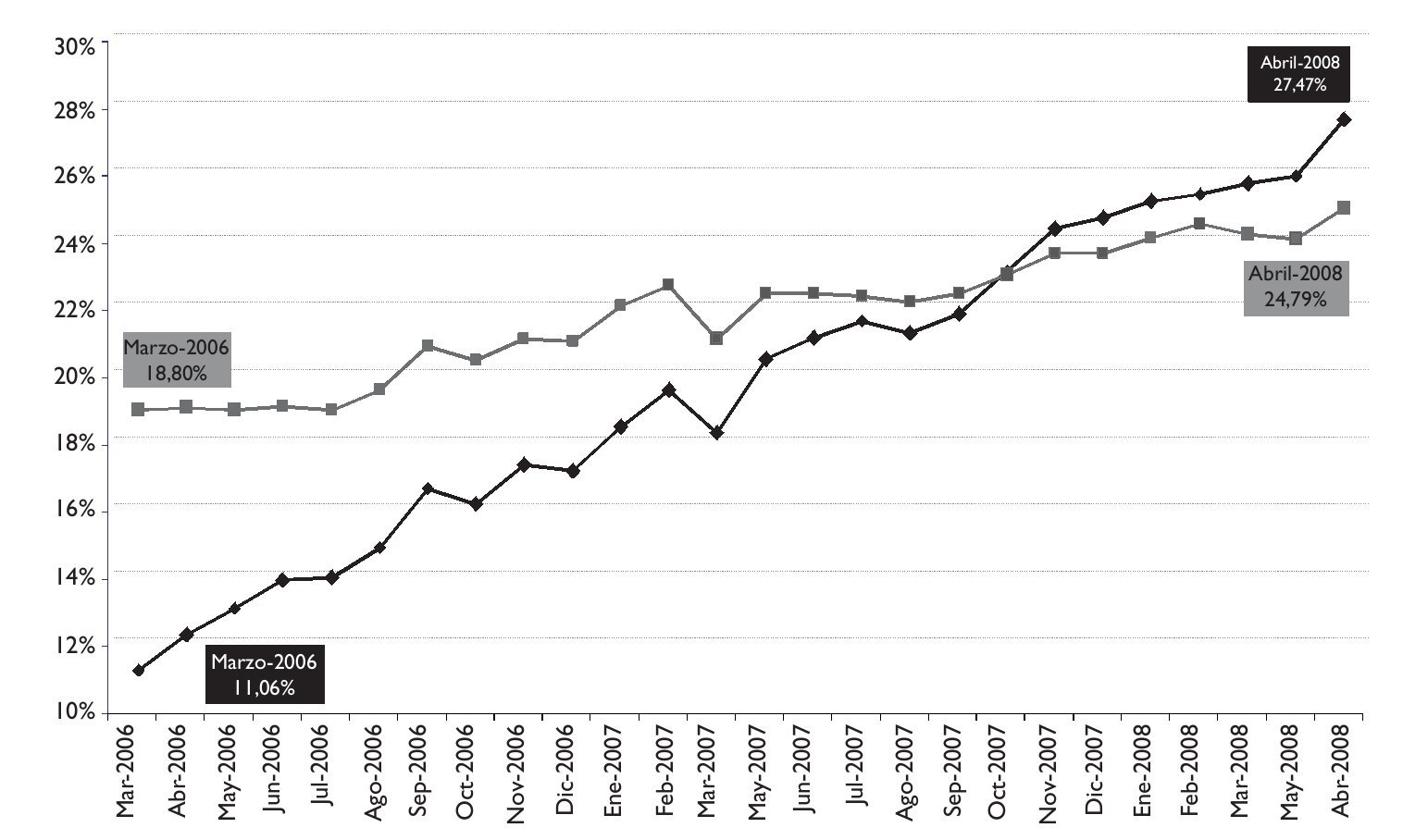
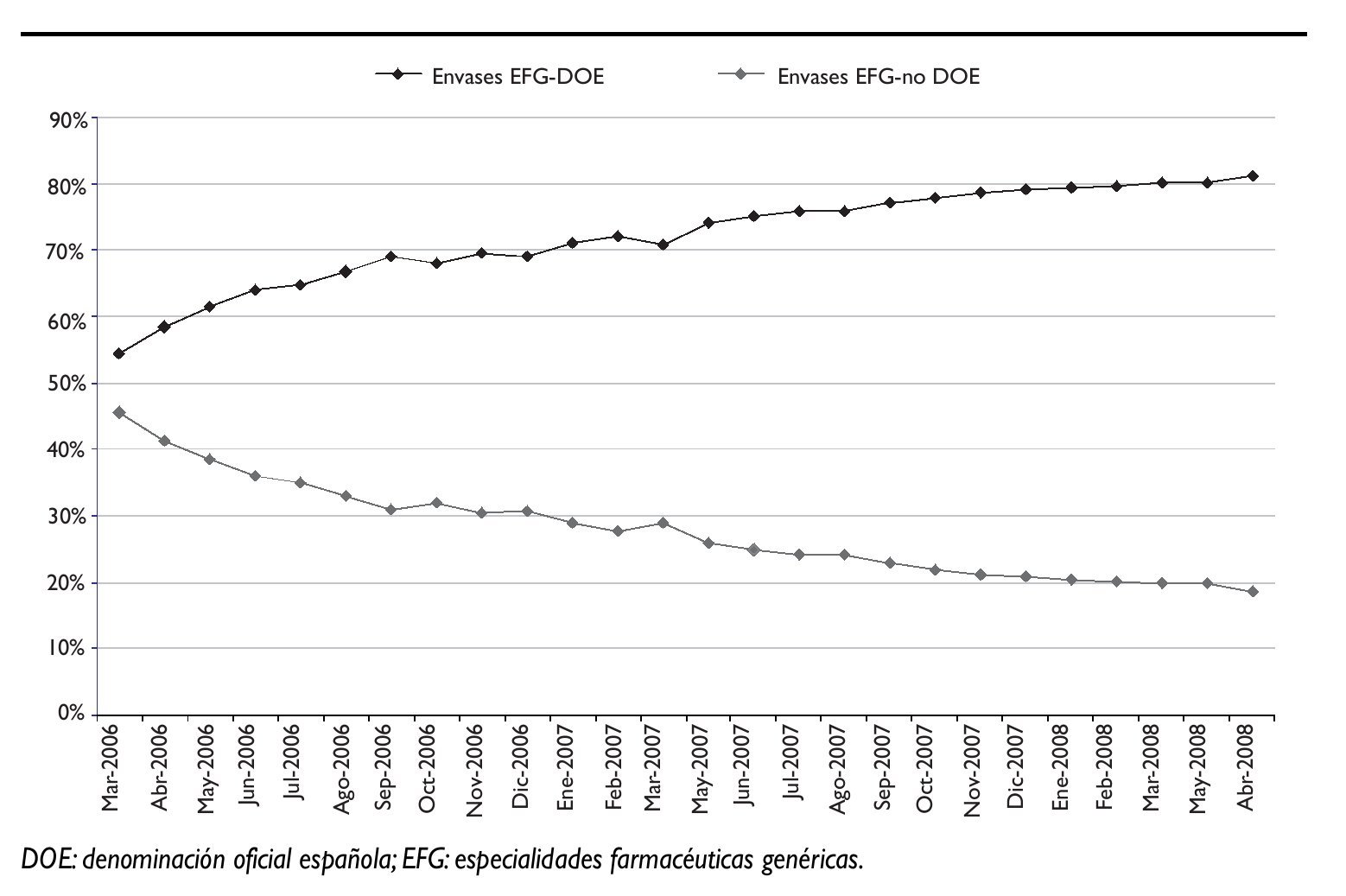
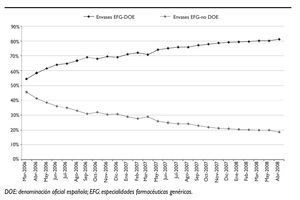
De hecho, las figuras 1 y 2 muestran la creciente proporción de genéricos prescritos por PPA, que en abril superó el 80%, y la también creciente utilización de genéricos que se encuentra cercana al 25%.
Figura 1.Evolución del porcentaje de especialidades farmacéuticas genéricas y del porcentaje de la prescripción por principio activo, en envases, sobre el total de especialidades farmacéuticas.
Figura 2.Porcentaje de genéricos prescritos como prescripción por principio activo y con identificación de laboratorio.
Por otra parte, inicialmente, la estimación realizada del gasto evitable que se podía producir con un 100% de PPA ascendía a 25,3 millones de euros, referido a datos de 2005,lo que suponía un 4% del conjunto del gasto farmacéutico en Castilla y León.
En cuanto al impacto en el periodo, si tenemos en cuenta el precio medio por envase de los medicamentos genéricos y de los de marca para los que existe genérico en el mercado, encontramos que la diferencia va de 6,45 hasta 11,60 euros en abril de 2008. Si a cada periodo de tiempo le aplicamos esa diferencia obtenemos un impacto estimado por la conjunción de ambas medidas, genéricos y DOE, de 133 millones de euros.
Conclusiones
El proyecto de promover la PPA forma parte de una estrategia a largo plazo sobre el conjunto de la prestación farmacéutica, que actúa sobre los hábitos de prescripción del médico, que son los que se han revelado más eficaces en el mantenimiento y mejora de la calidad de la prestación y la contención del crecimiento del gasto.
No obstante, este tipo de proyectos requiere el desarrollo de unas herramientas para la implantación, seguimiento y evaluación que son laboriosas y complejas, pero indispensables.
Los resultados sólo son visibles a medio y largo plazo, pero persisten en el tiempo y se retroalimentan si se incentivan de forma adecuada, alineando los objetivos de profesionales con los de las organizaciones sanitarias, garantizando el beneficio del paciente.
Por todo ello, el apoyo a estas medidas, ampliamente implantadas en países de nuestro entorno, permitirá contar con fondos adicionales para garantizar la financiación de las innovaciones y la sostenibilidad del SNS.
Para favorecer y mejorar estas medidas y la situación actual, podría ser de interés trabajar en aspectos tales como la bioapariencia o la educación al paciente en el uso de medicamentos.
Finalmente, para ratificar lo planteado en este documento, haremos una referencia a las declaraciones de la directora de desarrollo de negocio de IMS Health, en la Gaceta de los Negocios:
"Las medidas que se toman en los diferentes países para fomentar los genéricos pasan por la prescripción por principio activo, la prescripción electrónica..."
BIBLIOGRAFÍA RECOMENDADA
Consejo Andaluz de Colegios Oficiales de Farmacéuticos. Una encuesta sobre la prescripción por principio activo (PPA). Noviembre; 2005.
Ley 29/2006, de 26 de julio, de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios. BOE 178, de 27 de julio de 2006.
Mercado Genéricos. II Encuentro ibérico. AESEG-IMS. Noviembre; 2005.
Ministerio de Sanidad y Consumo. Evolución mensual del gasto farmacéutico.
Orden SCO 2874/2007, de 28 de septiembre, por la que se establecen los medicamentos que constituyen excepción a la posible sustitución por el farmacéutico con arreglo al artículo 86.4 de la Ley 29/2006, de 26 de julio de garantías y uso racional de los medicamentos y productos sanitarios.
Orden SCO 3867/2007,de 27 de diciembre, por la que se determinan los nuevos conjuntos de medicamentos y sus precios de referencia.
Orden SCO 3997/2006,de 28 de diciembre, por la que se determinan los conjuntos de medicamentos y sus precios de referencia y por la que se regulan determinados aspectos para la aplicación de lo dispuesto por la Ley 29/2006,de 26 de julio de garantías y uso racional de los medicamentos y productos sanitarios.
Prior M. La Gaceta de los Negocios (8 de noviembre de 2005).
UK: NHS Medicines Bill. Pharma Pricing and Reimbursment. 2008;13(5):