Introducción
La inmunoterapia con alergenos administrada por vía subcutánea demostró ser eficaz en el tratamiento de rinitis alérgica, asma alérgica y alergia a picadura de insectos,1 su administración conlleva también el riesgo de presentación de efectos adversos tanto locales (en el sitio de la aplicación de la inyección), además de sistémicas, como anafilaxia.2-4 Una reacción local consiste en la aparición de enrojecimiento, edema o prurito situados en los alrededores del sitio de la aplicación de la inyección con alergenos.5 Se reportó que la frecuencia de reacciones locales en pacientes que se aplican inmunoterapia con alergenos varía entre 26% y 82%, de 0.7% a 4.0% de reacciones locales por cada 100 inyecciones.6-8 Una reacción sistémica se caracteriza por la aparición de signos generalizados con o sin síntomas de anafilaxia.9 Los síntomas y signos que se presentan solos o en combinación en una reacción sistémica son: los cutáneos (prurito, urticaria, angioedema), los de vías respiratorias superiores e inferiores (disfonía, sibilancias), los gastrointestinales (náuseas, vómito, diarrea) y los cardiovasculares (síncope e hipotensión).10,11 Ambas reacciones pueden a su vez clasificarse de acuerdo al tiempo de inicio de los síntomas y signos en: Inmediatas, si los mismos aparecen durante los primeros 30 minutos de la aplicación; Tardías, si los mismos ocurren posterior a los 30 minutos.12 La frecuencia de las reacciones sistémicas debidas a la inmunoterapia con alergenos varía desde menos de 1% en pacientes que reciben inmunoterapia convencional, hasta más de 36% en pacientes que reciben inmunoterapia rápida.9,13 En cuanto a esto, en 1995 Tinkelman señaló una relación de una reacción sistémica por cada 1600 inyecciones o una reacción sistémica por cada 46 pacientes.14 En México, el único estudio que evaluó esta relación se publicó en 2002 por Rodríguez y colaboradores, quienes informaron sobre una relación de una reacción sistémica por cada 2615 aplicaciones, o una reacción sistémica por cada 57 pacientes.15
Diversos factores de riesgo pueden participar en el inicio de una reacción sistémica en pacientes tratados con inmunoterapia con alergenos, por ejemplo: el tipo de alergeno seleccionado al preparar una vacuna, la potencia y la formulación del extracto alergénico, el tratamiento farmacológico concomitante, el esquema de la inmunoterapia, la severidad y el tipo de enfermedad antes del tratamiento, la premedicación utilizada, el antecedente de reacciones sistémicas y la exquisita sensibilización a un alérgeno específico, la exposición al alérgeno durante una estación de polen relevante, el aumento de la dosis del extracto durante el periodo de incremento de la inmunoterapia en especial pacientes con asma o asma inestable y el uso de dosis altas de alergenos estandarizados, el uso de beta-bloqueadores y el uso de inmunoterapia rápida.9,16
Debido al riesgo de fatalidad y al número escaso de estudios nacionales relacionados a reacciones sistémicas por inmunoterapia con alergenos, nos propusimos llevar a cabo un estudio para conocer la frecuencia de las reacciones sistémicas asociadas al uso de inmunoterapia con alergenos, así como también conocer las características clínicas y los factores de riesgo probablemente involucrados en este tipo de reacciones en la población atendida en el Centro de Alergia e Inmunología Clínica del Hospital Universitario en Monterrey, Nuevo León.
Métodos
Realizamos un estudio retrospectivo y descriptivo mediante la revisión de los registros diarios de aplicación de inmunoterapia de los pacientes que acudieron a la administración de inmunoterapia con alergenos en el Centro Regional de Alergia e Inmunología Clínica del Hospital Universitario de Monterrey, Nuevo León durante el periodo comprendido entre el 1 de mayo de 2001 al 30 de abril de 2002.
Se utilizaron los alergenos de los proveedores Allerstand (Dermatophagoides farinae, Dermatophagoides pteronysinus, Phleum pratense, Holcus lanatus, Ligustrum vulgare, Cynodon dactylon), y Nelco (Bromus spp, Lolium perenne, Sorghum halepense, Amaranthus palmeri, Ambrosia elatior, Artemisa ludoviciana, Atriplex canescens, Cheno-podium ambrosioides, Helianthus annus, Salsola Kali, Fraxinus americana, Junglans regia, Juniperus sabinoides, Populus alba, Prosopis spp, Quercus spp, Periplaneta americana, Blatella germanica, Felis domesticus, Canis familiaries).
La fase de incremento consistió en la aplicación semanal de los viales en un periodo de un año y varió de acuerdo a la tolerancia del paciente, con aumento de 0.1 mL de la solución peso/volumen por cada antígeno hasta alcanzar la dosis proyectada de mantenimiento. La dosis proyectada de mantenimiento fue de 1:500 para cada uno de los antígenos.
Se identificaron las reacciones relacionadas con la inmunoterapia en los pacientes estudiados. Se consideraron como reacciones locales normales todas aquellas que midieron menos de 5 cm, mientras que aquellas con un diámetro mayor de 5 cm presentes a los 30 minutos de la inyección se clasificaron como reacciones locales grandes. Se consideró como reacción sistémica a las manifestaciones clínicas distantes al sitio de la inyección.
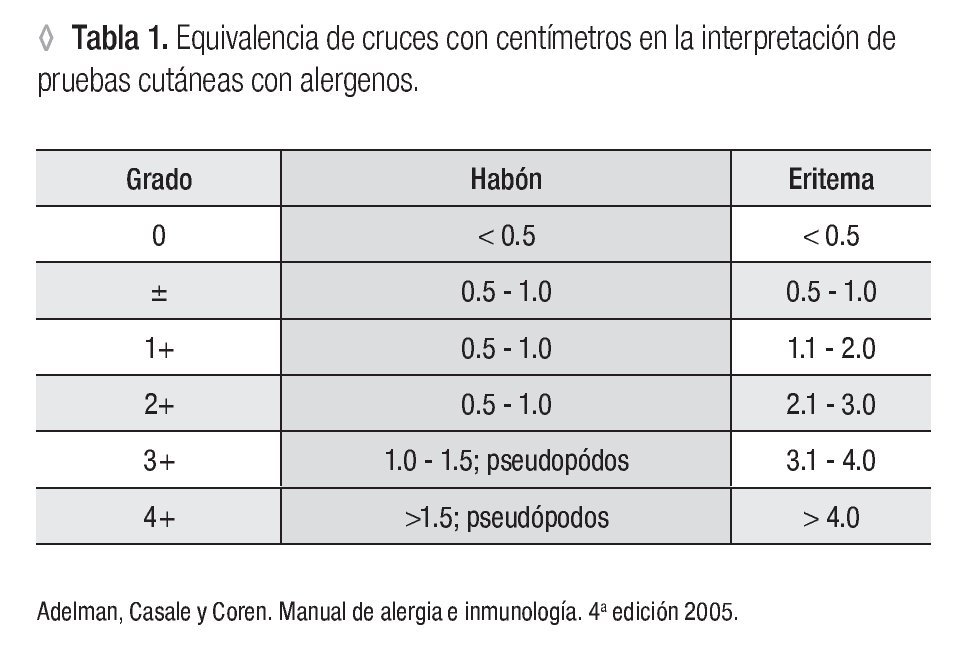
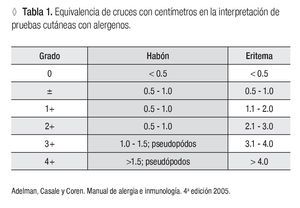
De los expedientes de los pacientes que presentaron reacciones sistémicas, se tomaron los resultados de sus PC, los cuales se reportaron en cruces de acuerdo al diámetro en milímetros de la roncha y del eritema (Tabla 1). Adicionalmente, se registró el grado de sensibilidad (determinado por el tamaño de la roncha), el apego al esquema de inmunoterapia y el antecedente de reacciones sistémicas previas. En caso de asma se documentó el nivel de control.
Se consideraron reacciones locales grandes aquellas con un diámetro mayor de 5 cm presente a los 30 minutos de aplicación de inmunoterapia.
El análisis de los datos se calculó mediante la estadística descriptiva, que incluyó la distribución de las frecuencias por porcentajes y los resultados se presentaron por medio de cuadros y figuras.
Resultados
Durante el periodo de tiempo estudiado, un total de 14 600 dosis de inmunoterapia específica con alergenos se administraron en 2319 pacientes. Las vacunas de alergenos de estos pacientes se formularon a base de extractos acuosos de pólenes, hongos, ácaros de polvo casero o cucarachas en diferentes combinaciones.
De este grupo, hombres 1213 (52%) el rango de edad se encontró entre uno y 82 años, con una media de 20 años.
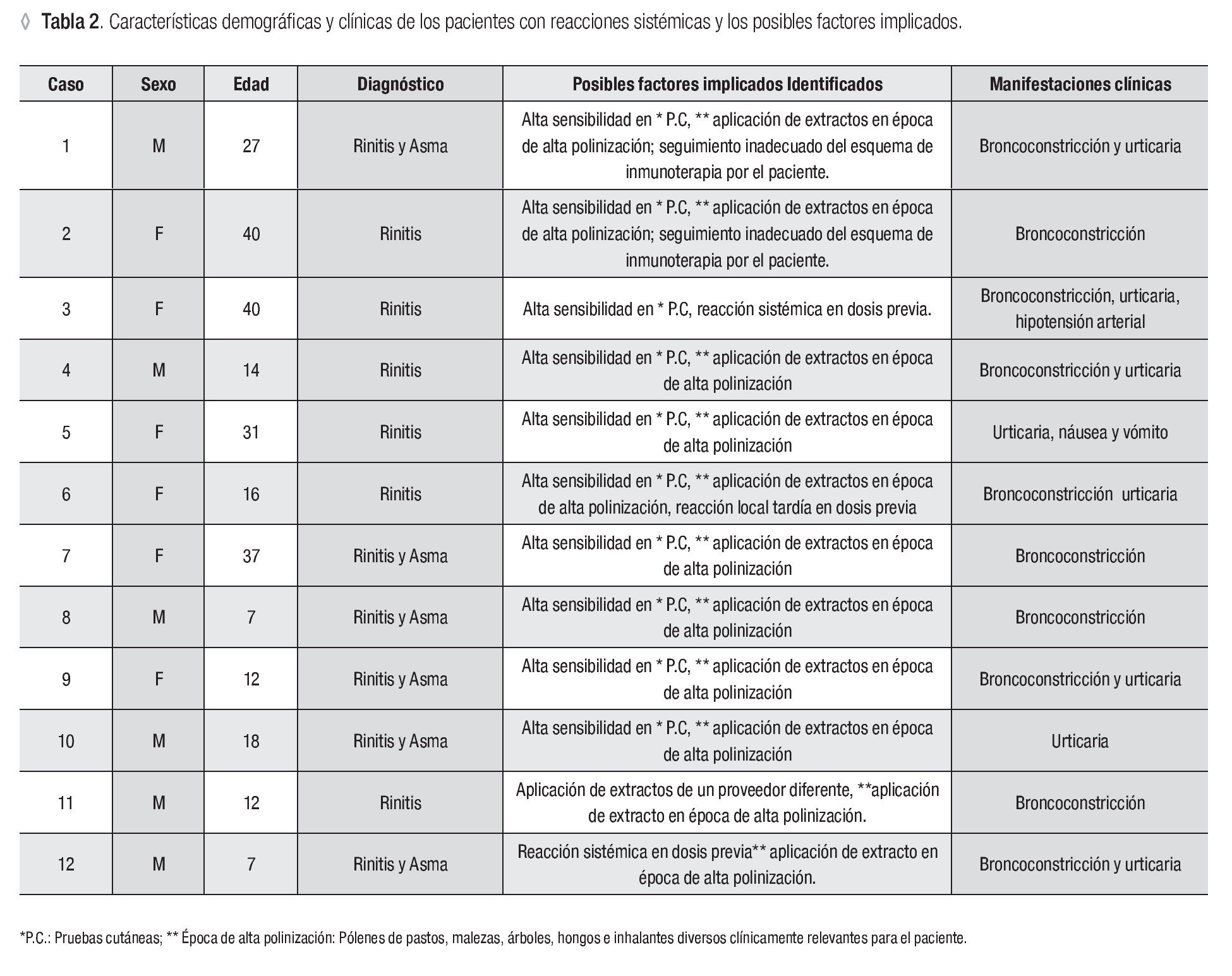
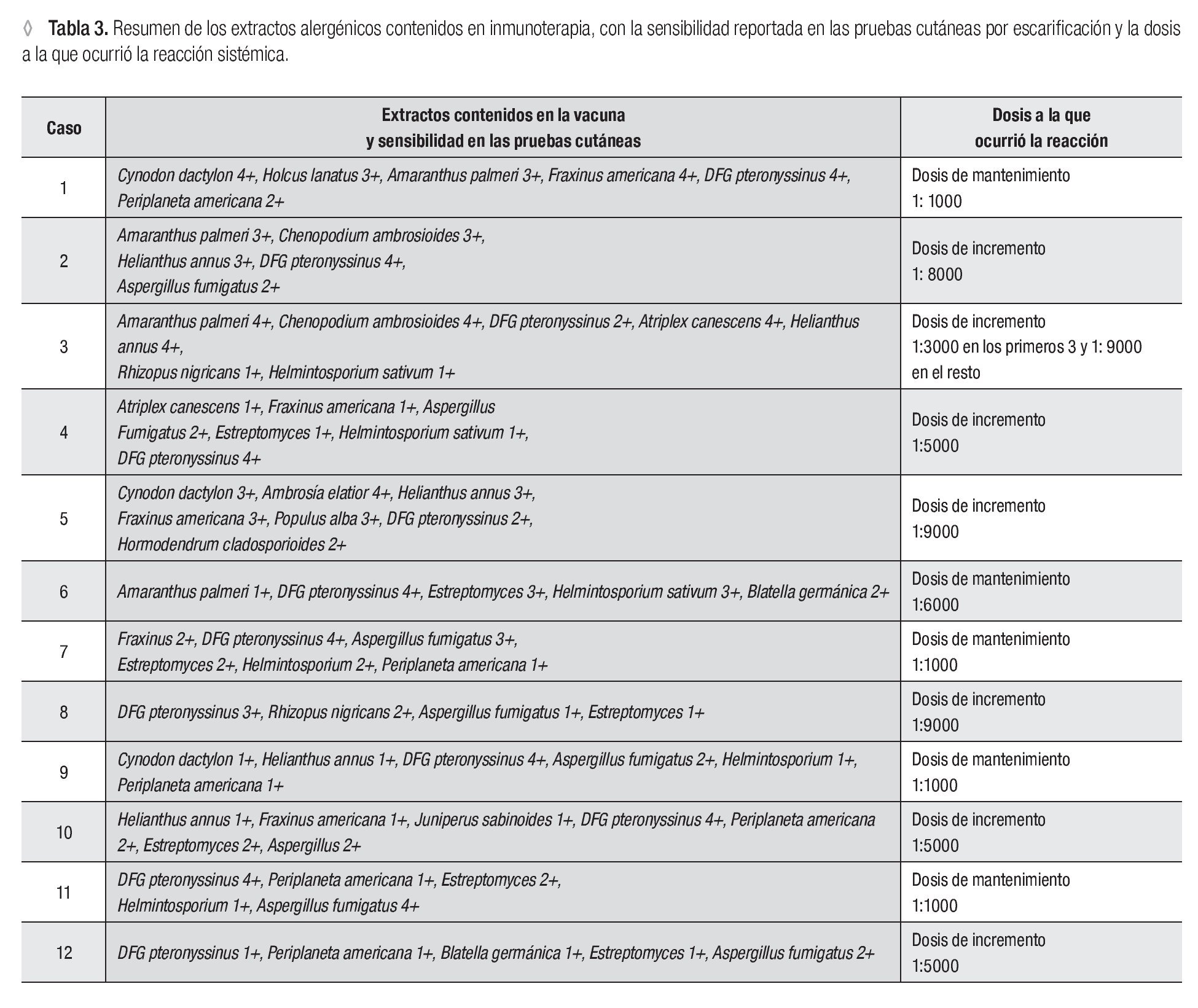
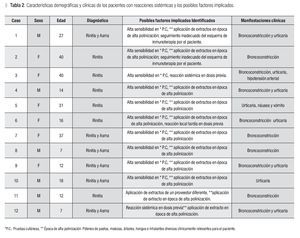
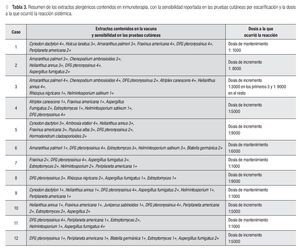
Presentaron reacciones sistémicas 12 pacientes, seis mujeres y seis hombres. Las edades de estos pacientes oscilaron entre siete y 40 años, con una media de 21 años, 100% con diagnóstico de rinitis alérgica y seis de ellos (50%), además con asma bronquial. Las características demográficas, el diagnóstico y las manifestaciones clínicas, así como los posibles factores implicados en el desarrollo de las reacciones sistémicas se presentan en la Tabla 2. El contenido de la inmunoterapia por paciente se encuentra descrito en la Tabla 3, así como la concentración al momento de la reacción.
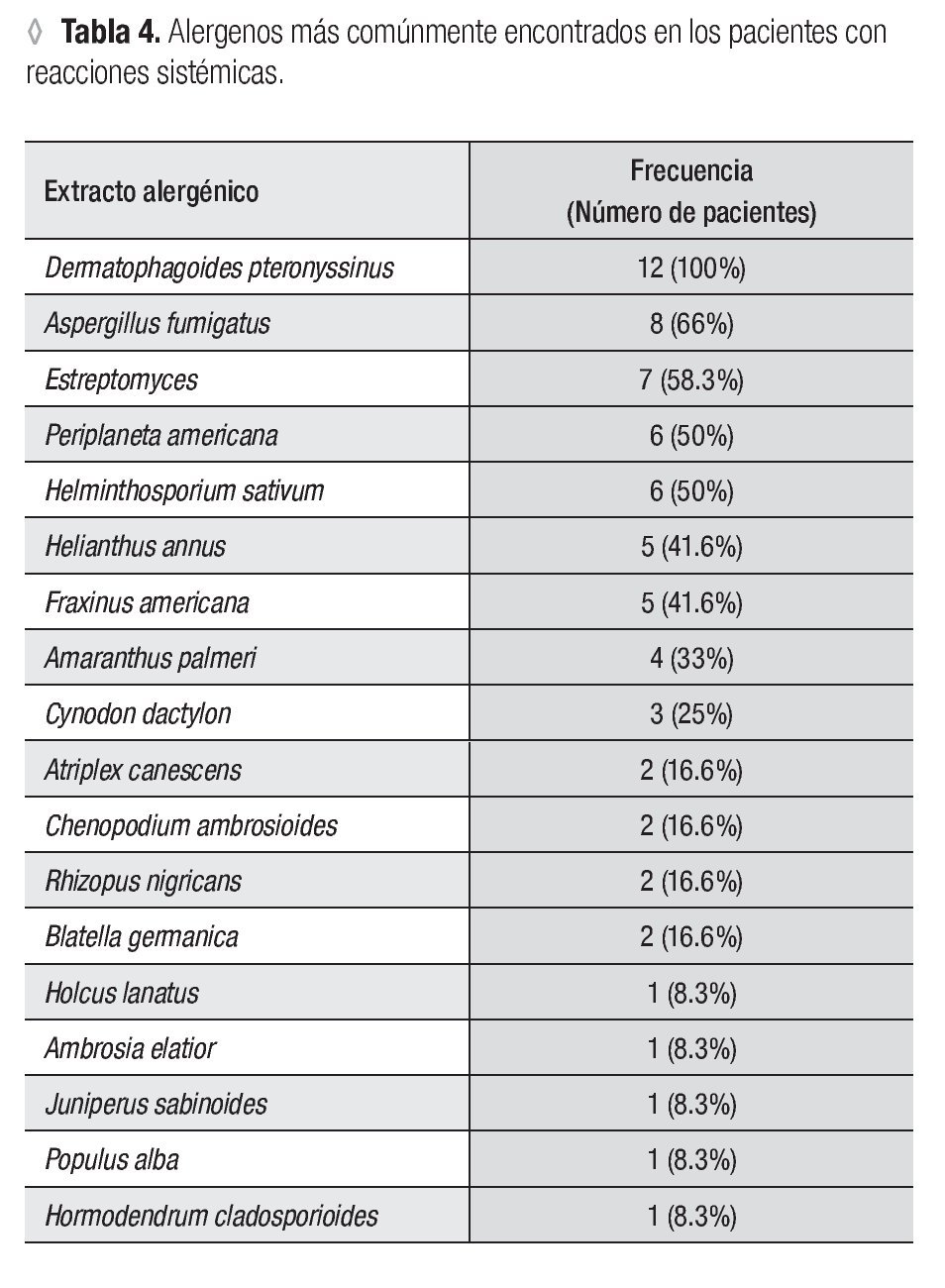
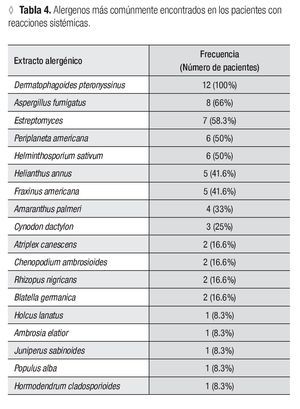
En la Tabla 4 se muestran los alergenos más comúnmente encontrados en los pacientes con reacciones sistémicas.
En relación con el número de inyecciones aplicadas, se presentó una reacción sistémica por cada 1216 inyecciones. Con respecto al número de pacientes que presentaron reacción sistémica, se presentó una reacción por cada 193 pacientes.
Los síntomas y signos que presentaron los pacientes con reacciones sistémicas incluyeron broncoespasmo en 10/12 (83%), urticaria en 8/12 (67%), síntomas gastrointestinales (náuseas y vómitos) en 1/12 (8.3%) e hipotensión arterial en 1/12 (8.3%). Siete de los doce pacientes (58%) presentaron anafilaxia; 4/12 pacientes (33%) presentaron solamente síntomas pulmonares y sólo síntomas dermatológicos en 1/12 pacientes (8.3%).
El inicio de las manifestaciones clínicas ocurridas por la administración de la inyección con el extracto alergénico se dio dentro de los primeros 30 minutos de la aplicación en 100% de los pacientes. En cuatro de ellos (33%), la reacción ocurrió fuera de la institución, después de 20 minutos, tiempo establecido por el centro como norma para valoración clínica luego de la aplicación del extracto alergénico y requirieron reevaluación en nuestro centro de atención.
Siete de doce pacientes (58%) presentaron la reacción sistémica durante la fase de incremento de la inmunoterapia y cinco de 12 (42%), durante la fase de mantenimiento. En nueve pacientes (75%) la reacción sistémica ocurrió con la primera inyección de un frasco nuevo de inmunoterapia y en los tres restantes (25%) con la segunda inyección.
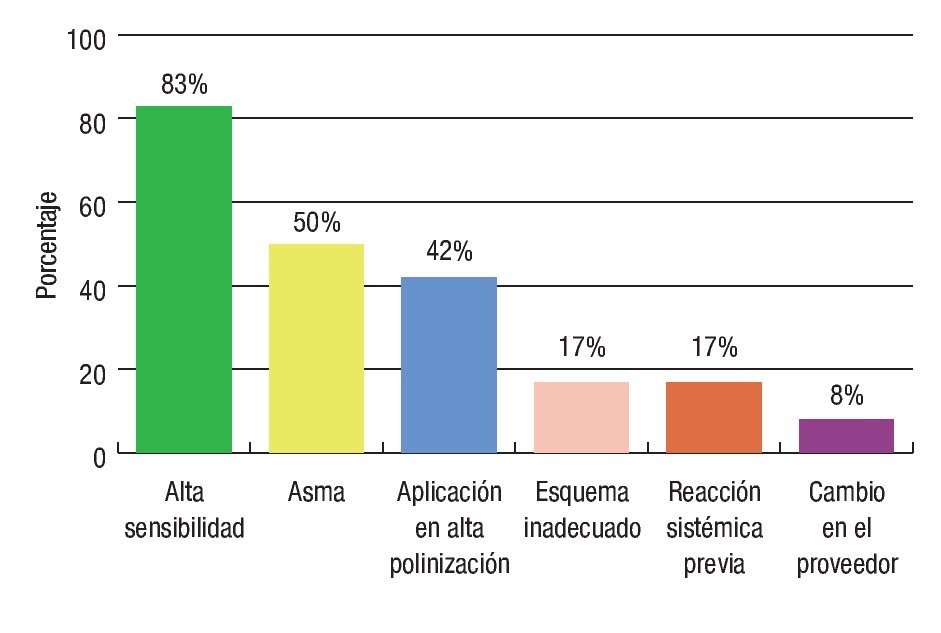
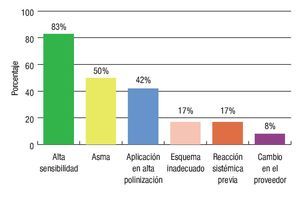
Los factores identificados como los posiblemente implicados en la aparición de las reacciones sistémicas y que estuvieron presentes de manera aislada o combinada en los pacientes afectados fueron los siguientes: sensibilidad identificada por reacciones grandes en las pruebas cutáneas, pacientes con asma bronquial parcialmente o no controlada, aplicación de extractos alergénicos de polen durante una época de polinización alta, un seguimiento inadecuado del esquema de inmunoterapia por parte del paciente, antecedentes de una reacción sistémica previa y cambio en el proveedor del extracto alergénico utilizado en la elaboración de la inmunoterapia (Figura 1).
◊ Figura 1. Posibles factores relacionados con la aparición de las reacciones sistémicas.
En relación con los meses de presentación de las reacciones sistémicas, se observaron dos picos de aparición. De las reacciones, 50% ocurrió durante los meses de septiembre y octubre, y 17% se presentó durante el mes de marzo. Entre los meses de abril y julio, así como en diciembre, no hubo casos informados.
Discusión
La inmunoterapia con alergenos demostró ser eficaz para reducir los síntomas alérgicos; sin embargo, se sabe que puede conllevar el riesgo de presentar efectos adversos tanto locales como sistémicos. Estos últimos pueden manifestarse con diferentes grados de severidad y pueden llevar al paciente a un evento fatal. A pesar de esto, la frecuencia de RS debidas a IT convencional es limitada y se presentan en menos de 1%.3,4,9
Este estudio examinó una población de niños y adultos que presentaron reacciones sistémicas secundarias a la aplicación de inmunoterapia convencional y se encontró una frecuencia de 1:1216 inyecciones o 1:193 pacientes.
La frecuencia de RS se puede afectar por diversos factores, como el número de sujetos incluidos en un estudio, el número de inyecciones aplicadas, la concentración de la dosis, la fase de la inmunoterapia, el número de alergenos incluidos en ésta, lo que hace difícil la comparación de nuestros resultados con las observaciones obtenidas por otros autores.
Tinkelman encontró en población pediátrica y adulta norteamericana una frecuencia de reacciones sistémicas de 1:1600 inyecciones o 1:46 pacientes; en tanto que en población igualmente pediátrica y adulta en México, Rodríguez informó una frecuencia de RS de 1:2615 inyecciones o 1:57 pacientes. En Turquía, Dursun señaló una tasa de reacciones sistémicas por inyección de 0.9% y Greenberg de 0.25%.17,18
Es importante mencionar que un grupo de pacientes atendidos en nuestro centro, recibe la aplicación de su inmunoterapia en otros servicios de salud, por lo que no se incluyeron las reacciones sistémicas u otros eventos que pudieron ocurrir en algunos de estos pacientes.
Las RS pueden presentarse a cualquiera edad; en nuestro estudio se presentaron entre los siete y 40 años de edad y fueron más frecuentes en la segunda y cuarta década de la vida, que en conjunto correspondieron a 74.9% de los casos. Rodríguez, en México, encontró RS entre los 0 y 49 años de edad y fueron más frecuentes entre los 15 y 24 años (44%); mientras que Tinkelman, en población norteamericana, evidenció estas reacciones entre los ocho y 55 años de edad, predominantemente entre la tercera y quinta década de la vida (69%). Es importante mencionar que 17% de las RS reportadas en nuestros pacientes se presentaron en la primera década de la vida, comparable con el 10% encontrado por Tinkelman, por lo que es importante considerar la posibilidad de este tipo de reacciones en niños que reciben IT alergeno específica.
A diferencia de los hallazgos de Rodriguez y Tinkelman, en los que hay una mayor incidencia en las mujeres sobre los hombres en rango de 1.4:1 hasta 3:1; en nuestro grupo de estudio no hubo diferencias por sexo.
La frecuencia de RS por diagnóstico fue de 50% para los pacientes con rinitis alérgica y asma, el 50% restante se presentó en los pacientes con diagnóstico de rinitis alérgica. Tinkelman señaló 66% de RS en pacientes con rinitis alérgica, en tanto que Rodríguez, 55% en pacientes con rinitis alérgica más asma. Para ambos autores, la menor frecuencia de reacciones sistémicas se presentó en los grupos de pacientes con asma exclusivamente, de 9% y 10% respectivamente.
El inicio de presentación de nuestras RS concuerda con lo publicado en estudios previos, en los que éstas se presentan con mayor frecuencia dentro de los primeros 30 minutos de la aplicación del extracto alergénico; sin embargo, algunos autores reportaron que pueden aparecer hasta seis horas después.9,14,15 Los Parámetros Prácticos para la Alergia de la Joint Task Force, recomiendan un periodo de 20 a 30 minutos de evaluación clínica posterior a la aplicación de la inmunoterapia con alergenos, mientras que la Sociedad Británica de Alergia e Inmunología Clínica recomienda un periodo de 60 minutos.19 La Academia Americana de Alergia Asma e Inmunología (AAAAI) recomienda un periodo de evaluación de mayor tiempo para los pacientes de riesgo alto.20
El mayor porcentaje de las RS (58%) se presentó durante la fase de incremento de dosis de la IT con alergenos, hecho que coincide con los hallazgos de otros autores, que reportan una frecuencia entre 70% y 88% de aparición de estas reacciones durante esta fase.2,14,21-23 Lo anterior es de esperarse debido a que el paciente se somete a dosis progresivamente mayores de alergenos; sin embargo, las dosis altas durante la fase de mantenimiento también pueden aumentar el riesgo de RS.10
Los factores que detectamos como posiblemente implicados en la aparición de las reacciones sistémicas que se presentaron con mayor frecuencia fueron la sensibilidad identificada por reacciones grandes en las pruebas cutáneas, el asma bronquial y la aplicación de extractos alergénicos de polen durante una época de alta polinización. Al igual que lo señalado en la bibliografía, la presencia de asma bronquial, y en especial asma no controlada, en nuestro estudio fue uno de los principales factores que posiblemente influyó en la aparición de una RS; por lo que se recomienda realizar evaluaciones de pico flujo o espirometría en este grupo de pacientes de alto riesgo antes de la administración de las inyecciones con alergenos.9,14,23,24 De igual forma la aplicación de extractos alergénicos de polen durante una época de alta polinización, fue otro de los factores que posiblemente influyó en la presentación de estas reacciones y que se presentó con una frecuencia relativamente alta. Lo anterior se hizo evidente debido a que la mayor frecuencia de reacciones se presentó durante los meses de marzo, septiembre y octubre; meses en los cuales Rocha y cols. demostraron mayor polinización en el área metropolitana de Monterrey.25
Para lograr una oportuna identificación de estos factores de riesgo, es importante realizar una adecuada historia clínica enfocada en la búsqueda de los mismos con el fin de prevenir complicaciones que podrían incluso hasta llegar a ser mortales.
Conclusiones
La frecuencia de las reacciones sistémicas asociadas a inmunoterapia en nuestra población fue similar a lo informado en otros estudios y la anafilaxia fue la de mayor incidencia (1:331 pacientes). El involucro respiratorio fue la característica clínica mas prevalente. Todas las reacciones se presentaron en los primeros 30 minutos, la mayoría durante la fase de incremento y durante la primera aplicación de un nuevo vial. Los pacientes de riesgo alto para presentar reacciones sistémicas se relacionaron con el grado de sensibilidad, la estación del año, el mal apego a la aplicación de inmunoterapia, el cambio de proveedor de los extractos para inmunoterapia y el antecedente de una reacción sistémica.
Deben identificarse los factores de riesgo y se recomienda a todo paciente que recibe extractos alergénicos, aplicárselos en instalaciones debidamente equipadas y con personal altamente capacitado para tratar cualquier RS, en especial el choque anafiláctico, para poder así disminuir la frecuencia y severidad de las mismas.
Correspondencia: Sandra Nora González-Díaz.
Edificio anexo a Barragán (Geriatría) 4º Piso. Av. Francisco I. Madero y Gonzalitos S/N, Col. Mitras Centro,
Monterrey, Nuevo León. 64460.
Teléfono: (81) 8346 2515, fax: (81) 8347 6798.
Correo electrónico:sgonzalezdiaz@yahoo.com