La colocación, manipulación o retirada de un catéter epidural en pacientes que reciben doble antiagregación como profilaxis secundaria plantea una compleja decisión, intentando equilibrar el riesgo de hematoma epidural al continuar con el tratamiento antiagregante y el riesgo de trombosis al interrumpirlo. El nivel de evidencia científica en el manejo de la terapia antitrombótica en estos pacientes es bajo, lo que dificulta la toma de decisiones en la práctica clínica.
Esta compleja situación queda ejemplificada en el caso que presentamos. Se trata de un varón de 80 años al que se le colocó un catéter epidural para analgesia por isquemia arterial de miembros inferiores. Presentó posteriormente un síndrome coronario agudo, que precisó el implante de un stent farmacoactivo y terapia con doble antiagregación, siendo necesario retirar el catéter por disfunción y signos de infección. El manejo incluyó una terapia puente sustitutiva con tirofibán como alternativa a considerar.
The positioning, manipulation or removal of an epidural catheter in patients receiving dual antiplatelet therapy as secondary prophylaxis involves complex decisions, trying to balance the risk of epidural haematoma by continuing antiplatelet therapy and the risk of thrombosis on interrupting it. Unfortunately, the level of scientific evidence in the management of antithrombotic therapy in these patients is low, thus it is difficult to make decisions in clinical practice.
This complex situation is illustrated by the case presented, which involved a man of 80 years old who needed an epidural catheter for analgesia because of arterial ischaemia of the lower limbs. He presented with an acute coronary syndrome that required implantation of a drug-eluting stent, as well as dual antiplatelet therapy. The catheter needed to be removed due to dysfunction and signs of infection. The management included a bridge replacement therapy with tirofiban, as an alternative to consider.
Aproximadamente entre un 5-15% de los pacientes portadores de un stent coronario se someten a algún procedimiento quirúrgico dentro de los 2 primeros años, tras su implantación1. Muchos de estos procedimientos no son diferibles y es necesario interrumpir la terapia dual antiagregante previo al procedimiento, presentando un mayor riesgo de trombosis del stent. Esta doble terapia utilizada como prevención secundaria normalmente está compuesta por ácido acetilsalicílico (AAS) y un antagonista del receptor P2Y (en su mayoría clopidogrel, pero también pueden incluir prasugrel o ticagrelor).
Valorar las estrategias de suspensión y sustitución de fármacos antiagregantes en pacientes con stent coronario implica conocer el delicado equilibrio entre el riesgo isquémico y hemorrágico, teniendo en cuenta el perfil de eficacia y seguridad de los fármacos antitrombóticos.
El caso que presentamos expone una terapia puente con tirofibán, tras la suspensión de la doble antiagregación para la retirada de un catéter epidural. Este manejo puede suponer una alternativa en el manejo de pacientes portadores de stent coronario con alto riesgo trombótico por evento coronario reciente, que vayan a someterse a procedimientos de alto riesgo hemorrágico.
Caso clínicoVarón de 80 años ingresado a cargo de cirugía vascular por isquemia arterial crónica grado iv de miembros inferiores, según clasificación de Fontaine. Como antecedentes se destaca un accidente cerebro-vascular isquémico, en tratamiento farmacológico con AAS 100mg/día. Al ingreso se colocó un catéter epidural a nivel de L3-L4 para control analgésico. Cinco días después, el paciente sufrió un síndrome coronario agudo (SCA) con elevación del ST. Se le realizó una coronariografía de urgencia, y se implantó un stent farmacoactivo en el tronco coronario. Se inició tratamiento con doble antiagregación y heparina de bajo peso molecular (HBPM) a dosis terapéuticas.
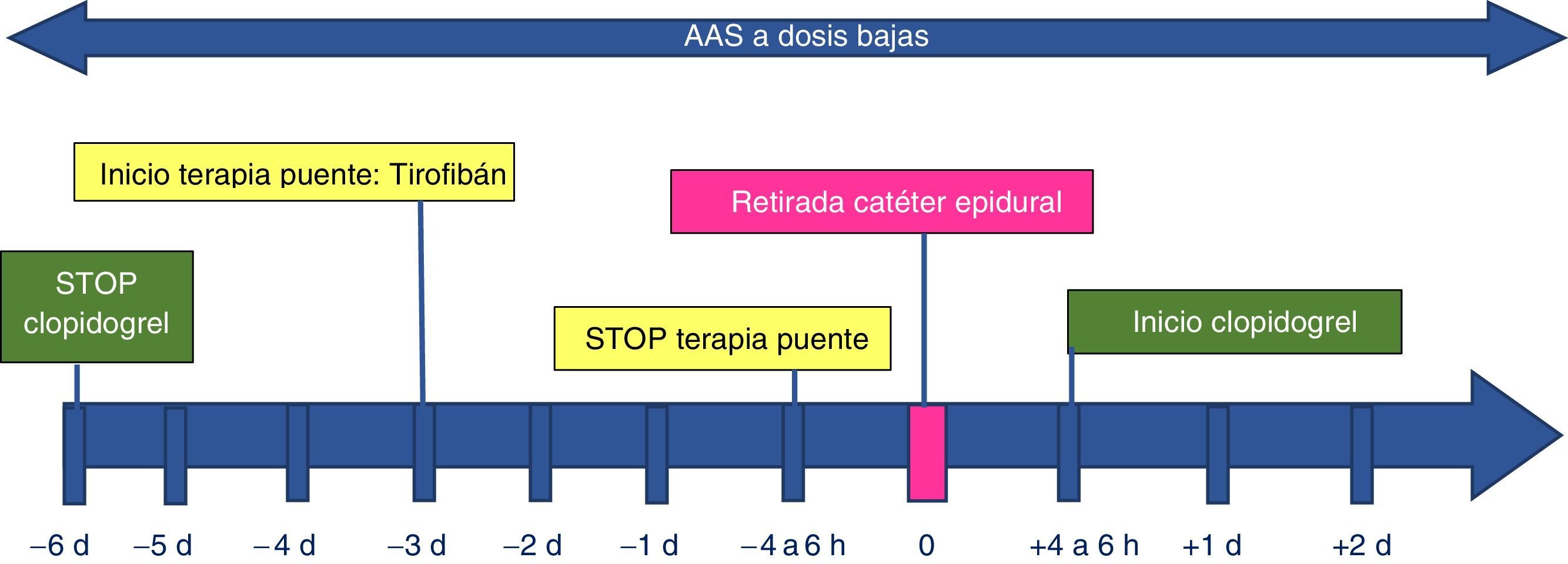
A los 8 días de la colocación del catéter epidural, se objetivó mal funcionamiento y enrojecimiento en el punto de entrada del catéter, precipitando este hecho la necesidad de su retirada. Se llevó a cabo una sesión clínica conjunta con el servicio de cardiología y el servicio de cirugía vascular. Se decidió suspender el clopidogrel 6 días antes de la retirada del catéter epidural, y se mantuvo el AAS a una dosis de 100mg/día. Tres días después se inició el tratamiento con una perfusión intravenosa de tirofibán a 0,1μg·kg−1·min−1 durante 72h. El día de la retirada del catéter, dicho tratamiento se suspendió 4h antes. A las 6h de la retirada del catéter se reinició el tratamiento con clopidogrel con dosis de carga, sin incidencias (fig. 1). El paciente evolucionó de forma favorable sin nuevas complicaciones a lo largo de su ingreso. Fue dado de alta hospitalaria 5 días después.
Esquema del manejo de la antiagregación con terapia puente en el caso clínico expuesto ante un elevado riesgo hemorrágico y trombótico.
Este caso clínico plantea la compleja decisión del manejo de la doble antiagregación, balanceando el equilibrio entre un elevado riesgo hemorrágico (hematoma epidural) y un elevado riesgo trombótico (trombosis del stent en SCA reciente)2. Para la retirada de un catéter epidural en pacientes que reciben doble antiagregación como prevención secundaria se recomienda mantener al menos un antiagregante3,4, idealmente AAS 100mg, e interrupción del clopidogrel de 7 a 10 días antes del procedimiento5. Sin embargo, es bien conocido que la suspensión precoz de la doble antiagregación es un factor independiente de trombosis del stent, especialmente antes de su endotelización6,7. Se recomienda la terapia dual antiagregante durante al menos un mes tras implantar un stent sin recubrir en pacientes con enfermedad arterial coronaria estable, y durante 6 meses tras implantar un stent farmacoactivo de nueva generación8. En pacientes con SCA de alto riesgo, se recomienda la doble terapia durante un año independientemente del tipo de stent que se emplee9.
Por tanto, es preciso discutir qué estrategia seguir y valorar de forma cuidadosa e individualizada el equilibrio entre el riesgo trombótico (asociado a la suspensión del fármaco) y el riesgo hemorrágico inherente de su acción terapéutica10.
El caso que presentamos ejemplifica un paciente con riesgo trombótico muy elevado, como es un SCA reciente de menos de 6 semanas de evolución tratado con un stent farmacoactivo1. En este caso el procedimiento invasivo (retirada del catéter epidural) no podía ser diferido (riesgo de infección), y además implicaba un elevado riesgo hemorrágico (hematoma epidural). El abordaje debe ser multidisciplinario, si bien, una alternativa propuesta por Sierra et al. en la guía de práctica clínica sobre el manejo perioperatorio de antiagregantes plaquetarios en cirugía no cardíaca1 indica en cirugía de alto riesgo hemorrágico el mantenimiento de AAS a dosis bajas (100mg/día) y la suspensión del clopidogrel durante 3-5 días valorando una terapia puente. En este caso debido al alto riesgo trombótico se decidió iniciar una terapia antiagregante puente que disminuyera los tiempos de retirada del catéter y el riesgo hemorrágico, a la vez que se asegurara, en la medida de lo posible, la no trombosis del stent recién implantado.
El agente puente ideal debería ser eficaz para lograr la inhibición plaquetaria similar a la del inhibidor del receptor P2Y oral, con un rápido inicio de acción, y también desplazamiento rápido (corta duración de acción). La evidencia sobre la eficacia y seguridad de los fármacos antitrombóticos de acción corta como la heparina no fraccionada, HBPM o antagonistas de la glucoproteína IIb/IIIa de acción corta (como tirofibán o eptifibatide) en el ajuste perioperatorio, son escasos. Sin embargo, es importante destacar qué, si la terapia puente es necesaria, los agentes antiplaquetarios se prefieren a los anticoagulantes2,3. En este contexto, los únicos agentes aprobados con acción rápida y efectos inhibidores plaquetarios potentes con relativamente corta duración de acción son los inhibidores de la glicoproteína IIb/IIIa (tirofibán y eptifibatide).
Una estrategia puente perioperatoria con tirofibán es factible y razonablemente segura en pacientes con stent recientemente implantado4. Después del procedimiento invasivo, el clopidogrel debe reanudarse en las primeras 6-48h2.
En conclusión, el manejo de la doble antiagregación en pacientes con riesgo trombótico que se someten a un procedimiento con elevado riesgo hemorrágico, continúa siendo motivo de controversia. Aunque los algoritmos y guías de actuación son de gran ayuda en la toma de decisiones, es imprescindible una evaluación individualizada y multidisciplinaria. En este contexto, la terapia puente con tirofibán puede suponer una alternativa válida y segura para disminuir los tiempos óptimos de suspensión de la terapia antiagregante, y minimizar el riesgo de sangrado y trombosis.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.