Adjuvant! Online calcula el riesgo de recidiva y muerte a 10 años y proporciona estimaciones del beneficio del tratamiento adyuvante en pacientes con cáncer de mama. Testamos su aplicabilidad y analizamos únicamente estimaciones de mortalidad.
MétodoPresentamos las estimaciones de 66 pacientes intervenidas de cáncer de mama unilateral y unicéntrico, sin enfermedad residual ni metástasis. Las variables analizadas fueron edad, comorbilidad, receptores de estrógenos, grado histológico, tamaño tumoral, ganglios metastásicos, tipo de tratamiento hormonal y de quimioterapia.
ResultadosLa estimación de la mediana de supervivencia fue del 77%, de mortalidad por cáncer fue del 18% y por otras causas fue del 5%. La media de reducción absoluta del riesgo (RAR) de mortalidad con tratamiento hormonal fue del 4%, con quimioterapia fue del 4,5% y con tratamiento combinado fue del 7%.
Todas las pacientes con algún beneficio decidieron recibir tratamiento hormonal. Cuarenta y tres pacientes (65%) decidieron recibir quimioterapia y 23 pacientes (35%) decidieron no recibirla. La media de reducción del riesgo con quimioterapia fue del 2% en quien decidió no recibir quimioterapia y fue del 8% en quien decidió recibirla. Existe asociación entre la decisión de quimioterapia y la estimación del riesgo de mortalidad por cáncer (p=0,0001), del riesgo de mortalidad por otras causas (p=0,038) y de la RAR (p=0,0001). El 6% de las pacientes con RAR del 1%, el 50% de las que tenían RAR entre el 2–5%, y el 61,8% con RAR entre el 6–10% eligieron la quimioterapia.
ConclusionesTodas las mujeres optan por el tratamiento hormonal independientemente del beneficio. Las razones para elegir la quimioterapia fueron el propio pronóstico vital y la magnitud del beneficio. Algunas pacientes deciden elegir quimioterapia con beneficios mínimos.
Adjuvant! Online estimates 10-year recurrence and mortality outcomes for breast cancer patients and predicts the effect of each type of treatment. Our purpose was to test the applicability by only analysing mortality estimations.
MethodWe present estimations of 66 women with definitive surgery and axillary staging for unilateral, unicentric, invasive adenocarcinoma, without metastatic or residual disease. Age, co-morbidity, estrogen receptor status, histological grade, tumor size, number of positive nodes, and hormone therapy or chemotherapy option, were the variables required.
ResultsMedian of survival estimations was 77%, cancer mortality 18% and mortality for other reasons 5%. The average of absolute risk reduction (ARR) with hormone therapy was 4%, with chemotherapy 4.5% and with combined treatment 7%.
All the patients with some benefit decided to receive hormone therapy. Forty-three patients (65%) decided to receive chemotherapy and 23 (35%) did not. The average risk reduction with chemotherapy was 2% in those who decided not to receive chemotherapy and 8% in those who decided to receive it. There was an association between a chemotherapy decision and the estimation of the risk of breast cancer mortality (P=0.0001), risk of mortality for other reasons (P=0.038), and the ARR (P=0.0001). There were 6% of the patients with an ARR of 1%, 50% between 2–5% and 61.8% between 6–10%, who chose chemotherapy.
ConclusionsAll women opted for hormone therapy regardless of benefit. The reasons for choosing chemotherapy were the prognosis itself and the magnitude of benefit. Some patients decided to choose chemotherapy even when the benefit was minimal.
La finalidad de la herramienta de ayuda en la toma de decisiones Adjuvant! Online es ayudar a los profesionales de la salud y a sus pacientes con cáncer de mama a discutir los riesgos y los beneficios de recibir un tratamiento adicional tras la cirugía (quimioterapia o tratamiento hormonal adyuvantes, o ambas). Se trata de una aplicación informática de libre acceso en Internet que calcula el riesgo de recidiva y de muerte a 10 años sin ningún tratamiento adyuvante. Realiza también estimaciones sobre la reducción absoluta de este riesgo al recibir quimioterapia, tratamiento hormonal o ambas. Estas estimaciones están basadas en las características de cada paciente y de su tumor mamario y se presentan en forma de gráfico1,2. El modelo se ha validado, la comunidad de oncólogos clínicos lo consultan ampliamente, y se ha demostrado que influye en las decisiones de tratamiento sistémico adyuvante de las pacientes con cáncer de mama3.
La supervivencia global se considera el estándar de oro de los resultados de salud de pacientes con cáncer. La supervivencia libre de enfermedad puede estar condicionada por episodios (segundo cáncer de mama o recidiva local) con escasa repercusión en la supervivencia global2. El objetivo del presente trabajo es analizar la aplicabilidad de un formato simplificado de la herramienta y presentar a las pacientes únicamente las estimaciones de supervivencia global.
Material y métodosSe trata de un estudio prospectivo y descriptivo de una serie de casos de pacientes llevado a cabo entre enero de 2008 y mayo de 2009. Durante el proceso de decisión de tratamiento sistémico adyuvante hemos presentado la estimación de riesgo de mortalidad a 10 años, mediante Adjuvant! Online, versión 8.0, a 66 pacientes con carcinoma infiltrante de mama unilateral y unicéntrico a las que se les había realizado una cirugía mamaria y una estadificación quirúrgica axilar sin enfermedad residual y en las que no había evidencia de enfermedad metastásica. En todas se disponía de la información requerida en el programa informático Adjuvant! Online y otorgaron su consentimiento informado para recibir información acerca de su pronóstico vital y de los beneficios obtenidos con las diferentes opciones de tratamiento. Las variables requeridas por el programa informático fueron la edad, la comorbilidad (salud perfecta, problemas menores, media para la edad y problemas mayores), receptores de estrógenos (positivos o negativos), el grado histológico (1, 2 o 3), el tamaño del tumor (0,1–1cm; 1,1–2cm; 2,1–3cm; 3,1–5cm, y mayor de 5cm), ganglios con metástasis (0; 1–3; 4–9 y >9), el tipo de tratamiento hormonal (tamoxifeno durante 5 años, inhibidor de aromatasa durante 5 años, tamoxifeno durante 2–3 años seguido de inhibidor de aromatasa durante 2–3 años, ablación ovárica y ablación ovárica más tamoxifeno) y el tipo de quimioterapia (regímenes de primera, segunda y tercera generación).
El análisis estadístico de los datos se realizó con el programa SPSS® versión 14.0. En la estadística descriptiva se realizó una distribución de frecuencias de las variables categóricas y las medidas de tendencia central y de dispersión de las cuantitativas. Para estudiar las diferencias entre las variables se utilizó, en el caso de las cualitativas, el test de la t de Student para la comparación de 2 grupos (o ANOVA para más de 2 grupos) y, en el caso de las variables cuantitativas, la correlación de Pearson (o correlación de Spearman en el análisis de grupos pequeños de pacientes). Se consideraron significativas las diferencias con un valor de p≤0,05.
ResultadosLa mediana de edad fue 55 años (27–70). En cuanto a la morbilidad previa, 53 pacientes (80%) tenían salud perfecta, 8 pacientes (12%) tenían problemas menores y 5 pacientes (8%) tenían problemas mayores. Los receptores hormonales fueron positivos en 56 casos (85%) y fueron negativos en 10 casos (15%). El tamaño tumoral fue entre 0,1–1cm en 10 mujeres (15%), entre 1,1–2cm en 30 mujeres (46%), de entre 2,1–3cm en 14 mujeres (21%), entre 3,1–5cm en 11 mujeres (17%) y mayor de 5cm en una mujer (1%). Cuarenta y tres pacientes (65%) tenían axila negativa, 17 pacientes (26%) presentaban 1–3 ganglios positivos, 5 pacientes (8%) presentaban 4–9 ganglios positivos y una paciente (1%) presentaba más de 9 ganglios positivos.
A 18 pacientes (27%) se les propuso tamoxifeno adyuvante, a 21 pacientes (32%) se les propuso inhibidores de aromatasa, a 16 pacientes (24%) se les propuso tamoxifeno seguido de inhibidor de aromatasa y a una paciente (1%) se le propuso ablación ovárica más tamoxifeno. A 12 pacientes (18%) se les propuso quimioterapia adyuvante de primera generación, a 48 pacientes (73%) se les propuso quimioterapia adyuvante de segunda generación y a 6 pacientes (9%) se les propuso quimioterapia adyuvante de tercera generación. A 36 pacientes (55%) se les propuso una combinación de tratamiento hormonal y quimioterapia.
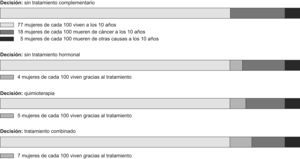
Las estimaciones a 10 años arrojaron una mediana de supervivencia del 77% (22–95), de mortalidad por cáncer de mama del 18% (1–77) y de mortalidad por otras causas del 5% (1–47). La media de reducción absoluta del riesgo (RAR) de mortalidad con tratamiento hormonal fue del 4% (0–14), con quimioterapia fue del 4,5% (0–29) y con tratamiento combinado fue del 7% (0–40) (fig. 1).
Con las estimaciones descritas, todas las pacientes con algún beneficio decidieron recibir tratamiento hormonal, 43 pacientes (65%) decidieron recibir quimioterapia y 23 pacientes (35%) decidieron no recibirla.
La media de RAR de mortalidad con quimioterapia fue del 2% (desviación estándar de 2,5) en las que decidieron no recibir quimioterapia y fue del 8% (desviación estándar de 5,5) en las que sí decidieron recibirla. La decisión de elegir quimioterapia no estuvo condicionada por la edad (p=0,24) ni por la estimación de supervivencia global (p=0,18). Existió asociación estadísticamente significativa entre la decisión de elegir quimioterapia y la estimación del riesgo de mortalidad por cáncer de mama (p=0,0001); también entre esta decisión y el riesgo de mortalidad por otras causas (p=0,038). Por último, la decisión de elegir quimioterapia estuvo también condicionada por la RAR de mortalidad (p=0,0001). De esta forma, el 6% de las pacientes con RAR de mortalidad de sólo el 1% eligió quimioterapia, también la eligió el 50% de las que tenían RAR de mortalidad entre el 2–5% y la eligió el 61,8% con RAR de mortalidad entre el 6–10%.
DiscusiónEl análisis de la influencia de las estimaciones de mortalidad generadas por Adjuvant! Online sobre las decisiones de las pacientes en un contexto asistencial concreto es importante porque nos permite conocer las motivaciones y las interpretaciones que realizan las mujeres. Sin duda, las características del tratamiento hormonal (vía oral, escasa toxicidad aguda y buena tolerancia a largo plazo) es la causante de que todas las mujeres opten por recibirlo independientemente de la magnitud del beneficio4.
El equilibrio entre el beneficio y los efectos secundarios constituye el principal escollo para la decisión de quimioterapia adyuvante, sobre todo en el subgrupo de pacientes con ganglios negativos y enfermedad sensible a las hormonas5. Poco es conocido acerca del efecto de las herramientas de ayuda en la toma de decisiones sobre la elección del tratamiento quimioterápico. Es conocido que en América la mayoría de las pacientes eligen la quimioterapia a pesar de obtener mínimos beneficios en la supervivencia, lo que refleja el deseo de la mayoría de prevenir la mortalidad a pesar de los efectos secundarios de este tratamiento6. En nuestro estudio detectamos 2 modos diferentes de decisión. Por una parte, hay pacientes que eligen la quimioterapia a pesar de obtener beneficios mínimos (el 6% de las que obtienen un beneficio del 1% de mortalidad a 10 años la elige). Por otra parte, hay pacientes que la rechazan a pesar de obtener un beneficio significativo (el 38% de las que obtienen un beneficio entre el 6–10% de mortalidad a los 10 años la rechaza). Las principales motivaciones de las pacientes para la elección de la quimioterapia fueron su propio pronóstico vital, tanto a causa del cáncer de mama como por su comorbilidad y la magnitud del beneficio con este tratamiento.
A pesar de todo, los clínicos que usan Adjuvant! Online deben ser conscientes de sus limitaciones e inconvenientes. Una de las incertidumbres es la validación de las estimaciones en nuestro medio. Recientemente Adjuvant! Online se ha validado en una larga serie europea. La aplicación informática predijo de forma segura los resultados de supervivencia a los 10 años en una serie holandesa de 5.380 pacientes, aunque los resultados fueron menos seguros en algunos subgrupos, como el de las pacientes menores de 40 años7. Otra de las limitaciones deriva del desconocimiento de la verdadera efectividad de la comunicación establecida entre oncólogos y pacientes tras la presentación de las estimaciones pronósticas con Adjuvant! Online. Dos recientes estudios demuestran que pocas pacientes son capaces de mejorar su nivel de información y de recordar su pronóstico a la salida de la consulta8,9.
En la actualidad, los autores están analizando el impacto en las decisiones de tratamiento adyuvante mediante la presentación conjunta de las estimaciones de supervivencia global y libre de enfermedad.
FinanciaciónLos Dres. José Manuel Baena y Esperanza Arriola han recibido financiación del Fondo de Investigaciones Sanitarias (FIS 07/0141).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.