La cirugía cardiaca mínimamente invasiva sobre la válvula mitral ha crecido en popularidad. El objetivo del estudio es valorar la morbilidad y eficacia de la técnica a medio plazo en una serie inicial.
Material y métodos212 pacientes fueron sometidos a cirugía sobre la válvula mitral entre los años 2009 y 2013; 44 mediante cirugía mínimamente invasiva por toracotomía y 168 por esternotomía media. Se realizó un emparejamiento estadístico para la obtención del grupo control por regresión logística y nivelación del grado de propensión considerando las principales variables de riesgo. Se registró la morbilidad y calidad de la reparación o sustitución. Se realizó un análisis univariante y multivariante para un evento compuesto de morbimortalidad, eficacia y requerimientos de hemoderivados.
ResultadosFueron incluidos 44 pacientes por grupo. La media de seguimiento fue de 26,6 (14,6) y 28,4 (1,1) meses en el grupo de estudio y control, respectivamente. Se realizó reparación de la válvula mitral en el 70,5% en el grupo estudio y en el 68,2% en el grupo control. No se encontraron diferencias en la morbimortalidad perioperatoria. El número de pacientes que desarrollaron insuficiencia mitral moderada o severa durante el seguimiento fue del 9,1% en el grupo estudio y 11,4% en el control (p=1,0). Tanto en el análisis univariante como multivariante la cirugía mínimamente invasiva fue un predictor independiente de menor transfusión.
ConclusiónLa cirugía mínimamente invasiva no es inferior a la esternotomía en morbilidad hospitalaria, ni en la calidad de la técnica quirúrgica en un programa de iniciación.
Minimally-invasive mitral valve cardiac surgery has become increasingly popular. The objective of this study is to assess morbidity and efficiency of the technique in the medium run in an initial series.
Material and methods212 patients underwent mitral valve surgery between 2009 and 2013; 44 with minimally-invasive thoracotomy and 168 via median sternotomy. Statistical pairing was conducted to obtain the control group by means of logistic regression and propensity score matching considering the main risk variables. Morbidity and repair or replacement quality were registered. A univariate and multivariate analysis was carried out for an event comprising morbidity and mortality, efficiency and blood component requirements.
ResultsEach group included 44 patients. Average follow-up time was 26.6 (14.6) and 28.4 (1.1) months in the study group and control group respectively. Mitral valve repair was performed in 70.5% of patients in the study group and in 68.2% of patients in the control group. No differences were found in perioperative morbidity and mortality. The number of patients who developed moderate or severe mitral insufficiency during follow-up was 9.1% in the study group and 11.4% in the control group (p=1.0). Minimally-invasive surgery was an independent predictor for lower transfusion in both the univariate and multivariate analyses.
ConclusionMinimally-invasive surgery is not inferior to sternotomy in hospital morbidity or in the quality of surgical technique in an initial program.
El abordaje más utilizado en la cirugía de la válvula mitral es la esternotomía media (CEM) que permite una adecuada exposición del corazón y de los grandes vasos. En la segunda mitad de los años noventa del siglo pasado se desarrollaron abordajes menos invasivos para acceder a la válvula mitral, siguiendo la filosofía de minimizar el traumatismo quirúrgico a través de incisiones pequeñas. La cirugía cardiaca mínimamente invasiva introduce cambios alternativos en la canulación, como el empleo de cánulas arteriales y venosas pequeñas y no colapsables que, combinadas con la aplicación de presión negativa, permiten maximizar el drenaje a través de incisiones pequeñas, en el pinzamiento aórtico, traducido en pinzamiento endovascular o externo y en la administración de la cardioplejía1.
Los objetivos comunes son una reparación o recambio valvular mitral efectivo y seguro, con una reducción del trauma quirúrgico que logre disminuir el dolor, acelere la recuperación postoperatoria y la incorporación a la vida diaria2,3 y por ende, reduzca la estancia hospitalaria y el consumo de recursos4 y, además, mejore los resultados estéticos y la satisfacción del paciente5.
Por otra parte, los cambios en las indicaciones quirúrgicas, motivados por un mejor conocimiento de la historia natural de la insuficiencia mitral funcional o degenerativa, y el aumento en el número de reparaciones mitrales, hacen que la indicación de la cirugía sea más precoz en pacientes con insuficiencia mitral severa asintomáticos6.
A pesar de la difusión de estas técnicas y de la adopción por parte de algunos grupos como estándar (“standard of care”)1, hay pocos estudios clínicos aleatorizados7,8 que comparen el abordaje mínimamente invasivo mediante minitoracotomía (CMI) con la CEM por la dificultad para homogeneizar los grupos de comparación. Dado que los resultados de la literatura corresponden a datos observacionales de las grandes series y a centros con alto volumen de intervenciones, es necesario contrastarlos con los resultados de los grupos incipientes y centros de menor volumen para establecer los beneficios y riesgos de la generalización de este nuevo abordaje.
El objetivo de este trabajo es valorar la morbilidad y eficacia de la técnica quirúrgica a corto y medio plazo en una serie inicial de pacientes sometidos a CMI sobre válvula mitral y compararla con la CEM.
Material y métodosEl estudio fue aprobado por el comité de investigación y ética de nuestro centro. Se recogieron de manera retrospectiva los datos de una serie consecutiva de pacientes sometidos a cirugía sobre la válvula mitral, bien recambio valvular o bien reparación, asociada o no a reparación tricuspídea, entre los años 2009-2013. Los datos fueron extraídos de los datos recogidos prospectivamente en la base de datos Palex Data (Palex Medical, Barcelona, España) del servicio de cirugía cardiaca.
En el grupo de estudio fueron incluidos todos los pacientes mayores de 18 años, programados y sometidos a CMI vía minitoracotomía sobre la válvula mitral (con o sin plastia tricuspídea) por enfermedad degenerativa o reumática, desde la incorporación de este programa a las técnicas quirúrgicas de dicho servicio entre los años 2009 a 2013.
Se realizó un emparejamiento estadístico para la obtención del grupo control por técnicas de regresión logística y nivelación del grado de propensión, considerando las principales variables de riesgo perioperatorio y comorbilidad para identificar los controles adecuados dentro del grupo de CEM. Dichas variables incluyeron: edad, sexo, Euroscore logístico 1, índice de masa corporal, hipertensión arterial, diabetes mellitus, enfermedad pulmonar obstructiva, enfermedad vascular periférica, enfermedad neurológica, disfunción renal preoperatoria, hipertensión pulmonar, clase funcional según la NYHA, reintervención cardiaca, etiología de la valvulopatía mitral y antecedentes de cardiopatía isquémica previa (Anexo 1).
Se aplicaron los siguientes criterios de exclusión: pacientes sometidos a cirugía valvular mitral a la que se asociaba otro procedimiento quirúrgico (revascularización coronaria, cirugía sobre la válvula aórtica o pulmonar o sobre la aorta torácica, o asociación de cirugía de ablación de la FA), reintervenciones cardiacas, procedimientos urgentes y cirugía valvular mitral por patología secundaria funcional.
Técnica quirúrgica. La CMI, en nuestro centro, se realiza mediante una incisión torácica de 5-7cm. en el hemitórax derecho a nivel del quinto espacio intercostal y en la línea medio-clavicular. La circulación extracorpórea (CEC) se instaura a través de la canulación periférica por la arteria femoral derecha (cánula de 18-20 F) y vena femoral derecha (cánula de 21-23F) y canulación de la vena yugular interna derecha (cánula de 18F). Una vez establecida la CEC se realiza el pinzamiento aórtico mediante clampaje transtorácico externo y se administra cardioplejía anterógrada fría a través de aguja, repitiendo la dosis cada 20 minutos. Tras el inicio de la CEC se administra CO2 con un flujo de 2-4 litros/min. en el campo quirúrgico con el fin de facilitar el purgado del aire intracavitario al despinzar la aorta.
La instauración del bypass cardiopulmonar difiere poco de la CEM. Pueden presentarse limitaciones al flujo por el tamaño más pequeño de las cánulas periféricas. La inserción de una cánula adicional al circuito, aunque excepcional, puede ser necesaria si las presiones y resistencias en la línea arterial son elevadas. Las dosis de heparina para la anticoagulación durante la CEC son igual en la CMI que en la CEM con la diferencia de que en nuestro centro en la CMI la heparina es administrada vía intravenosa por el anestesiólogo responsable y en la CEM es administrada intracardiaca por el cirujano. El nivel objetivo de tiempo de coagulación activada (ACT) es idéntico en ambos casos, con rangos>300 segundos.
Técnica anestésica. La inducción de la anestesia se llevaba a cabo con midazolam, fentanilo, propofol y cisatracurio o rocuronio como bloqueante neuromuscular. Como técnica de mantenimiento se empleó sevoflurano y perfusión endovenosa de remifentanilo, así como cloruro mórfico como analgesia para el postoperatorio inmediato.
Desde el inicio de la cirugía se procedía a la ventilación unipulmonar con bloqueo del pulmón derecho. El método para lograr la ventilación unipulmonar es la inserción de un tubo de doble luz izquierdo o un tubo endotraqueal y bloqueadores bronquiales guiados por fibrobroncoscopia.
La monitorización hemodinámica consistió en la medición de la presión arterial invasiva, presión venosa central, ecocardiografía transesofágica (ETE), oximetría de pulso, electrocardiograma con 5 derivaciones y análisis computarizado del segmento ST. Se determinó la temperatura nasofaríngea y diuresis horaria. La monitorización respiratoria incluyó CO2 teleespiratorio (ETCO2), concentración inspiratoria y espiratoria del sevoflurano y espirometría con volúmenes y presiones en la vía aérea. La profundidad anestésica se monitorizó mediante el índice biespectral (BIS, Covidien, Boulder CO, EEUU) y el metabolismo cerebral mediante la saturación regional de oxígeno cerebral a nivel de región temporal derecha o izquierda (INVOS, Covidien, Boulder CO, EEUU). Se utilizó sistemáticamente la ETE como monitorización semiinvasiva en los procedimientos de CMI. La monitorización ecocardiográfica ocupa un lugar relevante en la CMI ya que la visibilidad del cirujano de las cámaras cardiacas y los grandes vasos es muy limitada. También es útil como asistencia para la colocación de las cánulas mediante la visualización de las guías y la posición definitiva de las cánulas, así como la colocación del clamp aórtico y la administración de cardioplejía.
Se analizó la morbilidad perioperatoria durante el ingreso hospitalario, la mortalidad quirúrgica durante el ingreso hospitalario y a los 30 días de cualquier causa y estancia hospitalaria. Se registró la supervivencia al año y durante el período de seguimiento, así como la recurrencia de insuficiencia mitral o disfunción protésica durante el seguimiento. Las definiciones se recogen en el Anexo 1. Se crearon tres variables compuestas: morbimortalidad mayor (que incluyó mortalidad, complicaciones cardiacas mayores, respiratorias, renales y neurológicas), transfusión de derivados hemáticos (requerimiento de concentrados de hematíes, plaquetas o plasma fresco congelado) y eficacia de la técnica quirúrgica (definida como período libre de nueva intervención quirúrgica sobre dicha válvula o de insuficiencia mitral con grado igual o mayor que moderado y de complicaciones derivadas de la válvula protésica o de la reparación como: la trombosis, la endocarditis, la dehiscencia y la fuga periprotésica, etc).
Análisis estadístico. Se realizó un análisis estadístico entre los casos y los controles emparejados para: las variables descriptivas, mortalidad y morbilidad mayor perioperatoria, eficacia, requerimientos transfusionales y estancia hospitalaria. Los datos descriptivos se expresan como porcentajes y media (DE) o mediana (rango intercuartílico). Se realizó, así mismo, un análisis univariante y multivariante para los eventos compuestos de morbilidad mayor, eficacia y requerimientos de hemoderivados para la detección de predictores independientes. Se aceptó un nivel previo de significación de p<0,2 en el análisis univariante para entrar en el modelo multivariante. Los resultados obtenidos por regresión logística binaria mediante método progresivo (stepwise method) se expresan como coeficiente de regresión (B), nivel de significación del coeficiente de regresión y la razón de verosimilitud (odds ratio, OR) predicha, con un intervalo de confianza del 95% para cada una de las variables introducidas en el modelo de estudio.
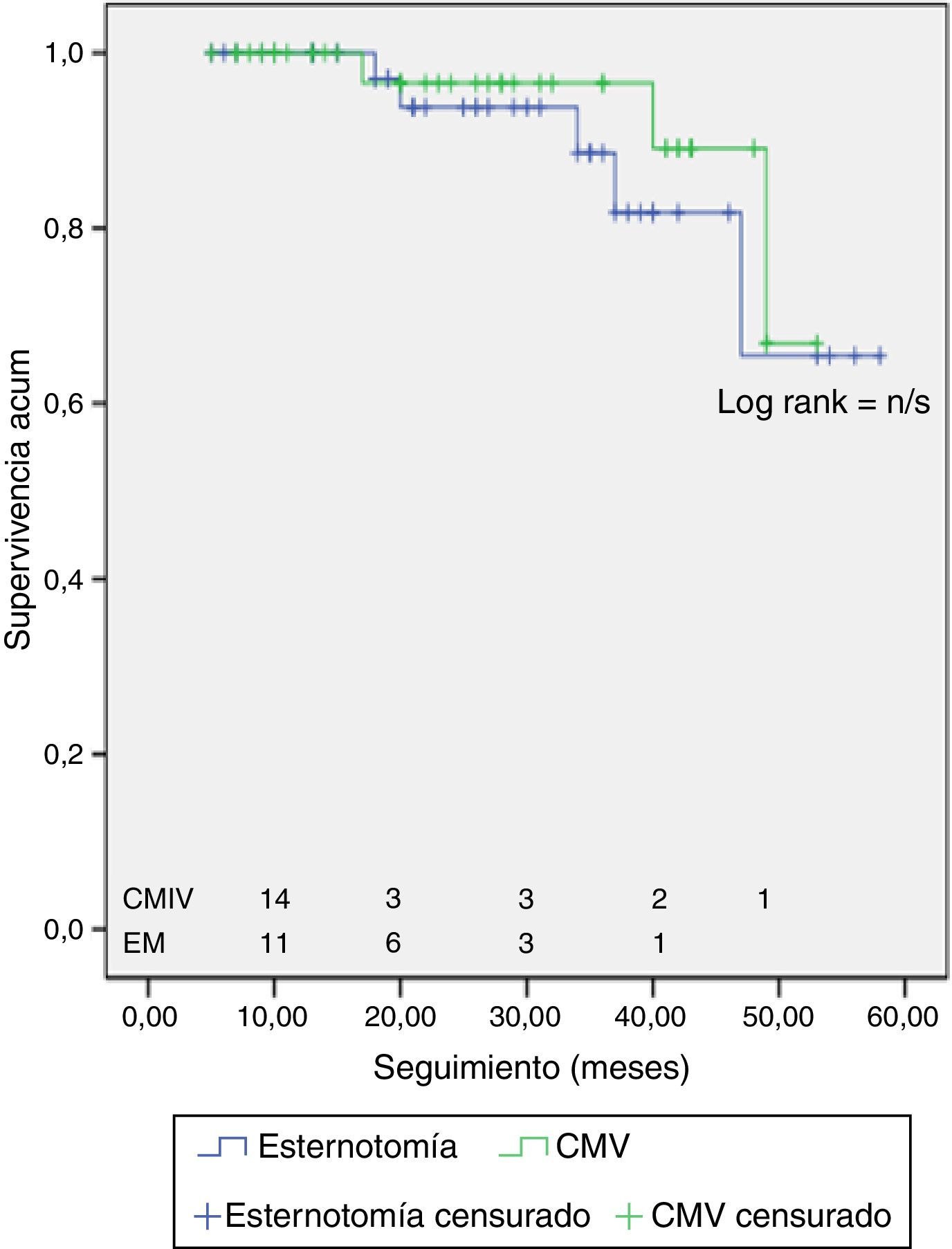
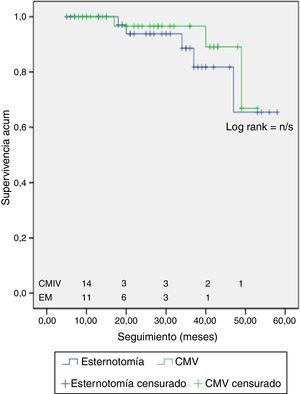
Se utilizaron el método de curvas de supervivencia de Kaplan Meier y el test log-rank para encontrar diferencias entre los grupos en la supervivencia libre de enfermedad, definida como ausencia de insuficiencia mitral igual o mayor que moderada, o necesidad de reintervención por disfunción de la reparación o de la válvula a largo plazo.
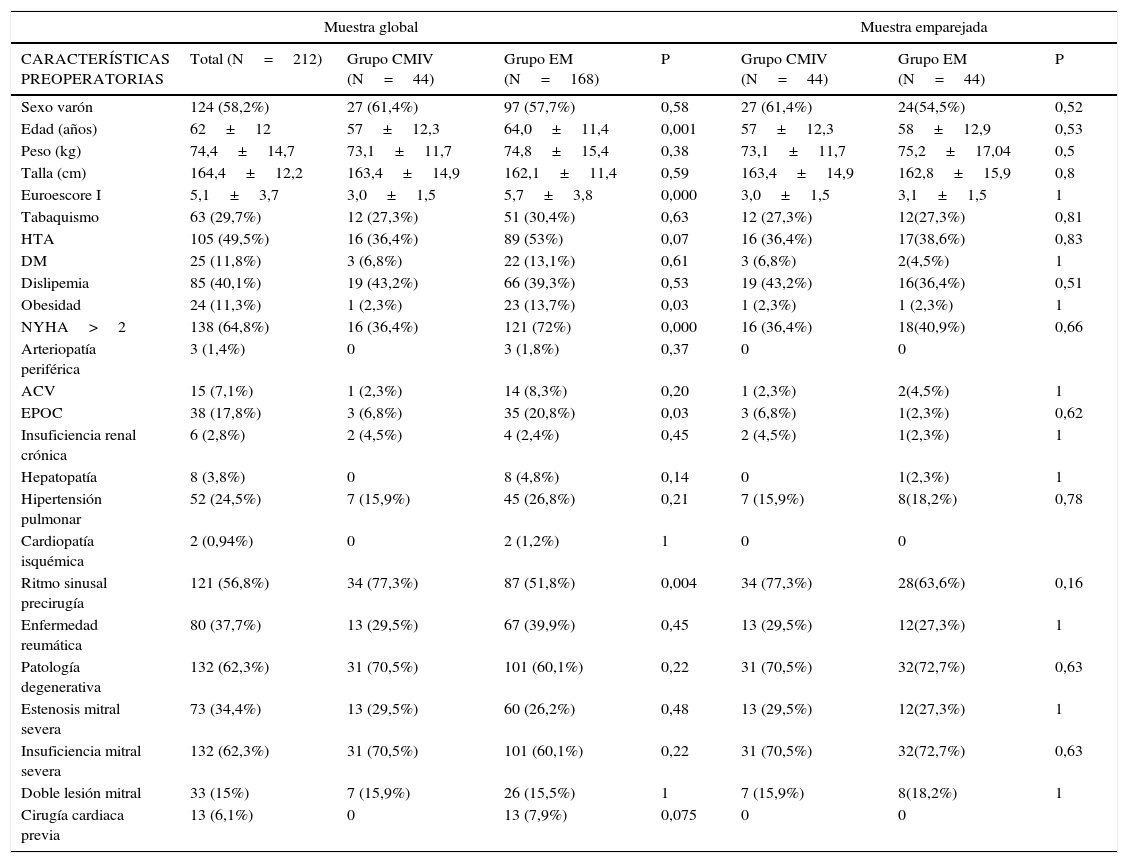
ResultadosSe analizaron 212 pacientes sometidos a cirugía sobre la válvula mitral. Cuarenta y cuatro procedimientos se realizaron mediante CMI y 168 se realizaron por CEM. La bondad de ajuste del método fue evaluado por el test de Hosmer-Lemeshow, que resultó no significativo (p=0,31). La capacidad discriminativa del modelo fue evaluada mediante una curva de característica operativa del receptor (COR), contrastando la probabilidad de pertenecer al grupo de CMI de acuerdo a la regresión logística, frente a la ubicación real de cada caso en cada grupo. Resultó en un área bajo la curva de 0,83 (IC95% 0,79-0,89). Las características preoperatorias se muestran en la tabla 1.
Características preoperatorias de la población de estudio
| Muestra global | Muestra emparejada | ||||||
|---|---|---|---|---|---|---|---|
| CARACTERÍSTICAS PREOPERATORIAS | Total (N=212) | Grupo CMIV (N=44) | Grupo EM (N=168) | P | Grupo CMIV (N=44) | Grupo EM (N=44) | P |
| Sexo varón | 124 (58,2%) | 27 (61,4%) | 97 (57,7%) | 0,58 | 27 (61,4%) | 24(54,5%) | 0,52 |
| Edad (años) | 62±12 | 57±12,3 | 64,0±11,4 | 0,001 | 57±12,3 | 58±12,9 | 0,53 |
| Peso (kg) | 74,4±14,7 | 73,1±11,7 | 74,8±15,4 | 0,38 | 73,1±11,7 | 75,2±17,04 | 0,5 |
| Talla (cm) | 164,4±12,2 | 163,4±14,9 | 162,1±11,4 | 0,59 | 163,4±14,9 | 162,8±15,9 | 0,8 |
| Euroescore I | 5,1±3,7 | 3,0±1,5 | 5,7±3,8 | 0,000 | 3,0±1,5 | 3,1±1,5 | 1 |
| Tabaquismo | 63 (29,7%) | 12 (27,3%) | 51 (30,4%) | 0,63 | 12 (27,3%) | 12(27,3%) | 0,81 |
| HTA | 105 (49,5%) | 16 (36,4%) | 89 (53%) | 0,07 | 16 (36,4%) | 17(38,6%) | 0,83 |
| DM | 25 (11,8%) | 3 (6,8%) | 22 (13,1%) | 0,61 | 3 (6,8%) | 2(4,5%) | 1 |
| Dislipemia | 85 (40,1%) | 19 (43,2%) | 66 (39,3%) | 0,53 | 19 (43,2%) | 16(36,4%) | 0,51 |
| Obesidad | 24 (11,3%) | 1 (2,3%) | 23 (13,7%) | 0,03 | 1 (2,3%) | 1 (2,3%) | 1 |
| NYHA>2 | 138 (64,8%) | 16 (36,4%) | 121 (72%) | 0,000 | 16 (36,4%) | 18(40,9%) | 0,66 |
| Arteriopatía periférica | 3 (1,4%) | 0 | 3 (1,8%) | 0,37 | 0 | 0 | |
| ACV | 15 (7,1%) | 1 (2,3%) | 14 (8,3%) | 0,20 | 1 (2,3%) | 2(4,5%) | 1 |
| EPOC | 38 (17,8%) | 3 (6,8%) | 35 (20,8%) | 0,03 | 3 (6,8%) | 1(2,3%) | 0,62 |
| Insuficiencia renal crónica | 6 (2,8%) | 2 (4,5%) | 4 (2,4%) | 0,45 | 2 (4,5%) | 1(2,3%) | 1 |
| Hepatopatía | 8 (3,8%) | 0 | 8 (4,8%) | 0,14 | 0 | 1(2,3%) | 1 |
| Hipertensión pulmonar | 52 (24,5%) | 7 (15,9%) | 45 (26,8%) | 0,21 | 7 (15,9%) | 8(18,2%) | 0,78 |
| Cardiopatía isquémica | 2 (0,94%) | 0 | 2 (1,2%) | 1 | 0 | 0 | |
| Ritmo sinusal precirugía | 121 (56,8%) | 34 (77,3%) | 87 (51,8%) | 0,004 | 34 (77,3%) | 28(63,6%) | 0,16 |
| Enfermedad reumática | 80 (37,7%) | 13 (29,5%) | 67 (39,9%) | 0,45 | 13 (29,5%) | 12(27,3%) | 1 |
| Patología degenerativa | 132 (62,3%) | 31 (70,5%) | 101 (60,1%) | 0,22 | 31 (70,5%) | 32(72,7%) | 0,63 |
| Estenosis mitral severa | 73 (34,4%) | 13 (29,5%) | 60 (26,2%) | 0,48 | 13 (29,5%) | 12(27,3%) | 1 |
| Insuficiencia mitral severa | 132 (62,3%) | 31 (70,5%) | 101 (60,1%) | 0,22 | 31 (70,5%) | 32(72,7%) | 0,63 |
| Doble lesión mitral | 33 (15%) | 7 (15,9%) | 26 (15,5%) | 1 | 7 (15,9%) | 8(18,2%) | 1 |
| Cirugía cardiaca previa | 13 (6,1%) | 0 | 13 (7,9%) | 0,075 | 0 | 0 | |
Datos como media (DE) o número de pacientes o valor (%).
HTA: Hipertensión arterial. DM: Diabetes mellitus. FA: Fibrilación auricular. EPOC: Enfermedad pulmonar obstructiva crónica. ACV: Accidente cerebrovascular. NYHA: Clase funcional de la New York Heart Association. Art periférica: Arteriopatía periférica. CMIV: Cirugía cardiaca mínimamente invasiva. EM: Esternotomía media.
La etiología de la valvulopatía mitral basal en ambos grupos no fue diferente. La enfermedad reumática supuso el 29,5% del grupo de CMI y en el 27,3% del grupo de CEM, p=1,0. La patología degenerativa constituyó la entidad principal en 31 pacientes (70,5%) en el grupo CMI, frente 32 (72,7%) en el grupo CEM, p=0,63.
La cirugía sobre la válvula mitral realizada con más frecuencia fue la cirugía de reparación mitral en 31 pacientes (70,5%) en el grupo de CMI frente a 30 pacientes (68,2%), en el grupo de CEM, p=0,82. La reparación mitral se asoció a anuloplastia en todos los casos. Se llevó a cabo la cirugía concomitante con la valvuloplastia tricuspídea en 6 pacientes (13,6%) frente a 5 pacientes (11,4%), respectivamente, p=0,74 mediante anuloplastia. No hubo conversiones de pacientes programados para CMIV y en los que finalmente se realizara EM. Los tiempos de circulación extracorpórea no fueron estadísticamente diferentes (116,1±24,8 vs. 121,2±35,9, p=0,8) y pinzamiento aórtico (89,3±20,5 vs. 97,3±27,1, p=0,7) entre CMIV vs. EM, respectivamente.
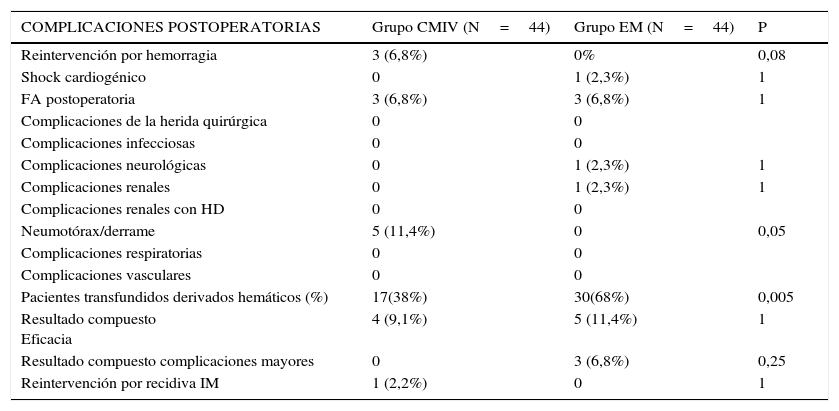
No se hallaron diferencias en relación con las variables preoperatorias o comorbilidad así como en la morbimortalidad perioperatoria, ni en la calidad de la reparación a largo plazo entre los casos de CMI y los controles emparejados de CEM (tabla 2). El seguimiento medio fue de 26,6 (14,6) meses para el grupo de CMI y 28,4 (1,1) meses para la CEM, p=0,63.
Complicaciones perioperatorias
| COMPLICACIONES POSTOPERATORIAS | Grupo CMIV (N=44) | Grupo EM (N=44) | P |
|---|---|---|---|
| Reintervención por hemorragia | 3 (6,8%) | 0% | 0,08 |
| Shock cardiogénico | 0 | 1 (2,3%) | 1 |
| FA postoperatoria | 3 (6,8%) | 3 (6,8%) | 1 |
| Complicaciones de la herida quirúrgica | 0 | 0 | |
| Complicaciones infecciosas | 0 | 0 | |
| Complicaciones neurológicas | 0 | 1 (2,3%) | 1 |
| Complicaciones renales | 0 | 1 (2,3%) | 1 |
| Complicaciones renales con HD | 0 | 0 | |
| Neumotórax/derrame | 5 (11,4%) | 0 | 0,05 |
| Complicaciones respiratorias | 0 | 0 | |
| Complicaciones vasculares | 0 | 0 | |
| Pacientes transfundidos derivados hemáticos (%) | 17(38%) | 30(68%) | 0,005 |
| Resultado compuesto Eficacia | 4 (9,1%) | 5 (11,4%) | 1 |
| Resultado compuesto complicaciones mayores | 0 | 3 (6,8%) | 0,25 |
| Reintervención por recidiva IM | 1 (2,2%) | 0 | 1 |
Datos como número de pacientes (%).
ECO: Ecografía cardiaca. FA: fibrilación auricular. IM: Insuficiencia mitral. CMIV: Cirugía cardiaca mínimamente invasiva. EM: esternotomía media.
No observamos diferencias significativas en el evento compuesto de morbimortalidad mayor (0% frente a 6,8%, p=0,25) y eficacia (9,1% frente a 11,4%, p=1,0) entre la CMI frente CEM, respectivamente. La reoperación por sangrado (6,8% frente a 0%, p=0,08) y la incidencia de neumotórax y derrames pleurales que requirieron drenaje (11,4% frente a 0%, p=0,05) tuvo una incidencia mayor en el grupo de CMI. El número de pacientes que requirieron transfusión fue significativamente menor en el grupo de CMI (38% frente a 59%, p=0,01). El número de concentrados de hematíes [0 (0-9) frente a 1 (0-7), p=0,03] y plasma fresco congelado administrado [0 (0-3) frente a 0 (0-5), p=0,01] fue significativamente menor en el grupo de CMI. No hubo diferencias en el número de unidades de plaquetas trasfundidas [0 (0-1) frente a 0 (0-2), p=0,35].
Los días de estancia en UCI 2,1 (0,9) frente a 2,8 (1,2) días (p=0,001) y de estancia hospitalaria 6 (3,4) frente a 7,2 (2,9) días (p=0,08) fueron menos en el grupo CMI.
La supervivencia acumulada libre de enfermedad o disfunción valvular más que moderada fue del 93% en el grupo CMI frente al 88,4% para el grupo CEM, con una supervivencia, global, de un 90,7% (fig. 1). Un paciente perteneciente al grupo de CMI tuvo que ser sometido a reoperación e implante de prótesis mitral por fracaso de la técnica quirúrgica a los dos años de la primera cirugía consistente en plastia mitral y anuloplastia y otros tres siguen en seguimiento con IM moderada. En el grupo de EM cuatro pacientes siguen en seguimiento con IM moderada tras reparación mitral y otro paciente presenta una fuga periprótesica moderada tras SMV. No se produjo ningún éxitus durante el seguimiento en ninguno de los dos grupos.
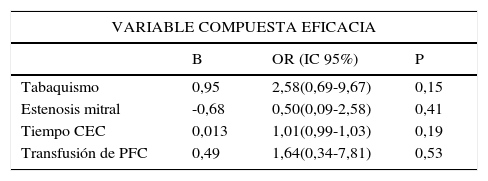
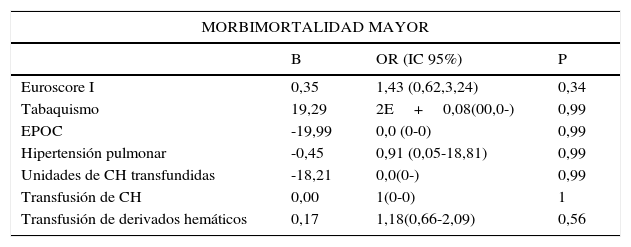
En el análisis univariante y multivariante la técnica quirúrgica mediante CMI o mediante CEM no constituyó un predictor de morbimortalidad mayor, OR 0,65 (IC95% 0,1-4,1, p=0,65), ni de eficacia de la técnica quirúrgica o recambio valvular OR 0,81 (IC95% 0,23-0,88, p=0,74) (tablas 3 y 4). No encontramos predictores estadísticamente significativos para la variable compuesta de eficacia de la técnica quirúrgica.
Análisis multivariante para la variable compuesta de eficacia de la técnica quirúrgica tras seguimiento
| VARIABLE COMPUESTA EFICACIA | |||
|---|---|---|---|
| B | OR (IC 95%) | P | |
| Tabaquismo | 0,95 | 2,58(0,69-9,67) | 0,15 |
| Estenosis mitral | -0,68 | 0,50(0,09-2,58) | 0,41 |
| Tiempo CEC | 0,013 | 1,01(0,99-1,03) | 0,19 |
| Transfusión de PFC | 0,49 | 1,64(0,34-7,81) | 0,53 |
Análisis multivariante para mobimortalidad mayor perioperatoria
| MORBIMORTALIDAD MAYOR | |||
|---|---|---|---|
| B | OR (IC 95%) | P | |
| Euroscore I | 0,35 | 1,43 (0,62,3,24) | 0,34 |
| Tabaquismo | 19,29 | 2E+0,08(00,0-) | 0,99 |
| EPOC | -19,99 | 0,0 (0-0) | 0,99 |
| Hipertensión pulmonar | -0,45 | 0,91 (0,05-18,81) | 0,99 |
| Unidades de CH transfundidas | -18,21 | 0,0(0-) | 0,99 |
| Transfusión de CH | 0,00 | 1(0-0) | 1 |
| Transfusión de derivados hemáticos | 0,17 | 1,18(0,66-2,09) | 0,56 |
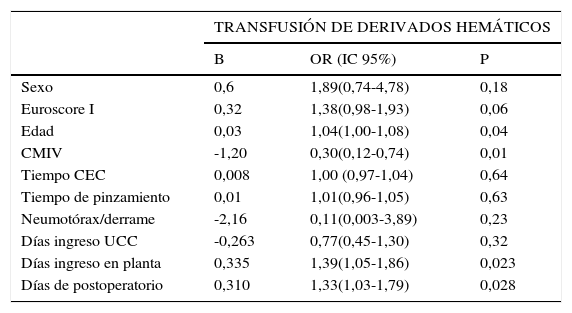
No obstante, la CMI sí resulto ser un predictor de protección para la necesidad de transfusión de derivados hemáticos, OR 0,29 (IC95% 0,12-0,71, p=0,006) y para la transfusión de concentrados de hematíes OR 0,35 (IC95% 0,15-0,85, p=0,02). Además, para la variable resultado transfusión de derivados hemáticos, observamos que la edad, OR 1,03 (IC95% 1,00-1,07, p=0,02), el Euroescore I logístico, OR 1,41 (IC95% 1,05-1,90, p=0,02), la estatura, OR 0,96 (IC95% 0,92-1,0, p=0,05), el tiempo de CEC, OR 1,01 (IC95% 1,00-1,04, p=0,03), los días en sala de hospitalización, OR 1,48 (IC95% 1,10-1,98, p=0,008) y días de ingreso hospitalario, OR 1,33 (IC95% 1,07-1,65, p=0,009), resultaron predictores de transfusión (tabla 5).
Análisis multivariante para la transfusión de derivados hemáticos en el perioperatorio
| TRANSFUSIÓN DE DERIVADOS HEMÁTICOS | |||
|---|---|---|---|
| B | OR (IC 95%) | P | |
| Sexo | 0,6 | 1,89(0,74-4,78) | 0,18 |
| Euroscore I | 0,32 | 1,38(0,98-1,93) | 0,06 |
| Edad | 0,03 | 1,04(1,00-1,08) | 0,04 |
| CMIV | -1,20 | 0,30(0,12-0,74) | 0,01 |
| Tiempo CEC | 0,008 | 1,00 (0,97-1,04) | 0,64 |
| Tiempo de pinzamiento | 0,01 | 1,01(0,96-1,05) | 0,63 |
| Neumotórax/derrame | -2,16 | 0,11(0,003-3,89) | 0,23 |
| Días ingreso UCC | -0,263 | 0,77(0,45-1,30) | 0,32 |
| Días ingreso en planta | 0,335 | 1,39(1,05-1,86) | 0,023 |
| Días de postoperatorio | 0,310 | 1,33(1,03-1,79) | 0,028 |
La CMI ha revolucionado numerosas facetas de la práctica quirúrgica en la cirugía y en la cirugía cardiaca, en particular en las últimas décadas e incluye un número importante de procedimientos. La CMI tiene como objetivo alcanzar mayor seguridad que la cirugía convencional con las ventajas añadidas de minimizar el trauma quirúrgico y mejorar el resultado estético, acelerar la recuperación y acortar la estancia hospitalaria y por tanto los costes.
A pesar de los resultados prometedores obtenidos en grandes instituciones con gran volumen de pacientes, la adopción de las técnicas de CMI aplicadas a la reparación o recambio de válvula mitral no ha sido uniforme en los centros de nuestro ámbito por la limitada exposición de la válvula, las potenciales lesiones arteriales y las dificultades en la deaireación del corazón, que pueden resultar en un incremento de los accidentes cerebrovasculares y la morbilidad global. Además, la información disponible hasta ahora se basa fundamentalmente en: series retrospectivas, metaanálisis9–11 y revisiones de la literatura con dos estudios aleatorizados de pequeño tamaño muestral únicamente7,8. En España no hay publicadas hasta la fecha series que comuniquen sus resultados, ni que los comparen con las técnicas convencionales.
Nuestros resultados muestran que la CMI se asocia a una menor proporción de pacientes transfundidos, menor transfusión de hemoderivados y menor estancia en UCI, sin que esto se asocie a una mayor morbimortalidad perioperatoria, ni a un impacto negativo en la seguridad ni en la duración de la reparación o del recambio valvular.
En las últimas décadas se demandan procedimientos menos invasivos, al mismo tiempo que se debe garantizar la misma seguridad y eficacia de la cirugía. La adopción de cualquier nuevo procedimiento médico o quirúrgico debe ser: analizado y cuantificado para garantizar los estándares de calidad de las técnicas convencionales y su comparabilidad con los centros de mayor experiencia. Hay que destacar que cada vez son más los propios pacientes candidatos a cirugía, los que demandan este tipo de intervención por motivos estéticos.
La literatura ofrece escasa información sobre los resultados a largo plazo en CMI sobre la válvula mitral. Los estudios que lo comunican hacen un seguimiento variable de 1 a 9 años y no muestran diferencias entre los grupos, en términos de: la mortalidad, la calidad de vida, la presencia de disfunción protésica o las fugas perivalvulares, el grado de insuficiencia mitral, el riesgo de endocarditis y/o la reintervención a largo plazo9. Cheng y Cols., comunican una mortalidad al año del 0,9% en el abordaje por CMI frente 1,3% en la CEM (RR 1,07, IC95% 0,19-6,05; dos estudios), a los 3 años de 0,5% en ambos grupos, (RR 1,06, IC95% 0,07-16,79; un estudio) y a los 9 años de 0% frente a 3,7%, (RR 0,19, IC95% 0,01-3,64; un estudio)9.
Recientemente, Goldstone y Cols.12, en un análisis comparativo mediante nivelación del riesgo, compararon los resultados de 201 pacientes sometidos a CMI por patología mitral degenerativa frente a 201 sometidos a CEM. Realizaron un seguimiento de 4,2 años sin hallar diferencias en la supervivencia ni en la durabilidad de la reparación. Obtuvieron una supervivencia acumulada a 1, 5 y 9 años de 96% en cada punto de seguimiento para el grupo de CMI y para el grupo de CEM de 97%, 92% y 89% (p=0,8).
La dificultad técnica añadida a la CMI por la limitada exposición de la válvula mitral, asociada a la curva de aprendizaje inherente a cualquier procedimiento puede llevar asociado un detrimento de la calidad de la reparación o el implante de la válvula. La literatura al respecto ha intentado cuantificar este efecto y en nuestra serie hemos hecho un seguimiento de la funcionalidad de las válvulas reparadas y las prótesis implantadas. Cheng y Cols.9, observaron que no existen diferencias en el grado de la insuficiencia mitral residual entre ambas técnicas, ni en el tiempo libre de reoperación por complicaciones valvulares al año (RR 1,03, IC95% 0,97-1,1; un estudio). No obstante, a los 8 años los pacientes sometidos a CMI presentaron un menor riesgo de ser reintervenidos por problemas de la válvula (RR 1,04, IC95% 1,01-1,08; un estudio)13. Cuando se combinaron los estudios que hacían seguimiento a largo plazo se observó también que los pacientes sometidos a CMIV presentaban menores reintervenciones sobre la válvula mitral (RR 1,04, IC95% 1,01-1,06; tres estudios)13–15.
Raanani y Cols.15 en un estudio restrospectivo no aleatorizado, comunicaron datos similares a los nuestros. Un 3% de los pacientes sometidos a CMI frente a un 5% de CEM (p=0,637) para la reparación mitral por prolapso aislado de velo posterior, necesitaron reintervención por fracaso de la reparación, tras un período de seguimiento medio de 4 años. La supervivencia libre de reintervención fue del 97% frente a 95% (p=0,6). Como en nuestro estudio, no hallaron predictores de reintervención tardía. Por otra parte en el seguimiento a largo plazo, observaron una recurrencia de IM mayor que moderada en el 18% del grupo de CMI frente a 9% de CEM (p=0,11). Los autores afirman en su discusión que esta tendencia a una IM residual tras cirugía subóptima en CMI es el reflejo del inicio de la curva de aprendizaje de su serie.
Otra gran serie de 1.071 pacientes sometidos a CMI por patología mitral degenerativa durante una década, fue publicada por Galloway y Cols.13, con un seguimiento medio de 8 años. Sus tasas de supervivencia libre de reoperación o de recurrencia de IM mayor que moderada fueron del 93% en la CMI frente al 90% en la cirugía convencional (p=0,3). La supervivencia libre de toda complicación relacionada con la válvula fue del 90% frente 86% (p=0,14), respectivamente. Similares resultados obtuvieron McClure y Cols.16, en una serie reciente de 1.000 pacientes sometidos a reparación mitral mediante CMI (75% realizados mediante hemiesternotomía y 25% mediante minitoracotomía). Observaron una incidencia de tiempo libre de recurrencia de IM más que moderada a 1, 5 y 10 años del 99, 87, y 69%, respectivamente.
Los resultados de nuestra serie están en consonancia con la literatura. La supervivencia libre de enfermedad definida como período libre de insuficiencia mitral más que moderada o reintervención relacionada con la válvula mitral fue del 88,4% en la CMI frente a 93% en la CEM (p=1) en el período de seguimiento. No observamos diferencias en los resultados al analizar los períodos estudiados, lo que sugiere que en nuestra serie la experiencia quirúrgica no tuvo un impacto en la calidad de la reparación.
Limitaciones del estudioDada la naturaleza retrospectiva de nuestro estudio no hemos podido analizar la complejidad de la patología mitral (prolapsos aislados posteriores, patología bilateral de ambos velos, endocarditis…) y las características de la reparación, lo cual podría tener un impacto en los resultados a medio y largo plazo.
Hay limitaciones propias de la metodología aplicada basada en el análisis restrospectivo de los datos, aunque los mismos fueron recogidos de forma prospectiva en un único centro. Por ello la generalización y reproducibilidad de estos resultados en otros centros puede estar limitada. El tamaño de la muestra es pequeño, comparado con los grandes centros de Estados Unidos o Europa. Sin embargo, nuestro programa es uno de los que incluye más volumen de pacientes de nuestro medio y hasta el momento no hay series publicadas de la experiencia en España de un programa de CMI y de sus resultados iniciales.
La comparación entre los pacientes sometidos a CIM con respecto a la población global es claramente heterogénea ya que los pacientes sometidos a la cirugía convencional presentaban mayor comorbilidad y por tanto sus resultados son peores. Las técnicas de emparejamiento mediante nivelación del riesgo pretenden homogeneizar las características preoperatorias de forma similar a los estudios randomizados. No obstante, los sesgos de selección no son evitados por completo mediante esta técnica. La complejidad de la valvulopatía mitral y la etiología de la misma no fueron características incluidas en el emparejamiento. Este factor ha podido influir en los resultados de eficacia de la técnica quirúrgica e incidencia de recidiva de la insuficiencia mitral.
Si bien es cierto que la CMI se ha preconizado como alternativa a la CEM en pacientes intervenidos previamente de cirugía cardiaca, en nuestra muestra no incluimos dichos casos. La puesta en marcha de cualquier programa exige la selección de los pacientes de forma cuidadosa y evitamos la introducción de pacientes que podrían añadir complicaciones técnicas.
En conclusión, nuestros resultados muestran que la CMI se asocia a una menor proporción de pacientes transfundidos, menor transfusión de hemoderivados, menor estancia en UCI, sin que esto se asocie a una mayor morbimortalidad perioperatoria, ni a un impacto negativo en la seguridad ni en la perdurabilidad de la reparación o del recambio valvular. Son necesarios estudios con mayor tamaño muestral y aleatorizados para dilucidar las ventajas netas de esta técnica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
AutoríaTodos los autores han participado en su diseño, realización y escritura.
Conflictos de interesesEl doctor Sergio Cánovas es colaborador de Edwards Lifesciences.
Los autores declaran no presentar ningún conflicto de intereses.
- 1.
Datos preoperatorios evaluados
- -
Edad.
- -
Sexo.
- -
Euroscore I logístico.
- -
Hábito tabáquico activo.
- -
Índice de masa corporal.
- -
Presencia de factores de riesgo cardiovascular: hipertensión arterial, dislipemia.
- -
Diabetes mellitus insulinodependiente.
- -
Antecedentes de accidente cerebrovascular.
- -
Enfermedad pulmonar obstructiva crónica en tratamiento prolongado con broncodilatadores o corticoides orales o inhalados.
- -
Episodios previos de insuficiencia cardiaca congestiva.
- -
Cardiopatía isquémica, definida como enfermedad coronaria diagnosticada por coronariografía. Antecedentes de infarto agudo de miocardio o angina inestable con o sin tratamiento de revascularización.
- -
Clase funcional según la NYHA.
- -
Historia de endocarditis. Presencia de endocarditis activa.
- -
Enfermedad vascular periférica, definida por la presencia de claudicación intermitente de miembros inferiores, oclusión mayor al 50% de la arteria carótida, amputación por enfermedad arterial, cirugía previa o prevista sobre la aorta abdominal o las arterias de miembros inferiores.
- -
Insuficiencia renal crónica definida como creatinina preoperatoria>2,2mg/dL y/o necesidad de hemodiálisis preoperatoria.
- -
Hipertensión pulmonar severa definida como hipertensión pulmonar sistólica mayor de 50mmHg.
- -
Deficiencia del sistema inmunológico.
- -
Historia de arritmias ventriculares malignas.
- -
Portador de marcapasos permanente.
Datos de la valvulopatía quirúrgica
- -
Etiología de la valvulopatía mitral: inflamatoria (reumática, esclerosis y secundaria a lupus eritematoso) o degenerativa (deficiencia fibroelástica, enfermedad de Barlow).
- -
Grado de severidad de la lesión mitral.
- -
Cirugía cardiaca previa.
- -
- 2.
Intraoperatorio
- -
Tipo de intervención quirúrgica realizada.
- -
- 3.
Morbimortalidad postoperatoria (ver definiciones en el punto 4)
- -
Mortalidad quirúrgica a los 30 días de cualquier causa o durante el ingreso hospitalario.
- -
Complicaciones clínicas.
- -
Derivados hemáticos transfundidos por paciente (número): concentrados hemáticos, plasma fresco congelado y plaquetas. Se consideró, así mismo, si el paciente fue transfundido o no, como variable categórica.
- -
Estancia hospitalaria (días): Estancia en UCI y hospitalaria.
- -
La evolución y complicaciones a largo plazo fueron definidas de acuerdo a:
- •
Supervivencia al año.
- •
Reingresos hospitalarios durante el primer año.
- •
Período libre de nueva intervención quirúrgica o reaparación de insuficiencia mitral con grado más que moderada.
- •
Complicaciones derivadas de la válvula protésica o de la reparación: trombosis, endocarditis, dehiscencias y fugas periprotésicas, etc.
- •
- -
- 4.
Definición de variables clínicas dependientes o de resultado9
- 4.1.
Mortalidad periprocedimiento, definida como muerte en los primeros 30 días de cualquier causa9. Clasificada como de causa cardiovascular o no cardiovascular.
- *
Muerte de causa cardiovascular:
- o
Muerte de causa cardiaca: infarto de miocardio, taponamiento cardiaco, empeoramiento de la insuficiencia cardiaca.
- o
Muerte de causa no coronaria: eventos neurológicos, tromboembolismo pulmonar, ruptura de aneurisma de aorta, aneurisma disecante u otra patología vascular.
- o
Muertes relacionadas con el procedimiento, incluyendo aquellas relacionadas con cualquier complicación del procedimiento.
- o
Muertes relacionadas con la disfunción valvular.
- o
Muerte súbita o no presenciada.
- o
Muerte de causa desconocida.
- o
- *
Muerte de causa no cardiovascular: relacionada con cualquier otra condición médica (traumatismo, cáncer, suicidio…).
- *
- 4.2.
Definición de infarto de miocardio.
- *
Infarto de miocardio periprocedimiento (en las primeras 72 horas), definido mediante la asociación de algún evento de los siguientes:
- o
Nuevos síntomas de isquemia (dolor torácico típico o disnea) o signos (arritmias ventriculares, empeoramiento de los signos de insuficiencia cardiaca, nuevas alteraciones del segmento ST, inestabilidad hemodinámica, nuevas ondas Q en al menos dos derivaciones contiguas, imagen de pérdida de miocardio viable o nuevas alteraciones de la contractilidad segmentaria.
- o
Elevación de biomarcadores (preferiblemente troponina I y CK-MB) en las primeras 72 horas: elevación en alguna muestra analizada antes de las 72 horas cuyo valor exceda 15 veces el límite superior de normalidad en la troponina I y 5 veces el límite superior en CK-MB. Si los marcadores ya estaban elevados de forma basal por encima del percentil 99, un incremento en al menos el 50% postprocedimiento es necesario para ser considerado positivo.
- o
- *
Infarto de miocardio tras las primeras 72 horas, definido por cualquiera de los siguientes criterios:
- o
Elevación de biomarcadores (preferiblemente troponina I) con al menos uno de los valores por encima del percentil 99 junto con evidencia de isquemia miocárdica definida (ver a continuación).
- o
Síntomas de isquemia.
- o
Cambios en ECG sugestivos de isquemia como nuevo bloqueo de rama izquierda y alteraciones de segmento ST.
- o
Nuevas ondas Q patológicas en al menos dos derivaciones contiguas.
- o
Imagen de pérdida de viabilidad de miocardio o nuevas alteraciones de la contractilidad regional.
- o
Muerte súbita con parada cardiaca precedida de síntomas sugestivos de infarto de miocardio acompañado de presumiblemente elevación de segmento ST o nuevo bloqueo de rama izquierda y evidencia de trombo fresco en coronariografía y/o autopsia.
- o
Hallazgos anatomopatológicos de infarto agudo de miocardio.
- o
- *
- 4.3.
Accidente cerebrovascular, infarto o accidente isquémico transitorio: definidos como disfunción neurológica global o focal causada por la lesión vascular cerebral, espinal o en la retina causada por una hemorragia o infarto. Confirmación del diagnóstico por al menos uno de los siguientes.
- •
Por un neurólogo especialista. Puede ser diagnosticado sólo por signos clínicos
- •
Por técnica de imagen: tomografía computarizada o resonancia magnética.
- •
- 4.4.
Hemorragia que compromete la vida, definida por alguno de los siguientes10: sangrado asociado a un descenso en el nivel de hemoglobina de al menos 3g/dL o que precisa transfusión de 2 o 3 concentrados de hematíes; o que precisa revisión quirúrgica y que no incluya los criterios de sangrado que amenaza la vida.
- 4.5.
Lesión renal aguda11, definida como incremento en la creatinina sérica basal 2 veces el rango basal o creatinina sérica>4mg/dL con un incremento agudo de al menos 0,5mg/dL o gasto urinario<0,3ml/kg/h durante>24horas o anuria durante>12horas, así como pacientes con necesidad de terapia renal sustitutiva.
- 4.6.
Alteraciones de la conducción y arritmias.
- 4.7.
Aparición de fibrilación o flúter auricular.
- 4.8.
Necesidad de marcapasos permanente.
- 4.9.
Aparición de arritmias que condicionen inestabilidad hemodinámica o que precisen terapia.
- 4.10.
Complicaciones pulmonares: intubación prolongada>48 horas, necesidad de traqueostomía, neumonía postoperatoria definida como la presencia de infiltrados pulmonares nuevos o progresivos con signos de infección sistémica (leucocitosis, fiebre), cambios en las características del esputo y detección de un agente microbiológico causal12–14, o síndrome de distrés respiratorio agudo (SDRA)15, definido como hipoxemia (PaO2/FIO2 ≤ 300mmHg), infiltrados pulmonares radiológicos, complianza del sistema respiratorio ≤ 40mL/cm H2O, necesidad de PEEP ≥ 10cm H2O y de un volumen corregido expiratorio por minuto de ≥ 10 L/min.
- 4.11.
Lesiones vasculares mayores: disección aórtica o ruptura aórtica, perforación del ventrículo izquierdo, lesión vascular en puertos de acceso (disección, estenosis, perforación, ruptura, fístula arterio-venosa, hematoma, lesión nerviosa irreversible, síndrome compartimental) que condicione la muerte o hemorragia mayor que amenaza la vida, isquemia visceral o lesiones neurológicas.
- 4.12.
Conversión quirúrgica a esternotomía o ampliación de la toracotomía por alguna complicación relacionada con el procedimiento.
- 4.13.
Reintervención por sangrado quirúrgico o taponamiento durante el postoperatorio inmediato.
- 4.14.
Calidad de la reparación valvular: grado de insuficiencia residual al alta y al seguimiento.
- 4.15.
Calidad del recambio valvular: evaluación de la funcionalidad de la válvula al alta y durante el seguimiento.
- 4.16.
Infección de la herida quirúrgica.
- 4.1.