La disfunción ventricular izquierda en la enfermedad cardíaca isquémica puede ocurrir por aturdimiento, hibernación o necrosis. Las técnicas de imagen cardíaca no invasiva evalúan diferentes objetivos en la identificación de miocardio potencialmente viable, variando en la sensibilidad y especificidad para su identificación, lo que dificulta la extrapolación de estudios de viabilidad miocárdica entre diferentes modalidades. La resonancia magnética cardíaca permite evaluar la viabilidad miocárdica por la respuesta bifásica a la dobutamina, o por la captación de gadolinio en el miocardio ventricular. La técnica más usada es el realce tardío con gadolinio, en el cual se evalúa la transmuralidad de necrosis como factor pronóstico en recuperación de la contractilidad miocárdica.
Left ventricular dysfunction in ischaemic heart disease can occur due to stunning, hibernation, or necrosis. The non-invasive cardiac imaging techniques evaluate different objectives in the identification of potentially viable myocardium, by varying their sensitivity and specificity in order to identify them. This makes it very difficult to extrapolate myocardial viability studies between different modes. Cardiac magnetic resonance can help to evaluate by its biphasic response to dobutamine, or by gadolinium uptake in the ventricular myocardium. The most used technique is the late gadolinium enhancement, in which the transmurality of the necrosis is evaluated as a prognostic factor in the recovery of myocardial contractility.
La falla cardíaca es una enfermedad con alta prevalencia mundial, que se asocia a altas tasas de morbilidad y mortalidad. La etiología más frecuente de la falla cardíaca es la enfermedad coronaria, que puede generar hasta dos tercios de todos los casos1. En el contexto de falla cardíaca asociada a enfermedad coronaria y baja fracción de eyección, la posibilidad de recuperación de la función ventricular es un objetivo terapéutico estratégico, ya que la optimización de la función ventricular posterior a una revascularización podría mejorar el pronóstico de manera significativa. Es aquí donde el concepto de viabilidad miocárdica adquiere importancia, pues denota la presencia de tejido miocárdico disfuncional, aunque no necrosado, y con potencial de recuperar su función contráctil. Este hecho se describió ya en los primeros estudios de revascularización miocárdica quirúrgica desarrollados en la década de los 702, confirmándose en series posteriores controladas3, aunque la metodología empleada para la demostración de viabilidad miocárdica sigue siendo hoy día motivo de debate. Al tener varias técnicas de imagen que evalúan viabilidad miocárdica es importante entender que cada una de ellas se basa en hallazgos diferentes para determinar la presencia de viabilidad. En cardiorresonancia magnética la viabilidad se define como la ausencia de cicatriz isquémica miocárdica en un segmento disfuncionante en pacientes con enfermedad arterial coronaria, mientras que otras técnicas de imagen usan marcadores subrogados para establecer la presencia de miocardio viable sin determinar las características del tejido.
Conceptos en viabilidad miocárdicaLa viabilidad miocárdica es importante en la práctica cardiológica por su significado clínico, ya que es un determinante del pronóstico y de la decisión sobre estrategias de revascularización en los pacientes con disfunción cardiaca isquémica. En la década de los 80 se usó por primera vez el término “miocardio hibernado”4, para referirse a aquel tejido con reducción de su contractilidad en reposo debido a una situación de isquemia crónica, con potencial de recuperación al restaurar el flujo coronario reducido. La reducción de la función contráctil sería la expresión de una regulación a la baja del gasto energético miocárdico, adecuándose a la reducción del flujo sanguíneo. Es importante resaltar que, definido en estos términos, el miocardio hibernado es un diagnóstico retrospectivo, ya que debe cumplir tres criterios: (a) debe de existir una situación de isquemia crónica, con disminución subsecuente de la contractilidad, (b) debe demostrarse recuperación de la contractilidad, y (c) que ésta tenga lugar después de una revascularización efectiva.
Un concepto similar al del miocardio hibernado es el de “aturdimiento miocárdico”, en el que la disfunción contráctil es el resultado de un evento isquémico transitorio, la cual persiste aún por un tiempo después de restaurado el flujo5. Tal fenómeno puede expresarse después de un síndrome coronario agudo revascularizado o, simplemente, tras un episodio de isquemia aguda transitoria y se ha atribuido a la reacción inflamatoria subsecuente al evento isquémico y al propio proceso de reperfusión. Se ha postulado6 que la hibernación miocárdica es el resultado de episodios repetidos de aturdimiento, aunque no hay un límite claro de tiempo para definir cuándo se produce esa conversión, y en la práctica habitual esta diferenciación no es siempre posible. Para efectos prácticos, no obstante, lo relevante es la detección de miocardio disfuncional viable en un paciente con enfermedad arterial coronaria significativa.
Existen varios métodos para determinar viabilidad. Para poder entender mejor las diferencias entre estos métodos es importante tener claros los conceptos de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo, además de los objetivos valorados para definir viabilidad según la técnica. Entre los diferentes objetivos a evaluar se encuentran la presencia de necrosis miocárdica, detectable por cardiorresonancia magnética, que permite diferenciar entre tejido miocárdico sano y cicatriz miocárdica; la reserva contráctil, evaluada a través de la medición del grosor de la pared miocárdica, la mejoría y posterior deterioro de la contractilidad (respuesta bifásica) durante la infusión de dobutamina, sea con control ecocardiográfico o también por cardiorresonancia magnética; y el metabolismo celular valorado con la captación de material radioactivo por el tejido metabólicamente activo en estudios de imagen nuclear. Según el método a utilizar y por ende el objetivo que se evalúe, se tendrá diferente sensibilidad o especificidad para diferenciar el miocardio viable del miocardio necrosado, y también para predecir la recuperación de la contractilidad posterior a la revascularización.
En cualquier caso, es crucial discriminar el miocardio viable del no viable para así planificar adecuadamente el tratamiento. Las indicaciones de revascularización se dividen en dos grupos, el control de síntomas y la mejoría del pronóstico, guiándose dichas indicaciones por criterios clínicos y anatómicos, en los cuales la evaluación de viabilidad no es requisito para la realización de estos procedimientos7. Al guiarse solamente por criterios de la severidad de las lesiones coronarias, es posible caer en el peligro de realizar revascularización miocárdica sin alterar el pronóstico de los pacientes8. Practicar este tipo de procedimientos en miocardio no viable, no altera el pronóstico a largo plazo; en cambio, al no hacer revascularización en pacientes con miocardio viable, la morbilidad y mortalidad empeoran en mayor medida que en aquellos pacientes que no presentan viabilidad9, alterando de manera significativa su pronóstico.
La cardiorresonancia magnética posee la capacidad de evaluar diferentes aspectos del corazón; durante un estudio se puede evaluar la contractilidad global, la contractilidad segmentaria en reposo y bajo estrés farmacológico, el grosor de la pared miocárdica, la perfusión miocárdica en reposo y bajo estrés y, el más importante en la evaluación de viabilidad, la caracterización del tejido con diferenciación entre fibrosis/necrosis miocárdica y tejido miocárdico viable.
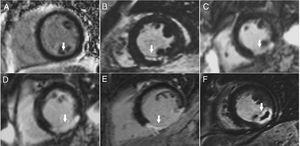
Métodos de valoración de viabilidad por cardiorresonancia magnéticaRealce tardío con gadolinioEl gadolinio es un ion paramagnético de distribución exclusivamente extravascular, incapaz de atravesar la membrana celular intacta, cuyo volumen de distribución en el miocardio sano es reducido, siendo además lavado del mismo con relativa rapidez. En el miocardio normal, o en aquél que sufre un evento isquémico sin afectar a la integridad de la membrana celular miocárdica (miocardio aturdido), la concentración tisular de gadolinio es mínima, lo que lo hace indetectable en las secuencias de resonancia magnética obtenidas un cierto tiempo (10min) después de la administración del contraste. En caso de un evento isquémico, con necrosis y posterior pérdida de la integridad de la pared celular miocárdica, el gadolinio se acumula dentro de las células, aumentando su volumen de distribución local, con subsecuente detección en las secuencias de contraste tardío. Ello es factible tanto en el infarto agudo o subagudo, como en caso de necrosis crónica, donde el tejido miocárdico es reemplazado con tejido fibrótico (con aumento del espacio extracelular y del volumen de distribución del gadolinio). Aplicando secuencias especiales de cardiorresonancia magnética, como las de inversión/recuperación10, se pueden magnificar las diferencias de concentración de gadolinio, observándose el realce tardío como zonas con gran aumento de intensidad de señal (brillantes) en el miocardio ventricular (fig. 1), lo cual se ha demostrado que guarda correlación histopatológica con la presencia y extensión del infarto, tanto en la etapa aguda, por daño en la membrana celular, y luego de ocho semanas por captación en la cicatriz fibrótica miocárdica11.
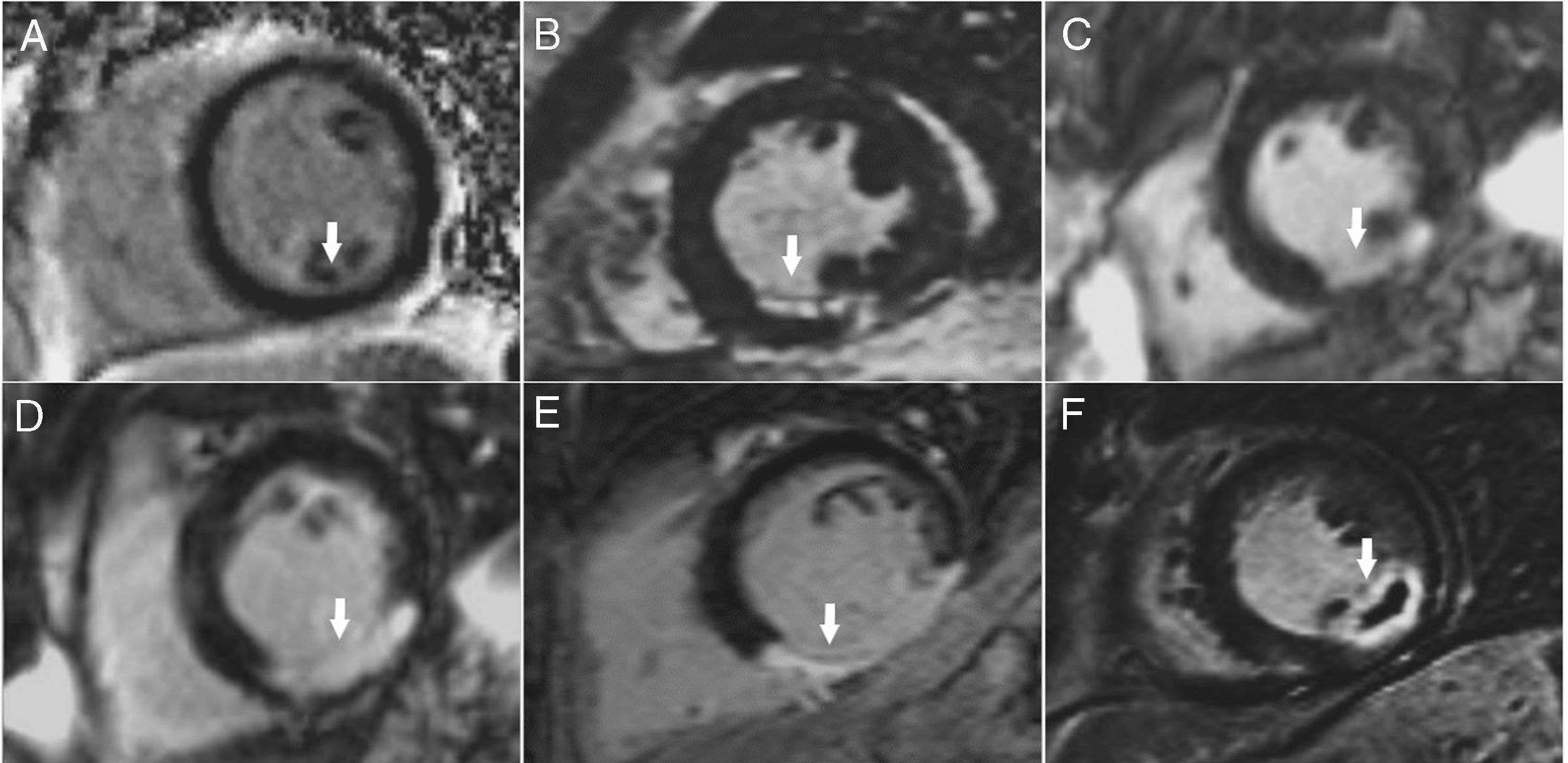
Secuencias de realce tardío en el eje corto medial de diferentes pacientes, en quienes se observa miocardio de características normales (color negro, flecha en recuadro A) y miocardio con fibrosis/necrosis miocárdica (color blanco). A. Corte sin captación de gadolinio (normal). B. Infarto subendocárdico en cara inferior menor del 25% del grosor de la pared inferior (ver flecha). C. Infarto subendocárdico en cara inferior del 50% (ver flecha). D. Infarto subendocárdico en cara inferior mayor del 50% (ver flecha). E. Infarto transmural de cara inferior (ver flecha). F. Infarto transmural de cara inferior con área de obstrucción microvascular (ver flecha) que corresponde al área negra rodeada de miocardio necrosado en la cual hay obstrucción al paso de contraste.
La detección de infarto por los diferentes métodos diagnósticos (ECG, ultrasonidos, radionúclidos, cardiorresonancia magnética) mejora a medida que aumenta la cantidad de miocardio afectado. En los casos de infarto transmural la sensibilidad en el diagnóstico de infarto es similar entre ellos, pero a medida que disminuye la transmuralidad (infarto subendocárdico) la sensibilidad para la detección de infarto de miocardio disminuye en todos excepto en la cardiorresonancia magnética. El realce tardío con gadolinio es capaz de percibir infartos subendocárdicos no detectados por otros métodos12, lo cual mejora la capacidad diagnóstica y pronóstica13, y además proporciona información sobre la presencia, localización y extensión de infarto agudo y crónico14. El infarto de miocardio detectado por cardiorresonancia magnética, es un marcador pronóstico independiente de la fracción de eyección y de la presencia o no, de alteraciones de la contractilidad. La enfermedad isquémica no siempre desarrolla sintomatología típica que permita diagnosticar de manera oportuna síndrome coronario agudo; en el seguimiento de una cohorte del estudio MESA15 evaluada por cardiorresonancia magnética, la prevalencia de algún tipo de cicatriz miocárdica fue del 7,9%, del cual el 78% no fue diagnosticada previamente por métodos convencionales16.
El criterio más importante para determinar la posibilidad de viabilidad por cardiorresonancia magnética es la relación entre el grosor de la cicatriz por gadolinio comparado con el grosor de la pared17. A medida que aumenta la transmuralidad de la necrosis, disminuye la posibilidad de recuperación de función miocárdica (fig. 1). En un metaanálisis realizado por Romero et al., el realce tardío con gadolinio ocupando menos del 50% del grosor de la pared miocárdica afectada demostró una sensibilidad del 95% con una especificidad del 51%, valor predictivo positivo del 69% y valor predictivo negativo del 90% en la predicción de mejoría de la contractilidad regional posterior a revascularización18. El realce tardío con gadolinio tiene, por tanto, gran sensibilidad para detectar miocardio viable (fig. 2). Aún en etapas tempranas de un síndrome coronario agudo el realce con gadolinio ha demostrado que el porcentaje de miocardio salvado posterior a la revascularización disminuye de manera significativa después de los primeros 90 minutos posterior al evento isquémico (fig. 3)19. Además, durante la evaluación en el primer mes posterior a un síndrome coronario agudo, predice cuáles pacientes tendrán disfunción ventricular y aumento de morbimortalidad en los seis meses posteriores al evento isquémico20, y es capaz de evaluar y cuantificar la presencia de obstrucción microvascular21,22, el cual es un marcador efectivo para determinar complicaciones cardiovasculares tras el evento inicial.
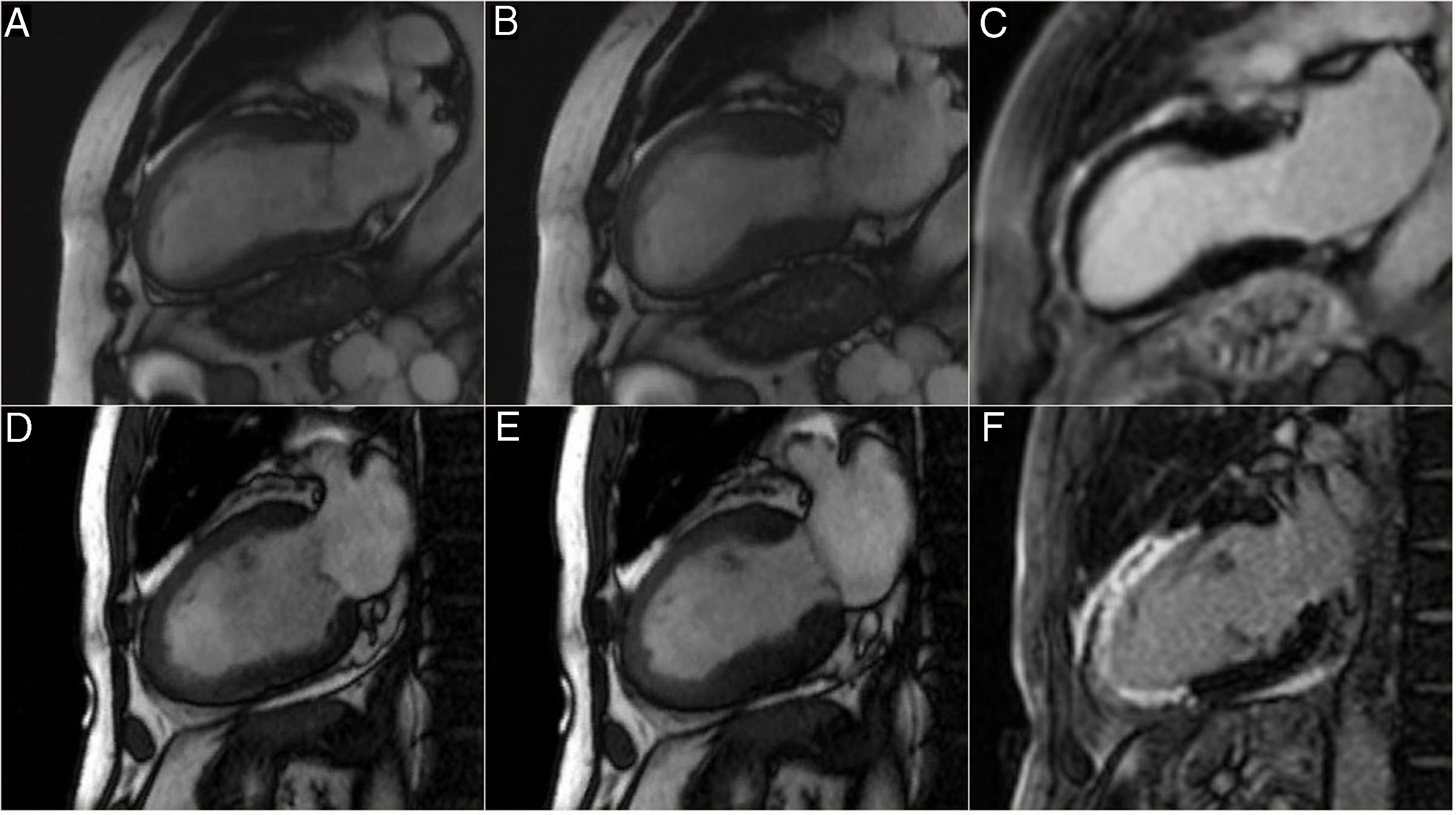
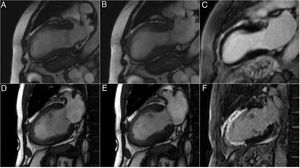
Imágenes A-C. Secuencias de cine en eje vertical largo en diástole (A) y sístole (B) de un paciente con oclusión crónica de arteria descendente anterior: se observa adelgazamiento de la pared anterior medial y del ápex en comparación con segmentos basales, además de defecto concomitante de la contractilidad y alteración de la morfología ventricular. En la secuencia de realce tardío (C) se aprecia miocardio viable sin fibrosis/necrosis miocárdica (miocardio color negro, sin realce tardío). Por tanto, las secuencias de cine sugieren defecto de contractilidad en un segmento que no presenta necrosis miocárdica. Imágenes D-F. Secuencias de cine en eje vertical largo de un paciente con infarto agudo de miocardio en diástole (D) y sístole (E) con alteración de la contractilidad de la pared anterior medial y del ápex. En la secuencia de realce tardío se observa captación transmural de gadolinio (no viable) en la pared anterior medial y el ápex (miocardio color blanco). El defecto de contractilidad corresponde en este caso a una región con necrosis miocárdica transmural.
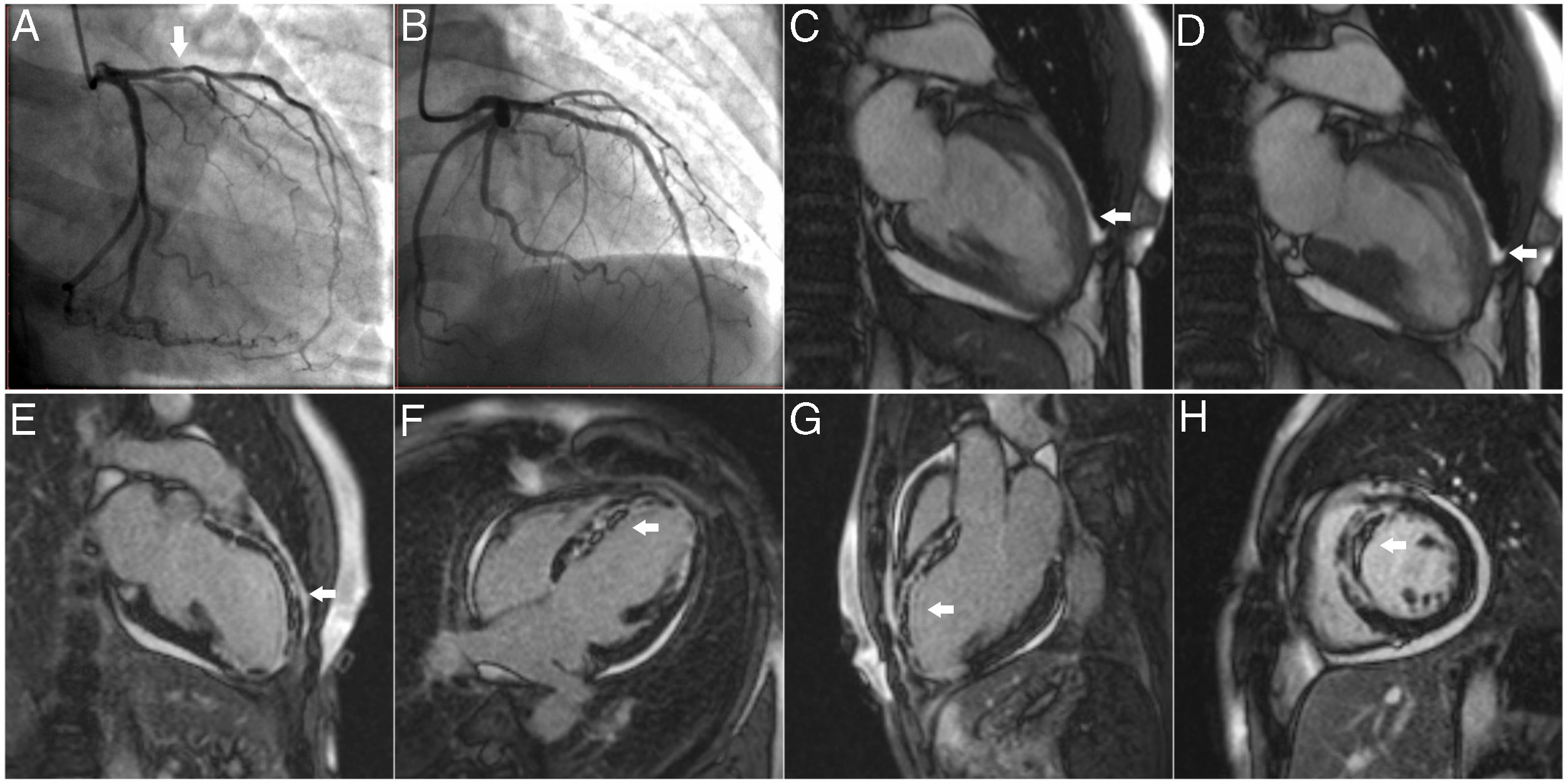
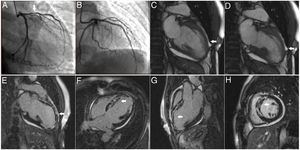
Paciente de 47 años, que ingresa con infarto con elevación del ST en territorio de la arteria descendente anterior, de seis horas de evolución. En la angiografía diagnóstica (A) se evidencia lesión crítica (flecha) en arteria descendente anterior la cual se trata con la colocación de stent (B). En las secuencias de cine por resonancia en dos cámaras en diástole (C) y sístole (D), se observa aquinesia del ápex y de la pared anterior en todos los segmentos. Posteriormente, en las secuencias de realce tardío, se aprecia captación anormal de gadolinio y obstrucción microvascular (ver flechas en cuadros E, F, G, H) en el territorio irrigado por la arteria descendente anterior en dos cámaras (E), cuatro cámaras (F), tres cámaras (G) y eje corto medial (H). Esto indica ausencia de viabilidad en el territorio afectado a pesar de presentar arteria abierta al momento de la angiografía diagnóstica con un flujo TIMI 3.
En comparación con la evaluación de la reserva contráctil, la valoración del realce tardío con gadolinio no requiere monitorización y conlleva menor riesgo para el paciente; además la tasa de eventos adversos del gadolinio es extremadamente baja, siendo consideradas leves la mayoría de reacciones23. Sin embargo, en presencia de falla renal con depuración de creatinina menor de 30ml/min, existe contraindicación del uso de gadolinio debido al riesgo de fibrosis sistémica nefrogénica.
El grosor de la pared miocárdica es un criterio aún utilizado para la valoración de la viabilidad; un grosor de pared miocárdica menor de 5.5mm es indicativo de cicatriz miocárdica por ecocardiografía. Por cardiorresonancia magnética se ha demostrado que lo más importante es el porcentaje del grosor de la cicatriz miocárdica en comparación con el miocardio ventricular sano; aún en paredes miocárdicas consideradas atróficas mediante ecocardiograma, se logra la recuperación de la contractilidad posterior a revascularización24.
Reserva contráctil con dobutaminaLa valoración de la contractilidad durante la infusión de dobutamina fue la primera técnica utilizada en cardiorresonancia magnética para el diagnóstico de viabilidad. El protocolo utilizado es similar al que se usa en valoración de la reserva contráctil con dobutamina por medio de ecocardiografía, con aumento progresivo de dosis (5, 10 y 20 mcg/kg/min) y valoración por secuencia de cine de la contractilidad en cada etapa de la infusión, siendo el aumento de la misma el marcador de viabilidad (fig. 4). En comparación con la ecocardiografía de estrés con dobutamina, la cardiorresonancia magnética tiene mayor sensibilidad dada por mejor calidad de imágenes de la resonancia en comparación con la ecocardiografía25.
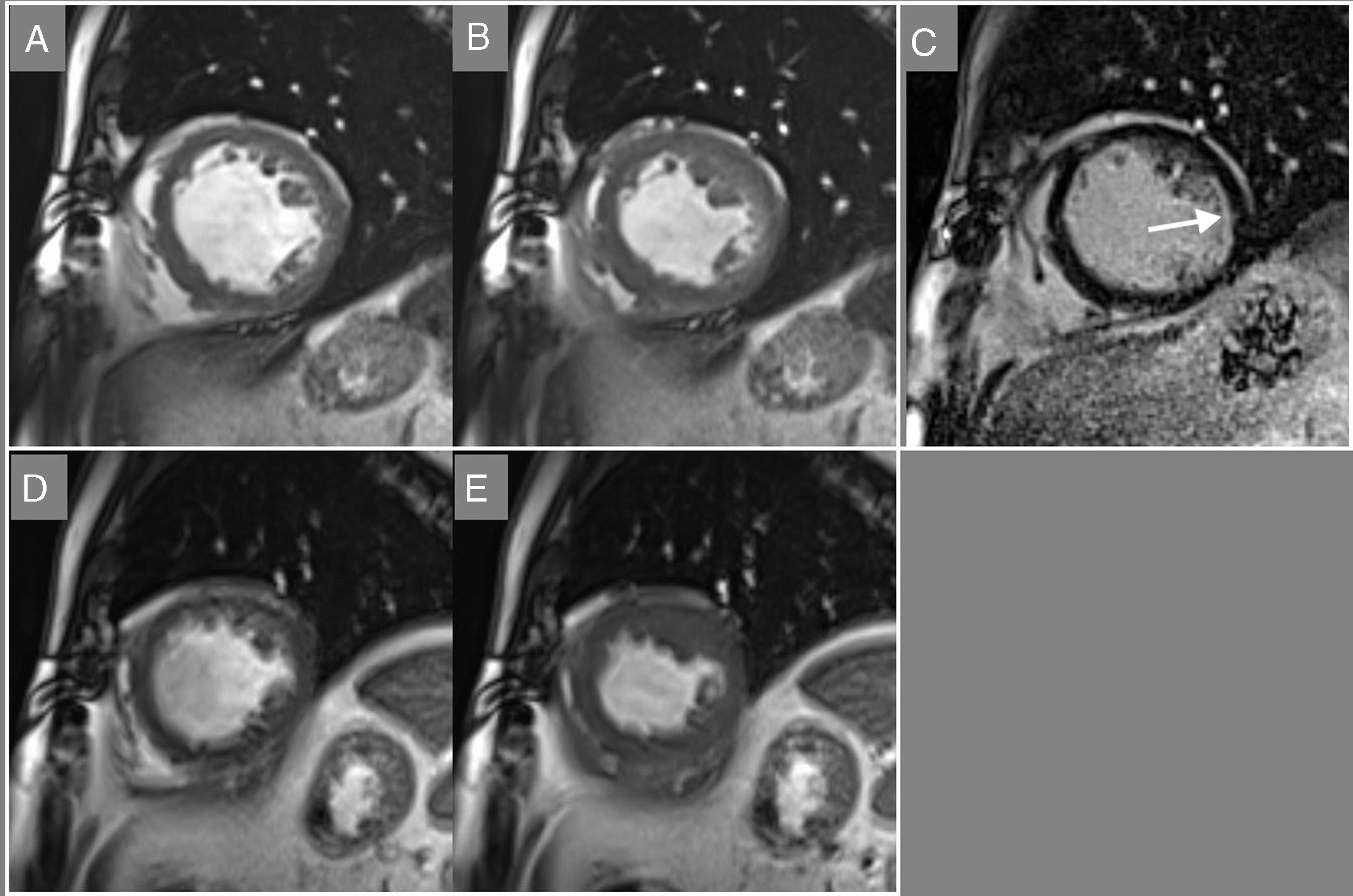
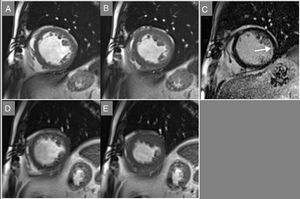
Paciente con miocardiopatía isquémica. A y B: imágenes diastólica y sistólica de una secuencia de cine en eje corto que muestra hipoquinesia de todos los segmentos. C: Imagen de contraste tardío que demuestra necrosis subendocárdica (25% del grosor de pared) localizada en la región lateral medial (flecha). D y E: imágenes diastólica y sistólica de una secuencia de cine en eje corto durante la estimulación con dobutamina a dosis de 20 mcg/kg/min, que muestra incremento de la contractilidad de todos los segmentos, lo que confirma la presencia de reserva contráctil, y apoya la presencia de viabilidad miocárdica.
En el metaanálisis de Romero et al.18, el resultado de nueve estudios con valoración de reserva contráctil con dobutamina a bajas dosis, tuvo sensibilidad del 81%, especificidad del 91%, valor predictivo positivo del 93% y valor predictivo negativo del 75%. Sin embargo, debido a que requiere una logística especial dentro del área de cardiorresonancia magnética, no está disponible en todos los centros que aplican la técnica.
Relevancia de la viabilidad miocárdica en la práctica clínicaEn estudios previos de viabilidad miocárdica, el pequeño tamaño de los grupos y la variabilidad en los métodos de medición de la viabilidad, no había permitido confirmar el concepto de la viabilidad como marcador determinante de pronóstico en la revascularización. En un metaanálisis de 200226 se demostró que la revascularización de los territorios no viables no tiene impacto significativo en la mortalidad, y que sólo la revascularización en territorios viables mejora el pronóstico, justificando el riesgo de revascularización aún en pacientes con disminución de la fracción de eyección. Aunque el concepto de viabilidad es lógico y simple, estudios clínicos aleatorizados no han podido demostrar el beneficio derivado de la revascularización en presencia de viabilidad. El estudio PARR-227, cuyo objetivo principal era determinar si los pacientes a los que se les realizaba detección de viabilidad con FDG PET (tomografía de emisión de positrones con F-18 fluorodeoxyglucosa) tenían mejores desenlaces clínicos que aquellos en quienes se realizaba manejo estándar, a pesar de la poca adherencia a las recomendaciones del tratamiento del estudio, demostró una tendencia hacia la mejoría de los pacientes revascularizados con presencia de viabilidad pero sin llegar a resultados estadísticamente significativos. Posteriormente, el estudio HEART28, el cual buscaba comparar las diferencias del manejo médico y de la revascularización en pacientes con miocardio viable, fue suspendido de manera prematura sin poder responder el interrogante de cómo el miocardio viable afecta el pronóstico una vez revascularizado en pacientes con baja fracción de eyección. El estudio STICH29, por su parte, trató de resolver el interrogante de valoración de la viabilidad y utilidad para cambiar desenlaces clínicos en pacientes con fracción de eyección disminuida, aunque aspectos discutibles en la metodología, como el uso solamente de ecodobutamina y SPECT como métodos de viabilidad, la falta de viabilidad como criterio de inclusión del estudio, o la realización de revascularización sin tener en cuenta los resultados de viabilidad, no respondieron la pregunta acerca de cómo la viabilidad puede ser el determinante antes de proceder a una revascularización miocárdica para disminuir el riesgo de mortalidad. Estudios de menor volumen que han utilizado la cardiorresonancia magnética9, muestran que revascularizar o no miocardio sin viabilidad no afecta la mortalidad, pero si se detecta miocardio viable mejora el pronóstico con la revascularización, en cuyo caso el grupo con peor pronóstico es aquel en el cual se detecta miocardio viable y no se realiza revascularización.
En resumen, la viabilidad miocárdica se puede valorar a través de diferentes métodos, cada uno de los cuales valora diferentes aspectos como marcador subrogado de la presencia de miocardio potencialmente recuperable luego de revascularización, con lo que debe mejorar el pronóstico a largo plazo de los pacientes. Por medio de la cardiorresonancia magnética es factible evaluar tanto la presencia y extensión de cicatriz miocárdica, como la presencia de reserva contráctil en aquellos segmentos disfuncionantes sin necrosis transmural. En segmentos miocárdicos con cicatriz miocárdica menor del 50% del grosor de la pared, el realce tardío es el marcador más sensible para predecir recuperación de función, mientras que la reserva contráctil en la cardiorresonancia magnética con dobutamina a dosis bajas es el marcador más específico30.
Conflicto de interesesNinguno.