Las recomendaciones de las guías vigentes están basadas en evidencia de baja calidad. Se requiere su actualización periódica considerando la evidencia reciente.
ObjetivoSintetizar la mejor evidencia clínica disponible sobre eficacia y seguridad de antidepresivos y antipsicóticos de segunda generación en pacientes con anorexia nerviosa.
MétodosRevisión sistemática (CRD42020150577). Se buscaron en PubMed, SCOPUS, Ovid(Cochrane), EMBASE y LILACS los ensayos clínicos aleatorizados realizados en pacientes con anorexia nerviosa que evaluasen el uso de antipsicóticos de segunda generación o antidepresivos orales a cualquier dosis y por cualquier tiempo en el tratamiento ambulatorio y/u hospitalario tomando como resultados el peso (índice de masa corporal), las entidades psicopatológicas y la seguridad.
ResultadosSe incluyeron 5 estudios, 4 catalogados como con alto riesgo de sesgo. La evidencia indica que los pacientes que reciben tratamiento con olanzapina o fluoxetina tienden a mantenerse por más tiempo dentro de los programas de tratamiento. La olanzapina mostró resultados favorables (un estudio) en cuanto al aumento de peso, pero no mostró los mismos resultados en psicopatología, donde la evidencia es contradictoria.
ConclusionesEn concordancia con las revisiones anteriores, nuestro trabajo permite concluir que hay información contradictoria sobre la eficacia de los psicofármacos para la anorexia nerviosa. El trabajo futuro debe enfocarse en desarrollar ensayos clínicos de alta calidad metodológica.
The recommendations of the current guidelines are based on low quality evidence. Periodic updating is required, taking recent evidence into consideration.
ObjectiveTo synthesise the best available clinical evidence on the efficacy and safety of second-generation antidepressants and antipsychotics in patients with anorexia nervosa.
MethodsSystematic review (CRD42020150577). We searched PubMed, SCOPUS, Ovid(Cochrane), EMBASE and LILACS for randomised clinical trials performed in patients with anorexia nervosa that evaluated the use of second-generation antipsychotics or oral antidepressants, at any dose and for any length of time, in outpatient and/or hospital treatment, taking weight (body mass index), psychopathological entities and safety as results.
ResultsFive studies were included, with four assessed as having a high risk of bias. The evidence indicates that patients receiving treatment with olanzapine or fluoxetine tend to stay in treatment programmes for longer. Olanzapine showed favourable results (one study) in terms of weight gain, but did not show the same results in psychopathology, where the evidence is contradictory.
ConclusionsIn accordance with previous reviews, our work allows us to conclude that there is contradictory information on the efficacy of psychotropic drugs in the treatment of anorexia nervosa. Future work should focus on developing clinical trials of high methodological quality.
La anorexia nerviosa (AN) se define como una alteración de la conducta alimentaria caracterizada por una pérdida de peso excesiva, que se inicia o se mantiene voluntariamente, acompañada de una distorsión en la imagen corporal1,2. La AN tiene una prevalencia de hasta el 4% de las mujeres jóvenes3; típicamente se inicia a los 18 años y tiende a cronificarse y a las comorbilidades como la diabetes mellitus4, el trastorno afectivo bipolar, el trastorno depresivo mayor y los trastornos de ansiedad1.
Estas condiciones del paciente con AN implican un difícil tratamiento, con fracaso terapéutico en un 35-79% de los pacientes que han recibido algún tipo de tratamiento médico4. La alta tasa de fracaso terapéutico conlleva demanda de servicios hospitalización, tratamiento de complicaciones, polifarmacia e incapacidades, lo que haciendo que el costo de su atención para los sistemas de salud sea muy alto5-7. La recaída después del tratamiento es muy común y la AN tiene la mayor letalidad de todas las enfermedades psiquiátricas8.
Actualmente, la piedra angular del tratamiento de la AN es la terapia psicológica, alternativas como la terapia cognitivo conductual, el modelo de Maudsley y el manejo clínico de apoyo especializado son recomendadas como equivalentes; sin embargo, la evidencia que respalda esta recomendación es de baja calidad9,10. En cuanto al manejo farmacológico, se dan recomendaciones basadas en evidencia de baja calidad a favor de dosis bajas de antipsicóticos, especialmente olanzapina, con moderada utilidad para el aumento de peso, tratamiento de síntomas ansiosos y pensamientos obsesivos7.
Sobre los mecanismos de acción, se sabe que el aumento de la neurotransmisión de serotonina a través del núcleo arqueado del hipotálamo produce señales de saciedad e inhibe la alimentación, razón por la cual la neurotransmisión de serotonina parece importante en la etiología y la farmacoterapia de la AN11-13. Además, la serotonina está implicada en otras desregulaciones conductuales como la depresión, la ansiedad y la psicosis, que ocurren con frecuencia en pacientes con AN8,14,15.
Por lo tanto, se señala que medicamentos con un mecanismo de acción predominantemente serotoninérgico pueden tener algún efecto terapéutico en los pacientes con AN16.
No obstante, en cuanto al uso de antidepresivos la evidencia es contradictoria. Las guías alemanas dan recomendaciones contra del uso de inhibidores de la recaptación de serotonina9, mientras las guías de la Federación Mundial de Sociedades de Psiquiatría Biológica y la Asociación Estadounidense de Psiquiatría17 los recomiendan con precaución.
El hecho de que las guías vigentes estén basadas en evidencia de baja calidad hace prioritaria la actualización periódica de los procesos de síntesis de evidencia incluyendo los últimos estudios clínicos, de forma tal que las recomendaciones puedan ser actualizadas y reevaluadas buscando disminuir la incertidumbre asociada con la calidad metodológica y la fuerza de la recomendación.
Así las cosas, el objetivo de este estudio es sintetizar la mejor evidencia clínica disponible sobre eficacia y seguridad de antidepresivos y antipsicóticos de segunda generación en pacientes con AN, eficacia medida por ganancia de peso a través del índice de masa corporal (IMC).
MétodosProtocolo y registroEl protocolo de revisión se desarrolló siguiendo el manual de revisiones sistemáticas de intervenciones de Cochrane18 y fue registrado en el repositorio PROSPERO (Código: CRD42020150577). Este artículo sigue las sugerencias de reporte de la declaración PRISMA (Preferred Reporting Items for Systematic Reviews and MetaAnalyses)19.
Criterios de elegibilidad de los estudios y fuentes de informaciónSe consideraron elegibles los estudios sobre: (P) pacientes mayores de 14 años con diagnóstico de anorexia nerviosa por criterios DSM IV y DSM 5 (I), uso de antipsicóticos de segunda generación o antidepresivos orales a cualquier dosis y por cualquier tiempo en el tratamiento ambulatorio y/u hospitalario, bien sea solos o en combinación con otras terapias farmacológicas o no farmacológicas, con (C) tratamiento convencional, placebo o lista de espera y en quienes se hayan valorado, mediante escalas psicométricas válidas o entrevista clínica (O), los cambios en el peso medido por IMC, además de entidades psicopatológicas, como síntomas afectivos, ansiosos u obsesivos. Solo se incluyeron (S) los ensayos clínicos aleatorizados con seguimiento de (T) al menos 4 semanas de duración. Se consideraron artículos en inglés, español e italiano publicados hasta la fecha de la última búsqueda (18 de septiembre de 2019) en PubMed, SCOPUS, Ovid (Cochrane), EMBASE y LILACS. Como fuentes adicionales se verificaron las referencias de los estudios incluidos y se buscaron estudios en curso en clinicaltrials.gov.
Estrategia de búsqueda y selección de los estudiosLa estrategia de búsqueda empleada en PUBMED fue: “anorexia[Title/Abstract] AND (aripiprazol[Title/Abstract] OR haloperidol[Title/Abstract] OR olanzapine[Title/Abstract] OR amitriptiline[Title/Abstract] OR bupropion[Title/Abstract] OR citalopram[Title/Abstract] OR clomipramine[Title/Abstract] OR desvenlafaxine[Title/Abstract] OR duloxetine[Title/Abstract] OR escitalopram[Title/Abstract] OR fluoxetine[Title/Abstract] OR fluvoxamine[Title/Abstract] OR imipramine[Title/Abstract] OR mirtazapine[Title/Abstract] OR paroxetine[Title/Abstract] OR Quetiapine[Title/Abstract] OR Risperidone[Title/Abstract] OR sertraline[Title/Abstract] OR venlafaxine[Title/Abstract]) AND (random*[Title/Abstract] OR efficac*[Title/Abstract])”.
Con la misma estrategia se buscó en las restantes fuentes de información cambiando únicamente la sintaxis correspondiente.
Todos los registros de estudios identificados fueron almacenados en una hoja de Excel en la cual se eliminaron los repetidos. Cinco investigadores (ASL, JMS, CVM, MCM y FVE) tamizaron los títulos y resúmenes excluyendo los no pertinentes a la pregunta PICO; en los casos en que no se pudo establecer, el artículo se mantuvo para revisión a texto completo. Las mismas investigadoras revisaron a texto completo los artículos elegibles excluyendo los no pertinentes a PICO o que no cumplían con el tipo de estudio. El consenso de los estudios incluidos en la revisión narrativa se dio entre todos los investigadores.
Variables PICO y proceso de extracción de datosCada artículo incluido fue leído a texto completo de forma independiente por dos investigadores y la información extraída fue registrada en hoja de Excel; las discrepancias fueron resueltas revisando en conjunto el documento original. Las características extraídas fueron: (P) distribución por edad y sexo, características clínicas, contexto geográfico o institucional; (I, C) terapia del grupo experimental y del grupo control, cointervenciones, características del operador y tamaño de muestra; (O) atributos, instrumento de medición, características del operador y valores basales y al final del estudio; (T) tiempo de seguimiento, y (S) apellido del primer autor, año de publicación, año de ejecución y tipo de estudio. Las características de los estudios se presentan en tabla 1.
Valoración del riesgo de sesgo en los estudios individualesPara cada estudio incluido, dos investigadores realizaron la valoración del riesgo de sesgo a nivel de estudio; las diferencias fueron resueltas por consenso entre todos los investigadores. El instrumento empleadao fue Risk of Bias 2.0 (RoB 2.0) considerando sus 5 dimensiones: proceso de aleatorización, desviaciones de las intervenciones, datos perdidos en el desenlace, medición del desenlace y reporte selectivo de resultados; se hizo una valoración global del riesgo de sesgo del estudio20. La valoración se realizó en consenso entre los 4 investigadores partiendo de la recomendación del instrumento. Los estudios considerados con alto riesgo de sesgo fueron excluidos de la síntesis de evidencia. Se presenta la tabla con la valoración de cada estudio en cada ítem y una figura resumen del riesgo de sesgo de todos los estudios incluidos.
Medidas de resumen y síntesis de resultadosPara cada desenlace se tomó la diferencia de medias entre grupos de intervención junto con el intervalo de confianza del 95% (IC95%). Como se planteó por protocolo, no se realizó metanálisis por diferencias entre estudios en características metodológicas.
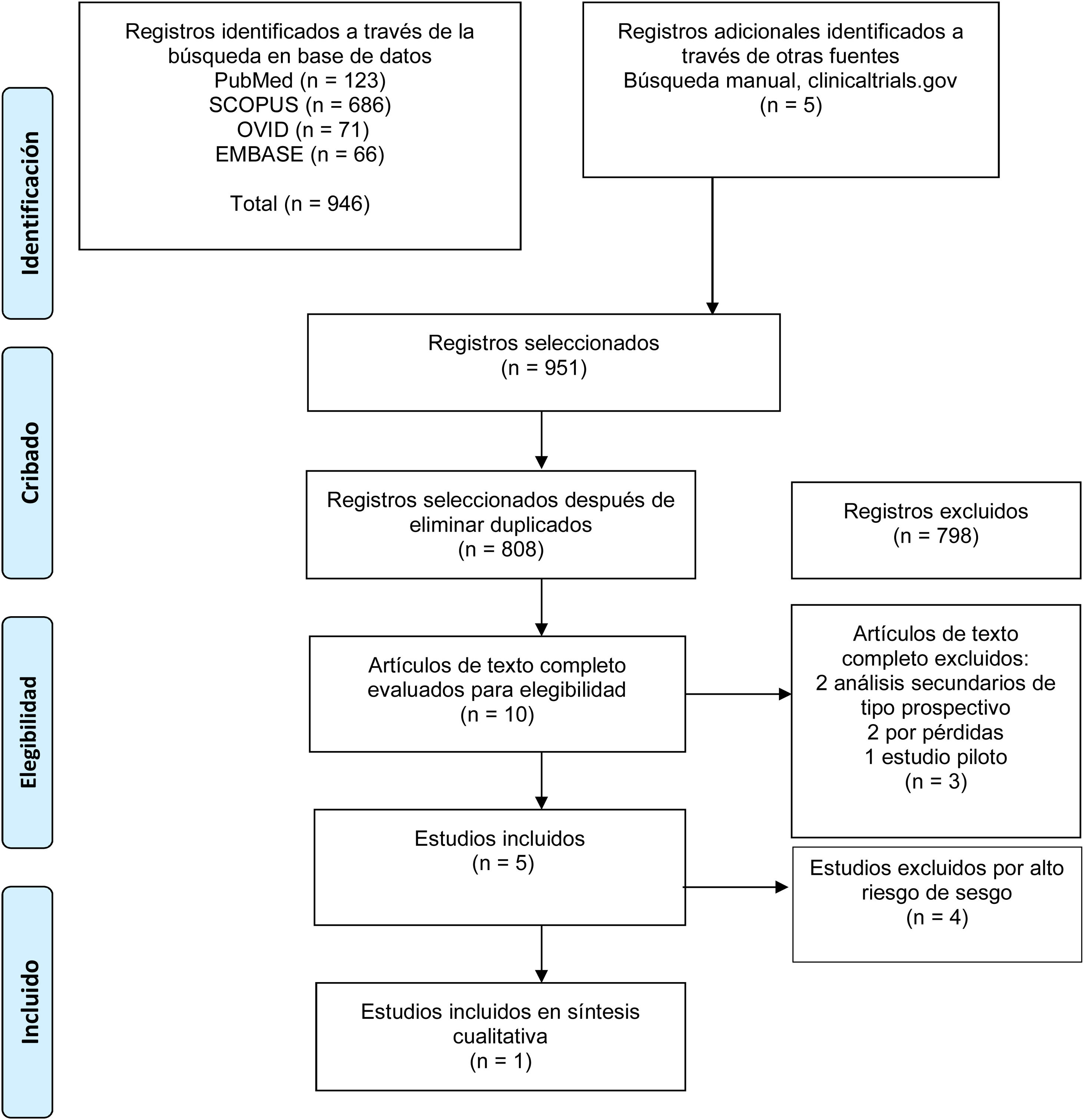
ResultadosResultados de la búsquedaLa figura 1 describe el diagrama de flujo del proceso de selección de estudios. Se identificaron 808 referencias después de excluir los duplicados. Mediante lectura de título y resumen, se descartaron 798. Los 10 restantes fueron revisados a texto completo y se excluyeron 5: 2 por tratarse de análisis secundarios, 2 por la magnitud de las pérdidas en el seguimiento y 1 estudio piloto. Un total de 5 ensayos clínicos aleatorizados fueron incluidos en la extracción de datos y la valoración del riesgo de sesgo.
Flujograma PRISMA. Tomado de Moher et al.19.
De los 5 estudios incluidos, 2comparaban olanzapina con placebo, 2 comparaban fluoxetina con placebo y 1 comparaba olanzapina con clorpromazina. Con un total de 340 participantes con AN, el tamaño muestral oscilaba entre 26 y 152 participantes y la duración de los estudios estaba entre 6 y 52 semanas. Las mujeres participantes en todos los ensayos clínicos incluidos fueron más del 95%. La tabla 1 presenta un resumen de las principales características de cada estudio.
Características de los estudios incluidos
| Estudio | Muestra | Media de edad (años) | Intervención | Comparador | Duración | Desenlaces | Pérdidas | Financiación |
|---|---|---|---|---|---|---|---|---|
| Walsh 2006 | 93 | 22,4 (grupo fluoxetina), 24,2 (grupo placebo) | Fluoxetina+TCC | Placebo+TCC | 12 meses | Tiempo hasta la recaída, medida por IMC | 0 | Apoyado por subvenciones del Instituto Nacional de Salud. Eli Lilly suministró la fluoxetina y el placebo |
| Bissada 2008 | 34 | 23,6 (grupo olanzapina), 29,6 (grupo placebo) | Olanzapina | Placebo | 10 semanas | Tasa de aumento de peso medida con IMC | 12 | Apoyado por una subvención de Eli Lilly |
| Mondraty 2005 | 26 | 25,3 (grupo olanzapina y clopromazina) | Olanzapina | Clorpromazina | 12 meses | Inventario de trastornos alimentarios (EDI) 2 y el Inventario de Padua | 0 | No se describe |
| Kaye 2001 | 35 | 23 (grupo fluoxetina), 22 (grupo placebo) | Fluoxetina | Placebo | 12 meses | Tiempo hasta la recaída medida por IMC | 22 | Corporación Eli Lilly y el Instituto Nacional de Salud Mental |
| Attia 2019 | 152 | 28 (grupo olanzapina), 30 (grupo placebo) | Olanzapina | Placebo | 16 semanas | Tasa de cambio en el peso corporal y la tasa de cambio en la obsesionalidad | 69 | Apoyado por Instituto Nacional de Salud. Eli Lilly proporcionó la olanzapina y píldoras de placebo combinadas, pero no proporcionó apoyo financiero |
IMC: índice de masa corporal; TCC: terapia cognitivo-conductual.
El estudio de Walsh21, contó con una muestra de 93 pacientes, quienes recibieron tratamiento intensivo hospitalario o en el programa de hospital de día del Instituto Psiquiátrico del Estado de Nueva York o el Hospital General de Toronto. Fueron asignados aleatoriamente para recibir fluoxetina o placebo. Las listas de aleatorización, estratificadas por sitio y subtipo de purga compulsiva, fueron generadas por un programa de computadora utilizando un generador de números aleatorios. La dosis de medicación se mantuvo en 60 mg/día a menos que hubiera efectos adversos, en cuyo caso la dosis se redujo a discreción del psiquiatra. Fueron tratados durante 12 meses o hasta que cumplieron los criterios para la retirada prematura del estudio o se retiraron voluntariamente. Se recopilaron evaluaciones cada 4 semanas usando: el Inventario de trastornos de la alimentación, el Inventario de depresión de Beck, el Inventario de ansiedad de Beck y la Escala de autoestima de Rosenberg.
El estudio de Bissada22, conto con una muestra de 34 pacientes con diagnóstico de AN asignados aleatoriamente a tratamiento con olanzapina más hospital de día o placebo más tratamiento en hospital de día; la aleatorización se estratificó según el subtipo de AN (restricción o atracón/purga). La olanzapina se prescribió de acuerdo con un régimen de dosis flexible, comenzando con la dosis mínima de 2,5mg/día y titulada lentamente en incrementos de 2,5mg/semana hasta una dosis máxima de 10mg/día. La duración del estudio fue de 13 semanas. El modelo lineal jerárquico se utilizó para modelar las trayectorias de cambio de la curva de crecimiento para el IMC de cada paciente.
El estudio de Mondraty23 contó con una muestra de 26 pacientes, de los que 15 fueron asignados al azar en un diseño de bloque equilibrado, 8 a olanzapina y 7 a clorpromazina (controles). Un investigador externo al estudio llevó a cabo la aleatorización. La secuencia de números aleatorios se generó arrojando una moneda. Ambos medicamentos se iniciaron con una dosis baja y aumentaron hasta que se produjo un efecto satisfactorio, una dosis máxima o un efecto secundario. Se aplicó como parte de la evaluación el Inventario de trastornos alimentarios (EDI) 2 y el Inventario de Padua. La duración del estudio fue de 12 meses.
El estudio de Kaye24 contó con una muestra de 35 pacientes con AN de tipo restrictivo aleatorizados a fluoxetina (n=16) o placebo (n=19) después del aumento de peso en pacientes hospitalizados y luego se observaron como pacientes ambulatorios durante 1 año.
El estudio de Attia25 contó con una muestra de 152 pacientes ambulatorios con AN, se realizó en 5 sitios en Norteamérica. Los participantes fueron asignados aleatoriamente en proporción de 1:1 a recibir olanzapina o placebo y fueron vistos semanalmente durante 16 semanas. Las medidas de resultado primarias fueron la tasa de cambio en el peso corporal y el cambio en los síntomas de obsesiones, y compulsiones relacionadas con la comida y el cuerpo fueron medidas con el YBOC-ED (Yale Brown Obsessive Compulsive ED Scale).
Riesgo de sesgoCuatro de los 5 estudios incluidos en la revisión están clasificados según el RoB 2.0 como con alto riesgo de sesgo (fig. 2). Hubo deficiencias en dominio de aleatorización en el estudio de Kaye24, ya que no hubo descripción clara de este proceso. En el estudio de Mondraty23 hubo desviaciones de las mediciones previstas, ya que los datos no fueron analizados en concordancia con un plan especificado previo a que los resultados estuvieran disponibles. En los estudios de Mondraty, Kaye y Bissada22, había inconcordancias, ya que no se utilizó un análisis apropiado para estimar el efecto de la intervención y no todos los pacientes e interventores estaban enmascarados. Además, en los ensayos clínicos realizados por Bissada y Kaye se usaron múltiples medidas y análisis para un mismo resultado, lo que incrementa la posibilidad de resultados sesgados. Y por último, con respecto a la pérdida de datos del desenlace, se encontró un alto riesgo en los estudios de Kaye y Walsh21; en el primero solo finalizaron el seguimiento el 63% de los pacientes del grupo de intervención y el 16% del grupo de placebo, y en el segundo, solo el 43%.
Resultados de los estudios individualesEn el ensayo clínico de Kaye, se comparó el efecto en la prevención de recaídas de la fluoxetina frente a placebo en pacientes ambulatorios con AN. El 63% de los pacientes del grupo de fluoxetina y el 16% del de placebo completaron el seguimiento a 1 año, con tendencia a completar el estudio en el grupo de intervención. Los autores compararon 4 grupos (fluoxetina frente a placebo y los que completaron el seguimiento frente a los que no). Al final los 4 grupos mostraron una interacción significativa para la puntuación Y-BOCS y una tendencia para la HDRS. Este análisis no mostró diferencias en el peso, la puntuación HARS o la puntuación de obsesiones y compulsiones relacionadas con el trastorno alimentario. Mediante la prueba de la t para datos apareados, el grupo que permaneció con fluoxetina durante 1 año mostró una diferencia significativa, en términos de aumento de peso y reducciones en ansiedad, depresión, obsesiones, compulsiones y síntomas cardinales del trastorno alimentario.
En otro de los ensayos clínicos21, se comparó la fluoxetina con placebo. Se asignó a 49 pacientes a fluoxetina y 44 a placebo. De los 93 pacientes, 40 completaron el curso completo del tratamiento y 53 terminaron prematuramente. El análisis del tiempo hasta la recaída, en el que se consideró que la terminación prematura por cualquier motivo significaba una recaída, no encontró diferencias significativas entre los grupos de fluoxetina y placebo (r=−0,133; SE=0,288; df=1; p=0,64).
Tres ensayos clínicos evaluaron el uso de olanzapina. En el estudio de Mondraty se comparó la olanzapina con la clorpromazina. Con 8 participantes en el brazo de olanzapina y 7 en el de control. El aumento de peso promedio de todos los pacientes fue 5,5 kg, sin diferencias significativas entre los 2 grupos. Se encontró una reducción en las rumiaciones, que fue significativamente mayor en el grupo de olanzapina que en el grupo de control (el 54 frente al 9%). La disminución de la gravedad de las cogniciones fue clínicamente significativa en todas las subescalas (EDI-2) para olanzapina.
En otro ensayo clínico22 se evaluó el efecto de la olanzapina en el aumento de peso de pacientes con AN, con una dosis promedio de 6,61mg/día durante 10 semanas. Todos los pacientes tuvieron aumento significativo de peso en el IMC (β10=0,29; t=7,44, df=32; p <0,001); el grupo de olanzapina tuvo mayores tasas de aumento del IMC que el grupo de placebo (β11=–0,06; t=–2,25; df=31; p=0,03). En el análisis de supervivencia, el 55,6% de los pacientes con placebo y el 87,5% de aquellos con olanzapina alcanzaron la restauración del peso; el tiempo promedio de supervivencia fue 8±0,68 (IC95%, 6,74-9,39) semanas con olanzapina y 10±0,67 (IC95%, 8,75-11,36) con placebo.
En un estudio multisitio25, 152 pacientes ambulatorios fueron asignados para recibir medicación o placebo (75 en el grupo de olanzapina y 77 en el grupo de placebo). La olanzapina se asoció con una tasa significativamente mayor de aumento de peso (aumento mensual del IMC, 0,259±0,051) que con placebo (aumento mensual del IMC, 0,095±0,053; F=4,98, df=1,1435; p=0,026). No hay evidencia de que la olanzapina tenga un impacto significativo en la psicopatología de la AN, como las obsesiones y la preocupación excesiva con el aumento de peso.
Seguridad y tolerabilidadEn 4 de los 5 estudios incluidos, se hicieron descripciones sobre seguridad y tolerabilidad. En relación con la clorpromazina, hubo 3 reportes de efectos adversos: uno de sedación, otro de visión borrosa y el último de hipotensión postural, pero fueron relacionados con mayor dosis del antipsicótico.
Dos de los 3 estudios que evaluaron la olanzapina no encontraron efectos adversos relevantes, pero en el estudio de Attia sí se comunicaron efectos descritos como moderados-graves relacionados con la olanzapina, entre los que se incluyen dificultad para concentrarse (el 14,5 frente al 32,7%; χ2=5,45; p=0,02), dificultad para quedarse quieto (el 6,5 frente al 18,2%; χ2=3,81; p=0,05), problemas para conciliar el sueño (el 9,7 frente al 30,9%; χ2=8,32; p=0,004) y problemas para permanecer dormido (el 14,5 frente al 40,0%; χ2=9,72; p=0,002).
Un paciente de 17 años asignado a fluoxetina hizo un intento de suicidio durante el estudio pero, dado el pequeño tamaño de muestra y las bajas tasas de finalización de los 2 ensayos de fluoxetina, no podemos determinar si este intento de suicidio en un adolescente en tratamiento con fluoxetina en el estado de bajo peso difiere de alguna manera del tratamiento de individuos de peso normal con otros diagnósticos psiquiátricos.
En general, las tasas de interrupción atribuidas a eventos adversos no difirieron significativamente entre los medicamentos individuales.
DiscusiónEsta revisión sistemática busca identificar la eficacia de los antipsicóticos y antidepresivos en el tratamiento de la AN mediante una actualización de la evidencia con base en estudios practicados en los últimos 19 años. En resumen, la evidencia no es suficiente para recomendar psicofármacos para el tratamiento de la anorexia.
De los estudios incluidos, encontramos que los pacientes que reciben tratamiento con algún psicofármaco, sea olanzapina o fluoxetina, tienden a mantenerse por más tiempo dentro de los programas de tratamiento, pero en cuanto al aumento de peso el único medicamento del que se demostró un impacto fue la olanzapina en uno de los estudios, pero sin los mismos resultados en la psicopatología, donde la evidencia es bastante contradictoria, por lo que no es posible tener claridad sobre el impacto del tratamiento en las rumiaciones u obsesiones relacionadas con el peso.
Sobre la seguridad y la tolerabilidad no hay efectos adversos severos o importantes reportados en los estudios, solo un intento de suicidio en un paciente en tratamiento con fluoxetina el cual no podría atribuirse como tal al medicamento. Estos resultados provienen de estudios de baja calidad metodológica y alto riesgo de sesgo en 4 de 5 por lo que no es posible dar recomendaciones basadas en la evidencia.
Una revisión sistemática de Bulik16 de 2007 evaluó estudios aleatorizados que estudiaban los tratamientos con fluoxetina, amitriptilina y fármacos hormonales, y concluyó que no había evidencia que respalde el uso de psicofármacos en el tratamiento de la AN, puesto que no hay un impacto significativo en la ganancia de peso ni en los síntomas psicológicos, además de las altas tasas de interrupción en los grupos de tratamiento. En la presente revisión sistemática se identificó alto riesgo de sesgo por datos perdidos en el desenlace y algunas preocupaciones por desviaciones en el protocolo, lo cual indica que el panorama de la calidad de la evidencia en relación con las tasas de interrupción no ha cambiado y sigue siendo un punto de pérdida de calidad metodológica de los estudios de tratamiento farmacológico de la AN.
Para terminar, en cuanto a las recomendaciones de las guías de tratamiento, en una revisión de Resmark9 que resume las guías alemanas publicadas más recientemente para el tratamiento de la AN (enero de 2019), encontramos una síntesis bastante completa que incluye las principales recomendaciones de otras guías recientes como la NICE, la australiana, la alemana, la española, la danesa y la de la APA. Una guía más reciente que no se incluye en la revisión de Resmark es la canadiense de tratamiento de niños y adolescentes con trastornos alimentarios26. En general, las guías hacen gran énfasis en la falta de evidencia sobre el tratamiento farmacológico y la gran variabilidad en cuanto a las recomendaciones de tratamiento con psicofármacos para los pacientes con AN.
En comparación con la poca evidencia que existe para el tratamiento farmacológico, está clara la utilidad de la psicoterapia como piedra angular del tratamiento de la AN, aunque aún con bajo nivel de evidencia. Por las diferentes guías, se concluye que en general la terapia cognitivo-conductual, la MANTRA y la SSCM son igual de efectivas y todas son consideradas como primera línea, pero sin evidencia de la superioridad de alguna de las terapias sobre las demás9.
Sin embargo, estos resultados deben ser interpretados teniendo en cuenta las limitaciones de la revisión. La principal limitación es la escasez de estudios y los tamaños de muestra pequeños, ya que condujo a una disminución de la potencia para detectar diferencias en los efectos que se muestran en los resultados por los grandes intervalos de confianza encontrados en la mayoría de los análisis, sumado a que la representatividad de las muestras de estudio no está clara. Otro defecto metodológico importante de los ensayos controlados con placebo incluidos aquí fue su corta duración: uno de ellos tuvo una duración de solo 6 semanas y sin periodo de seguimiento; este periodo es demasiado corto para evaluar el efecto de un antidepresivo en una afección con trastornos psicopatológicos de naturaleza duradera y un curso de recuperación típicamente lento. Además, la validez de la dosificación en la mayoría de los estudios es cuestionable debido a que no se utilizaron análisis de las concentraciones séricas para garantizar la adherencia al tratamiento, teniendo en cuenta que la mala adherencia es una de las principales características de los pacientes con AN.
Este estudio tiene varias fortalezas notables, como una pregunta de revisión específica, criterios de elegibilidad explícitos centrados solo en estudios controlados aleatorizados como los estudios de evaluación de tratamiento más empíricos y una búsqueda bibliográfica exhaustiva y metódica.
Los evidencia disponible en la actualidad acerca de la eficacia y la seguridad del tratamiento de la AN en diferentes poblaciones de pacientes que antipsicóticos y antidepresivos tiene una amplia variabilidad en los resultados y muestra una tendencia a la ganancia de peso y mejoría de la psicopatología relacionada con la AN al administrar olanzapina y fluoxetina; sin embargo, estos resultados no pueden ser generalizados y aplicados con certeza en la práctica clínica a la población, debido a los limitados diseños metodológicos encontrados en la mayoría de los estudios incluidos en esta revisión sistemática, cuyo problema común es un alto riesgo de sesgo en la interpretación de los resultados.
Dadas la gravedad y alta letalidad de la AN en la población, es previsible que en los próximos años esta enfermedad continúe siendo un problema importante de salud pública, por lo que el establecimiento de planes de salud mental que modifiquen la enfermedad continuará mereciendo prioridad. Asimismo es fundamental desarrollar ensayos clínicos de buena calidad metodológica con el fin de determinar el tratamiento más adecuado y permitir la evaluación de los resultados con un seguimiento suficiente y adecuado en este grupo de pacientes.
En concordancia con las revisiones anteriores16,27,28, nuestro trabajo permite concluir que existe información contradictoria sobre la eficacia de los psicofármacos para la AN. A pesar de la falta de tratamientos de elección para la AN, debe tenerse en cuenta el tratamiento conjunto con psicoterapia, y un tratamiento de elección es la terapia cognitivo-conductual.
Conflicto de interesesLos autores declaran no tener conflictos de intereses.