La relación entre eventos adversos y aplicación de medicamentos biológicos en pacientes con diagnóstico de artritis reumatoide ha sido documentada a escala mundial, pero con escasa evidencia en Colombia. Si se asume que los eventos adversos o reacciones medicamentosas con hallazgos clínicos relevantes en la salud, como consecuencia de este tratamiento terapéutico, recaen sobre la calidad de vida del paciente e influyen en los indicadores de salud a escala nacional y en los recursos del sistema, se hace importante evaluar su impacto.
ObjetivosDeterminar la frecuencia de eventos adversos o reacciones adversas relacionados con el uso de medicamentos biológicos en una cohorte de pacientes con diagnóstico de artritis reumatoide de una aseguradora nacional, en el periodo comprendido entre los años 2000 y 2019.
MetodologíaSe realizó un estudio descriptivo, transversal y retrospectivo, con alcance analítico, en pacientes diagnosticados de artritis reumatoide, con terapia biológica, en una aseguradora a escala nacional, con registros en historias clínicas del año 2000 al 2019.
ResultadosSe analizaron 252 registros clínicos de usuarios con diagnóstico de artritis reumatoide y terapia biológica. El 62,7% presentó al menos una reacción adversa y se evaluaron 9 fármacos: tocilizumab, etanercept, adalimumab, abatacept, certolizumab, golimumab, infliximab, rituximab y tofacitinib. Este último es un fármaco incluido en este estudio por solicitud de la aseguradora fuente de la información.
ConclusionesEn la terapia biológica de pacientes con artritis reumatoide las reacciones adversas son frecuentes, y en un 27,3% resultan severas, lo cual describe una situación previamente desconocida en Colombia.
The relationship between adverse events and the application of biological drugs in patients with a diagnosis of rheumatoid arthritis has been documented worldwide, but with little evidence of the situation in Colombia. If adverse events and / or drug reactions with relevant clinical findings in health because of this therapeutic treatment affect the patient's quality of life and influence health indicators at the national level and system resources, it is important to assess their impact.
ObjectivesTo determine the frequency of adverse events and / or adverse reactions related to the use of biological drugs in a cohort of patients diagnosed with rheumatoid arthritis from a national insurer, in the period from 2000 to 2019.
MethodologyA descriptive, cross-sectional, and retrospective study with analytical scope was carried out in patients diagnosed with rheumatoid arthritis, on biological therapy, under a nationwide insurer, with records in their medical records from 2000 to 2019.
Results252 clinical records of users with a rheumatoid arthritis diagnosis and biological therapy were analysed; 62.7% had at least one adverse reaction; nine drugs were evaluated in this study: Tocilizumab, Etanercept, Adalimumab, Abatacept, Certolizumab, Golimumab, Infliximab, Rituximab, and Tofacitinib. Tofacitinib was included in this study at the request of the insurer providing the information.
ConclusionsAdverse reactions with biological therapy in patients with rheumatoid arthritis are frequent and were severe in 27.3%. This is a situation previously unknown in Colombia.
La artritis reumatoide (AR) es considerada una enfermedad inflamatoria crónica que se caracteriza por la destrucción progresiva de las articulaciones sinoviales, con la presentación de signos clínicos característicos que permiten, en ocasiones, determinar una alta sospecha a partir del examen semiológico acucioso1. La AR se clasifica como una enfermedad autoinmune por su comportamiento fisiopatológico determinado por la presencia de autoanticuerpos como el factor reumatoide y los anticuerpos anticitrulinas, los cuales tienen una utilidad clínica especial por ser diagnósticos, por estar precededidos de manifestaciones clínicas más complejas y por tener un valor pronóstico en el tratamiento y en la progresión de la enfermedad.
La AR está íntimamente relacionada con la discapacidad permanente; la Organización Panamericana de la Salud estima que 34 millones de personas la padecen2, lo cual impacta directamente en la capacidad laboral y en el desempeño funcional; por consiguiente, el diagnóstico temprano y el tratamiento oportuno son pilares fundamentales para disminuir la prognosis de esta enfermedad, así como para lograr disminuir su severidad1. El manejo de la AR puede realizarse con múltiples intervenciones asistenciales3, con medicación disease-modifying anti-rheumatic drugs o, alternativamente, con medicamentos biológicos, según el criterio del especialista clínico tratante4; sin embargo, esta alternativa es costosa y cada vez está más relacionada con efectos para la salud de los pacientes y eventos adversos (EA), definidos por la Organización Mundial de la Salud como cualquier lesión o daño no intencional causado por la intervención asistencial, mas no por la enfermedad de base5.
Además del impacto clínico y para la salud pública, los EA asociados con el manejo de enfermedades autoinmunes con fármacos biológicos representan un impacto económico equivalente al 1% del costo total anual del tratamiento6, cifra subestimada, puesto que se carece de estudios globales de mayor exactitud7. En los países desarrollados la literatura científica ha reportado un aumento en la frecuencia de EA asociados al manejo con fármacos biológicos de diversas enfermedades autoinmunes, como la enfermedad de Crohn y la espondilitis anquilosante, además de la AR, entre los que se encuentran, principalmente, efectos neurológicos (activación de esclerosis múltiple), cardiovasculares (exacerbación de fallo cardiaco) y mayor riesgo de infecciones oportunistas (reactivación de tuberculosis)8. Lo anterior ha llevado a la construcción de argumentos de consenso que cuestionan la seguridad de dichos medicamentos en el manejo de estas enfermedades.
En Colombia la AR tiene una prevalencia del 0,56% y para su tratamiento se usa la terapia biológica (TB)6,9; el Ministerio de Salud y de Protección Social adapta la definición internacional de fármacos biológicos como aquellos procedimientos terapéuticos sin uso de información genética10. El Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) reglamenta el uso y la comercialización de este tipo de fármacos, los cuales deben ser registrados, y es obligatorio el reporte de los eventos adversos documentados en los pacientes. Hasta el 2019, el Invima había aprobado los siguientes fármacos de este tipo para el manejo de la AR: infliximab, rituximab, etanercept, abatacept, certolizumab pegol, golimumab, adalimumab y tofacitinib11. Este último se incluyó en este estudio luego de considerar que es una alternativa de manejo de los pacientes con AR, sin embargo, no se clasifica como medicamento biológico, ya que forma parte de la categoría de los sintéticos blanco específico.
A pesar de que en Colombia existe una guía de práctica clínica para el manejo de la AR con medicamentos biológicos, en el país los reportes y la evidencia de EA en AR aún son limitados12, y no existe una línea de base que permita el seguimiento de estos pacientes. Así mismo, se reconoce la seguridad de la TB y su efecto en el mejoramiento de las condiciones de salud, enfermedad e incapacidad funcional de los pacientes13. El objetivo de esta investigación fue identificar los EA o reacciones adversas a medicamentos (RAM) en sujetos con diagnóstico de AR que fueron manejados con TB, entre los años 2000 y 2019.
Población y área de estudioMateriales y métodosTipo de estudioSe realizó una investigación operativa mediante un estudio descriptivo, transversal, con alcance analítico y recolección de la información de manera retrospectiva.
Fuente de informaciónComo fuente de información se tomaron los registros clínicos de una entidad administradora de planes de beneficios (EAPB) que opera a escala nacional, por medio de sus instituciones prestadoras de servicios de salud (IPS) y de una IPS especializada, de una cohorte de pacientes diagnosticados con AR y sometidos a TB del 2000 al 2019. Se usó la clasificación Aranson11,14 de la severidad para el estudio de los RAM, haciendo uso de sus grados y variaciones según la fuente de información. Lo anterior se describe con detalle en los resultados.
Criterios de selecciónInclusión: se incluyeron registros de usuarios con diagnóstico confirmado de AR, que hubieran recibido una sola dosis, varias dosis, suspensión de dosis o cambio del fármaco biológico de manera parcial o definitiva. Debía haber como mínimo 2 consultas en el intervalo definido con anterioridad.
Exclusión: se excluyeron registros de usuarios con diagnóstico de AR psoriásica, AR juvenil, con dificultades en la dispensación del fármaco o con historia clínica incompleta.
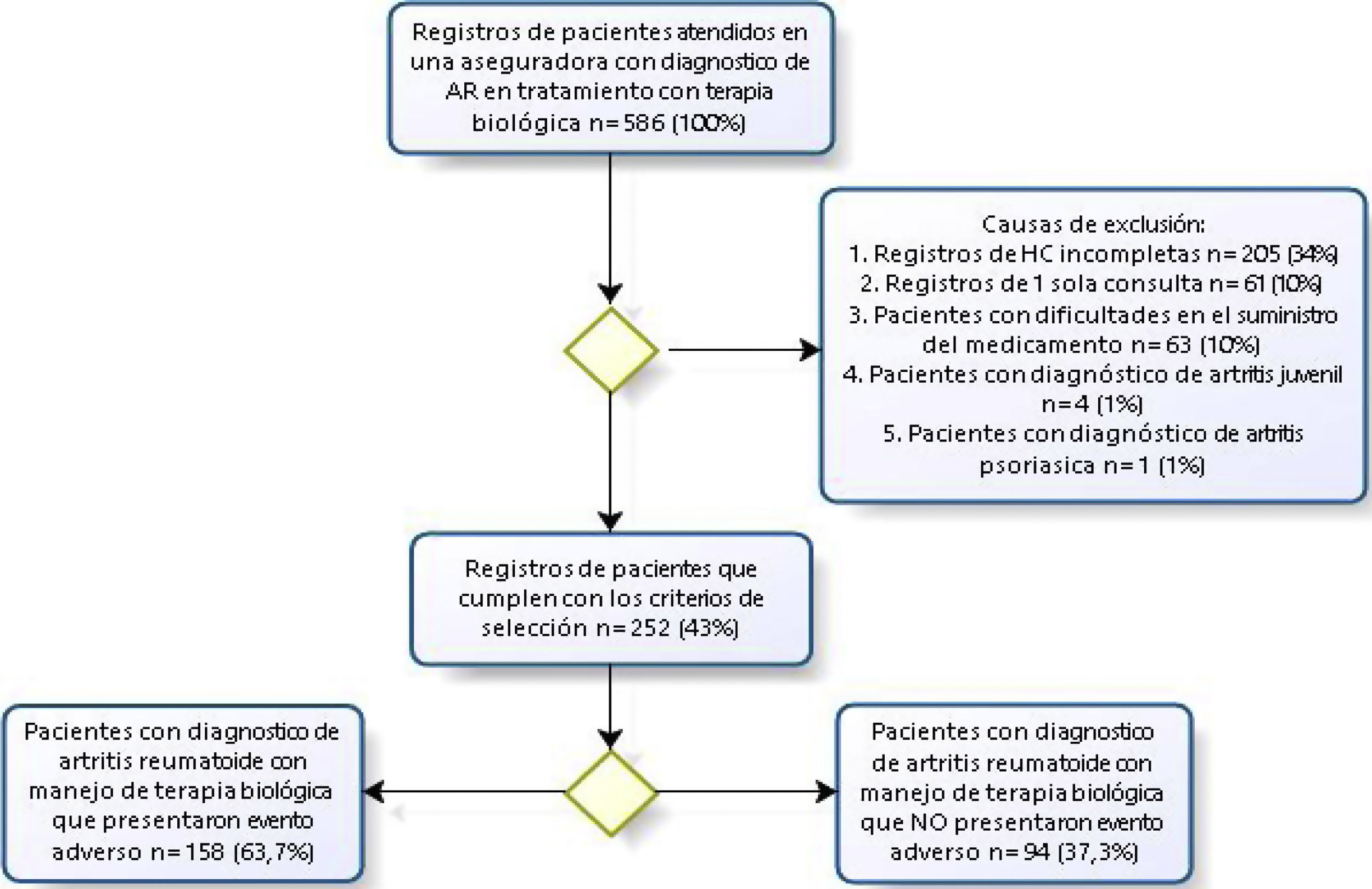
Tamaño de la muestraSe incluyeron 252 registros de historias clínicas de pacientes que cumplieron con los criterios de selección ya definidos, dichos registros se analizaron desde 2 fuentes: IPS especializada e IPS primarias de atención; se recopiló información en una ventana de tiempo que comprendió desde el 1.o de enero del 2000 hasta el 31 de junio del 2019, como se muestra en la figura 1. Se elaboró un instrumento de recolección de datos que facilitó la consecución de información, la construcción de las características estudiadas y su subsecuente análisis estadístico. Para la calidad del dato se hicieron dobles revisiones de registros, se tomaron aleatoriamente 30 ya documentados y se auditaron los datos obtenidos.
Manejo de datos y análisis estadísticoEl análisis univariado se realizó utilizando el software Stata14® (StataCorp, College Station, Texas, EE. UU.), se aplicó estadística descriptiva, y para las variables numéricas se empleó la prueba Shapiro-Wilk. En el caso de las características clínicas y demográficas se evaluó su distribución y la calidad de los datos, se calcularon las medias con su respectiva desviación estándar, en tanto que las variables nominales se resumieron por medio de proporciones; para todas se consideraron diferencias estadísticamente significativas con valores de p≤0,05.
Para el análisis bivariado se utilizó el cálculo de la relación de momios (RM) entre quienes presentaron y quienes no presentaron EA o RAM. Teniendo en cuenta que todos los usuarios revisados en los registros estuvieron expuestos a uno o varios fármacos biológicos, se buscaron diferencias significativas mediante las odds ratio (OR), con sus respectivos intervalos de confianza de 95% y sus valores significativos de p≤0,05, a partir de las pruebas de verificación «t» de Fisher y de distribución de la normalidad de las variables con la prueba Shapiro-Wilk. También se utilizó el cálculo de la relación de prevalencia, realizando tablas de 2×2 para explorar las posibles asociaciones frente a los distintos tipos de exposición y sus hallazgos clínicos. Por último, se realizó un análisis multivariado mediante una regresión logística para revisar las variables que tuvieron correlación con EA o RAM en el análisis bivariado.
Consideraciones éticasEsta investigación fue aprobada como una investigación sin riesgo por los comités de ética de la EAPB, de la IPS especializada y de la Universidad Libre, según la normativa nacional consignada en la Resolución 8430 de 1993 del Ministerio de Salud de Colombia, recogida en el Acta 010-2019.
ResultadosLos criterios de selección fueron aplicados a una población de 586 usuarios con diagnóstico de AR, expuestos a medicamentos biológicos, pertenecientes a una cohorte de una EAPB con cobertura nacional, para lo cual se revisaron los registros médicos del año 2000 hasta el primer semestre del 2019. Se excluyó el 57% (334/586) de los registros de usuarios y se analizó la información del 43% (252/586) restante que cumplía a cabalidad los criterios de inclusión.
La caracterización sociodemográfica de la población de estudio arrojó que las mujeres constituyen la gran mayoría de los usuarios, con un 91% (227/252); la mediana de edad fue de 57 años (RIC: 26-88). La mayoría de los usuarios provenía de la región del Caribe colombiano: 44% (111/252), laboralmente activos en el 54% (136/252) de los casos (tabla 1).
Características sociodemográficas de la población con AR en TB en una aseguradora de Colombia entre los años 2000 y 2019
| Características | Descripción | Medida de resumen |
|---|---|---|
| Edad en años | Años | Media: 56,6; DE: 12,7 |
| Sexo | Hombre | 25 (9%) |
| Mujer | 227 (91%) | |
| Procedencia | Caribe | 111 (44%) |
| Suroccidente | 84 (33,3%) | |
| Nororiente | 35 (13,9%) | |
| Centroriente | 16 (6,3%) | |
| Eje cafetero | 6 (2,4%) | |
| Actividad laboral | Sí | 136 (54%) |
| No | 116 (46%) | |
| Tipo de afiliación | Cotizante | 175 (69,4%) |
| Beneficiario | 77 (30,6%) | |
| Ingresos socioeconómicos | Un salario mínimo | 187 (74%) |
| Más de un salario mínimo | 65 (26%) |
DE: desviación estándar.
La AR se presenta con mayor frecuencia en edades entre 56 y 57 años; el 54% se encontró activo laboralmente.
En las revisiones realizadas se identificaron 30 tipos diferentes de hallazgos clínicos, los cuales se clasificaron como RAM por su soporte bibliográfico o su relevancia clínica, como también por la persistente referencia dentro del grupo de sujetos evaluados como, por ejemplo, adinamia y astenia, comúnmente referenciados por los pacientes con varios medicamentos y encontrados de forma repetitiva (tabla 2).
Frecuencia de reacciones adversas esperadas y no esperadas en los pacientes con AR en TB reportadas en los registros clínicos del año 2000 al 2019
| Reacciones adversas esperadas | N | % |
|---|---|---|
| Mialgias/artralgias | 89 | 24,2 |
| Cefalea severa (migraña) | 53 | 14,4 |
| Síndromes gripales de repetición | 51 | 13,9 |
| Síndrome de Sjögren | 39 | 10,6 |
| Dislipidemia | 22 | 6,0 |
| TBC | 19 | 5,2 |
| Urticaria en el sitio de punción | 15 | 4,1 |
| Herpes zoster | 13 | 3,5 |
| Exacerbación de EPOC | 12 | 3,3 |
| Elevación de transaminasas | 9 | 2,4 |
| Adinamia y astenia | 8 | 2,2 |
| Psoriasis | 5 | 1,4 |
| Exacerbación fallo cardiaco | 6 | 1,6 |
| Hepatitis B | 2 | 0,5 |
| LES de novo | 2 | 0,5 |
| Vasculitis | 1 | 0,3 |
| Desmielinización miembros superiores | 1 | 0,3 |
| Prurito en el sitio de punción | 1 | 0,3 |
| Reacciones adversas no esperadas | N | % |
|---|---|---|
| Esteatosis hepática | 4 | 1,1 |
| Fiebre durante la administración | 3 | 0,8 |
| Mareo/vértigo | 3 | 0,8 |
| Dermatitis | 2 | 0,5 |
| CA de tiroides | 1 | 0,3 |
| Alopecia | 1 | 0,3 |
| Bradicardia durante la administración | 1 | 0,3 |
| Diarrea | 1 | 0,3 |
| IVU de repetición | 1 | 0,3 |
| Hematoma en el sitio de punción | 1 | 0,3 |
| Dolor torácico y disnea durante la administración | 1 | 0,3 |
| Taquicardia y dolor torácico durante la administración | 1 | 0,3 |
Las reacciones adversas esperadas hacen referencia a las documentadas en la bibliografía, en tanto que las reacciones adversas no esperadas se documentan como hallazgos clínicos a partir de la casuística postaplicación de la terapia biológica, en la cual las mialgias/artralgias son las más frecuentes en el primer grupo, mientras que la esteatosis hepática es la más frecuente en el segundo grupo.
CA: cáncer; EPOC: enfermedad pulmonar obstructiva crónica; IVU: infección de vías urinarias; LES: lupus eritematoso sistémico; TBC: tuberculosis.
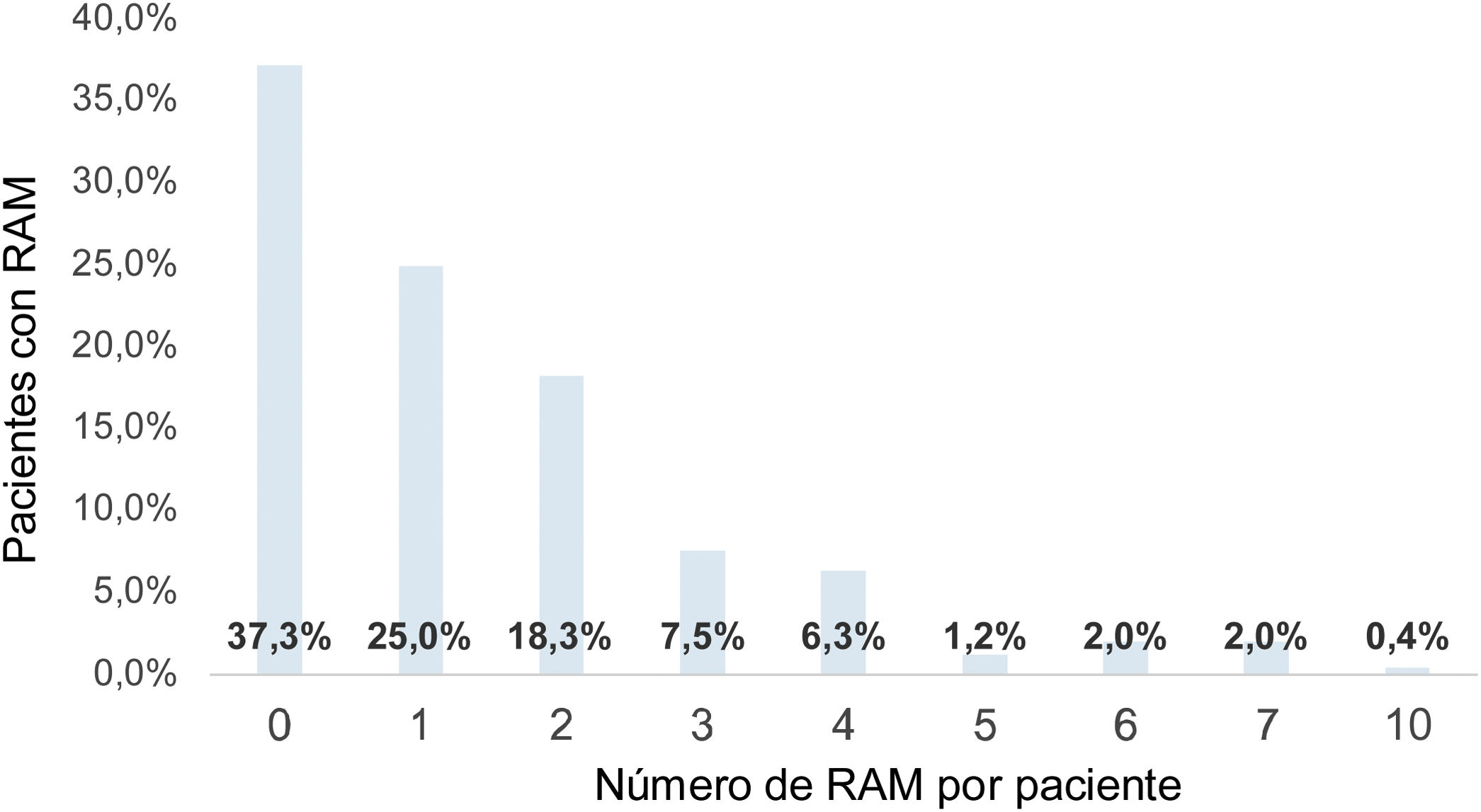
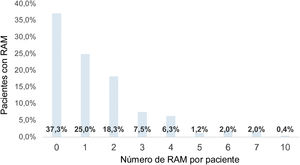
El etanercept fue el medicamento con más RAM identificadas (20 diferentes), así como el infliximab fue el fármaco que presentó menos tipos de RAM (ocho diferentes); el número promedio de RAM por paciente fue de 1,5 eventos (σ: 1,71, lim inf: 0 - lim sup: 10); por tanto, cada paciente con AR expuesto a TB tuvo la presencia de al menos una RAM durante el tratamiento indicado (fig. 2).
El análisis bivariado mostró una relación entre la exposición al medicamento biológico y la presencia de hallazgos clínicos clasificados en nuestro estudio como RAM. En tal sentido, se encontraron diferencias significativas en tres factores revisados: mayor riesgo para el género masculino (OR: 2,5; IC 95%: 1,02-6,67; p=0,02), mayor riesgo en tiempo de exposición al medicamento biológico por más de dos años (OR: 3,1; IC 95%: 1,6-5,56; p=0,0001) y factor protector para presentar RAM relacionado con el hecho de recibir TB con un medicamento vs. recibir más de un medicamento (OR: 0,3; IC 95%: 0,17-0,62; p=0,0002) (tabla 3).
Factores relacionados con la presencia de RAM en pacientes con diagnóstico de AR con TB, documentada en los registros clínicos de los años 2000 al 2019
| Características | Descripción | N | RAM | OR | IC 95% | valor p | |
|---|---|---|---|---|---|---|---|
| Sí | No | ||||||
| Sexo | Hombre | 25 | 15 | 10 | 2,5 | 1,02 – 6,65 | 0,02 |
| Mujer | 227 | 84 | 143 | ||||
| Edad | Mayor igual 60 años | 111 | 71 | 40 | 1,1 | 0,7 – 1,9 | 0,7 |
| Menores 60 años | 141 | 87 | 54 | ||||
| Tipo de afiliación | Cotizante | 175 | 107 | 68 | 0,8 | 0,43 – 1,45 | 0,4 |
| Beneficiario | 77 | 51 | 26 | ||||
| Ingresos socioeconómicos | Un salario mínimo | 187 | 120 | 67 | 1,3 | 0,69 – 2,36 | 0,4 |
| Más de un salario mínimo | 65 | 38 | 27 | ||||
| Actividad laboral | Inactivo | 136 | 85 | 51 | 1 | 0,57 – 1,70 | 0,94 |
| Activo | 116 | 73 | 43 | ||||
| Numero de medicamentos biológicos recibidos | Un biológico | 168 | 92 | 76 | 0,3 | 0,17 – 0,62 | 0,0002 |
| Más de un biológico | 84 | 66 | 18 | ||||
| Tiempo de utilización de la terapia biológica | Más de 2 años con terapia biológica | 177 | 125 | 52 | 3,1 | 1,6 – 5,56 | 0,0001 |
| Menos de 2 años con terapia biológica | 75 | 33 | 42 | ||||
Los factores de riesgo más característicos para ocasionar RAM fueron: sexo masculino, OR: 2,5; exposición a TB por más de 2 años, OR: 3,1; y uso de más de un medicamento biológico, OR: 0,3.
AR: artritis reumatoide; IC: intervalo de confianza; OR: odds ratio; RAM: reacción adversa a medicamento; TB: terapia biológica.
Sin embargo, al correr el modelo de regresión logística se logró el ajuste de los OR crudos y se encontraron dos variables modificadoras del efecto: tiempo de exposición al medicamento biológico por más de dos años y TB con un medicamento vs. recibir más de un medicamento. Esta inversión de los valores OR es un hallazgo exótico que plantea nuevos interrogantes, como la evaluación de distintos rangos de tiempo frente a la exposición propuesta por cada medicamento, lo cual no fue posible para este estudio debido a que el dato específico de duración por cada biológico no se pudo obtener desde la fuente de información, pero sí se tuvo claridad en el dato de inicio y finalización de la TB en general. Con la otra variable modificadora del efecto: TB con un medicamento vs. recibir más de un medicamento, se requiere también una evaluación más profunda.
De esta manera se pone el énfasis en la necesidad de estudios analíticos que evalúen estas dos variables con un mejor control del sesgo de información. Se determinó el género masculino como variable confusora en el ajuste con este mismo modelo. No se encontraron diferencias significativas entre las características sociodemográficas y la presencia de RAM. El modelo de regresión logística utilizado fue automatizado (stepwise), lo cual impidió operar manualmente las variables en cuestión (tabla 4).
Regresión logística aplicada al tiempo de inicio del medicamento biológico y número de medicamentos biológicos recibidos en los registros clínicos de pacientes con AR entre los años 2000 y 2019
| Característica | Descripción | N | RAM | OR | IC (95%) | valor p | OR ajustado | IC (95%) | Valor de p | |
|---|---|---|---|---|---|---|---|---|---|---|
| Sí | No | |||||||||
| Número de | Un | 168 | 92 | 76 | ||||||
| medicamentos | biológico | 0,3 | 0,17-0,62 | 0,0002 | 2,02 | 1,31-3,14 | 0,002 | |||
| biológicos recibidos | Más de un biológico | 84 | 66 | 18 | ||||||
| Tiempo de uso | Más de 2 años | 177 | 125 | 52 | 0,81- | |||||
| de la TB | 3,1 | 1,6-5,56 | 0,0001 | 0,89 | 0,98 | 0,020 | ||||
| Menos de 2 años | 75 | 33 | 42 | |||||||
El número de biológicos recibidos y el tiempo de uso de TB son características que permiten predecir una tendencia a presentar RAM.
AR: artritis reumatoide; IC: intervalo de confianza; OR: odds ratio; RAM: reacción adversa a medicamento; TB: terapia biológica.
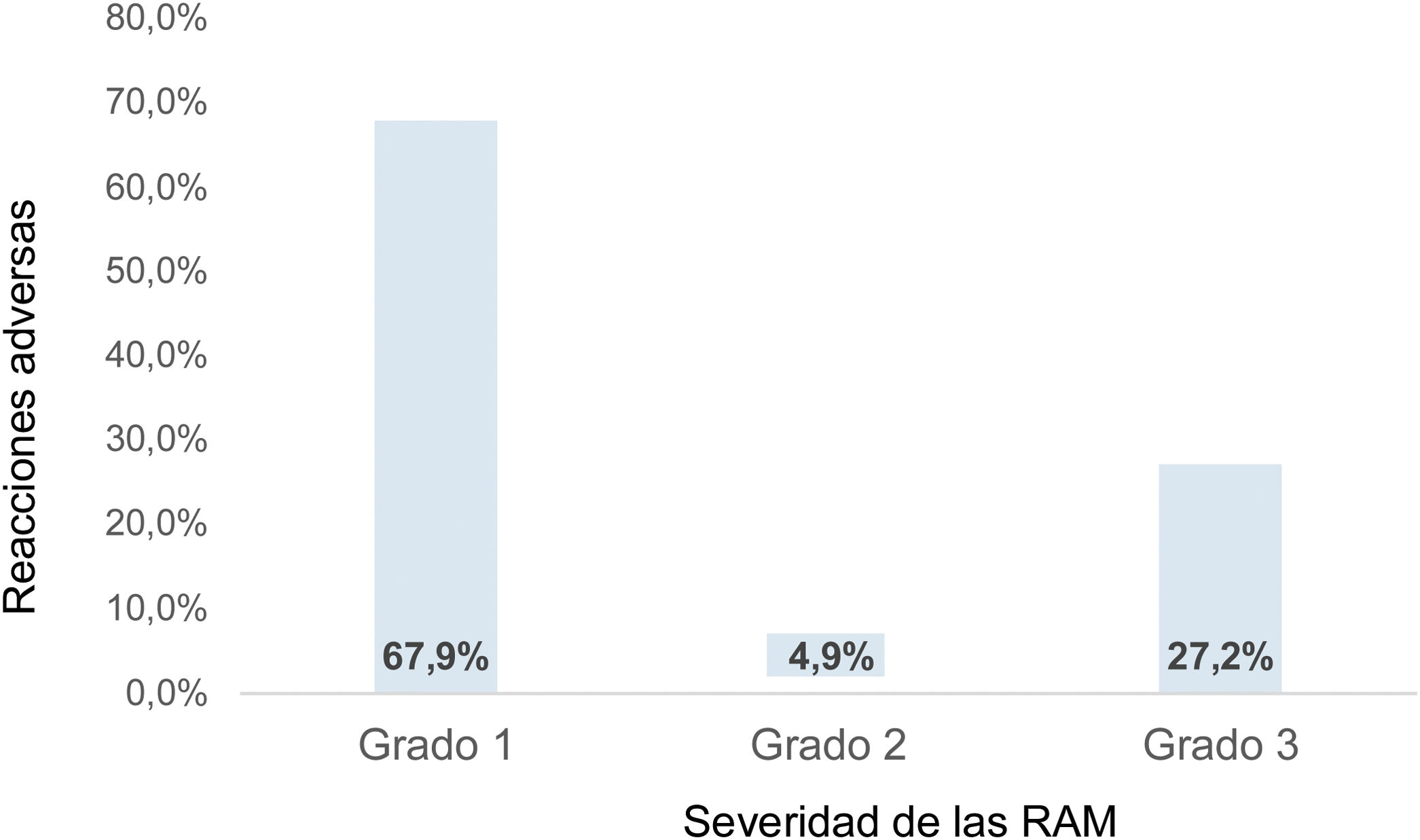
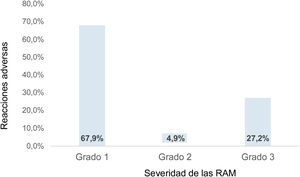
De acuerdo con la clasificación Aranson11,14 de la severidad para el estudio de los RAM, teniendo en cuenta que en el grado 1 no se requiere cambio en la dosificación, que en el grado 2 se necesita el cambio de la dosis y que en el grado 3 se precisa la suspensión del tratamiento, se realizó la clasificación según la conducta tomada por el médico tratante. Debido a las limitaciones de los registros médicos no se usaron los subtipos A, B o C. De esta manera, se relacionan 368 RAM totales que ocurrieron en esta población, de los cuales el 67,9% (250/368) se clasificó como RAM grado 1 (fig. 3).
Distribución de la severidad del total de RAM reportados en los registros médicos de los pacientes con AR entre los años 2000 y 2019.
El 27,2% de las RAM se clasificó con el grado más severo de la escala Aranson. Los registros clínicos impidieron establecer una tendencia del número de RAM por año.
RAM: reacción adversa a medicamento.
Las RAM más frecuentes fueron las mialgias/artralgias en el 24,2% (89/368), la cefalea (migraña) en el 14,4% (53/368) y los síndromes gripales de repetición en el 13,9% (51/368).
Las RAM que se presentaron con todos los medicamentos biológicos fueron: síndrome de Sjögren, migraña, mialgias/artralgias y síndromes gripales de repetición. En cuanto a la razón de prevalencias de los RAM comparada entre medicamentos, se encontró que la psoriasis es cinco veces más prevalente en rituximab (RP=5,0), la descompensación de la enfermedad pulmonar obstructiva crónica es 4,2 veces más prevalente con infliximab (RP=4,2) y la elevación de las transaminasas fue 3,6 veces más prevalente con tocilizumab (tabla 5).
Detalle de las RAM según el medicamento biológico recibido y reportados en los registros médicos de los pacientes con AR entre los años 2000 y 2019
| Hallazgos clínicos RAM | ABA | ADA | CTZ | ETN | GOL | IFX | RTX | TCZ | TOF |
|---|---|---|---|---|---|---|---|---|---|
| Mialgias/artralgias | 16,7% | 19,4% | 27,9% | 20,8% | 36,0% | 25,0% | 27,3% | 32,0% | 44,4% |
| Cefalea severa (migraña) | 16,7% | 19,4% | 9,3% | 9,4% | 24,0% | 12,5% | 18,2% | 20,0% | 22,2% |
| Síndromes gripales de repetición | 13,6% | 12,9% | 7,0% | 13,4% | 16,0% | 25,0% | 13,6% | 16,0% | 33,3% |
| Síndrome deSjögren | 10,6% | 3,2% | 4,7% | 11,4% | 4,0% | 25,0% | 13,6% | 8,0% | 11,1% |
| Dislipidemia | 4,5% | 6,5% | 4,7% | 6,0% | 12,0% | 0,0% | 0,0% | 12,0% | 11,1% |
| TBC | 1,5% | 3,2% | 2,3% | 6,7% | 4,0% | 0,0% | 4,5% | 16,0% | 0,0% |
| Urticaria en el sitio de punción | 4,5% | 9,7% | 2,3% | 3,4% | 0,0% | 12,5% | 4,5% | 4,0% | 0,0% |
| Herpes zoster | 4,5% | 3,2% | 2,3% | 5,4% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Exacerbación de EPOC | 4,5% | 0,0% | 0,0% | 2,7% | 4,0% | 12,5% | 0,0% | 12,0% | 0,0% |
| Elevación de transaminasas | 1,5% | 6,5% | 0,0% | 1,3% | 0,0% | 0,0% | 4,5% | 12,0% | 0,0% |
| Adinamia y astenia | 0,0% | 3,2% | 2,3% | 2,7% | 0,0% | 0,0% | 4,5% | 4,0% | 11,1% |
| Exacerbación fallo cardiaco | 0,0% | 0,0% | 2,3% | 2,0% | 4,0% | 0,0% | 0,0% | 4,0% | 0,0% |
| Psoriasis | 0,0% | 3,2% | 0,0% | 1,3% | 0,0% | 0,0% | 9,1% | 0,0% | 0,0% |
| Esteatosis hepática | 1,5% | 0,0% | 0,0% | 1,3% | 0,0% | 0,0% | 4,5% | 0,0% | 0,0% |
| Fiebre durante la administración | 1,5% | 3,2% | 2,3% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Mareo/vértigo | 0,0% | 3,2% | 0,0% | 1,3% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Hepatitis B | 0,0% | 0,0% | 2,3% | 0,7% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| LES de novo | 0,0% | 0,0% | 0,0% | 0,7% | 0,0% | 12,5% | 0,0% | 0,0% | 0,0% |
| Dermatitis | 0,0% | 0,0% | 0,0% | 0,0% | 4,0% | 0,0% | 4,5% | 0,0% | 0,0% |
| Vasculitis | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 12,5% | 0,0% | 0,0% | 0,0% |
| Desmielinización miembros superiores | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 11,1% |
| CA de tiroides | 0,0% | 3,2% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Alopecia | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 11,1% |
| Bradicardia durante la administración | 1,5% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Diarrea | 0,0% | 0,0% | 0,0% | 0,7% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| IVU de repetición | 0,0% | 0,0% | 0,0% | 0,7% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Prurito en el sitio de punción | 0,0% | 0,0% | 2,3% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Hematoma en sitio de punción | 0,0% | 0,0% | 0,0% | 0,7% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Dolor torácico y disnea durante la administración | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 4,0% | 0,0% |
| Taquicardia y dolor torácico durante la administración | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 4,5% | 0,0% | 0,0% |
Se registraron 368 RAM en la muestra. El rituximab se evidencia en tendencia con la RAM psoriasis, así como la EPOC con el infliximab y la elevación de transaminasas con la aplicación de tocilizumab.
ABA: abatacept; ADA: adalimumab; AR: artritis reumatoide; CA: cáncer; CTZ: certolizumab; EPOC: enfermedad pulmonar obstructiva crónica; ETN: etanercept; GOL: golimumab; IFX: infliximab; IVU: infección de vías urinarias; LES: lupus eritematoso sistémico; RTX: rituximab; TBC: tuberculosis; TCZ: tocilizumab; TOF tofacitinib.
En Colombia se ha podido establecer la prevalencia de la AR y sus características sociodemográficas9, sin embargo, la evidencia respecto a la seguridad del paciente frente a las opciones terapéuticas, incluida la TB, es aún escasa15. Esta investigación reveló un panorama situacional y contextual en una EAPB con cobertura en el territorio, sobre las RAM relacionadas con los medicamentos biológicos para el manejo de esta enfermedad.
Las consideraciones analizadas aquí parten del estudio de otros aspectos sociodemográficos como la edad, la ubicación territorial, el tipo de afiliación y la actividad laboral, que no mostraron ningún vínculo con el efecto en la salud del usuario durante la exposición a la TB16.
Entre las características clínicas relevantes se encontró que el 37,5% de las RAM se relaciona con la aplicación del etanercept, que a pesar de ser el más frecuente no se estableció una tendencia en relación con las RAM severas; al compararse con otros medicamentos dentro de la muestra evaluada este hallazgo también fue referenciado en la literatura7.
Determinar las RAM más frecuentes cuestiona el verdadero impacto del uso de medicamentos biológicos para el manejo de la AR, ya que las mialgias y las artralgias fueron las condiciones que más se encontraron en este estudio, teniendo en cuenta que podría ser un determinante importante para la calidad de vida del usuario y su potencial laboral, en términos de discapacidad temporal y permanente, que se asocia con las cifras mencionadas por los organismos de salubridad a escala internacional2,17.
Otra RAM relevante fue la presencia de tuberculosis posterior a la TB18,19, con una proporción del 5,2% (252/19), la cual sin ser una RAM de alta frecuencia debe tener un interés de control y vigilancia por parte de los médicos tratantes, ya que es una enfermedad de alto impacto en la salud pública en Colombia; estos hallazgos fueron reportados también en Canadá y en países europeos, luego de evaluarse la relación de esta enfermedad con la exposición a TB18,19.
Entre las RAM de bajo impacto estadístico, pero con relevancia clínica en este estudio, deben mencionarse la presencia de un caso de desmielinización de miembros superiores20, al igual que, como se referencia en un reporte de casos en Irlanda, la relación entre rituximab y enfermedades desmielinizantes21. Además, se describió un solo caso de CA de tiroides22, lo cual se puede relacionar con la alteración de la respuesta inmunológica que puede favorecer la activación de la oncogénesis.
Las RAM descritas en esta investigación impactan considerablemente la calidad de vida y el bienestar de los usuarios de TB, teniendo en cuenta que el 63% de los usuarios presentó al menos una RAM que comprometía su seguridad bajo la aplicación de esta tecnología. La revisión de la evidencia es controvertida con relación a la presencia de RAM y el uso de medicamentos biológicos, debido a que los conflictos de intereses median en mostrar resultados objetivos e imparciales; incluso en revisiones de RAM en otras enfermedades susceptibles de ser tratadas con esta terapia no se encontraron datos precisos de diferentes desenlaces.
Por otra parte, es posible que exista una relación entre el tiempo de exposición a TB y la presencia de RAM, así como también con recibir un medicamento biológico o recibir más de uno frente a la presencia de RAM; los análisis estadísticos obtenidos solamente permiten plantear estas relaciones como nuevas hipótesis que deben ser verificadas con nuevos estudios. En la literatura científica revisada no se encontraron seguimientos a cohortes completas de pacientes con todo tipo de TB; se encontraron, principalmente, reportes de casos aislados23 o evaluaciones económicas de hasta tres medicamentos7, lo que fortaleció la necesidad de este estudio.
La severidad grado 3 en la presentación de RAM tuvo una proporción importante (27%), lo cual puede influir en el panorama de seguridad de estos medicamentos; por tanto, estos resultados son una aproximación inicial para que las instituciones de salud que manejan este tipo de terapias realicen ajustes en sus procesos de seguridad del paciente, como lo recomienda la guía del Ministerio de Salud24.
LimitacionesEl análisis secundario de una base de datos limitó la información sobre las definiciones de desenlaces clínicos o RAM o EA, ya que en los registros clínicos analizados, la calidad del dato (sesgo de información) era variable y heterogénea, lo que hizo difícil la determinación de EA o RAM y su clasificación. Esto, sumado a la reducción de registros clínicos de médicos especialistas, el desconocimiento del tema por parte de la red prestadora de servicios para indagar a fondo sobre los síntomas y los signos presentados por los pacientes luego del uso del medicamento biológico, así como la ausencia de un seguimiento continuo y juicioso de estos sucesos, resultó frecuente para esta investigación.
No fue posible cuantificar la característica de tiempo de exposición específica para cada medicamento, ya que algunos de los registros clínicos no tenían claridad sobre la fecha del inicio y la finalización de cada exposición al medicamento, lo que redujo significativamente la población intervenida, teniendo en cuenta que los registros analizados tuvieron un control de calidad desde el análisis del dato en las IPS especializadas y en las de atención primaria. Para el análisis de la información, los OR crudos presentaron una condición inusual, por lo cual la discusión y las conclusiones se exponen a partir de tendencias en la interpretación de la medición de variables, dejando para otros estudios el precedente de utilizar otras herramientas de medición, proyectando el aumento o no del tamaño de la muestra o generando un diseño investigativo de corte analítico.
ConclusionesLas RAM producidas por la exposición a la TB en la AR son frecuentes y severas; este estudio logró la proyección de un panorama previamente desconocido, indagando sobre el reajuste del concepto de riesgo-beneficio, tan conocido en la práctica clínica. Profundizar en la investigación sobre la seguridad del paciente permitirá generar alertas para la detección temprana por parte de médicos especialistas y médicos expertos, dado que el desconocimiento actual del tema puede ser parte del problema, puesto que no se indaga clínicamente en el paciente en búsqueda de posibles efectos negativos en su bienestar biopsicosocial derivados directa e indirectamente de la terapia.
El hecho de poner en evidencia el grado de severidad más grave (que implica la suspensión del medicamento por las RAM), como una proporción grande dentro de los grupos clasificados, ratifica la importancia manifestada previamente de ahondar en el tema de seguridad del paciente en relación con la medicación biológica de la terapia para la AR, considerando que el paciente expuesto a esta indicación durante su tratamiento debe ser evaluado de manera rutinaria, sistemática y acuciosa, con el fin de identificar oportunamente la presencia de RAM.
RecomendacionesSe considera que las EAPB, las IPS y los médicos especialistas relacionados con la atención de la AR deben contar con una herramienta tecnológica de fácil acceso que les permita medir el riesgo de presentar RAM durante la TB, haciendo un seguimiento estricto de estos usuarios mediante registros clínicos con información óptima, permitiendo prácticas clínicas seguras, mitigando el riesgo y beneficiando la calidad de vida de los usuarios. La comunicación efectiva y constante de toda la red de atención en salud de los programas de seguridad brindaría un soporte favorable para la prevención de RAM.
Este estudio promueve la realización de investigaciones relacionadas con las condiciones descritas en los hallazgos clínicos en salud pública, como la tuberculosis y la hepatitis B, haciendo énfasis en su impacto en la comunidad; también se recomienda incluir de forma detallada el costo de las RAM dentro de evaluaciones económicas de este tipo de terapia, para llegar a conclusiones integrales que permitan tomar decisiones clínicas acertadas. Con el advenimiento de nuevos tipos de medicamentos biológicos cada año, para distintas enfermedades, es recomendable un equipo de trabajo de profesionales especializados en seguridad del paciente de cada uno de los actores del sistema con miras a la vigilancia y prevención de las RAM.
Conflicto de interesesLos autores manifiestan no tener ningún conflicto de intereses.
A las instituciones de salud por permitir el acceso. A los pacientes por ser fuente anónima de información.