La hemoglobina A1c (HbA1c) es ampliamente utilizada en la determinación del estado glucémico de pacientes con diabetes mellitus. El objetivo de este estudio fue comparar 2 métodos automatizados para medir HbA1c basados en diferentes principios de medida, evaluar la correlación entre ambos y su practicabilidad.
MétodosSe analizaron 622 muestras mediante 2 sistemas analíticos con fundamentos diferentes de medición: cromatografía líquida de alta eficiencia (HPLC) (analizador ADAMS A1c HA-8160; A. Menarini Diagnostics, Italia) e inmunoturbidimetría (Tina-quant Hemoglobin A1c Gen.3, plataforma Cobas 6000; Roche Diagnostics, Suiza). Ambos métodos fueron calibrados según el procedimiento de referencia de la IFCC. Se valoró la correlación entre ambos métodos mediante los análisis de regresión de mínimos cuadrados y Passing-Bablok (R programa v.2.11.1). También se registró el tiempo de puesta en marcha, las tareas de mantenimiento diario y el rendimiento de los 2 instrumentos.
ResultadosLa correlación fue muy alta tanto por mínimos cuadrados (ordenada en el origen 0.05, pendiente 0.98) como en Passing-Bablok (ordenada en el origen 0,10, pendiente 1,00). El tiempo invertido diariamente para la puesta en marcha del analizador HA-8160 fue de 25min y el tiempo de finalización fue de 15min. Las tareas de mantenimiento del Cobas 6000 al inicio y fin del día son procesos automatizados. El rendimiento de los analizadores fue 20 muestras/h en el HA-8160 y 100 muestras/h en el Cobas 6000. El sistema analítico cuyo principio de medida es HPLC incluye también el análisis manual de cada cromatograma.
ConclusionesExiste una correlación excelente entre los métodos de HPLC e inmunoturbidimétrico. La ventaja del sistema analítico que utiliza la inmunoturbidimetría es la optimización del tiempo de procesamiento de las determinaciones de HbA1c, lo que reduce el coste unitario de la prueba.
Hemoglobin A1c (HbA1c) is widely used to assess glycemic status in patients with diabetes mellitus. The purpose of this study was to compare 2 automated analytical systems to measure HbA1c that use different measurement principles, evaluating the correlation between the two methods, as well as their ease of use.
MethodsA total of 622 samples were analyzed using 2 methods: high performance liquid chromatography (HPLC) (analyzer ADAMS A1c HA-8160; A. Menarini Diagnostics, Italy) and an immunoturbidimetric assay (Tina-quant Hemoglobin A1c Gen.3, Cobas 6000 analyzer; Roche Diagnostics, Switzerland). Both methods were calibrated in accordance with IFCC reference measurement procedure. The correlation between the two methods was assessed by least squares and Passing-Bablok linear regression analyses (R program v.2.11.1). The daily start-up time of the 2 instruments used, daily maintenance tasks, and determination of throughput were also recorded.
ResultsThere was a strong correlation between the results generated by the two test methods using both the least squares (intercept 0.54; slope 0.98) and Passing-Bablok (intercept 0.10; slope 1.00) regression methods. The time spent daily for the start-up of the HA-8160 analyzer was 25min and completion time was 15min. Maintenance tasks for the Cobas 6000 analyzer at the beginning and end of the day are automated processes. The throughput for the HA-8160 analyzer was 20 samples/h, and 100 samples/h for the Cobas 6000 analyzer. The HPLC method also included a time-consuming manual analysis of each chromatogram.
ConclusionsAn excellent correlation was observed between the HPLC and immunoturbidimetric methods. The advantages of the immunoturbidimetric method are optimization of processing time of HbA1c tests and a reduction in the unit cost per test.
En 1999, el International Expert Committee se pronunció a favor del diagnóstico de diabetes mellitus (DM) mediante la determinación de la B-hemoglobina glicada (HbA1c) debido a la correlación de esta con el estado glucémico a medio plazo1,2. Esta utilidad se suma a la habitual utilización de la hemoglobina glicada en pacientes con diabetes ya diagnosticada parámetro indicador del control glucémico crónico y del riesgo de sufrir complicaciones crónicas2.
Entre las ventajas de utilizar la HbA1c para el diagnóstico de la DM encontramos las siguientes: puede evaluarse sin condiciones horarias o de ingesta previa específicas (por ejemplo, sin necesidad de períodos de ayuno previos) y es menos susceptible de verse alterada por factores externos como el estrés o procesos infecciosos que pueden modificar el resultado de las pruebas clásicas de glucemia3.
En la búsqueda y desarrollo de métodos más sensibles y específicos para la evaluación de parámetros analíticos relacionados con la glucemia existen numerosas evidencias que consideran que los resultados de la medición de la HbA1c tienen una adecuada concordancia con la concentración media de glucosa plasmática4 y son útiles para el seguimiento de pacientes con DM y su cribado en población asintomática1,5.
En 2001 fue aprobado el método referencia desarrollado por la International Federation of Clinical Chemistry and Laboratory Medicine (IFCC), basado en el corte por acción de una endoproteinasa del hexapéptido N-terminal de las cadenas β, tanto glicado (HbA1c) como no glicado (HbA1o), quedando definida la HbA1c como la β-hemoglobina glicada en la valina N-terminal −β-N(1-deoxi)-fructosil-hemoglobina−6,7, y expresándose como milimoles de deoxifructosil-hemoglobina por mol de hemoglobina total. A partir de este método de referencia se ha conseguido un sistema de estandarización internacional8.
Es posible cuantificar la HbA1c mediante diversos métodos analíticos basados en las diferentes propiedades que presenta la HbA1c con respecto a otras hemoglobinas glicadas. Los principios de medida más utilizados incluyen la cromatografía por intercambio de iones, la electroforesis, la cromatografía de afinidad y el inmunoanálisis, que evalúan diferentes productos glicados y se reportan en diferentes unidades. Estos métodos se diferencian, principalmente, en el procedimiento de medida, velocidad, características de los instrumentos y tipo de reactivos7.
El método de cromatografía líquida de alta eficiencia (HPLC, por sus siglas en inglés) cuantifica los valores de HbA1c en función de la determinación cromatográfica de intercambio catiónico en fase inversa; en cambio, las mediciones basadas en el inmunoanálisis turbidimétrico de inhibición para sangre total hemolizada permiten cuantificar la HbA1c mediante la determinación del analito definido por la IFCC. Ambos métodos deben calibrarse según el método de referencia de la IFCC2.
Debido a la nueva indicación de la HbA1c en el diagnóstico de la DM según las guías de la American Diabetes Association y al incremento de la prevalencia e incidencia de esta patología, lo que se traduce en un aumento importante en el número de determinaciones solicitadas de HbA1c, existe la necesidad de contar con analizadores altamente automatizados que permitan mejorar los tiempos de procesamiento de las muestras y obtención de resultados. El presente estudio se ha realizado con el objetivo de comparar 2 métodos automatizados para medir HbA1c basados en diferentes principios de medida, evaluando la correlación entre ambos así como su practicabilidad en la detección y seguimiento de los pacientes con DM.
Material y métodosSe analizaron muestras de pacientes mayores de 18 años sanos, sin hemoglobinopatías conocidas, y cuyas analíticas se realizaron como parte de un estudio multicéntrico llevado a cabo en 8 hospitales de España, que evaluaba la utilidad de la medición de la HbA1c versus la glucemia en ayunas como prueba diagnóstica de la DM, la correlación entre métodos y la influencia de parámetros hematológicos (anemia y ferropenia según criterios de la Organización Mundial de la Salud) en la población sana sin diagnóstico de DM. Para la evaluación de la concordancia entre métodos que aquí se presenta se incluyeron todas las muestras. Las determinaciones de HbA1c se realizaron de forma centralizada en uno de los hospitales participantes. Se excluyeron las muestras provenientes de mujeres embarazadas.
El protocolo de estudio fue aprobado por los Comités Éticos de referencia. Tras la autorización de los pacientes para la extracción, la muestra de sangre se obtuvo en tubo con anticoagulante EDTA, distribuyéndola posteriormente en 3 alícuotas de 0,8ml (una para procesamiento y 2 de reserva).
El análisis de las muestras se realizó con el método de HPLC (HPLC, analizador ADAMS A1c HA-8160; A. Menarini Diagnostics, Italia) y con el método inmunoturbidimétrico (Tina-quant Hemoglobin A1c Gen.3, plataforma Cobas 6000; Roche Diagnostics, Suiza), estandarizados ambos métodos al procedimiento de referencia de la IFCC.
Los datos obtenidos se procesaron y analizaron mediante pruebas de correlación de Pearson, de regresión lineal por el método de mínimos cuadrados y también por el método de Passing-Bablok. Asimismo, se valoraron las diferencias entre los métodos mediante el análisis de Bland-Altman (R programa v.2.11.1).
Se registraron los tiempos de puesta en marcha diarios de ambos autoanalizadores, así como el correspondiente a tareas de mantenimiento diarias y el rendimiento de los 2 instrumentos en función del número de pruebas realizadas por hora.
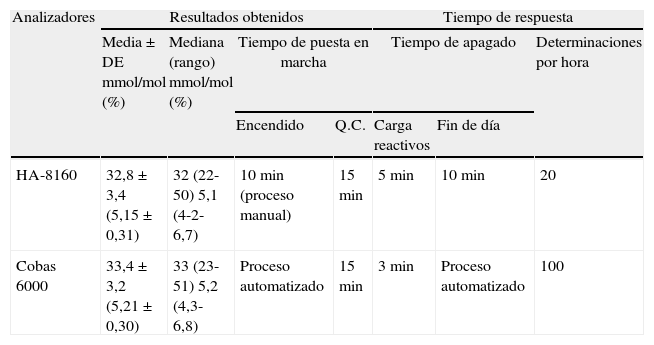
ResultadosLa comparación de métodos se realizó en función de 622 muestras procesadas con ambos analizadores, HA-8160 y Cobas 6000. Los resultados de tendencia central, medias y medianas así como de dispersión, desviación estándar (DE) y rangos se presentan en la tabla 1.
Resumen de los resultados en la determinación de la HbA1c en los analizadores HA-8160 y Cobas 6000
| Analizadores | Resultados obtenidos | Tiempo de respuesta | |||||
| Media±DE mmol/mol (%) | Mediana (rango) mmol/mol (%) | Tiempo de puesta en marcha | Tiempo de apagado | Determinaciones por hora | |||
| Encendido | Q.C. | Carga reactivos | Fin de día | ||||
| HA-8160 | 32,8±3,4 (5,15±0,31) | 32 (22-50) 5,1 (4-2-6,7) | 10min (proceso manual) | 15min | 5min | 10min | 20 |
| Cobas 6000 | 33,4±3,2 (5,21±0,30) | 33 (23-51) 5,2 (4,3-6,8) | Proceso automatizado | 15min | 3min | Proceso automatizado | 100 |
DE: desviación estándar; min: minutos; Q.C.: control de calidad.
Resumen de los resultados descriptivos. Los resultados de la media y DE por ambos métodos se indican con un decimal más en ambas unidades IFCC y DCCT.
La media de edad de los 622 pacientes fue de 40,82 años (rango: 18-92 años). La media de hemoglobina total de los pacientes fue de 14,2g/dL, siendo la DE de 1,42.
Las medias (DE) de los valores de HbA1c obtenidos por ambos analizadores fueron: por HPLC de 33±3mmol/mol (5,2±0,3%) y por inmunoturbidimetría de 33±3mmol/mol (5,2±0,3%) (tabla 1).
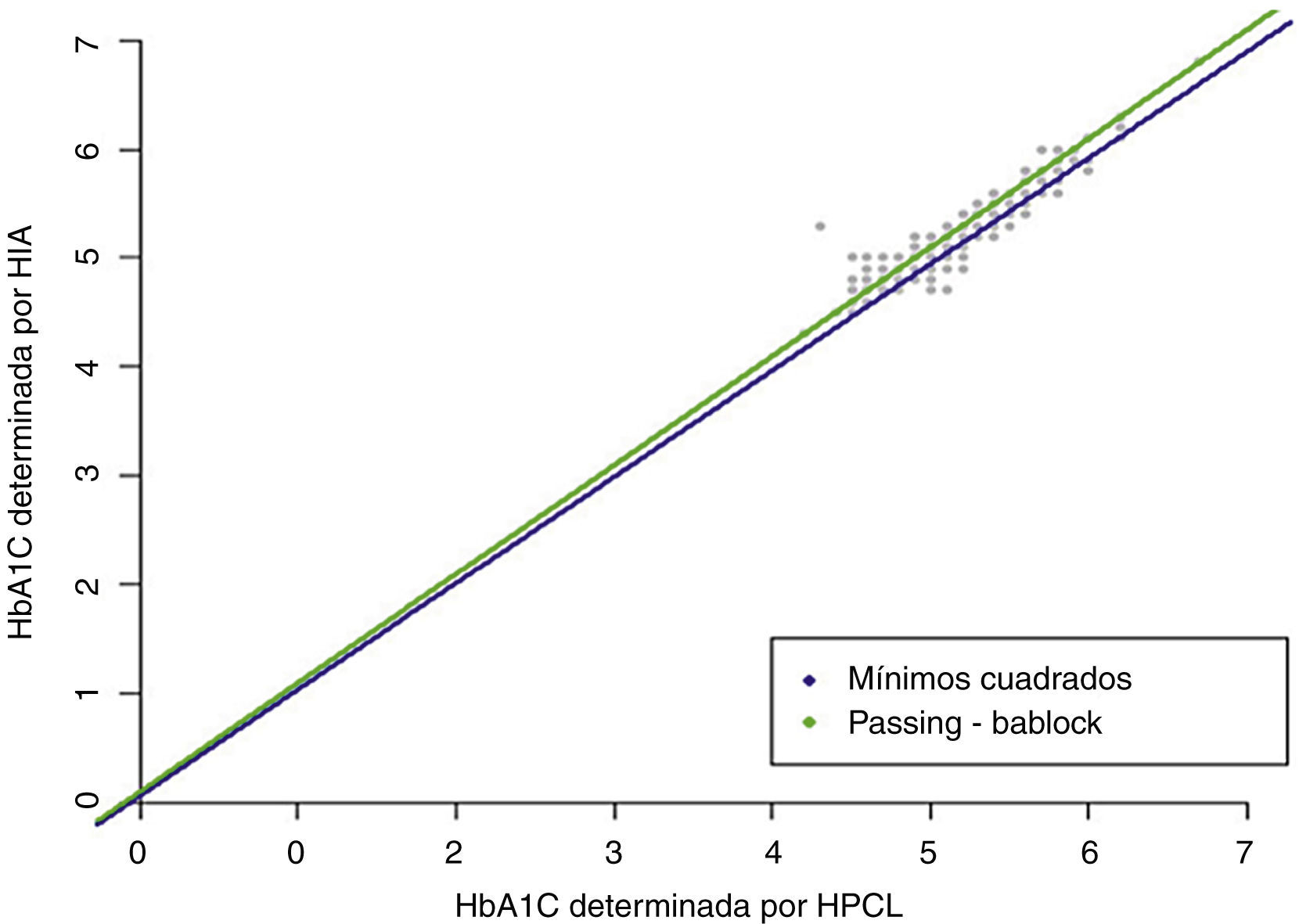
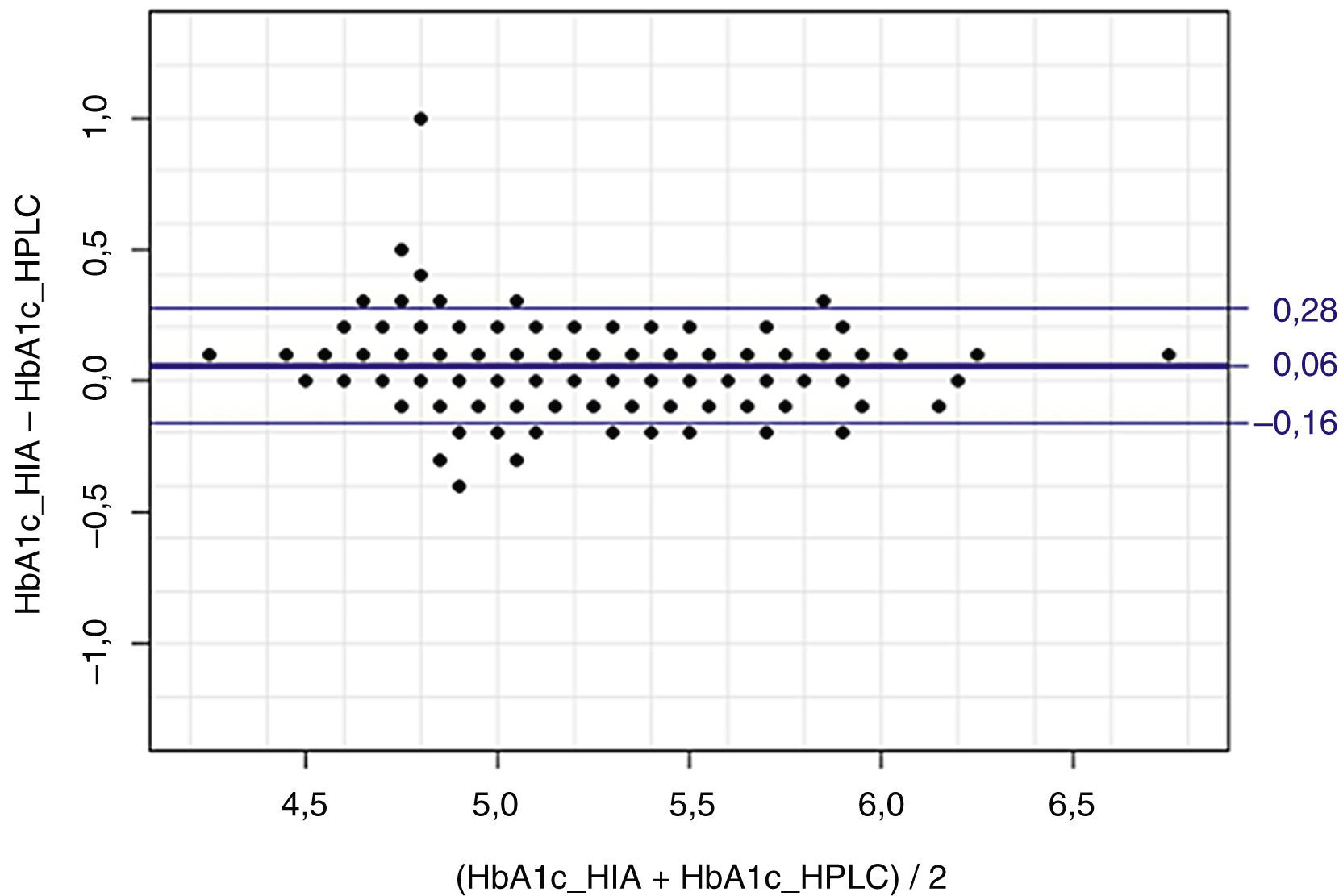
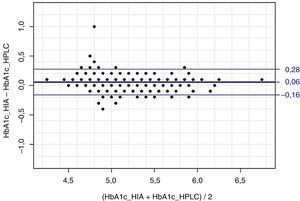
Se ha obtenido una correlación lineal de Pearson de 0.94 entre los métodos de HPLC y de inmunoturbidimetría (p<0,0001). Los resultados de los análisis de regresión lineal por el método de mínimos cuadrados fueron una ordenada en el origen de 0.05 (intervalo de confianza al 95% [IC95%] 0,0958-0,206) y una pendiente de 0.98; y para el análisis de Passing-Bablok de 0,10 (IC95% 0,10-0,10) y 1,00, respectivamente (fig. 1). La comparación entre ambos métodos utilizando el análisis de Bland-Altman indicó una diferencia de 0,06 (IC95% 0,005-0,007) (fig. 2).
Al registrar los datos relativos al tiempo de puesta en marcha de ambos analizadores, se encontró que el HA-8160 requiere 25min, incluyendo el encendido manual e inicialización del equipo (10min) y la implementación de los procedimientos de control de calidad (15min). Para la plataforma Cobas 6000 el inicio de día se realiza de forma automatizada mediante un «proceso de inicio» a las 6:30h, encontrándose el personal técnico a su llegada el autoanalizador preparado. El proceso de control de calidad está integrado en el sistema, solicitándose junto con el resto de los parámetros, lo que precisa 15min.
El tiempo de apagado, incluyendo los lavados correspondientes y la recarga y sustitución de reactivos fue de 15min en el HA-8160. En el Cobas 6000 la reposición del reactivo de HbA1c supone aproximadamente 3min, teniendo en cuenta que se carga junto con el resto de los reactivos, y el proceso fin de día se realiza de forma automatizada.
Al evaluar el rendimiento de cada analizador, se encontró que el HA-8160 es capaz de procesar 20muestras/h, cifra que para el Cobas 6000 correspondió a 100muestras/h, obteniéndose el primer resultado para este analizador a los 10min.
Todos los cromatogramas obtenidos por el HA-8160 fueron revisados por personal especializado con el fin de descartar la presencia de variantes de hemoglobina. No se encontraron variantes de hemoglobina en ningún paciente al revisar los cromatogramas obtenidos por el método HPLC. No se hallaron resultados por debajo del valor de referencia 20mmol/mol (4,0%), ni por encima de 140mmol/mol (15,0%) por ninguno de los 2 métodos (tabla 1).
DiscusiónLa importancia de la determinación de HbA1c está ampliamente aceptada como parte del protocolo de manejo del paciente con DM tanto para establecer riesgos de complicaciones crónicas como por su utilidad como prueba diagnóstica gracias a que refleja la glucemia media de las 6 a 10 semanas previas7. Además presenta ventajas técnicas respecto a la determinación de la glucosa plasmática, así como una menor variabilidad biológica y clínica9.
La comparación entre ambos métodos ha demostrado que los resultados son similares en la población sana estudiada (correlación lineal de Pearson de 0.94). Al comparar ambos sistemas de análisis entre sí mediante las pruebas de mínimos cuadrados y Passing-Bablok, se ha demostrado que existe un buen nivel de correlación y regresión lineal (fig. 1), y con el análisis de Bland-Altman (fig. 2) se ha evidenciado que las diferencias entre los 2 métodos son mínimas.
En el presente estudio realizado en condiciones de práctica clínica habitual, la determinación de los valores de HbA1c por inmunoturbidimetría ha mostrado ventajas evidentes en los tiempos de procesamiento y obtención de resultados, así como en una menor dedicación del personal técnico de laboratorio. Las diferencias más evidentes entre ambos métodos han sido sin duda las relativas a los tiempos de puesta en marcha y apagado de los 2 analizadores (un total de 20min de procesamiento manual por HPLC frente al proceso automatizado en el Cobas 6000) (tabla 1), así como las relativas al número de muestras procesadas por hora (20 por HPLC y 100 por Cobas 6000). El proceso automatizado de inicio de día y fin de día en el analizador Cobas 6000 optimiza la eficiencia del trabajo del personal técnico del laboratorio clínico.
La presencia de variantes de hemoglobina afecta a la mayoría de los métodos de determinación de HbA1c basados en la diferencia de carga tales como HPLC o electroforesis, mientras que los métodos basados en la diferencia de estructura como la cromatografía de afinidad o los inmunoanálisis se ven menos afectados, dependiendo del tipo de variante10. Diferentes publicaciones demuestran la interferencia de variantes específicas en el método HPLC valorado, HA-816011–16, de ahí la necesidad de revisar los cromatogramas.
Los inmunoanálisis no aportan información sobre la presencia de variantes, pero al utilizar un anticuerpo monoclonal específico frente a los 4-6 aminoácidos de la β-globina, solo se verían afectados por las variantes en las que se modifique alguno de esos aminoácidos del extremo N-terminal de la β-hemoglobina17. El inmunoanálisis valorado (Tina-quant Hemoglobin A1c Gen.3) utiliza un anticuerpo específico frente a los 4 últimos aminoácidos, por lo que consideramos que la posible interferencia por la presencia de variantes es bastante pequeña y los resultados fiables, no precisando los resultados de HbA1c tiempo adicional de revisión aparte de la validación clínica junto con el resto de los parámetros bioquímicos.
ConclusionesExiste una excelente correlación entre los resultados obtenidos por ambos analizadores, basados en los métodos de HPLC e inmunoturbidimetría, para determinar la concentración de HbA1c en sangre total en población sana. Las características de practicabilidad y rapidez de análisis de muestras para la determinación de HbA1c por el método inmunoturbidimétrico en el Cobas 6000 lo convierten en una alternativa más práctica y eficiente, lo que reduce el coste unitario de la prueba.
FinanciaciónLos reactivos fueron cedidos por la casa comercial Roche Diagnostics.
Conflicto de interesesRosa Corcoy declara que ha recibido honorarios de Roche como conferenciante y asesor. El resto de los autores no declara conflicto de intereses.
Nuestro agradecimiento a todos los centros y profesionales que han colaborado en este estudio. Todos los centros agradecen la asistencia y soporte de los servicios de medicina del trabajo, centros de atención primaria y a todo el personal de los servicios de laboratorio sin los cuales no hubiéramos podido disponer de muestras para este estudio.