El equipo AQT90 FLEX es un analizador de sobremesa para inmunoanálisis que presenta características que lo hacen útil para su empleo a la cabecera del paciente. En el presente trabajo comparamos el método de la troponina i en sangre total en este equipo frente a la medida en plasma con 2 inmunoanálisis usados en los laboratorios centrales, como son Stratus® CS y Dimension® EXL.
Material y métodosSe obtuvieron 68 muestras de sangre recogidas en tubo de heparina litio. Las muestras se analizaron primero en el AQT90 FLEX y una vez liberados los tubos se centrifugaron, analizándose el plasma resultante por Stratus® CS y Dimension® EXL.
ResultadosEl análisis de regresión arrojó los siguientes ecuaciones: AQT=0,006+0,22*Dimension con un coeficiente de correlación de 0,90 y AQT=0,001+0,29*Stratus, siendo el coeficiente de correlación de 0,97, aunque se observaron diferencias constantes y proporcionales. Para la comparación entre los 2 métodos usados como referencia frente al método a evaluar se obtuvo la siguiente ecuación: Stratus=0,0026+0,98*Dimension con un coeficiente de correlación de 0,99 en ausencia de errores.
AQT90 FLEX is a new bench top analyzer with performance characteristics that make it suitable for use in Point of Care. In this work we compare troponin i measured in whole blood with this analyzer and the plasma measurement using two immunoassays frequently used in core laboratories, such as Dimension® EXL and Stratus® CS.
MethodsWe collected 68 samples into lithium heparin tubes, which were analyzed on the AQT90 FLEX and then centrifuged and the plasma used for the measurement of troponin i using the Dimension® EXL and Stratus® CS.
ResultsThe regression analysis yielded the following equations: AQT=0.006+0.22*Dimension (r=0.90) and AQT=0.001+0.29*Stratus (r=0.97), although constant and proportional differences were observed in both comparisons. The comparison between Stratus® and Dimension® yielded the following equation: Stratus=0.0026+0.98*Dimension (r=0.99) with no constant errors in either of them.
La troponina cardiaca es la piedra angular sobre la que pivota el diagnóstico de los síndromes coronarios agudos, ya que el electrocardiograma solo es definitivo en la mitad de los casos de cardiopatía isquémica1, permitiendo además la detección de daños miocárdicos no evidenciables con los biomarcadores clásicos. Por ello los criterios de diagnóstico de síndromes coronarios agudos se redefinieron al comienzo del siglo2,3 con actualizaciones más recientes4,5, dando importancia vital a la elevación gradual de la concentración de troponina cardiaca en individuos con dolor torácico entre una primera muestra tomada al comienzo de los síntomas y una segunda tomada a las 6-9h, aunque en la última definición se recomienda la toma de muestras a tiempo 0, a las 3 y a las 6h5 debido a la creciente sensibilidad de los nuevos ensayos de troponina cardiaca. Las referidas guías clínicas establecen que el punto de corte que debe usarse como diagnóstico es el percentil 99 de una población de referencia, siempre que el coeficiente de variación del ensayo en ese punto sea del 10% o inferior4,7.
A diferencia de los anticuerpos frente la troponinaT que son producidos por un solo fabricante existen múltiples fabricantes de anticuerpos para la troponinai, situación que se complica por la heterogeneidad de la molécula. En efecto, la troponinai puede presentarse en forma defosforilada, mono y bifosforilada8, además de presentar otras modificaciones postraslacionales y formar complejos binarios y ternarios con troponinaT y troponinaC, lo que multiplica la complejidad de epítopos6. Esta heterogeneidad molecular de la troponina es la base de la diversidad de anticuerpos fabricados en cada ensayo, lo que hace que los valores obtenidos con un ensayo no sean directamente extrapolables a otro diferente. La falta de estandarización de los ensayos de troponina i ha motivado la existencia de un grupo de trabajo de la International Federation of Clinical Biochemistry (IFCC) que por el momento no ha alcanzado el objetivo. Por todo ello resulta esencial conocer la relación entre las 2 medidas, especialmente cuando se usan alternativamente en el mismo laboratorio6,7.
El equipo AQT90 FLEX (Radiometer Copenhagen®) es un analizador de sobremesa para inmunoanálisis que presenta características que lo hacen útil para su empleo a la cabecera del paciente (point of care testing [POCT]), siendo capaz de determinar en sangre total parámetros críticos como marcadores cardiacos, marcadores de sepsis y magnitudes relacionadas con la coagulación y la fibrinólisis9. Se trata de un equipo capaz de procesar con una productividad de hasta 30muestras por hora y un total de 240tests cuando el analizador está totalmente cargado, pudiéndose introducir una nueva muestra cada 2min. Trabaja con tubos cerrados, siendo capaz de procesar tanto sangre total como plasma, con un volumen mínimo de 2ml para sangre total y de 0,4ml para plasma. El resultado para la troponinai se obtiene en 18min.
En el presente trabajo se compara la medida de la troponinai cardiaca del AQT90 FLEX frente a la proporcionada por 2 equipos de uso ampliamente establecido, como son el Stratus® CS, equipo clásico para análisis de troponinai en point of care, y Dimension® EXL como equipo de referencia de laboratorio central.
Material y métodosEl analizador AQT90 FLEX utiliza un ensayo tipo sándwich de segunda generación para la troponinai cardiaca, en el que se emplean 3 anticuerpos monoclonales, 2 de ellos, inmovilizados, para la captura, y el tercero para la detección, estando este último marcado con europio9. Los anticuerpos de captura van dirigidos contra el fragmento medio, la zona más estable de la molécula de troponinai (epítopos 41-49) y los epítopos 190-196 de la zona C-terminal, mientras que el anticuerpo trazador va dirigido contra los epítopos 137-1499. El anticuerpo trazador va unido a europio y da lugar al desarrollo de la señal fluorescente, que es proporcional a la concentración de troponina. El límite de detección es de 0,010ng/ml y el percentil 99 de la población de referencia es 0,023ng/ml, correspondiendo el coeficiente de variación de 10% a una concentración de 0,039ng/ml9. El intervalo de linealidad según la información del fabricante es de 0,010 a 25ng/ml.
El método de Stratus® es un inmunoanálisis de partición radial (RPIA) con marcaje fluorescente siendo el límite de detección de 0,03ng/ml. Las características analíticas de este método han sido previamente publicadas12, presentando un percentil 99 en la población control de 0,07ng/ml, mientras que la concentración más próxima en la que el coeficiente de variación es inferior o igual al 10% es 0,06ng/ml. El intervalo de linealidad va desde 0,03 hasta 40ng/ml.
El método de Dimension® EXL, a diferencia de los otros 2, es un inmunoanálisis homogéneo, patentado por Siemens Healthcare Diagnostics® y conocido como Luminiscent Oxygen Channeling Immnunoassay (LOCI), que utiliza 2 partículas sintéticas. La primera (Chemibead) está recubierta por el anticuerpo específico contra la troponinai marcado con una sustancia luminiscente, mientras que la segunda (Sensibead) está cubierta por estreptavidina y contiene un marcaje fotosensible. Además, el reactivo contiene un anticuerpo unido a biotina que proporciona una unión de alta especificidad a la estreptavidina, de modo que cuando la troponinai de la muestra se une este anticuerpo biotinilado y al anticuerpo de la Chemibead mediante una unión tipo sándwich, al recibir una radiación de 680nm se produce luminiscencia. Las características analíticas de este método han sido publicadas1,14, aunque para la plataforma Dimension® VISTA, en lugar de la Dimension® EXL que usamos nosotros y que es de más reciente implantación. Este método presenta una sensibilidad analítica de 0,017ng/ml con un percentil 99 para la población de referencia de 0,056ng/ml y un punto de corte en el que el coeficiente de variación es inferior o igual al 10% de 0,050ng/ml. Su intervalo de linealidad va desde 0,017 a 40ng/ml13. No hay estudios en la literatura que comparen el método de Stratus con el método LOCI en la plataforma Dimension® EXL.
En nuestro estudio se obtuvieron 68 muestras de sangre recogidas en tubo de heparina litio procedentes de pacientes que acudieron a la puerta de urgencias con sospecha de síndrome coronario agudo o ingresados en la unidad de vigilancia intensiva después de un episodio cardiaco. La comparación de métodos se hizo siguiendo las recomendaciones de la Sociedad Española de Bioquímica y Patología Molecular para el estudio de la veracidad mediante la comparación de procedimientos de medida17. Entre la obtención de la muestra y su posterior análisis no transcurrieron más de 30min, usándose a lo largo de todo el estudio la misma curva de calibración en cada uno de los equipos. Las muestras se analizaron primero en el AQT90 FLEX y, una vez liberados los tubos, se centrifugaron a 1.710g durante 5min, analizándose el plasma resultante por Stratus® CS y Dimension® EXL durante 15series analíticas. Los resultados obtenidos se expresan en nanogramos por mililitro.
El tratamiento estadístico se realizó mediante el test de Passing-Bablok10, calculándose las ecuaciones de regresión y los coeficientes de correlación y representando los diagramas de Bland-Altman11.
ResultadosEl análisis de valores aberrantes mediante el procedimiento que se detalla en el documento citado17 produjo 3 de estos valores que fueron rechazados, por lo que el tamaño de la muestra resultó ser de 65.
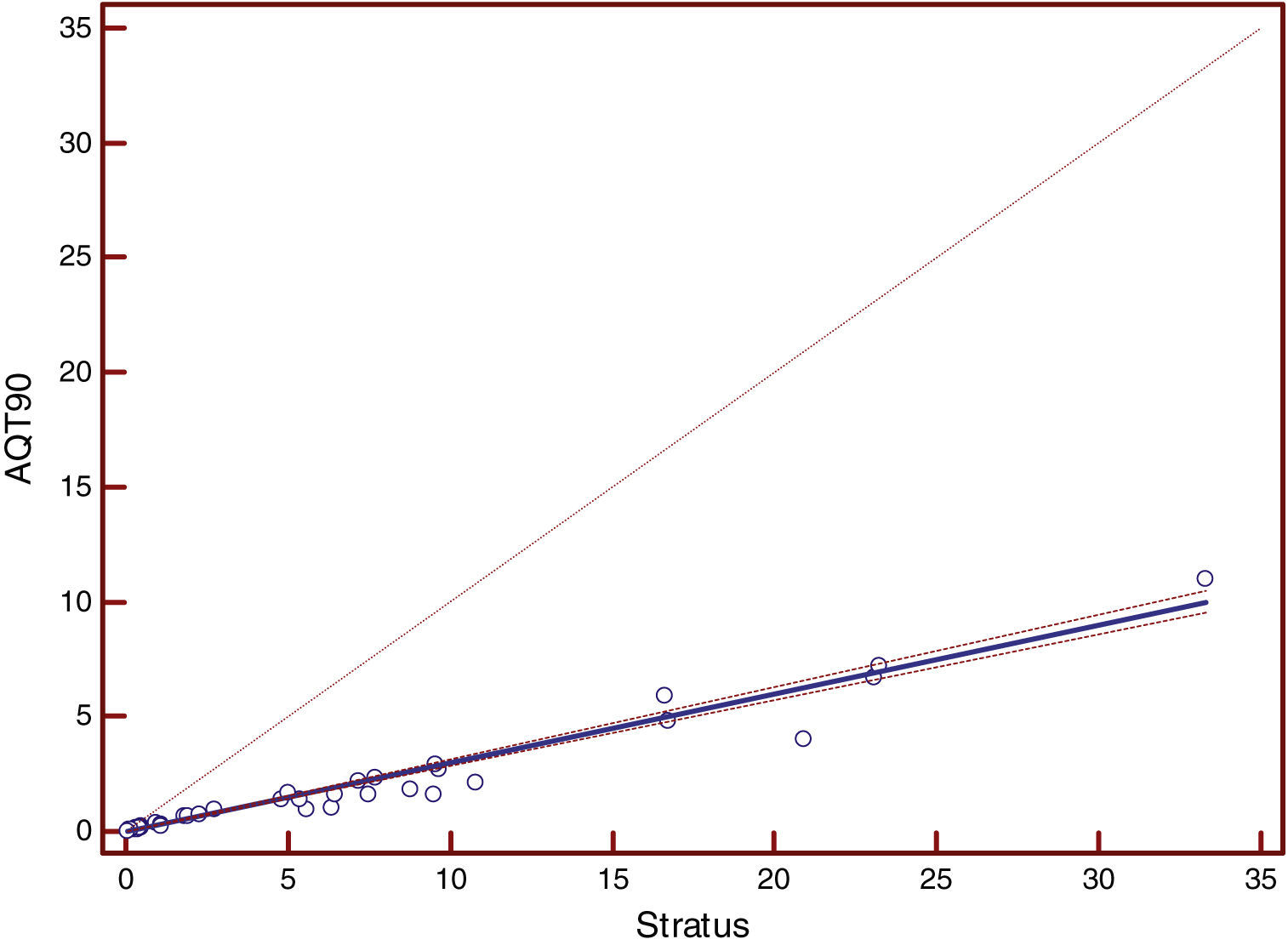
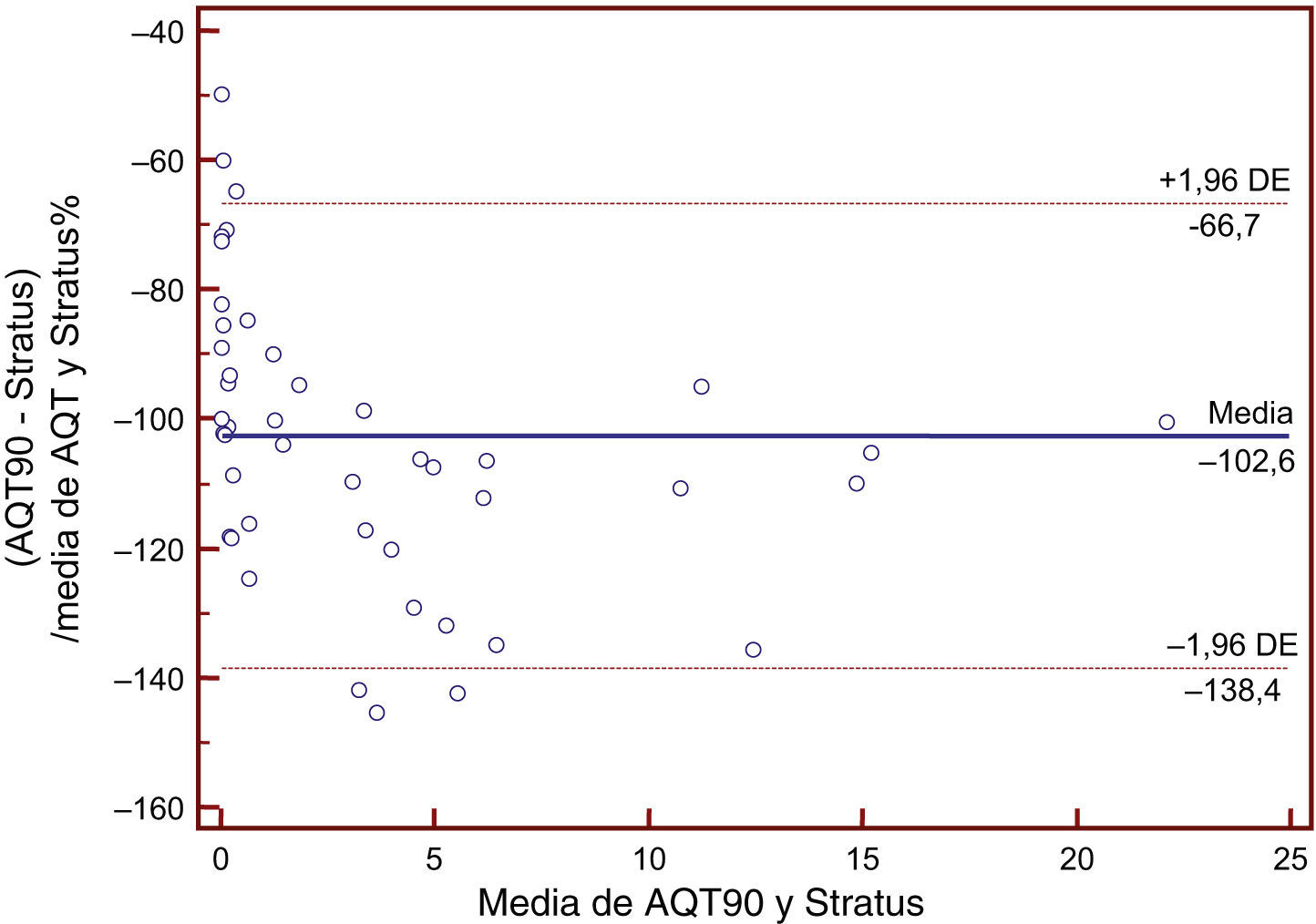
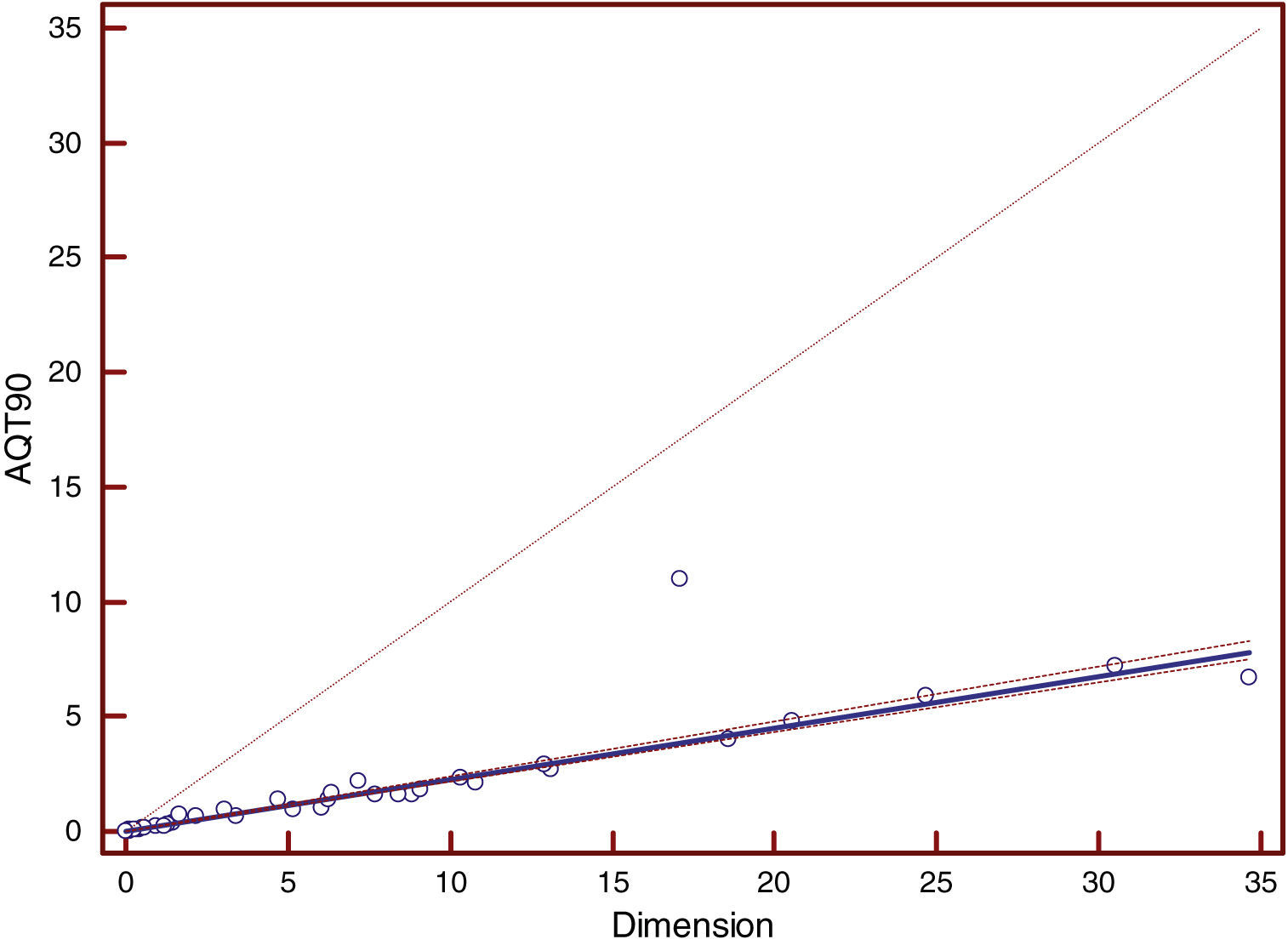
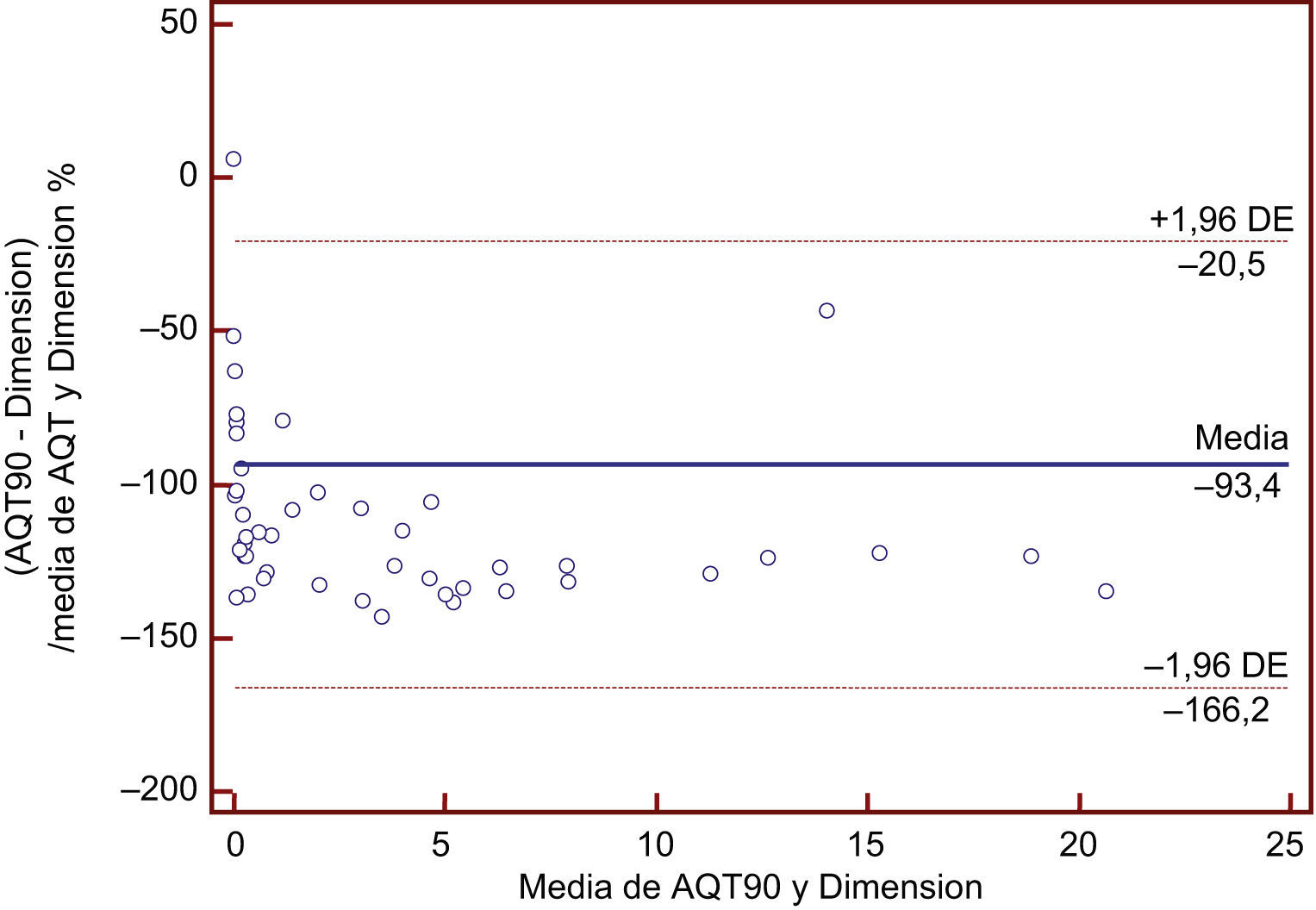
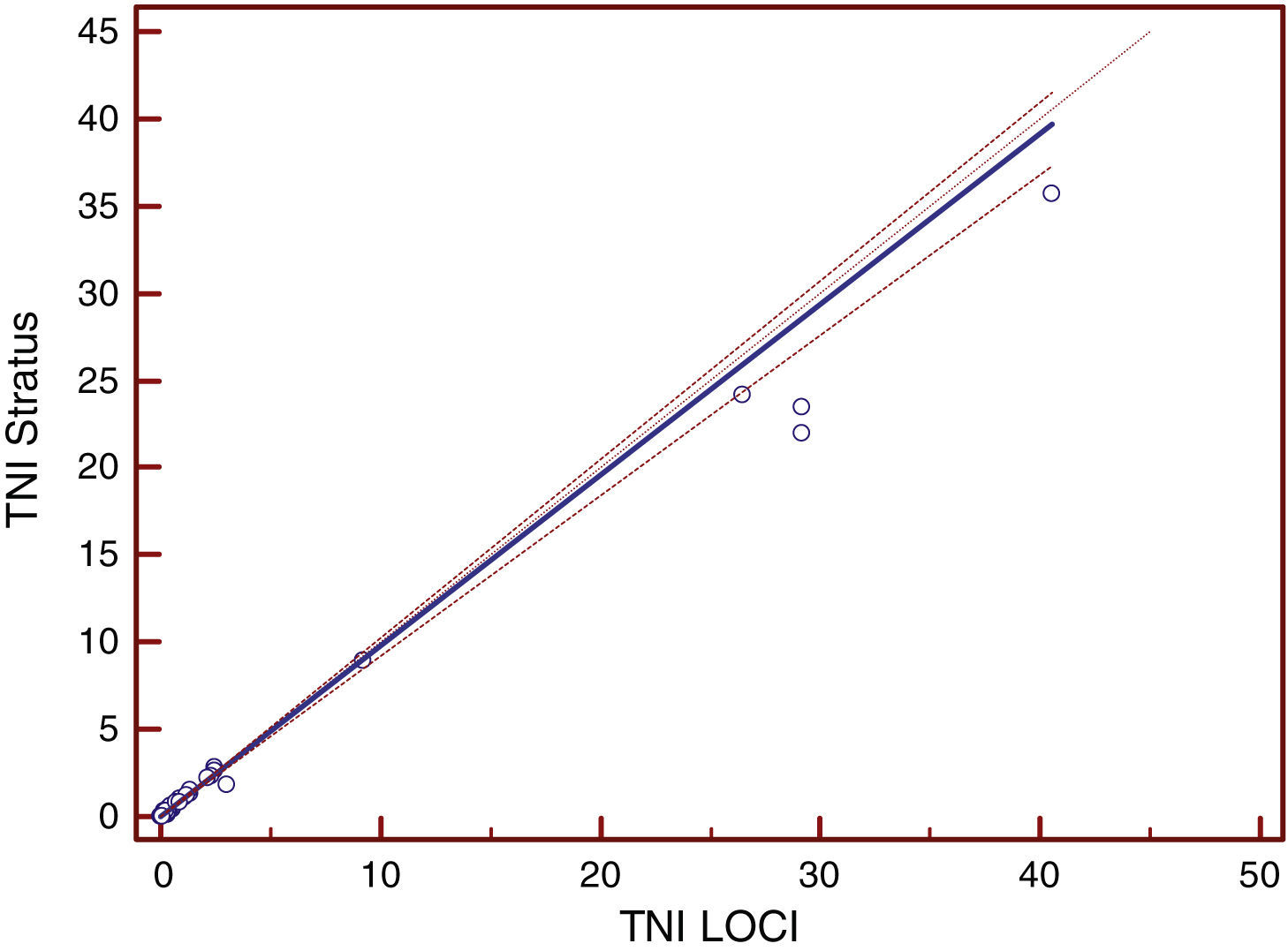
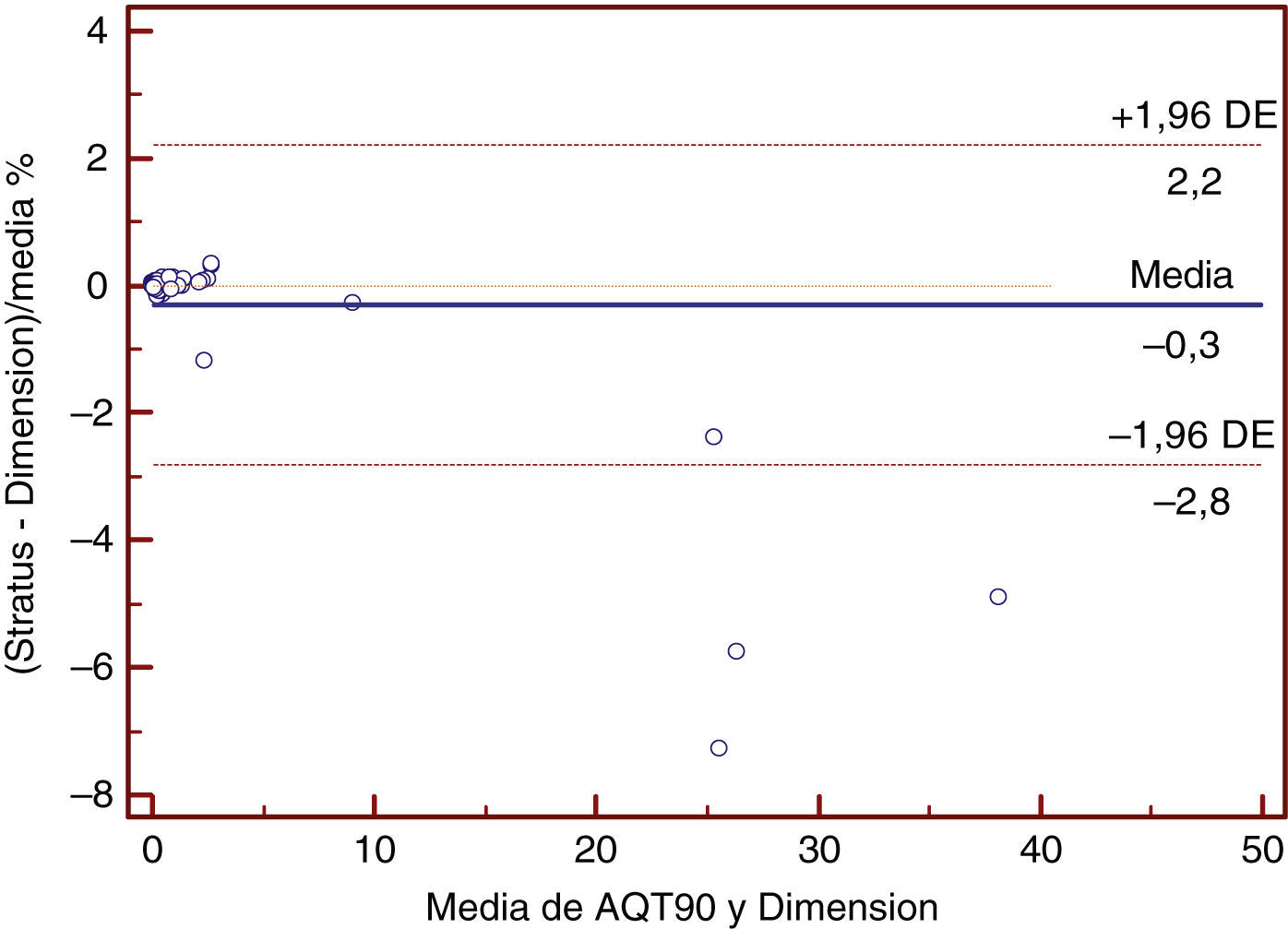
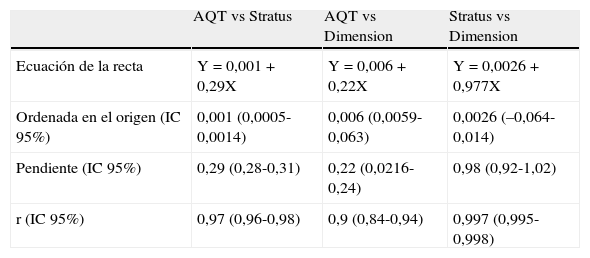
La media aritmética de los resultados obtenidos mediante el método a comparar es de 1,08ng/ml (intervalo 0,010-11), mientras que los valores obtenidos en Dimension® EXL arrojaron una media de 4,34ng/ml (0,017-34,62). La ecuación de regresión obtenida al comparar el método de AQT90 con Dimension® fue AQT=0,006+0,22*Dimension, con un intervalo de confianza para la pendiente de 0,21-0,24 y para la intersección entre 0,0059 y 0,0063. El coeficiente de correlación obtenido fue de 0,90 (intervalo de confianza: 0,84-0,94). En Stratus® se obtuvo un valor medio de 3,9ng/ml (intervalo: 0,03-33,28). Al comparar los resultados obtenidos con Stratus® con los de AQT90 obtuvimos la ecuación AQT=0,001+0,29*Stratus, con un intervalo de confianza para la pendiente de 0,28 a 0,31 y para la ordenada en el origen entre 0,0005 y 0,001 siendo el coeficiente de correlación de 0,97 (intervalo de confianza: 0,96-0,99). En la tabla 1 se muestran los resultados obtenidos aplicando el análisis de regresión por el método de Passing-Babblok. En las figuras 1 y 3 se muestran las rectas de regresión obtenidas mediante el análisis comparativo, mientras que en las figuras 2 y 4 se representan los diagramas de Bland-Altman correspondientes a las comparaciones del AQT90 FLEX con los 2 métodos de referencia.
| AQT vs Stratus | AQT vs Dimension | Stratus vs Dimension | |
| Ecuación de la recta | Y=0,001+0,29X | Y=0,006+0,22X | Y=0,0026+0,977X |
| Ordenada en el origen (IC 95%) | 0,001 (0,0005-0,0014) | 0,006 (0,0059-0,063) | 0,0026 (–0,064-0,014) |
| Pendiente (IC 95%) | 0,29 (0,28-0,31) | 0,22 (0,0216-0,24) | 0,98 (0,92-1,02) |
| r (IC 95%) | 0,97 (0,96-0,98) | 0,9 (0,84-0,94) | 0,997 (0,995-0,998) |
Por otro lado, la comparación entre los 2 métodos usados como referencia frente al método a evaluar (Dimension® y Stratus®) arrojaron la siguiente ecuación de regresión: Stratus=0,0026+0,98*(Dimension), con intervalos de confianza para la pendiente de 0,92-1,02 y para la ordenada en el origen entre –0,0064 y 0,0014 siendo el coeficiente de correlación de 0,99 (intervalo de confianza: 0,995-0,998). Las figuras 5 y 6 muestran respectivamente la recta de regresión y el diagrama de Bland-Altman correspondiente a esta comparación.
Discusión y conclusionesEl objetivo de nuestro trabajo ha sido comparar un método para la medida de troponinai cardiaca en sangre total, ideado para el análisis de point of care frente a 2 inmunoanálisis clásicos y de uso ampliamente establecido, como son Stratus® CS y Dimension® EXL (Siemens Healthcare Diagnostics®). El Stratus® CS fue concebido inicialmente para su uso en point of care testing, mientras que el segundo está muy extendido en los laboratorios centrales de urgencias.
El límite de detección del método a comparar es 0,010ng/ml, frente a 0,03ng/ml de Stratus® y 0,017ng/ml de Dimension® EXL. El percentil 99 indicado por el fabricante es 0,023ng/ml, siendo el valor en el que la imprecisión es del 10% de 0,039ng/ml9. Según estudios posteriores (Comunicación al Congreso de la American Asociation for Clinical Chemistry [AACC]) de 2012 el percentil 99 es de 0,021ng/ml y el nivel de imprecisión inferior al 10% es de 0,025ng/ml. Estos niveles de decisión son inferiores a los que usamos en nuestro laboratorio según las recomendaciones del fabricante (0,07ng/ml para Stratus® y 0,050ng/ml para Dimension®), que han sido validadas por nosotros (comunicación al VCongreso Nacional de Laboratorio Clínico).
Hay una publicación donde se evalúa el rendimiento diagnóstico del AQT90 comparándolo con otros inmunoanálisis propios de laboratorios centrales, como el Access Accu TnI de Beckman Coulter® y Abbott cTnI ADV de Abbott Diagnostics®9, aunque no se evalúan sus prestaciones analíticas. En este estudio se concluye que el método de AQT90 para la troponina presenta un adecuado rendimiento diagnóstico, si bien es inferior a los métodos con los que se compara. No hay publicados estudios donde se compare nuestro método de POCT con otros, de ahí la originalidad de este trabajo.
De nuestro estudio se deduce que la correlación entre los 2 métodos usados en el laboratorio Core es excelente, con ausencia de error, lo que indica que los resultados obtenidos por ambos métodos son intercambiables. Sin embargo, al comparar el método a evaluar con los de Dimension® y Stratus® se observa un error proporcional y un pequeño error constante (prácticamente despreciable), lo que indica que las medidas de troponinai no son transferibles entre el AQT90 y los métodos del laboratorio Core.
La falta de armonización de las mediciones de troponinai cardiaca es un problema para la mayoría de los laboratorios debido a la diversidad de fabricantes de anticuerpos frente a esta molécula5,6,8. Por ello es esencial la comparación de los diferentes métodos para poder interpretar los resultados convenientemente cuando se cambia de plataforma analítica. Por otro lado, es fundamental la evaluación de equipos de point of care frente a los equipos de los laboratorios centrales, ya que la National Academy of Clinical Biochemistry (NACB) y la IFCC recomiendan un tiempo de respuesta total inferior a una hora ante la sospecha de síndrome coronario agudo, poniendo el énfasis en que si el laboratorio central no puede cumplir estos tiempos de respuesta se implementen sistemas de point of care15,16. Estos métodos a la cabecera del paciente deberán estar siempre controlados desde el laboratorio central, que debe asegurar su correcto uso y la calidad analítica de los resultados.
Conflicto de interesesLos autores declaran no tener ningún tipo de conflicto de interés con las firmas comerciales implicadas en el estudio.
Los autores agradecen a José Luis López Pumarega, de Radiometer Ibérica, sus comentarios y asistencia técnica.