El objetivo de este trabajo fué evaluar, mediante un estudio multicéntrico, la imprecisión y la veracidad de un elevado número de procedimientos de medida en el nuevo sistema analítico BioSystems BA 400®.
Material y métodoEl estudio de la imprecisión se llevó a cabo siguiendo recomendaciones establecidas y utilizando sueros control con 2 concentraciones distintas. El estudio de la veracidad se ha realizado mediante la comparación de los procedimientos de medida del nuevo sistema con los utilizados habitualmente en los centros evaluadores.
ResultadosLos resultados obtenidos para la imprecisión interdiaria con el nuevo analizador han sido en general excelentes en relación a los errores máximos permitidos. Se han encontrado algunas diferencias no despreciables y estadísticamente significativas entre los distintos procedimientos de medida, que son debidas a diferencias en el mensurando en algunos casos (transaminasas, inmunoanálisis) y a diferencias en los calibradores en otros.
ConclusionesLa evaluación ha demostrado las excelentes prestaciones de precisión y veracidad del sistema. El nuevo analizador proporciona resultados en muestras de pacientes que son equivalentes a los obtenidos con otros analizadores (Olympus AU5400 y AU2700, Roche Cobas C711 y Siemens ADVIA 2400, 1800 y BNII).
The purpose of the study was a multicentre evaluation of the imprecision and of the trueness of a wide variety of measurement procedures with the new analytical system BioSystems BA 400®.
MethodsThe imprecision study was performed following established recommendations and using control sera with two different concentrations. The trueness was studied by means of a comparison of the measurement procedures of the new analyser with those of routine use in the evaluating centres.
ResultsThe results obtained for the between-day imprecision with the new analyser have been in general excellent in relation to the maximum allowed errors. Several differences that are not worthless and that are statistically significant have been found between the measurement procedures. The differences are due to measurand differences in some cases (transaminases, immunoanalysis), and to the calibration in other.
ConclusionThe evaluation study has demonstrated the excellent performance of the system regarding precision and trueness. The results obtained for patient samples with the new analyzer are equivalent to those obtained with other analyzers (Olympus AU5400 y AU2700, Roche Cobas C711 y Siemens ADVIA 2400, 1800 y BNII).
En los últimos años, se ha observado en los laboratorios clínicos un incremento en el uso generalizado de sistemas analíticos, con un aumento paralelo en su capacidad analítica y una mayor diversidad de pruebas. Otra característica destacada es la integración de diferentes principios y métodos de medida en un mismo sistema analítico, favoreciendo la concentración de una gran cantidad de pruebas en unos pocos sistemas de trabajo1.
El BA 400® es un sistema automatizado para el análisis de magnitudes en muestras biológicas que utiliza los principios de medida de la espectrometría de absorción molecular, la turbidimetría y la potenciometría. El analizador emplea un avanzado sistema óptico basado en una batería de LEDs monocromáticos como fuente de luz. El BA 400® ha sido diseñado, desarrollado y fabricado por BioSystems, S. A. (Barcelona, España).
El sistema BA 400® comprende también un amplio panel de reactivos dedicados y se complementa con materiales de control y materiales de calibración, estos últimos con una adecuada descripción de la trazabilidad metrológica de los valores asignados.
El objetivo de este trabajo fué evaluar, mediante un estudio multicéntrico, la imprecisión y la veracidad de diversos procedimientos de medida del sistema BA 400®. Para estudiar la veracidad, se compararon los resultados obtenidos en el BA 400® con los obtenidos en otros sistemas de medida.
Material y métodosLaboratorios participantesEn esta evaluación multicéntrica han participado los laboratorios clínicos de los hospitales Vall d’Hebron, Universitari de Bellvitge y Clínic de Barcelona.
En cada uno de los centros se instaló el analizador BA 400® y, tras realizar una breve formación sobre su uso y sobre la funcionalidad básica del programa de usuario, se llevo a cabo un periodo de familiarización de 2-4 días realizando calibraciones y mediciones de los distintos materiales de control así como de muestras de pacientes (sueros y orinas).
Para el estudio de la veracidad se usaron como procedimientos de referencia los implantados de rutina en los laboratorios participantes en el estudio y que se detallan a continuación:
Centro A. Hospital Universitari Vall d’Hebron: Olympus AU5400 (muestras de suero) y AU2700 (muestras de orina), y Siemens BNII (sólo para C3 y C4).
Centro B: Hospital Universitari de Bellvitge: Roche Cobas C711 y Siemens BNII (C3, C4, IgA, IgG, IgM).
Centro C: Hospital Clínic de Barcelona: Siemens ADVIA 2400 (muestras de suero), Siemens ADVIA 1800 (muestras de orina) y Siemens BNII (IgA, IgG y IgM).
En el estudio de imprecisión, además de los anteriores, también participó el laboratorio de validaciones del diseño de Biosystems.
Procedimiento analíticoBioSystems BA 400®: Diariamente se inició el proceso con la calibración del módulo ISE y a continuación se procesaron las calibraciones de los procedimientos espectrométricos, siguiendo las instrucciones del fabricante del analizador. Para validar las series de medida, cada día se analizaron los diversos materiales de control y se verificó que los resultados estuvieran dentro de los intervalos de control establecidos. Los resultados de los controles se utilizaron en el estudio de la imprecisión interdiaria. Los calibradores y controles se reconstituyeron cada día (centro A) o bien se reconstituyeron, alicuotaron y congelaron, para luego ir utilizando las alícuotas necesarias diariamente (centros B y C). Todos los reactivos se mantuvieron en el rotor refrigerado del analizador y se fueron reponiendo según se agotaban. A continuación se programó y midió una lista de de trabajo de muestras de pacientes cuyos analitos habían sido previamente medidos en el sistema de referencia del laboratorio. Los resultados del BA 400® se transfirieron a una base de datos conjuntamente con los del sistema de referencia para realizar una comparación de los procedimientos de medida.
Analizadores de referencia: Se iniciaron, calibraron y controlaron siguiendo los procedimientos diarios habituales de cada laboratorio participante en el estudio.
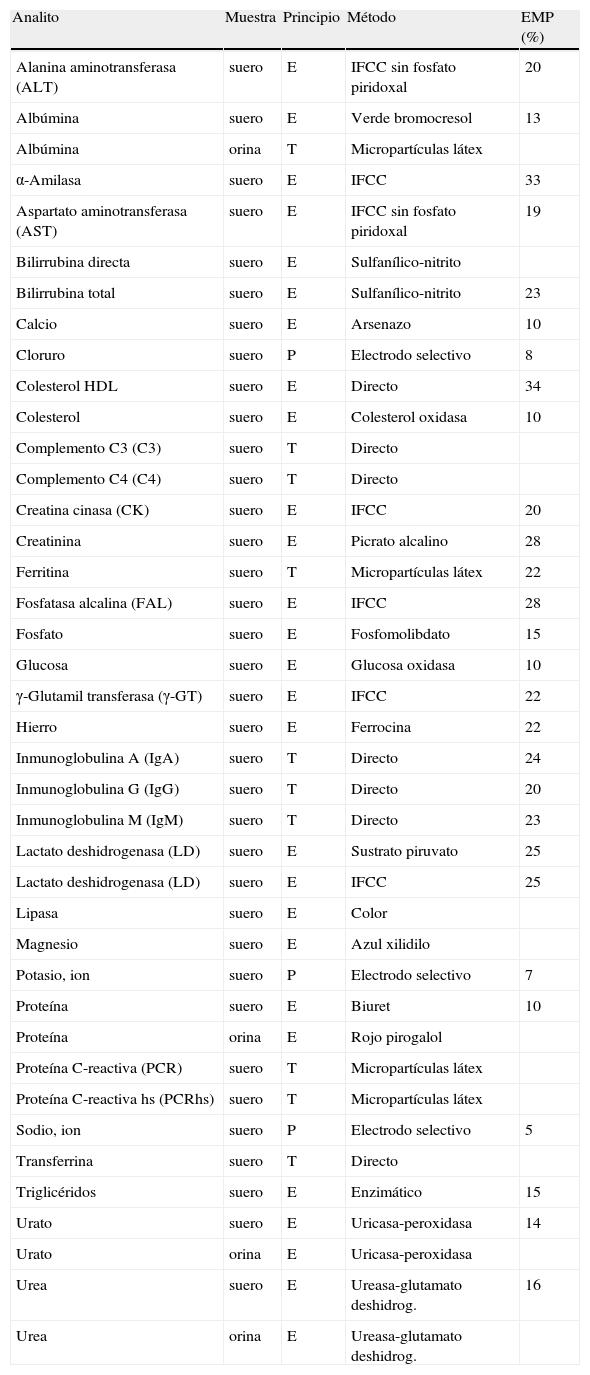
Analitos y métodosEn la tabla 1 se detallan los analitos y los tipos de muestra estudiados. Los procedimientos de medida evaluados y los de referencia están basados en los principios y en los métodos de medida que se muestran en la misma tabla. La única excepción es el caso de la ALT y AST ya que los laboratorios A y C utilizaron el procedimiento con fosfato de piridoxal.
Analitos estudiados
| Analito | Muestra | Principio | Método | EMP (%) |
| Alanina aminotransferasa (ALT) | suero | E | IFCC sin fosfato piridoxal | 20 |
| Albúmina | suero | E | Verde bromocresol | 13 |
| Albúmina | orina | T | Micropartículas látex | |
| α-Amilasa | suero | E | IFCC | 33 |
| Aspartato aminotransferasa (AST) | suero | E | IFCC sin fosfato piridoxal | 19 |
| Bilirrubina directa | suero | E | Sulfanílico-nitrito | |
| Bilirrubina total | suero | E | Sulfanílico-nitrito | 23 |
| Calcio | suero | E | Arsenazo | 10 |
| Cloruro | suero | P | Electrodo selectivo | 8 |
| Colesterol HDL | suero | E | Directo | 34 |
| Colesterol | suero | E | Colesterol oxidasa | 10 |
| Complemento C3 (C3) | suero | T | Directo | |
| Complemento C4 (C4) | suero | T | Directo | |
| Creatina cinasa (CK) | suero | E | IFCC | 20 |
| Creatinina | suero | E | Picrato alcalino | 28 |
| Ferritina | suero | T | Micropartículas látex | 22 |
| Fosfatasa alcalina (FAL) | suero | E | IFCC | 28 |
| Fosfato | suero | E | Fosfomolibdato | 15 |
| Glucosa | suero | E | Glucosa oxidasa | 10 |
| γ-Glutamil transferasa (γ-GT) | suero | E | IFCC | 22 |
| Hierro | suero | E | Ferrocina | 22 |
| Inmunoglobulina A (IgA) | suero | T | Directo | 24 |
| Inmunoglobulina G (IgG) | suero | T | Directo | 20 |
| Inmunoglobulina M (IgM) | suero | T | Directo | 23 |
| Lactato deshidrogenasa (LD) | suero | E | Sustrato piruvato | 25 |
| Lactato deshidrogenasa (LD) | suero | E | IFCC | 25 |
| Lipasa | suero | E | Color | |
| Magnesio | suero | E | Azul xilidilo | |
| Potasio, ion | suero | P | Electrodo selectivo | 7 |
| Proteína | suero | E | Biuret | 10 |
| Proteína | orina | E | Rojo pirogalol | |
| Proteína C-reactiva (PCR) | suero | T | Micropartículas látex | |
| Proteína C-reactiva hs (PCRhs) | suero | T | Micropartículas látex | |
| Sodio, ion | suero | P | Electrodo selectivo | 5 |
| Transferrina | suero | T | Directo | |
| Triglicéridos | suero | E | Enzimático | 15 |
| Urato | suero | E | Uricasa-peroxidasa | 14 |
| Urato | orina | E | Uricasa-peroxidasa | |
| Urea | suero | E | Ureasa-glutamato deshidrog. | 16 |
| Urea | orina | E | Ureasa-glutamato deshidrog. |
E: espectrometría; EMP: error máximo permitido; P: potenciometría; T: turbidimetría.
El estudio de la imprecisión se llevó a cabo siguiendo la recomendación de la SEQC2, utilizando sueros control con 2 concentraciones distintas (Biochemistry Control Serum, BioSystems, S.A.). La imprecisión intraserial (CVintra) fue estudiada únicamente en el laboratorio de BioSystems. La imprecisión interdiaria (CVinter) fue estudiada en los 3 laboratorios participantes y en el de BioSystems, en todos los casos realizando una calibración nueva cada día de cada procedimiento de medida.
El error de medida máximo permitido que se ha considerado en este trabajo se indica en la tabla 1 y se corresponde con las especificaciones mínimas de la calidad analítica establecidas por consenso3,4 entre la Asociación Española de Biopatología Médica (AEBM), la Asociación Española de Farmaceúticos Analistas (AEFA) y la Sociedad Española de Bioquímica Clínica y Patología Molecular (SEQC), tal como ha recomendado la Comisión de Metrología de la SEQC5.
El nivel sigma se estableció dividiendo el error de medida máximo permitido (EMP) por el CVinter, tal como recomienda la Comisión de Metrología de la SEQC6.
Comparación de procedimientos de medidaLa comparación se realizó siguiendo las recomendaciones establecidas por la SEQC7.
Las muestras de pacientes fueron obtenidas el mismo día de su análisis o el dia anterior y conservadas refrigeradas a 4-8°C. Se rechazaron las muestras hemolizadas, ictéricas (excepto en la medición de bilirrubina) y lipémicas (excepto en las mediciones de colesterol, colesterol de HDL y triglicéridos). Las muestras se seleccionaron de forma que los valores de concentración de cada uno de los analitos abarcaran un amplio intervalo de medida (véase tablas 3–5). Se analizaron un mínimo de 40 muestras por analito.
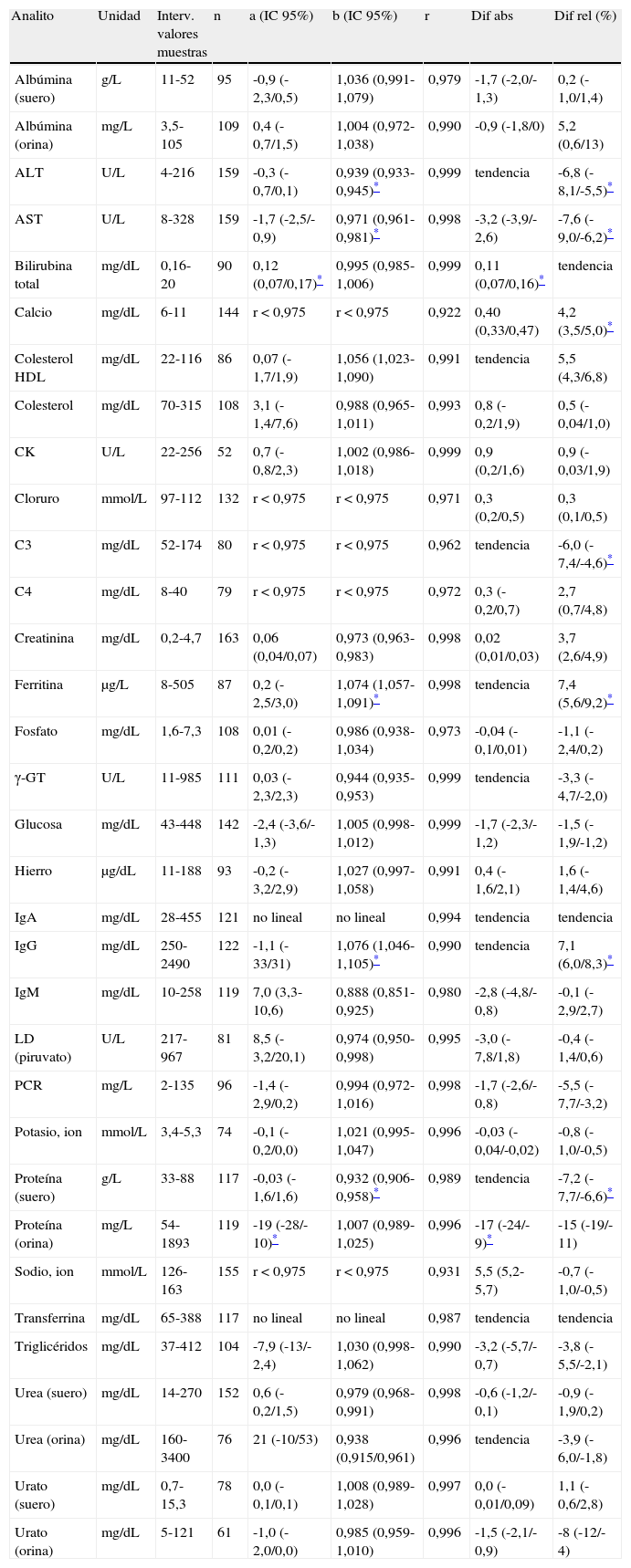
Comparación de procedimientos de medida, Centro A: Olympus AU5400 y AU2700 (orinas) y Siemens BNII (sólo C3 y C4)
| Analito | Unidad | Interv. valores muestras | n | a (IC 95%) | b (IC 95%) | r | Dif abs | Dif rel (%) |
| Albúmina (suero) | g/L | 11-52 | 95 | -0,9 (-2,3/0,5) | 1,036 (0,991-1,079) | 0,979 | -1,7 (-2,0/-1,3) | 0,2 (-1,0/1,4) |
| Albúmina (orina) | mg/L | 3,5-105 | 109 | 0,4 (-0,7/1,5) | 1,004 (0,972-1,038) | 0,990 | -0,9 (-1,8/0) | 5,2 (0,6/13) |
| ALT | U/L | 4-216 | 159 | -0,3 (-0,7/0,1) | 0,939 (0,933-0,945)* | 0,999 | tendencia | -6,8 (-8,1/-5,5)* |
| AST | U/L | 8-328 | 159 | -1,7 (-2,5/-0,9) | 0,971 (0,961-0,981)* | 0,998 | -3,2 (-3,9/-2,6) | -7,6 (-9,0/-6,2)* |
| Bilirubina total | mg/dL | 0,16-20 | 90 | 0,12 (0,07/0,17)* | 0,995 (0,985-1,006) | 0,999 | 0,11 (0,07/0,16)* | tendencia |
| Calcio | mg/dL | 6-11 | 144 | r < 0,975 | r < 0,975 | 0,922 | 0,40 (0,33/0,47) | 4,2 (3,5/5,0)* |
| Colesterol HDL | mg/dL | 22-116 | 86 | 0,07 (-1,7/1,9) | 1,056 (1,023-1,090) | 0,991 | tendencia | 5,5 (4,3/6,8) |
| Colesterol | mg/dL | 70-315 | 108 | 3,1 (-1,4/7,6) | 0,988 (0,965-1,011) | 0,993 | 0,8 (-0,2/1,9) | 0,5 (-0,04/1,0) |
| CK | U/L | 22-256 | 52 | 0,7 (-0,8/2,3) | 1,002 (0,986-1,018) | 0,999 | 0,9 (0,2/1,6) | 0,9 (-0,03/1,9) |
| Cloruro | mmol/L | 97-112 | 132 | r < 0,975 | r < 0,975 | 0,971 | 0,3 (0,2/0,5) | 0,3 (0,1/0,5) |
| C3 | mg/dL | 52-174 | 80 | r < 0,975 | r < 0,975 | 0,962 | tendencia | -6,0 (-7,4/-4,6)* |
| C4 | mg/dL | 8-40 | 79 | r < 0,975 | r < 0,975 | 0,972 | 0,3 (-0,2/0,7) | 2,7 (0,7/4,8) |
| Creatinina | mg/dL | 0,2-4,7 | 163 | 0,06 (0,04/0,07) | 0,973 (0,963-0,983) | 0,998 | 0,02 (0,01/0,03) | 3,7 (2,6/4,9) |
| Ferritina | μg/L | 8-505 | 87 | 0,2 (-2,5/3,0) | 1,074 (1,057-1,091)* | 0,998 | tendencia | 7,4 (5,6/9,2)* |
| Fosfato | mg/dL | 1,6-7,3 | 108 | 0,01 (-0,2/0,2) | 0,986 (0,938-1,034) | 0,973 | -0,04 (-0,1/0,01) | -1,1 (-2,4/0,2) |
| γ-GT | U/L | 11-985 | 111 | 0,03 (-2,3/2,3) | 0,944 (0,935-0,953) | 0,999 | tendencia | -3,3 (-4,7/-2,0) |
| Glucosa | mg/dL | 43-448 | 142 | -2,4 (-3,6/-1,3) | 1,005 (0,998-1,012) | 0,999 | -1,7 (-2,3/-1,2) | -1,5 (-1,9/-1,2) |
| Hierro | μg/dL | 11-188 | 93 | -0,2 (-3,2/2,9) | 1,027 (0,997-1,058) | 0,991 | 0,4 (-1,6/2,1) | 1,6 (-1,4/4,6) |
| IgA | mg/dL | 28-455 | 121 | no lineal | no lineal | 0,994 | tendencia | tendencia |
| IgG | mg/dL | 250-2490 | 122 | -1,1 (-33/31) | 1,076 (1,046-1,105)* | 0,990 | tendencia | 7,1 (6,0/8,3)* |
| IgM | mg/dL | 10-258 | 119 | 7,0 (3,3-10,6) | 0,888 (0,851-0,925) | 0,980 | -2,8 (-4,8/-0,8) | -0,1 (-2,9/2,7) |
| LD (piruvato) | U/L | 217-967 | 81 | 8,5 (-3,2/20,1) | 0,974 (0,950-0,998) | 0,995 | -3,0 (-7,8/1,8) | -0,4 (-1,4/0,6) |
| PCR | mg/L | 2-135 | 96 | -1,4 (-2,9/0,2) | 0,994 (0,972-1,016) | 0,998 | -1,7 (-2,6/-0,8) | -5,5 (-7,7/-3,2) |
| Potasio, ion | mmol/L | 3,4-5,3 | 74 | -0,1 (-0,2/0,0) | 1,021 (0,995-1,047) | 0,996 | -0,03 (-0,04/-0,02) | -0,8 (-1,0/-0,5) |
| Proteína (suero) | g/L | 33-88 | 117 | -0,03 (-1,6/1,6) | 0,932 (0,906-0,958)* | 0,989 | tendencia | -7,2 (-7,7/-6,6)* |
| Proteína (orina) | mg/L | 54-1893 | 119 | -19 (-28/-10)* | 1,007 (0,989-1,025) | 0,996 | -17 (-24/-9)* | -15 (-19/-11) |
| Sodio, ion | mmol/L | 126-163 | 155 | r < 0,975 | r < 0,975 | 0,931 | 5,5 (5,2-5,7) | -0,7 (-1,0/-0,5) |
| Transferrina | mg/dL | 65-388 | 117 | no lineal | no lineal | 0,987 | tendencia | tendencia |
| Triglicéridos | mg/dL | 37-412 | 104 | -7,9 (-13/-2,4) | 1,030 (0,998-1,062) | 0,990 | -3,2 (-5,7/-0,7) | -3,8 (-5,5/-2,1) |
| Urea (suero) | mg/dL | 14-270 | 152 | 0,6 (-0,2/1,5) | 0,979 (0,968-0,991) | 0,998 | -0,6 (-1,2/-0,1) | -0,9 (-1,9/0,2) |
| Urea (orina) | mg/dL | 160-3400 | 76 | 21 (-10/53) | 0,938 (0,915/0,961) | 0,996 | tendencia | -3,9 (-6,0/-1,8) |
| Urato (suero) | mg/dL | 0,7-15,3 | 78 | 0,0 (-0,1/0,1) | 1,008 (0,989-1,028) | 0,997 | 0,0 (-0,01/0,09) | 1,1 (-0,6/2,8) |
| Urato (orina) | mg/dL | 5-121 | 61 | -1,0 (-2,0/0,0) | 0,985 (0,959-1,010) | 0,996 | -1,5 (-2,1/-0,9) | -8 (-12/-4) |
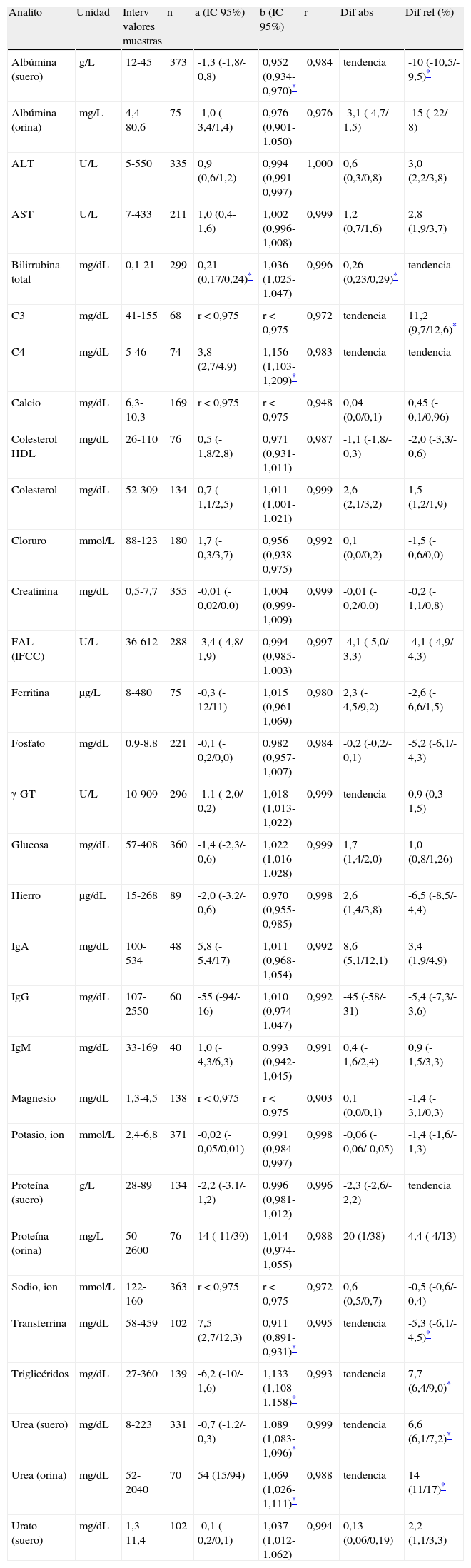
Comparación de procedimientos de medida, Centro B: Roche Cobas C711 y Siemens BNII (C3, C4, IgG, IgA, IgM)
| Analito | Unidad | Interv valores muestras | n | a (IC 95%) | b (IC 95%) | r | Dif abs | Dif rel (%) |
| Albúmina (suero) | g/L | 12-45 | 373 | -1,3 (-1,8/-0,8) | 0,952 (0,934-0,970)* | 0,984 | tendencia | -10 (-10,5/-9,5)* |
| Albúmina (orina) | mg/L | 4,4-80,6 | 75 | -1,0 (-3,4/1,4) | 0,976 (0,901-1,050) | 0,976 | -3,1 (-4,7/-1,5) | -15 (-22/-8) |
| ALT | U/L | 5-550 | 335 | 0,9 (0,6/1,2) | 0,994 (0,991-0,997) | 1,000 | 0,6 (0,3/0,8) | 3,0 (2,2/3,8) |
| AST | U/L | 7-433 | 211 | 1,0 (0,4-1,6) | 1,002 (0,996-1,008) | 0,999 | 1,2 (0,7/1,6) | 2,8 (1,9/3,7) |
| Bilirrubina total | mg/dL | 0,1-21 | 299 | 0,21 (0,17/0,24)* | 1,036 (1,025-1,047) | 0,996 | 0,26 (0,23/0,29)* | tendencia |
| C3 | mg/dL | 41-155 | 68 | r < 0,975 | r < 0,975 | 0,972 | tendencia | 11,2 (9,7/12,6)* |
| C4 | mg/dL | 5-46 | 74 | 3,8 (2,7/4,9) | 1,156 (1,103-1,209)* | 0,983 | tendencia | tendencia |
| Calcio | mg/dL | 6,3-10,3 | 169 | r < 0,975 | r < 0,975 | 0,948 | 0,04 (0,0/0,1) | 0,45 (-0,1/0,96) |
| Colesterol HDL | mg/dL | 26-110 | 76 | 0,5 (-1,8/2,8) | 0,971 (0,931-1,011) | 0,987 | -1,1 (-1,8/-0,3) | -2,0 (-3,3/-0,6) |
| Colesterol | mg/dL | 52-309 | 134 | 0,7 (-1,1/2,5) | 1,011 (1,001-1,021) | 0,999 | 2,6 (2,1/3,2) | 1,5 (1,2/1,9) |
| Cloruro | mmol/L | 88-123 | 180 | 1,7 (-0,3/3,7) | 0,956 (0,938-0,975) | 0,992 | 0,1 (0,0/0,2) | -1,5 (-0,6/0,0) |
| Creatinina | mg/dL | 0,5-7,7 | 355 | -0,01 (-0,02/0,0) | 1,004 (0,999-1,009) | 0,999 | -0,01 (-0,2/0,0) | -0,2 (-1,1/0,8) |
| FAL (IFCC) | U/L | 36-612 | 288 | -3,4 (-4,8/-1,9) | 0,994 (0,985-1,003) | 0,997 | -4,1 (-5,0/-3,3) | -4,1 (-4,9/-4,3) |
| Ferritina | μg/L | 8-480 | 75 | -0,3 (-12/11) | 1,015 (0,961-1,069) | 0,980 | 2,3 (-4,5/9,2) | -2,6 (-6,6/1,5) |
| Fosfato | mg/dL | 0,9-8,8 | 221 | -0,1 (-0,2/0,0) | 0,982 (0,957-1,007) | 0,984 | -0,2 (-0,2/-0,1) | -5,2 (-6,1/-4,3) |
| γ-GT | U/L | 10-909 | 296 | -1.1 (-2,0/-0,2) | 1,018 (1,013-1,022) | 0,999 | tendencia | 0,9 (0,3-1,5) |
| Glucosa | mg/dL | 57-408 | 360 | -1,4 (-2,3/-0,6) | 1,022 (1,016-1,028) | 0,999 | 1,7 (1,4/2,0) | 1,0 (0,8/1,26) |
| Hierro | μg/dL | 15-268 | 89 | -2,0 (-3,2/-0,6) | 0,970 (0,955-0,985) | 0,998 | 2,6 (1,4/3,8) | -6,5 (-8,5/-4,4) |
| IgA | mg/dL | 100-534 | 48 | 5,8 (-5,4/17) | 1,011 (0,968-1,054) | 0,992 | 8,6 (5,1/12,1) | 3,4 (1,9/4,9) |
| IgG | mg/dL | 107-2550 | 60 | -55 (-94/-16) | 1,010 (0,974-1,047) | 0,992 | -45 (-58/-31) | -5,4 (-7,3/-3,6) |
| IgM | mg/dL | 33-169 | 40 | 1,0 (-4,3/6,3) | 0,993 (0,942-1,045) | 0,991 | 0,4 (-1,6/2,4) | 0,9 (-1,5/3,3) |
| Magnesio | mg/dL | 1,3-4,5 | 138 | r < 0,975 | r < 0,975 | 0,903 | 0,1 (0,0/0,1) | -1,4 (-3,1/0,3) |
| Potasio, ion | mmol/L | 2,4-6,8 | 371 | -0,02 (-0,05/0,01) | 0,991 (0,984-0,997) | 0,998 | -0,06 (-0,06/-0,05) | -1,4 (-1,6/-1,3) |
| Proteína (suero) | g/L | 28-89 | 134 | -2,2 (-3,1/-1,2) | 0,996 (0,981-1,012) | 0,996 | -2,3 (-2,6/-2,2) | tendencia |
| Proteína (orina) | mg/L | 50-2600 | 76 | 14 (-11/39) | 1,014 (0,974-1,055) | 0,988 | 20 (1/38) | 4,4 (-4/13) |
| Sodio, ion | mmol/L | 122-160 | 363 | r < 0,975 | r < 0,975 | 0,972 | 0,6 (0,5/0,7) | -0,5 (-0,6/-0,4) |
| Transferrina | mg/dL | 58-459 | 102 | 7,5 (2,7/12,3) | 0,911 (0,891-0,931)* | 0,995 | tendencia | -5,3 (-6,1/-4,5)* |
| Triglicéridos | mg/dL | 27-360 | 139 | -6,2 (-10/-1,6) | 1,133 (1,108-1,158)* | 0,993 | tendencia | 7,7 (6,4/9,0)* |
| Urea (suero) | mg/dL | 8-223 | 331 | -0,7 (-1,2/-0,3) | 1,089 (1,083-1,096)* | 0,999 | tendencia | 6,6 (6,1/7,2)* |
| Urea (orina) | mg/dL | 52-2040 | 70 | 54 (15/94) | 1,069 (1,026-1,111)* | 0,988 | tendencia | 14 (11/17)* |
| Urato (suero) | mg/dL | 1,3-11,4 | 102 | -0,1 (-0,2/0,1) | 1,037 (1,012-1,062) | 0,994 | 0,13 (0,06/0,19) | 2,2 (1,1/3,3) |
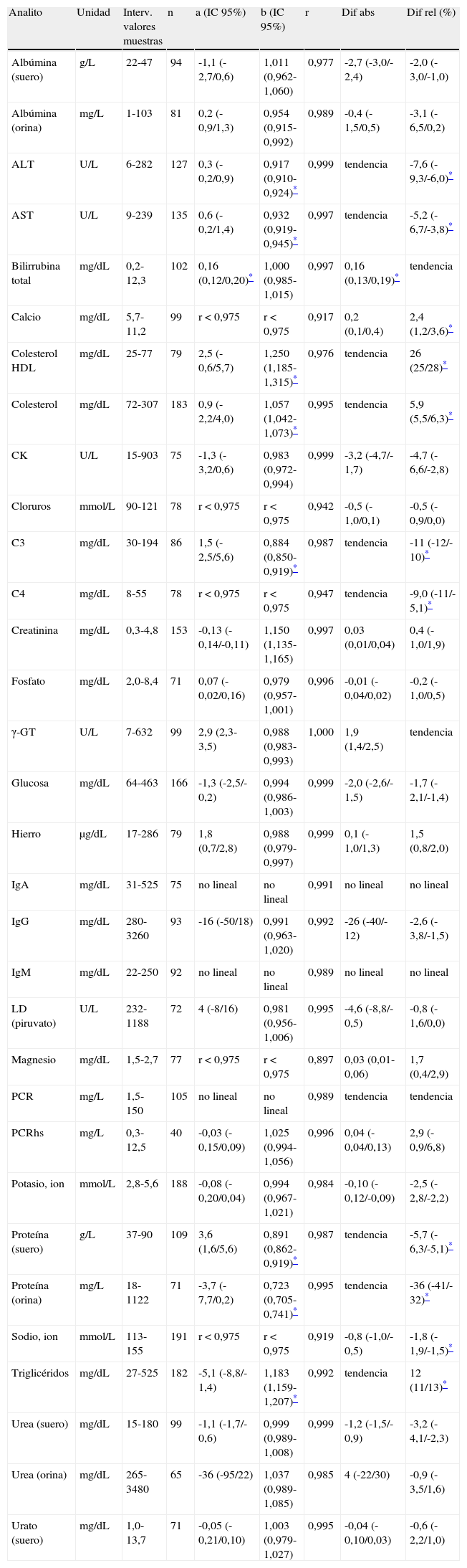
Comparación de procedimientos de medida, Centro C: Siemens ADVIA 2400, 1800 (orinas) y Siemens BNII (Ig A, G y M)
| Analito | Unidad | Interv. valores muestras | n | a (IC 95%) | b (IC 95%) | r | Dif abs | Dif rel (%) |
| Albúmina (suero) | g/L | 22-47 | 94 | -1,1 (-2,7/0,6) | 1,011 (0,962-1,060) | 0,977 | -2,7 (-3,0/-2,4) | -2,0 (-3,0/-1,0) |
| Albúmina (orina) | mg/L | 1-103 | 81 | 0,2 (-0,9/1,3) | 0,954 (0,915-0,992) | 0,989 | -0,4 (-1,5/0,5) | -3,1 (-6,5/0,2) |
| ALT | U/L | 6-282 | 127 | 0,3 (-0,2/0,9) | 0,917 (0,910-0,924)* | 0,999 | tendencia | -7,6 (-9,3/-6,0)* |
| AST | U/L | 9-239 | 135 | 0,6 (-0,2/1,4) | 0,932 (0,919-0,945)* | 0,997 | tendencia | -5,2 (-6,7/-3,8)* |
| Bilirrubina total | mg/dL | 0,2-12,3 | 102 | 0,16 (0,12/0,20)* | 1,000 (0,985-1,015) | 0,997 | 0,16 (0,13/0,19)* | tendencia |
| Calcio | mg/dL | 5,7-11,2 | 99 | r < 0,975 | r < 0,975 | 0,917 | 0,2 (0,1/0,4) | 2,4 (1,2/3,6)* |
| Colesterol HDL | mg/dL | 25-77 | 79 | 2,5 (-0,6/5,7) | 1,250 (1,185-1,315)* | 0,976 | tendencia | 26 (25/28)* |
| Colesterol | mg/dL | 72-307 | 183 | 0,9 (-2,2/4,0) | 1,057 (1,042-1,073)* | 0,995 | tendencia | 5,9 (5,5/6,3)* |
| CK | U/L | 15-903 | 75 | -1,3 (-3,2/0,6) | 0,983 (0,972-0,994) | 0,999 | -3,2 (-4,7/-1,7) | -4,7 (-6,6/-2,8) |
| Cloruros | mmol/L | 90-121 | 78 | r < 0,975 | r < 0,975 | 0,942 | -0,5 (-1,0/0,1) | -0,5 (-0,9/0,0) |
| C3 | mg/dL | 30-194 | 86 | 1,5 (-2,5/5,6) | 0,884 (0,850-0,919)* | 0,987 | tendencia | -11 (-12/-10)* |
| C4 | mg/dL | 8-55 | 78 | r < 0,975 | r < 0,975 | 0,947 | tendencia | -9,0 (-11/-5,1)* |
| Creatinina | mg/dL | 0,3-4,8 | 153 | -0,13 (-0,14/-0,11) | 1,150 (1,135-1,165) | 0,997 | 0,03 (0,01/0,04) | 0,4 (-1,0/1,9) |
| Fosfato | mg/dL | 2,0-8,4 | 71 | 0,07 (-0,02/0,16) | 0,979 (0,957-1,001) | 0,996 | -0,01 (-0,04/0,02) | -0,2 (-1,0/0,5) |
| γ-GT | U/L | 7-632 | 99 | 2,9 (2,3-3,5) | 0,988 (0,983-0,993) | 1,000 | 1,9 (1,4/2,5) | tendencia |
| Glucosa | mg/dL | 64-463 | 166 | -1,3 (-2,5/-0,2) | 0,994 (0,986-1,003) | 0,999 | -2,0 (-2,6/-1,5) | -1,7 (-2,1/-1,4) |
| Hierro | μg/dL | 17-286 | 79 | 1,8 (0,7/2,8) | 0,988 (0,979-0,997) | 0,999 | 0,1 (-1,0/1,3) | 1,5 (0,8/2,0) |
| IgA | mg/dL | 31-525 | 75 | no lineal | no lineal | 0,991 | no lineal | no lineal |
| IgG | mg/dL | 280-3260 | 93 | -16 (-50/18) | 0,991 (0,963-1,020) | 0,992 | -26 (-40/-12) | -2,6 (-3,8/-1,5) |
| IgM | mg/dL | 22-250 | 92 | no lineal | no lineal | 0,989 | no lineal | no lineal |
| LD (piruvato) | U/L | 232-1188 | 72 | 4 (-8/16) | 0,981 (0,956-1,006) | 0,995 | -4,6 (-8,8/-0,5) | -0,8 (-1,6/0,0) |
| Magnesio | mg/dL | 1,5-2,7 | 77 | r < 0,975 | r < 0,975 | 0,897 | 0,03 (0,01-0,06) | 1,7 (0,4/2,9) |
| PCR | mg/L | 1,5-150 | 105 | no lineal | no lineal | 0,989 | tendencia | tendencia |
| PCRhs | mg/L | 0,3-12,5 | 40 | -0,03 (-0,15/0,09) | 1,025 (0,994-1,056) | 0,996 | 0,04 (-0,04/0,13) | 2,9 (-0,9/6,8) |
| Potasio, ion | mmol/L | 2,8-5,6 | 188 | -0,08 (-0,20/0,04) | 0,994 (0,967-1,021) | 0,984 | -0,10 (-0,12/-0,09) | -2,5 (-2,8/-2,2) |
| Proteína (suero) | g/L | 37-90 | 109 | 3,6 (1,6/5,6) | 0,891 (0,862-0,919)* | 0,987 | tendencia | -5,7 (-6,3/-5,1)* |
| Proteína (orina) | mg/L | 18-1122 | 71 | -3,7 (-7,7/0,2) | 0,723 (0,705-0,741)* | 0,995 | tendencia | -36 (-41/-32)* |
| Sodio, ion | mmol/L | 113-155 | 191 | r < 0,975 | r < 0,975 | 0,919 | -0,8 (-1,0/-0,5) | -1,8 (-1,9/-1,5)* |
| Triglicéridos | mg/dL | 27-525 | 182 | -5,1 (-8,8/-1,4) | 1,183 (1,159-1,207)* | 0,992 | tendencia | 12 (11/13)* |
| Urea (suero) | mg/dL | 15-180 | 99 | -1,1 (-1,7/-0,6) | 0,999 (0,989-1,008) | 0,999 | -1,2 (-1,5/-0,9) | -3,2 (-4,1/-2,3) |
| Urea (orina) | mg/dL | 265-3480 | 65 | -36 (-95/22) | 1,037 (0,989-1,085) | 0,985 | 4 (-22/30) | -0,9 (-3,5/1,6) |
| Urato (suero) | mg/dL | 1,0-13,7 | 71 | -0,05 (-0,21/0,10) | 1,003 (0,979-1,027) | 0,995 | -0,04 (-0,10/0,03) | -0,6 (-2,2/1,0) |
En cada muestra se midió el analito de interés utilizando el BA 400® y el analizador de referencia. Los resultados fueron analizados mediante regresión lineal y análisis de las diferencias (Bland-Altman). Los valores aberrantes identificados mediante las reglas propuestas por Martínez et al.7, se eliminaron de los cálculos. En todos los casos, el número de aberrantes eliminados fué inferior al 4% de los resultados obtenidos.
Para la regresión lineal se representaron los valores de y (BA400) frente a los correspondientes valores de x (procedimiento de referencia) y se realizó una inspección visual para identificar una posible relación no lineal entre ambos procedimientos de medida a lo largo de todo el intervalo de medida evaluado7,8. Seguidamente, se obtuvieron los valores de la pendiente (b) y la ordenada en el origen (a) para las parejas de resultados, así como sus respectivos intervalos de confianza del 95%. También se calculó el coeficiente de correlación (r).
Para el análisis de las diferencias entre los pares de datos (Bland-Altman) se representaron en gráficas las diferencias (absolutas o relativas) frente al promedio de ambos valores9–11. Seguidamente, se calculó la media de las diferencias (absolutas o relativas) y su intervalo de confianza del 95%.
Los cálculos y el análisis estadístico se realizaron utilizando el programa Excel ® de Microsoft.
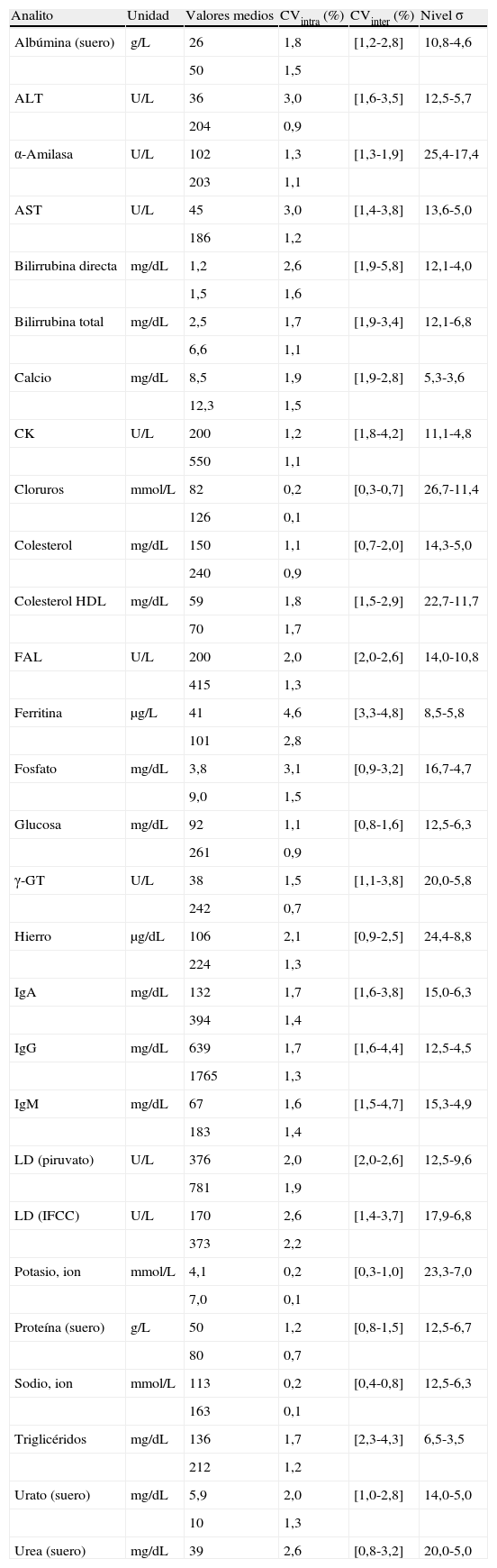
Resultados y discusiónImprecisiónLos resultados de la imprecisión intraserial e interdiaria se resumen en la tabla 2. La columna de valores medios indica las concentraciones medias de los dos sueros control empleados. El CVintra indica la imprecisión intraserial obtenida para los dos sueros control. El CVinter muestra el intervalo de valores de imprecisión interserial obtenido en los 4 centros participantes en el estudio y con los 2 materiales de control. El nivel sigma se ha calculado para el CVinter menor y para el CVinter mayor obtenido.
Imprecisión y nivel sigma (σ) del BA 400®
| Analito | Unidad | Valores medios | CVintra (%) | CVinter (%) | Nivel σ |
| Albúmina (suero) | g/L | 26 | 1,8 | [1,2-2,8] | 10,8-4,6 |
| 50 | 1,5 | ||||
| ALT | U/L | 36 | 3,0 | [1,6-3,5] | 12,5-5,7 |
| 204 | 0,9 | ||||
| α-Amilasa | U/L | 102 | 1,3 | [1,3-1,9] | 25,4-17,4 |
| 203 | 1,1 | ||||
| AST | U/L | 45 | 3,0 | [1,4-3,8] | 13,6-5,0 |
| 186 | 1,2 | ||||
| Bilirrubina directa | mg/dL | 1,2 | 2,6 | [1,9-5,8] | 12,1-4,0 |
| 1,5 | 1,6 | ||||
| Bilirrubina total | mg/dL | 2,5 | 1,7 | [1,9-3,4] | 12,1-6,8 |
| 6,6 | 1,1 | ||||
| Calcio | mg/dL | 8,5 | 1,9 | [1,9-2,8] | 5,3-3,6 |
| 12,3 | 1,5 | ||||
| CK | U/L | 200 | 1,2 | [1,8-4,2] | 11,1-4,8 |
| 550 | 1,1 | ||||
| Cloruros | mmol/L | 82 | 0,2 | [0,3-0,7] | 26,7-11,4 |
| 126 | 0,1 | ||||
| Colesterol | mg/dL | 150 | 1,1 | [0,7-2,0] | 14,3-5,0 |
| 240 | 0,9 | ||||
| Colesterol HDL | mg/dL | 59 | 1,8 | [1,5-2,9] | 22,7-11,7 |
| 70 | 1,7 | ||||
| FAL | U/L | 200 | 2,0 | [2,0-2,6] | 14,0-10,8 |
| 415 | 1,3 | ||||
| Ferritina | μg/L | 41 | 4,6 | [3,3-4,8] | 8,5-5,8 |
| 101 | 2,8 | ||||
| Fosfato | mg/dL | 3,8 | 3,1 | [0,9-3,2] | 16,7-4,7 |
| 9,0 | 1,5 | ||||
| Glucosa | mg/dL | 92 | 1,1 | [0,8-1,6] | 12,5-6,3 |
| 261 | 0,9 | ||||
| γ-GT | U/L | 38 | 1,5 | [1,1-3,8] | 20,0-5,8 |
| 242 | 0,7 | ||||
| Hierro | μg/dL | 106 | 2,1 | [0,9-2,5] | 24,4-8,8 |
| 224 | 1,3 | ||||
| IgA | mg/dL | 132 | 1,7 | [1,6-3,8] | 15,0-6,3 |
| 394 | 1,4 | ||||
| IgG | mg/dL | 639 | 1,7 | [1,6-4,4] | 12,5-4,5 |
| 1765 | 1,3 | ||||
| IgM | mg/dL | 67 | 1,6 | [1,5-4,7] | 15,3-4,9 |
| 183 | 1,4 | ||||
| LD (piruvato) | U/L | 376 | 2,0 | [2,0-2,6] | 12,5-9,6 |
| 781 | 1,9 | ||||
| LD (IFCC) | U/L | 170 | 2,6 | [1,4-3,7] | 17,9-6,8 |
| 373 | 2,2 | ||||
| Potasio, ion | mmol/L | 4,1 | 0,2 | [0,3-1,0] | 23,3-7,0 |
| 7,0 | 0,1 | ||||
| Proteína (suero) | g/L | 50 | 1,2 | [0,8-1,5] | 12,5-6,7 |
| 80 | 0,7 | ||||
| Sodio, ion | mmol/L | 113 | 0,2 | [0,4-0,8] | 12,5-6,3 |
| 163 | 0,1 | ||||
| Triglicéridos | mg/dL | 136 | 1,7 | [2,3-4,3] | 6,5-3,5 |
| 212 | 1,2 | ||||
| Urato (suero) | mg/dL | 5,9 | 2,0 | [1,0-2,8] | 14,0-5,0 |
| 10 | 1,3 | ||||
| Urea (suero) | mg/dL | 39 | 2,6 | [0,8-3,2] | 20,0-5,0 |
En base a los niveles sigma calculados, puede considerarse que la imprecisión interdiaria del instrumento es excelente (nivel sigma superior a 6,0) para la mayor parte de los procedimientos de medida estudiados. La imprecisión de los procedimientos de medida turbidimétricos fue algo superior a la obtenida para los espectrométricos. Los procedimientos potenciométricos fueron los que presentaron mejor precisión (CVinter ≤ 1,0%). Los peores resultados (niveles sigma entre 3,5 y 4,0) se obtuvieron para materiales con concentraciones bajas de bilirubina directa, calcio y triglicéridos.
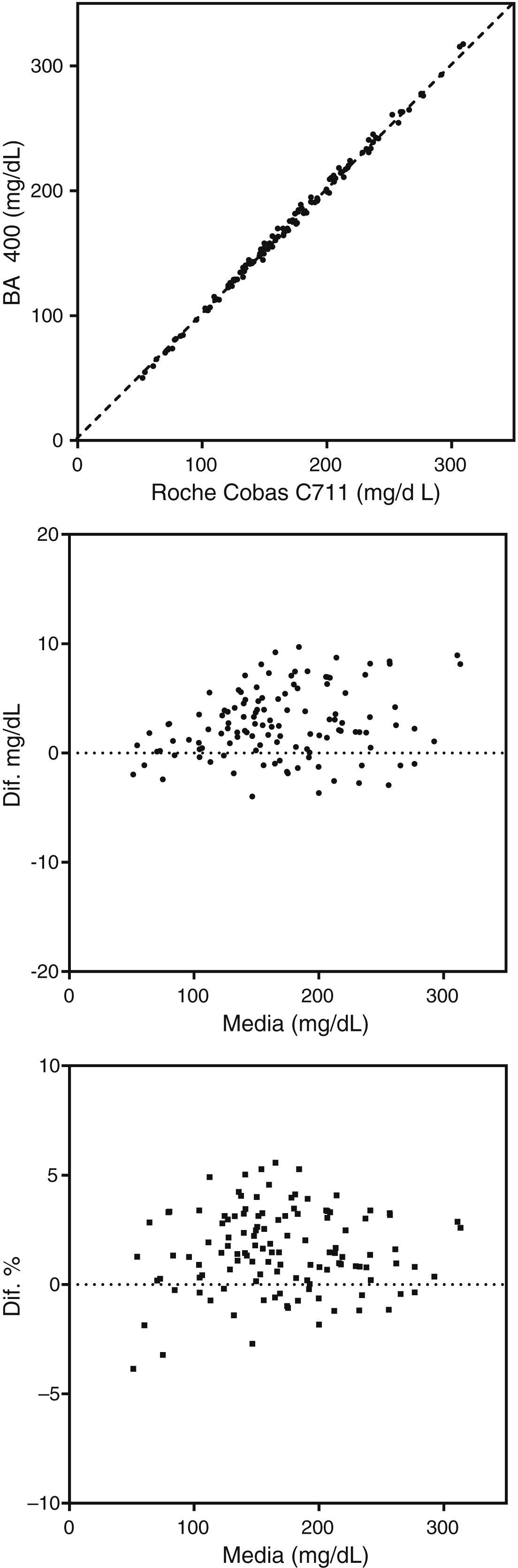
Comparación de procedimientos de medidaLas tablas 3–5 muestran los resultados obtenidos en el estudio de veracidad realizado en cada centro evaluador. Para cada analito se indica el intervalo de valores de las muestras analizadas, el valor e intervalo de confianza del 95% de la ordenada en el origen (a) y de la pendiente (b), el valor del coeficiente de correlación (r) y los valores e intervalos de confianza del 95% de la media de las diferencias expresada en valor absoluto y en valor relativo (%). Las figuras 1-3 son algunos ejemplos ilustrativos de las correspondientes gráficas.
Cuando el valor de r es inferior a 0,975 es indicativo de que el intervalo de valores estudiados no es adecuado o de que existen importantes diferencias de especificidad analítica entre los procedimientos de medida comparados7,8. En estos casos, no se han tenido en cuenta los resultados de la regresión lineal.
Los resultados de un análisis de regresión son válidos sólo si ciertos supuestos acerca de los datos son ciertos. Uno de ellos es que los valores de la variable x carezcan de error. En el laboratorio clínico esto no se cumple ya que cada medida tiene un error intrínseco. Sin embargo, si el intervalo de los datos es lo suficientemente amplio, el efecto de este error en las estimaciones de la regresión se puede considerar insignificante7.
Por otra parte, se han descrito métodos que son más robustos que la regresión lineal simple, como los de Deming o el de Passing-Bablok7,8,12. No obstante, cuando se comparan procedimientos de medida en el laboratorio clínico, los valores obtenidos para la ordenada en el origen y la pendiente son generalmente muy similares con los distintos métodos de regresión. De hecho, es más importante una distribución adecuada de los valores en el intervalo de mediciones que el modelo estadístico empleado7,12.
Las diferencias encontradas, pueden considerarse no despreciables y estadísticamente significativas cuando se cumplen las siguientes condiciones:
- a)
Se han podido realizar los dos tipos de análisis (regresión y diferencias) y ambos coinciden en la identificación de diferencias significativas.
- b)
La diferencia es de tipo proporcional y superior a 1/5 del error máximo permitido7.
- c)
La diferencia es de tipo constante y no es despreciable en comparación con el intervalo de valores medidos en las muestras estudiadas.
La figura 1 muestra un ejemplo de comparación en el que no se encontraron diferencias significativas de ningún tipo.
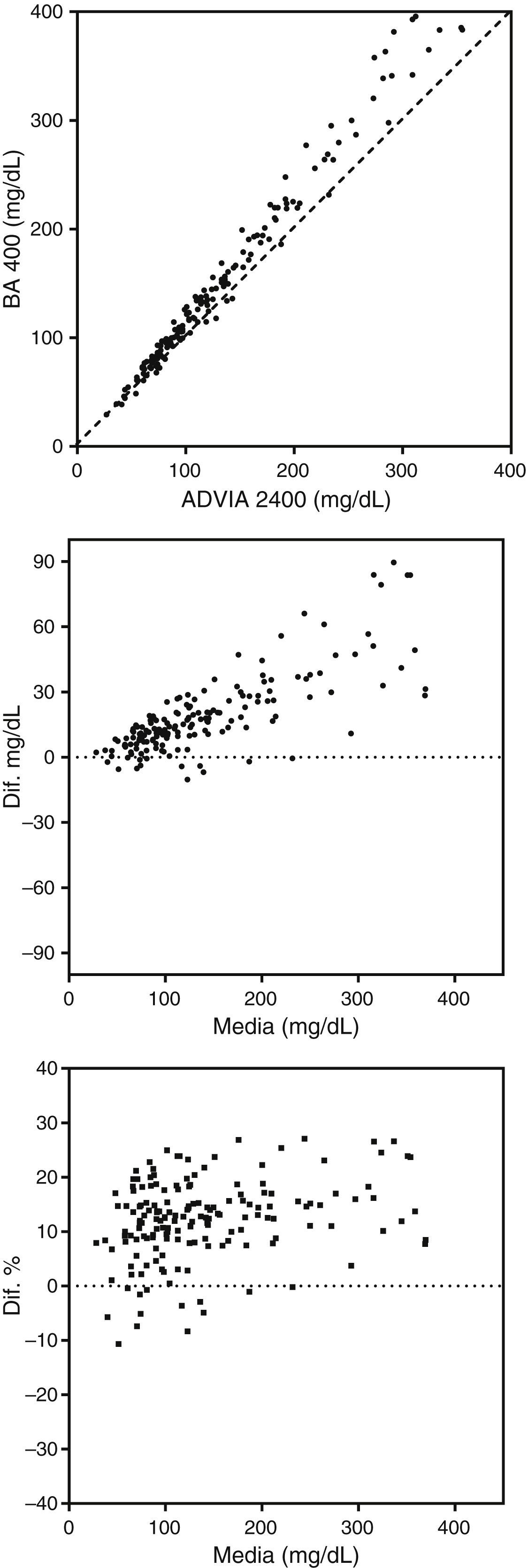
Cuando existe una diferencia de tipo proporcional entre los procedimientos de medida comparados, la representación gráfica de las diferencias absolutas muestra una tendencia (creciente o decreciente). En estos casos, la media de diferencias absolutas no tiene significación alguna. La figura 2 muestra un ejemplo de esta situación.
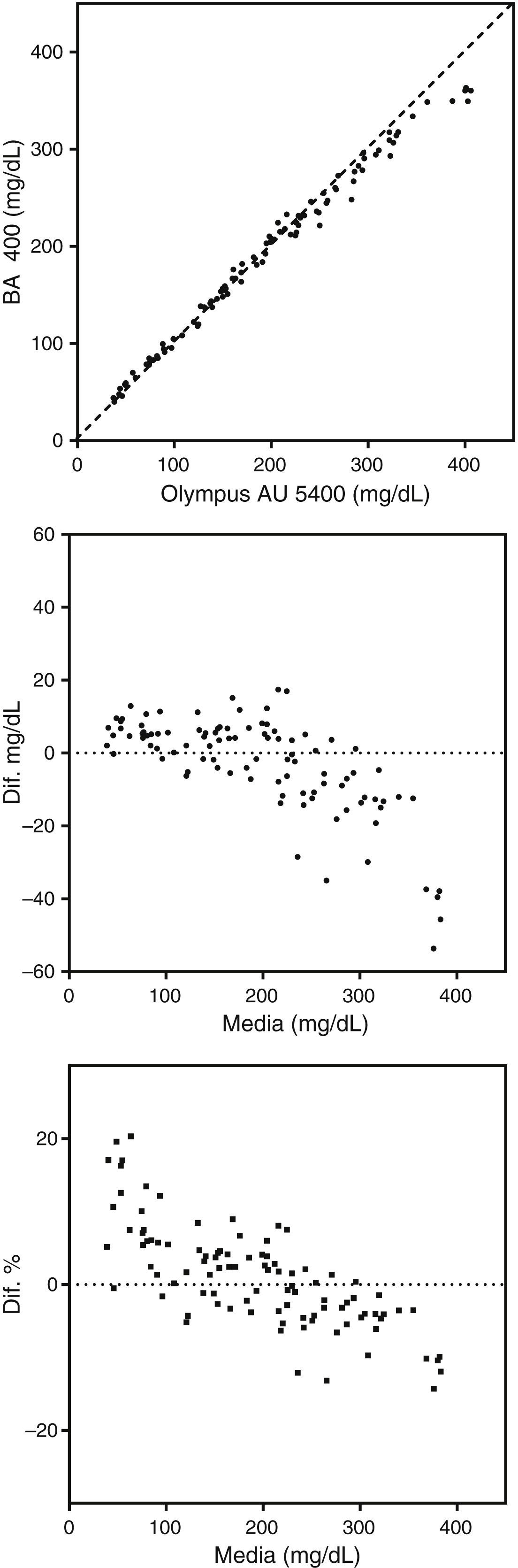
La figura 3 es un ejemplo de insuficiente linealidad en la recta de regresión. Esto puede ser debido a una deficiente linealidad en el procedimiento de medida evaluado, a diferencias en el proceso de calibración o a diferencias en la especificidad analítica de los procedimientos comparados. En estos casos las dos gráficas de las diferencias (absolutas y relativas) muestran tendencias.
Las diferencias significativas de tipo constante entre procedimientos de medida son de difícil interpretación. Pueden ser ocasionadas por un efecto de la matriz de la muestra sobre uno de los procedimientos comparados o por diferencias de la especificidad analítica de los procedimientos7.
Las diferencias significativas de tipo proporcional son generalmente ocasionadas por diferencias en la calibración. Las diferencias de tamaño moderado pueden ser debidas a defectos en el proceso de calibración o a la incertidumbre de los valores asignados a los calibradores. Un caso particular es el de las transaminasas (ALT y AST) en donde las diferencias encontradas se deben a la utilización o no de fosfato de piridoxal en el reactivo. Los procedimientos de medida con fosfato de piridoxal proporcionan valores algo más elevados.
Aunque en algunos procedimientos de medida del sistema BA 400® se han encontrado diferencias significativas con uno de los procedimientos de medida de referencia, estas diferencias no se confirmaron en las comparaciones con los otros dos sistemas de referencia. Este es el caso, por ejemplo, de albúmina (suero) y ferritina en el centro A, y de colesterol, colesterol HDL y proteína (orina) en el centro C.
ConclusionesLa evaluación del sistema Biosystems BA 400® realizada en varios centros ha demostrado las excelentes prestaciones de precisión y veracidad del sistema. El nuevo analizador, que incorpora una batería de LEDs monocromáticos como fuente de luz, proporciona resultados en muestras de pacientes que son equivalentes a los obtenidos con analizadores que tienen una lámpara halógena tradicional (Olympus AU5400 y AU2700, Roche Cobas C711 y Siemens ADVIA 2400, 1800 y BNII).
Conflicto de interesesF. Javier Gella Tomás es Director del Área de Reactivos de Biosystems, S.A.