Los resultados de los programas de garantía de calidad indican que existen diferencias significativas entre los métodos homogéneos disponibles para la medición del colesterol HDL. Sin embargo, la posible influencia de efectos matriz en las muestras liofilizadas empleadas y la ausencia de un valor verdadero en estas muestras, hace difícil la valoración completa de estos métodos. En este estudio experimental multicéntrico hemos comparado los métodos homogéneos más utilizados en nuestro medio, con respecto al de precipitación de ácido fosfotúngstico-MgCl2.
Material y métodosCada laboratorio procesó unas 100 muestras de suero de pacientes por uno o dos métodos homogéneos y envió alícuotas congeladas de las muestras analizadas al laboratorio central donde se procesaron por el método de precipitación.
ResultadosLas imprecisiones de los métodos homogéneos fueron buenas e inferiores a las de precipitación, que cumplía las especificaciones de calidad para sesgo y error total (ET). Sin embargo, no todos los métodos homogéneos cumplían los objetivos de calidad mínimos, pues algunos procedimientos producían sesgos positivos muy altos (en relación al método de comparación) y uno un sesgo negativo muy bajo. El estudio de la concordancia, realizado estratificando a los pacientes según las concentraciones de colesterol HDL, mostró diferencias entre los métodos.
ConclusionesEstos resultados sugieren que existen discrepancias en la valoración de las magnitudes obtenidas con los métodos homogéneos, probablemente generada por una elevada inexactitud en algunos de ellos y que es conveniente que los laboratorios conozcan las caracteristicas de imprecisión y sesgo del metodo directo que utilizan con respecto al de referencia.
The results of quality assurance programs suggest that there are significant differences between the homogeneous methods available for the measurement of HDL cholesterol. However, the possible influence of matrix effects in the lyophilized samples used and the absence of a true value in these samples means that a full assessment of these methods cannot be made. In this multicentre pilot study we compared the most used homogeneous methods in our country with the phosphotungstic acid-MgCl2 method.
Material and methodsEach laboratory processed about one hundred serum samples from patients with one or two homogeneous methods and sent frozen aliquots of the samples in special packaging with dry ice to the central laboratory where they were processed by the precipitation method.
ResultsThe imprecision of homogeneous methods were good and lower than those of the precipitation method, and met the quality specifications for bias and total error (TE). However, not all homogeneous methods met the minimum quality objectives, as some procedures produced a very high positive bias (relative to the comparison method) and one, a low negative bias. In addition, the study of the agreement between methods, made by stratifying patients according to HDL cholesterol concentrations, showed differences.
ConclusionsThese results suggest that there are discrepancies in the assessment of the levels obtained with homogeneous methods, probably due to a high inaccuracy in some of them, and it is advised that the laboratories be aware of the characteristics of inaccuracy and bias of the direct method used compared to the reference method.
Diversos estudios epidemiológicos han demostrado una asociación inversa entre el colesterol ligado a las lipoproteínas de alta densidad (cHDL) y la enfermedad cardiovascular1–4. Por ello, actualmente hay un acuerdo general en considerar al cHDL como un factor de riesgo independiente de la enfermedad coronaria. El National Colesterol Education Program (NCEP)5 en sus Guías Clínicas para el diagnóstico y tratamiento de la hipercolesterolemia, incluye la cuantificación del cHDL conjuntamente con la cuantificación del colesterol total en el estudio inicial de las mismas, considerando que concentraciones de cHDL por debajo de 40mg/dL indican mayor riesgo de aterosclerosis y concentraciones superiores o iguales a 60mg/dL se consideran protectoras. La Sociedad Europea de Aterosclerosis y otros grupos de consenso también recomiendan la inclusión del cHDL para el diagnóstico y manejo de los pacientes con riesgo incrementado de enfermedad coronaria6,7.
Por otra parte, los laboratorios clínicos utilizan los valores de cHDL para calcular, mediante la fórmula de Friedewald8, la concentración de colesterol LDL (cLDL) y, mediante la diferencia con el colesterol total, la concentración del colesterol no HDL. De esta manera, un error en la determinación del cHDL supone un cálculo erróneo del cLDL y del colesterol no HDL, el cual incluye a todas las lipoproteínas aterogénicas que contienen apo B y constituye una herramienta clínica confiable para valorar el riesgo de enfermedad cardiovascular en pacientes hipertrigliceridémicos9,10.
La gran importancia clínica y la existencia de unos valores discriminantes de aplicación universal determinan la necesidad de que la cuantificación del cHDL en el laboratorio sea precisa y exacta, y las magnitudes obtenidas sean comparables entre laboratorios y a lo largo del tiempo. Para ello, el NCEP estableció que a partir de 1998 los laboratorios clínicos cumplieran con unos criterios de calidad analíticos para la cuantificación del cHDL: el ET debería ser≤13%, compatible con una inexactitud ≤ 5% (comparado con el método de referencia del CDC) y una imprecisión≤4% (CV)11. El método de referencia12 es un método que combina una ultracentrifugación inicial a d=1,006 kg/L para separar las VLDL, seguido de una precipitación en el infranadante con heparina-MnCl2 de las lipoproteínas con apoB, y cuantificación del colesterol por el método de Abell-Kendall13.
En los laboratorios clínicos la cuantificación del cHDL hasta hace unas décadas se realizaba casi exclusivamente por métodos de precipitación, ensayos laboriosos y tediosos que requerían un paso de separación manual con reactivos precipitantes, seguido del análisis del contenido en colesterol mediante analizadores automatizados. La necesidad de mejorar la precisión de los métodos de precipitación, así como la contención del coste en los laboratorios clínicos y el aumento de la demanda tuvo como consecuencia el desarrollo de métodos completamente automatizados denominados métodos homogéneos, que emplean reactivos específicos para, con criterio selectivo, medir directamente el cHDL en la muestra de suero o plasma14.
Inicialmente los métodos homogéneos fueron validados satisfactoriamente frente al método de referencia. No obstante, los diversos cambios de formulación que han ido realizando los fabricantes con el paso del tiempo no siempre se han descrito ni evaluado completamente14. Por otra parte, los resultados de los programas de garantía de calidad externo de la Sociedad Española de Química Clínica y Patología Molecular (SEQC) de los últimos años15,16 sugieren que existen diferencias significativas entre los métodos homogéneos empleados habitualmente en nuestro medio. Sin embargo, la posible influencia de efectos matriz en las muestras liofilizadas empleadas y la ausencia en estas muestras de un valor verdadero u obtenido por un método de referencia hace imposible una valoración completa de estos métodos.
El objetivo del actual trabajo fue evaluar los métodos homogéneos de cuantificación del cHDL utilizados mayoritariamente en nuestro medio y compararlos con el método de precipitación, ácido fosfotúngstico-MgCl217 y determinación del colesterol con el método CHOD-PAP, ya que con este se obtienen resultados perfectamente transferibles a los del método de referencia y puede ser utilizado como método de comparación17. Por otra parte, los estudios clínicos y epidemiológicos en los que se basan los conocimientos sobre la asociación de las concentraciones de cHDL con la enfermedad arteriosclerótica fueron realizados con los métodos clásicos de precipitación.
Material y métodosDiseño y población del estudioEl diseño del estudio experimental fue multicéntrico. En él han participado los laboratorios de 8 centros españoles: Hospital Marqués de Valdecilla (Santander), Hospital de Galdakao (Vizcaya), Hospital Virgen Macarena (Sevilla), Hospital Dr. Negrín (Las Palmas de Gran Canaria), Hospital San Jorge (Huesca), Hospital Miguel Servet (Zaragoza), Complejo Hospitalario Univeristario A Coruña (A Coruña), y Hospital Gregorio Marañón (Madrid). Cada laboratorio seleccionó aproximadamente 100 muestras de pacientes (n=927), de forma aleatoria (las únicas condiciones de selección fueron que sobrase más de 1ml de suero tras realizar el resto de determinaciones solicitadas, y que en un mismo dia las concentraciones de las muestras fueran de diferente rango), con rango amplio de concentraciones de cHDL y las procesó por uno o dos métodos homogéneos de la forma que utilizaba habitualmente. En todos los laboratorios las determinaciones se realizaron en muestras de suero conservadas a 4°C durante un plazo máximo de 1-2 días tras su obtención. Siempre se utilizó suero sobrante de las peticiones solicitadas de forma habitual. Los resultados obtenidos en este estudio fueron anónimos y no se utilizaron con fines asistenciales. Los laboratorios participantes conservaron alícuotas de las muestras analizadas en recipientes adecuados y congeladas, a –20°C o –70°C, para envío al laboratorio central (Hospital Marqués de Valdecilla), que se realizó en envases especiales con hielo seco para asegurar la cadena de congelación. En el laboratorio central fueron conservadas a –70°C hasta el momento de su procesamiento por el método de comparación.
Estudio de imprecisión e inexactitudEl estudio de imprecisión se realizó siguiendo el protocolo EP5-A del CLSI (Clinical and Laboratory Standards Institute)18 con mediciones repetidas (duplicados) en dos ocasiones diarias, de un nivel de control durante un período de 21 días, para cada equipo-reactivo. La exactitud del método de comparación (precipitación) fue evaluado a través del programa de certificación del CDC. El error total (ET) se calculó como la suma del error sistemático y el error aleatorio19. El error sistemático se calculó por diferecia entre las medias de cada método respecto al de método de precipitación. El error aleatorio se define como 1,65×CVT del estudio de imprecisión.
Métodos de laboratorioMétodo de comparaciónLas muestras conservadas a –70°C, se descongelaron a 37°C, invirtiendo el contenedor varias veces para asegurar la homogeneidad de la muestra. Antes de realizar los ensayos se comprobó la ausencia de restos de fibrina, y en su caso se realizó una nueva centrifugación. Las muestras de suero no fueron sometidas a más de un proceso de congelación-descongelación durante el estudio. El suero se mezcló con ácido fosfotúngstico-MgCl2 (Biosystems®) en proporción 1/3,5, se incubó durante 20min a temperatura ambiente y se centrifugó durante 10min a 10.000xg. La concentración de colesterol se determinó en el sobrenadante en un equipo ADVIA 1650® a través de un canal abierto en el que se programó la relación muestra reactivo en 1/8 para obtener la mejor precisión fotométrica posible y utilizando un calibrador acuoso de colesterol (Biosystems®) con una concentración real de 15mg/dL.
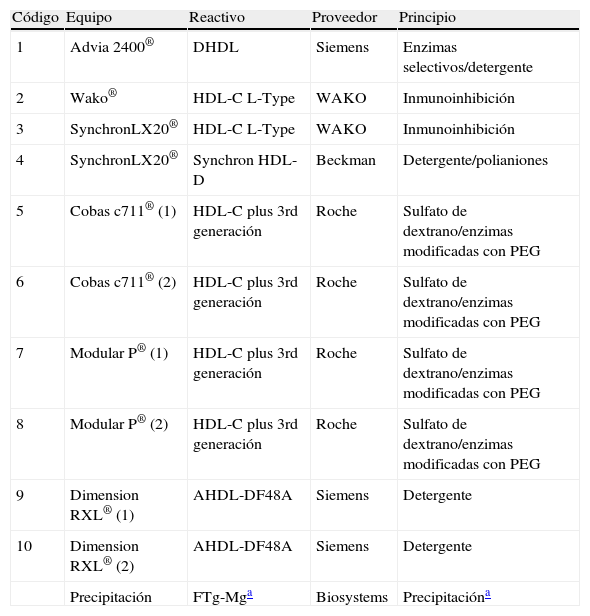
Métodos homogéneosLos métodos directos evaluados están indicados en la tabla 1. Se utilizó el equipo, reactivo y método proporcionados por el fabricante, siguiendo sus protocolos, sin introducir ninguna modificación relacionada con el estudio, con la excepción del método Wako® adaptado al analizador Wako. Los laboratorios realizaron las calibraciones en su instrumento de acuerdo a la práctica habitual: cuando el control de calidad lo aconsejaba o habían transcurrido 30 días desde la calibración anterior o había cambio del lote de reactivos. Han sido un total de 10 los sistemas analíticos (combinación de método e instrumento) evaluados.
Métodos y reactivos utilizados en la evaluación
| Código | Equipo | Reactivo | Proveedor | Principio |
| 1 | Advia 2400® | DHDL | Siemens | Enzimas selectivos/detergente |
| 2 | Wako® | HDL-C L-Type | WAKO | Inmunoinhibición |
| 3 | SynchronLX20® | HDL-C L-Type | WAKO | Inmunoinhibición |
| 4 | SynchronLX20® | Synchron HDL-D | Beckman | Detergente/polianiones |
| 5 | Cobas c711® (1) | HDL-C plus 3rd generación | Roche | Sulfato de dextrano/enzimas modificadas con PEG |
| 6 | Cobas c711® (2) | HDL-C plus 3rd generación | Roche | Sulfato de dextrano/enzimas modificadas con PEG |
| 7 | Modular P® (1) | HDL-C plus 3rd generación | Roche | Sulfato de dextrano/enzimas modificadas con PEG |
| 8 | Modular P® (2) | HDL-C plus 3rd generación | Roche | Sulfato de dextrano/enzimas modificadas con PEG |
| 9 | Dimension RXL® (1) | AHDL-DF48A | Siemens | Detergente |
| 10 | Dimension RXL® (2) | AHDL-DF48A | Siemens | Detergente |
| Precipitación | FTg-Mga | Biosystems | Precipitacióna |
Los pacientes se estratificaron en tres grupos según los valores utilizados habitualmente para valorar riesgo coronario: cHDL inferior a 40mg/dL, cHDL entre 40 y 60mg/dL y cHDL superior a 60mg/dL. Se estudió la concordancia en la clasificación de los pacientes con estos puntos de corte respecto al método de precipitación.
Influencia de la concentración de triglicéridosSe estudió el posible efecto de la concentración de triglicéridos en las diferencias entre el método de precipitación y los métodos homogéneos. Para ello se agruparon los resultados en tres grupos: a) triglicéridos <200mg/dL, b) entre 200 y 400mg/dL, y c) >400mg/dL, y se analizó si existían diferencias significativas respecto al método de precipitación en función de la concentración de triglicérido (los resultados se expresan como diferencia media entre la magnitud obtenida por precipitación menos la magnitud obtenida por el método directo).
La concentración de triglicéridos se cuantificó en cada laboratorio por el método utilizado habitualmente.
Análisis estadístico de los resultadosTratamiento estadísticoPara la comparación de los resultados obtenidos por cada método, con los obtenidos por precipitación, se calculó la diferencia de cada par de resultados, fueron agrupadas para cada sistema equipo-método, y éstas fueron sometidas a un análisis de varianza de una vía, utilizando el método de Bonferroni20 para las comparaciones post hoc múltiples entre sistemas (diferencias con el método de precipitación). Para los métodos en los que se obtuvieron datos de sistemas idénticos (equipo-reactivo) en dos laboratorios diferentes, se realizó un análisis de varianza univariante (modelo lineal general [MLG]) con el fin de estimar si las diferencias encontradas con el método de precipitación eran debidas al método o al centro. Se consideró significativo un valor de p<0,05. La comparación de los resultados de los métodos directos con el método de precipitación se realizó por análisis de regresión según Passing Bablok21. La concordancia en la clasificación de pacientes con los métodos directos estudiados respecto a la obtenida con el método de comparación de analizó mediante el índice kappa.
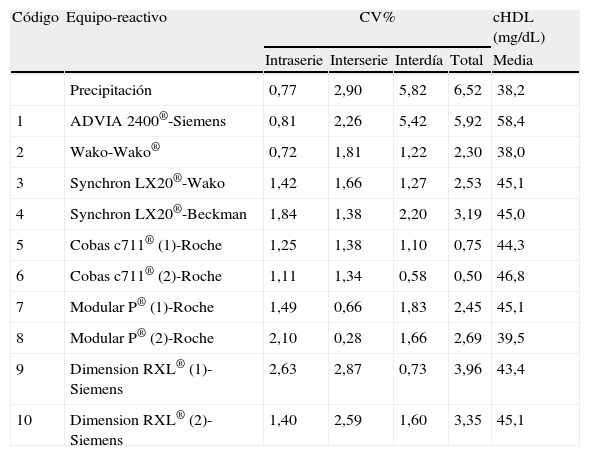
ResultadosAnálisis de imprecisión e inexactitudLos resultados del estudio de imprecisión de los métodos están reflejados en la tabla 2. Los CV% totales de los métodos directos están comprendidos entre el 0,77% y el 5,92%. El método de precipitación es el que muestra una mayor imprecisión (CV=6,52%). La desviación media del método de precipitación valorada dentro del programa del CDC es 2,02% (-1,08 a 4,46%), y el ET (errror sistemático+1,96 error aleatorio) del método de comparación es del 12,9%.
Estudio de la imprecisióna
| Código | Equipo-reactivo | CV% | cHDL (mg/dL) | |||
| Intraserie | Interserie | Interdía | Total | Media | ||
| Precipitación | 0,77 | 2,90 | 5,82 | 6,52 | 38,2 | |
| 1 | ADVIA 2400®-Siemens | 0,81 | 2,26 | 5,42 | 5,92 | 58,4 |
| 2 | Wako-Wako® | 0,72 | 1,81 | 1,22 | 2,30 | 38,0 |
| 3 | Synchron LX20®-Wako | 1,42 | 1,66 | 1,27 | 2,53 | 45,1 |
| 4 | Synchron LX20®-Beckman | 1,84 | 1,38 | 2,20 | 3,19 | 45,0 |
| 5 | Cobas c711® (1)-Roche | 1,25 | 1,38 | 1,10 | 0,75 | 44,3 |
| 6 | Cobas c711® (2)-Roche | 1,11 | 1,34 | 0,58 | 0,50 | 46,8 |
| 7 | Modular P® (1)-Roche | 1,49 | 0,66 | 1,83 | 2,45 | 45,1 |
| 8 | Modular P® (2)-Roche | 2,10 | 0,28 | 1,66 | 2,69 | 39,5 |
| 9 | Dimension RXL® (1)-Siemens | 2,63 | 2,87 | 0,73 | 3,96 | 43,4 |
| 10 | Dimension RXL® (2)-Siemens | 1,40 | 2,59 | 1,60 | 3,35 | 45,1 |
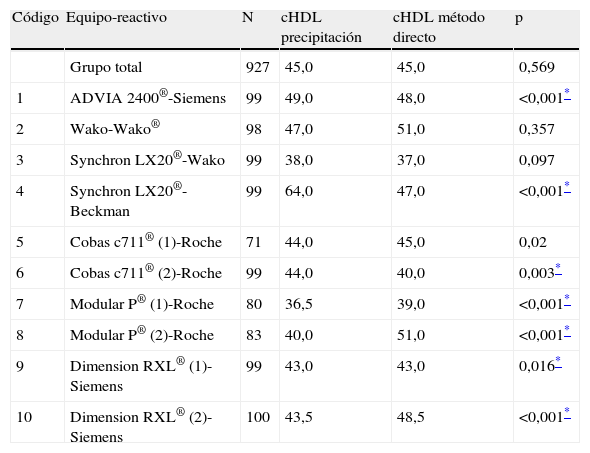
Las medianas de la concentración de cHDL obtenidas por el método de precipitación y por cada uno de los sistemas analíticos estudiados se incluyen en la tabla 3. No existen diferencias significativas entre las medianas (45,0mg/dL vs 45,0mg/dL) para el método de precipitación y la suma de los métodos directos. Los sistemas Wako-Wako, SynchronLX20®-Wako no muestran diferencias significativas de las medianas respecto al método de precipitación. El resto de sistemas utilizados muestran diferencias significativas en uno u otro sentido (cHDL por precipitación superior o inferior que el método directo).
Resultados de cHDL (mediana, mg/dL) obtenidos por precipitación y por los métodos directos
| Código | Equipo-reactivo | N | cHDL precipitación | cHDL método directo | p |
| Grupo total | 927 | 45,0 | 45,0 | 0,569 | |
| 1 | ADVIA 2400®-Siemens | 99 | 49,0 | 48,0 | <0,001* |
| 2 | Wako-Wako® | 98 | 47,0 | 51,0 | 0,357 |
| 3 | Synchron LX20®-Wako | 99 | 38,0 | 37,0 | 0,097 |
| 4 | Synchron LX20®-Beckman | 99 | 64,0 | 47,0 | <0,001* |
| 5 | Cobas c711® (1)-Roche | 71 | 44,0 | 45,0 | 0,02 |
| 6 | Cobas c711® (2)-Roche | 99 | 44,0 | 40,0 | 0,003* |
| 7 | Modular P® (1)-Roche | 80 | 36,5 | 39,0 | <0,001* |
| 8 | Modular P® (2)-Roche | 83 | 40,0 | 51,0 | <0,001* |
| 9 | Dimension RXL® (1)-Siemens | 99 | 43,0 | 43,0 | 0,016* |
| 10 | Dimension RXL® (2)-Siemens | 100 | 43,5 | 48,5 | <0,001* |
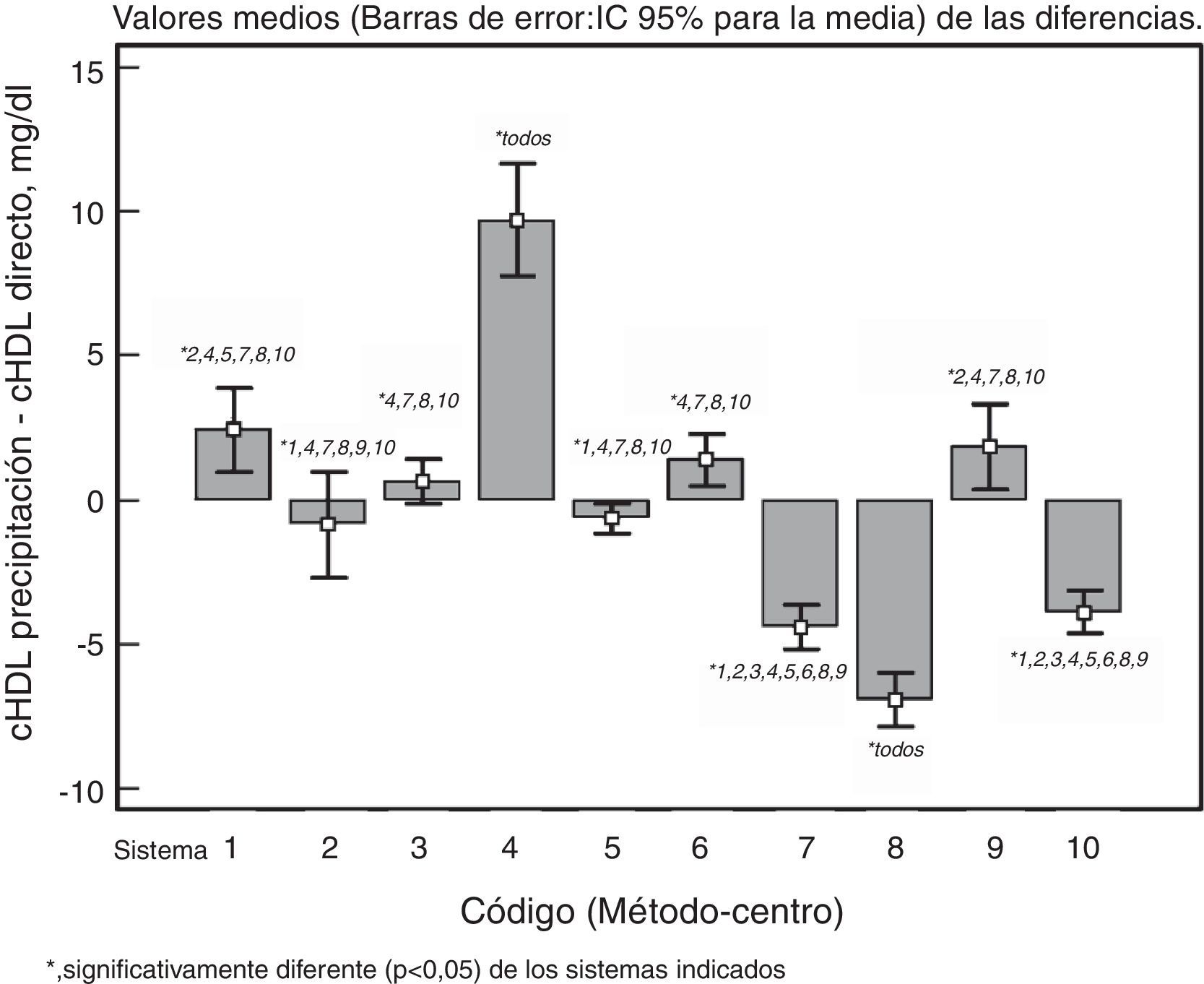
En la figura 1 se detallan las diferencias entre cada método y el de precipitación. Se observan diferencias medias (cHDL precipitación-cHDL directo, mg/dL), que oscilan entre -6,95mg/dL (IC del 95%: -7,88 a -6,02) (Modular P®[1]-Roche) y 9,70mg/dL (IC del 95%: 7,74 a 11,65) (SynchronLX20®-Beckman), siendo el sistema Cobas c711®-Roche® (diferencia media de -0,65mg/dL con un IC del 95%: -1,19 a -0,11mg/dL) y el método de inmunoinhibición de Wako adaptado en un equipo SynchronLX20® (diferencia media de 0,64mg/dL con un IC del 95%: -0,12 a 1,39mg/dL), las menores de todas ellas. Mediante el análisis de varianza univariante se observa que las diferencias obtenidas son significativamente distintas para la mayoría de los sistemas analizados entre sí (índices de la figura 1). Por tanto, las diferencias no son solo debidas al método, sino también al centro que lo utiliza.
En esta figura se esquematizan las diferencias medias de cada uno de los sistemas utilizados (método-centro) frente al método de precipitación. Entre paréntesis los sistemas frente a los que las diferencias son significativamente distintas. Cabe destacar que los sistemas 5-6, 7-8 y 9-10 son idénticos, pero que corresponden a centros diferentes.
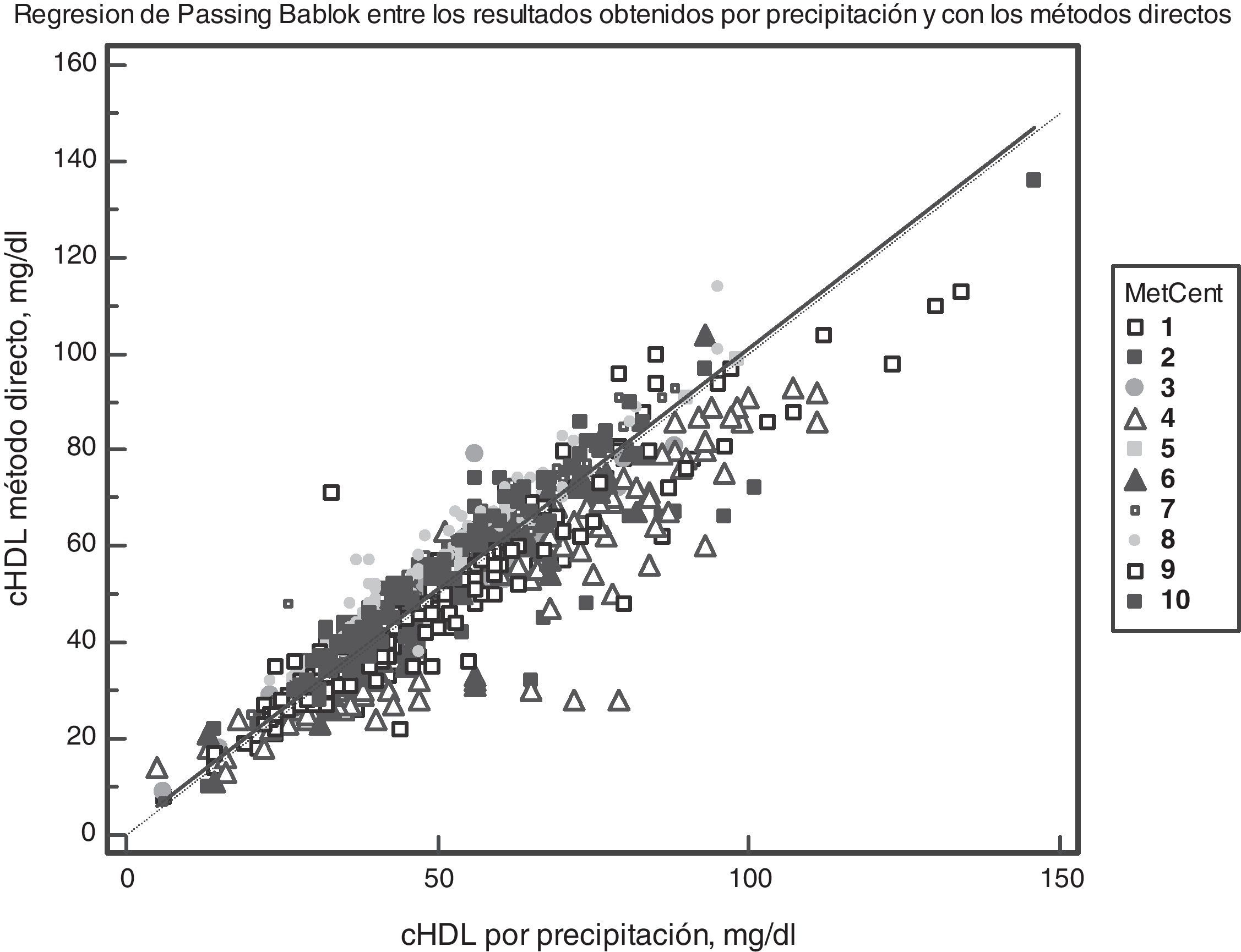
El análisis de regresión de Passing-Bablok se detalla en la figura 2. Los parámetros de intersección y pendiente para cada sistema (método-equipo) frente al procedimiento de comparación (precipitación) figuran en la tabla 4. Los sistemas Wako-Wako y DimensionRXL® (1)-Siemens presentan una intersección diferente de cero. Los sistemas de SynchronLX20®-Beckman, Modular P®-Roche (1 y 2) y DimensionRXL® (1 y 2) también presentan una pendiente significativamente diferente de 1.
Regresión de Passing Bablok entre el método de precipitación (x) y los métodos directos estudiados (y)
| Código | Equipo-reactivo | N | Intersección (IC del 95%) | Pendiente (IC del 95%) |
| 1 | ADVIA 2400®-Siemens | 99 | 1,27 (-2,00 a 4,37) | 0,944 (0,875 a 1,000) |
| 2 | Wako-Wako® | 98 | 4,00 (0,22 a 7,42) | 1,000 (0,917 a 1,074) |
| 3 | Synchron LX20®-Wako | 99 | 1,88 (0,00 a 3,47) | 0,941 (0,895 a 1,000) |
| 4 | Synchron LX20®-Beckman | 99 | -0,11 (-2,27 a 2,08) | 0,868 (0,821 a 0,909) |
| 5 | Cobas c711® (1)-Roche | 71 | 1,00 (-2,67 a 1,00) | 1,000 (1,000 a 1,067) |
| 6 | Cobas c711® (2)-Roche | 99 | -1,00 (-3,62 a 0,00) | 1,000 (0,974 a 1,053) |
| 7 | Modular P® (1)-Roche | 80 | 1,02 (-0,67 a 2,27) | 1,064 (1,029 a 1,111) |
| 8 | Modular P® (2)-Roche | 83 | 2,10 (-0,67 a 4,61) | 1,104 (1,045 a 1,167) |
| 9 | Dimension RXL® (1)-Siemens | 99 | 3,55 (0,80 a 5,97) | 0,889 (0,829 a 0,950) |
| 10 | Dimension RXL® (2)-Siemens | 100 | 1,03 (-1,29 a 2,95) | 1,071 (1,027 a 1,113) |
| Todos los métodos | 927 | 1 (1,00 a 1,00) | 1 (1,00 - 1,00) |
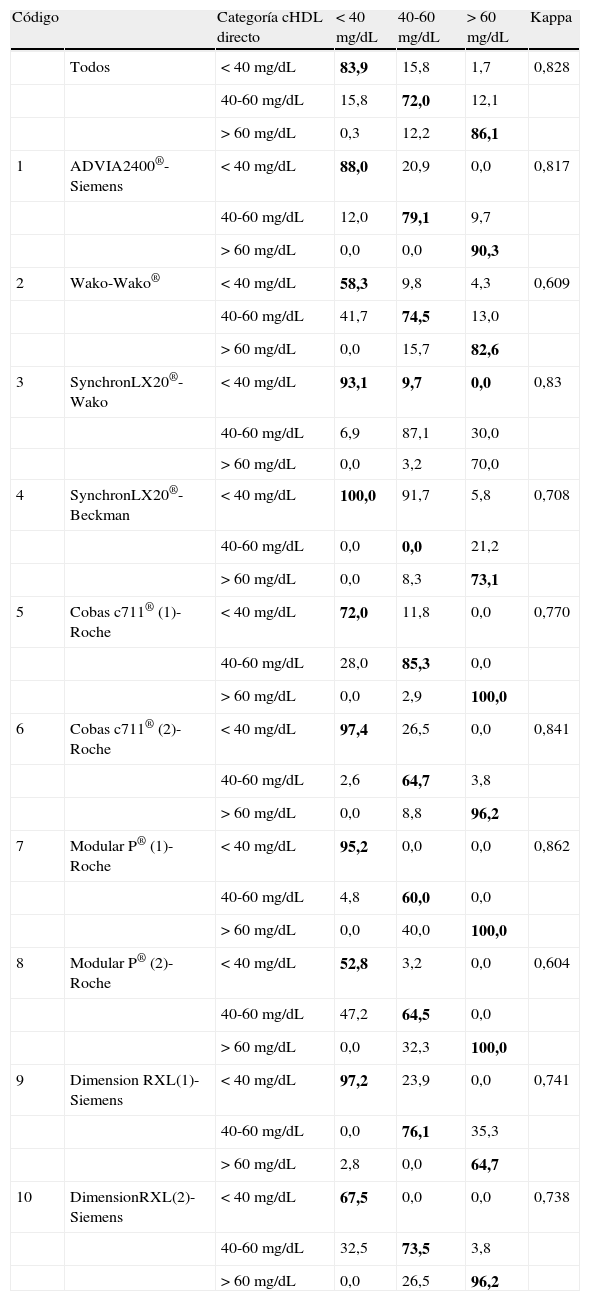
En la tabla 5 se muestran los resultados del análisis de concordancia. Pueden observarse unos índices kappa relativamente bajos, desde 0,604 para el sistema 8 a 0,841 para el 6. En general, las diferencias en la estratificación de los pacientes siguen la misma dirección que encontrábamos en el análisis de medias o en la regresión de Passing Bablok.
Índice de concordancia de los métodos directos con el método de precipitación
| Código | Categoría cHDL directo | <40mg/dL | 40-60mg/dL | >60mg/dL | Kappa | |
| Todos | < 40mg/dL | 83,9 | 15,8 | 1,7 | 0,828 | |
| 40-60mg/dL | 15,8 | 72,0 | 12,1 | |||
| > 60mg/dL | 0,3 | 12,2 | 86,1 | |||
| 1 | ADVIA2400®-Siemens | < 40mg/dL | 88,0 | 20,9 | 0,0 | 0,817 |
| 40-60mg/dL | 12,0 | 79,1 | 9,7 | |||
| > 60mg/dL | 0,0 | 0,0 | 90,3 | |||
| 2 | Wako-Wako® | < 40mg/dL | 58,3 | 9,8 | 4,3 | 0,609 |
| 40-60mg/dL | 41,7 | 74,5 | 13,0 | |||
| > 60mg/dL | 0,0 | 15,7 | 82,6 | |||
| 3 | SynchronLX20®-Wako | < 40mg/dL | 93,1 | 9,7 | 0,0 | 0,83 |
| 40-60mg/dL | 6,9 | 87,1 | 30,0 | |||
| > 60mg/dL | 0,0 | 3,2 | 70,0 | |||
| 4 | SynchronLX20®-Beckman | < 40mg/dL | 100,0 | 91,7 | 5,8 | 0,708 |
| 40-60mg/dL | 0,0 | 0,0 | 21,2 | |||
| > 60mg/dL | 0,0 | 8,3 | 73,1 | |||
| 5 | Cobas c711® (1)-Roche | < 40mg/dL | 72,0 | 11,8 | 0,0 | 0,770 |
| 40-60mg/dL | 28,0 | 85,3 | 0,0 | |||
| > 60mg/dL | 0,0 | 2,9 | 100,0 | |||
| 6 | Cobas c711® (2)-Roche | < 40mg/dL | 97,4 | 26,5 | 0,0 | 0,841 |
| 40-60mg/dL | 2,6 | 64,7 | 3,8 | |||
| > 60mg/dL | 0,0 | 8,8 | 96,2 | |||
| 7 | Modular P® (1)-Roche | < 40mg/dL | 95,2 | 0,0 | 0,0 | 0,862 |
| 40-60mg/dL | 4,8 | 60,0 | 0,0 | |||
| > 60mg/dL | 0,0 | 40,0 | 100,0 | |||
| 8 | Modular P® (2)-Roche | < 40mg/dL | 52,8 | 3,2 | 0,0 | 0,604 |
| 40-60mg/dL | 47,2 | 64,5 | 0,0 | |||
| > 60mg/dL | 0,0 | 32,3 | 100,0 | |||
| 9 | Dimension RXL(1)-Siemens | < 40mg/dL | 97,2 | 23,9 | 0,0 | 0,741 |
| 40-60mg/dL | 0,0 | 76,1 | 35,3 | |||
| > 60mg/dL | 2,8 | 0,0 | 64,7 | |||
| 10 | DimensionRXL(2)-Siemens | < 40mg/dL | 67,5 | 0,0 | 0,0 | 0,738 |
| 40-60mg/dL | 32,5 | 73,5 | 3,8 | |||
| > 60mg/dL | 0,0 | 26,5 | 96,2 |
En negrita la proporción de pacientes que se clasifican igual con el método de cHDL directo y el de cHDL por precipitación.
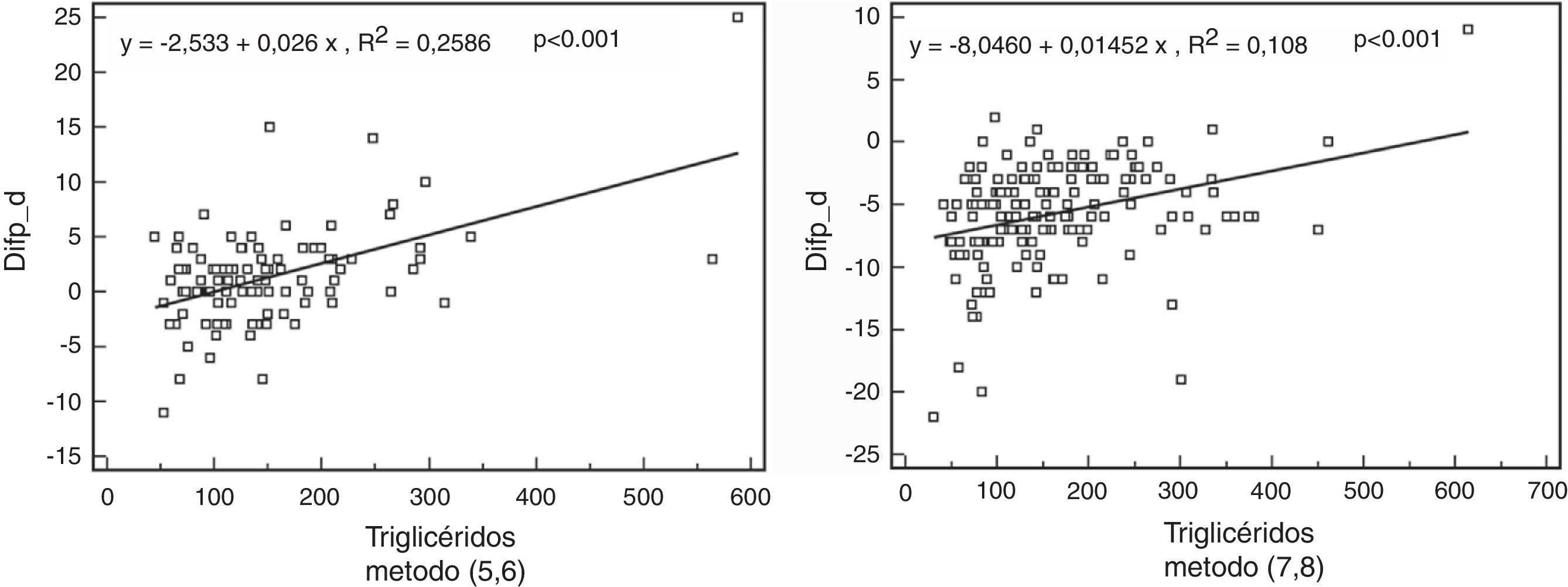
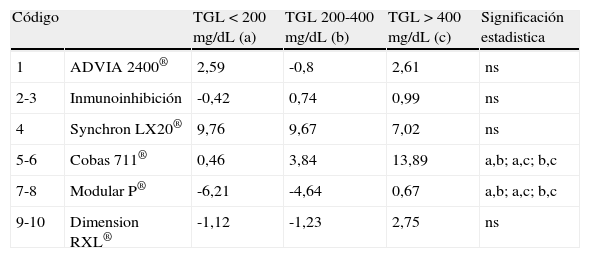
En ninguna de las muestras utilizadas para este estudio (en ningún caso la magnitud de la concentración de triglicéridos superó los 1.500mg/dl) pudo observarse un fallo de la precipitación con ácido fosfotúngstico-MgCl2 Por lo demás, en la tabla 6 podemos observar los resultados obtenidos. Los sistemas (5,6) y (7,8), que además son el mismo método pero adaptado a equipos diferentes, muestran una acusada sensibilidad a la concentración de triglicéridos; este mismo efecto puede observarse en las curvas de regresión lineal entre la diferencia cHDL precipitación-cHDL directo y la magnitud de la concentración de triglicérido (fig. 3). El resto de métodos muestran ligeras variaciones que no llegan a ser significativas para cada estrato de concentración de triglicéridos.
Diferencias medias entre los métodos directos y el método de precipitación en función de la concentración de triglicéridos
| Código | TGL<200mg/dL (a) | TGL 200-400mg/dL (b) | TGL>400mg/dL (c) | Significación estadistica | |
| 1 | ADVIA 2400® | 2,59 | -0,8 | 2,61 | ns |
| 2-3 | Inmunoinhibición | -0,42 | 0,74 | 0,99 | ns |
| 4 | Synchron LX20® | 9,76 | 9,67 | 7,02 | ns |
| 5-6 | Cobas 711® | 0,46 | 3,84 | 13,89 | a,b; a,c; b,c |
| 7-8 | Modular P® | -6,21 | -4,64 | 0,67 | a,b; a,c; b,c |
| 9-10 | Dimension RXL® | -1,12 | -1,23 | 2,75 | ns |
En esta tabla, los métodos son agrupados por plataformas (ver códigos en la tabla 5). Los datos hacen referencia a la diferencia media entre método de precipitación y método directo. La última columna (significación) indica si las diferencias medias son estadisticamente significativas (análisis post hoc de Bonferroni) entre los diferentes estratos de concentración de triglicéridos (cada uno de ellos identificados como a, b, o c).
ns: no significativo.
En esta tabla se presenta la correlación entre la magnitud de la concentración de triglicéridos y la diferencia de magnitudes del cHDL obtenido por métodos directos y el método de precipitación. Solo se representan las correspondientes a los sistemas (método-centro) 5 y 6 (mismo método, diferente centro) y los 7 y 8 (mismo método, diferente centro), ya que en el caso del resto de sistemas estudiados no existe relación significativa entre la concentración de triglicéridos y las diferencias obtenidas para cHDL.
Desde su aparición, las evaluaciones de los métodos directos de cHDL14 han descrito buenas imprecisiones (2-3%), que al ser comparadas con la relativamente elevada imprecisión de los métodos de precipitación (semiautomáticos), han hecho que la inmensa mayoría de los laboratorios clínicos adoptaran estos métodos también conocidos como homogéneos. En cuanto a la inexactitud, estos métodos comerciales están certificados frente al método de referencia, certificación que incluye el sistema completo, es decir instrumento, reactivo y materiales de calibración. No obstante, con el paso del tiempo los fabricantes han cambiado las formulaciones de los reactivos originales con el objetivo de ser más robustos en presencia de lipoproteínas anormales y otras moléculas como las inmunoglobulinas que causaron interferencias en los reactivos primitivos, incluyendo las interferencias por concentraciones de triglicéridos, que son variables entre los métodos, pero por encima de 1.200mg/dL ninguno es fiable por inefectividad de la separación química. Por otra parte, estos nuevos reactivos no han sido evaluados de forma exhaustiva en las condiciones de práctica habitual22 y además, una reciente evaluación llega a la conclusión, que aunque estos métodos cumplen con los objetivos de error total del NCEP en individuos sanos, fallan en lograr estos objetivos en pacientes con enfermedad cardiovascular y/o dislipemia23, por ello debemos ser cautos con las conclusiones encontradas en la literatura. Estas certificaciones del CDC24 son específicas para una determinada versión, instrumento y calibrador, no pudiendo ser aplicadas de forma universal para las diferentes versiones, instrumentos y lotes de calibradores.
Así, en el programa de garantía externa de la Calidad de la SEQC encontramos todavía unos datos que hacen pensar que estos objetivos no se están cumpliendo. En los años 2008 y 2009 (SEQC) las imprecisiones de todos los métodos fueron muy altas (>6%) y las desviaciones entre métodos muy elevadas15,16. Con estos datos no puede asegurarse que los métodos sean trazables.
El objetivo de esta evaluación de métodos directos de cHDL ha sido documentar la precisión y estudiar la exactitud frente al método de comparación mediante el análisis de resultados en sueros humanos congelados para evitar posibles influencias matriz en sueros liofilizados como los empleados en los programas del control de calidad externo, cuyos resultados nos orientan a que existe una gran dispersión de resultados, pero sin conocer cuál es el correcto.
Según nuestros resultados los métodos evaluados en los instrumentos utilizados (tabla 1) cumplen los requisitos de imprecisión total recomendados por el NCEP, si bien el reactivo de Siemens en el ADVIA2400® muestra un CV% total de 5,92% ligeramente superior a las especificaciones recomendadas. El método de Roche en el analizador Cobas c711® utilizado en dos laboratorios diferentes ofrece la imprecisión mas baja, mientras que ese mismo método en el analizador Modular P® presenta una mayor imprecisión, lo que indica una contribución importante del instrumento en la calidad de los resultados. La mayor imprecisión corresponde al método de precipitación como era de esperar, debido a los múltiples pasos del procedimiento. Sin embargo, el error sistemático de este método frente al método de referencia valorado a través de muestras del CDC con valores convencionalmente verdaderos es de 2,02% (-1,08 a 4,46%). Por tanto cumple los requisitos del NCEP de un ET <13% y podemos considerarlo adecuado como de comparación para el posterior análisis de los métodos directos.
Al enfrentar los resultados de los métodos directos frente al método de comparación observamos una gran diferencia entre métodos con desviaciones porcentuales entre -16,5 y 14,9% en los sistemas SynchronLX20®-Beckman y Modular P®-Roche. Todo lo anterior nos indica que las diferencias obtenidas son debidas a una mezcla no homogénea de diferencias sistemáticas y proporcionales, que no dependen solo del método sino también del laboratorio que lo utiliza.
En cuanto a la clasificación de pacientes, los sistemas de Wako y el Modular P®-Roche son los que muestran índices kappa más bajos, y por lo tanto peor concordancia en la clasificación de pacientes en los puntos de corte de 40 y 60mg/dL. En el caso del método inmunológico, esto contrasta con el hecho de que es uno de los métodos con medias más próximas al método de comparación; no obstante, esta aparente discordancia, podría ser debida a la variabilidad de los resultados obtenidos con el método inmunológico, variabilidad que lo es en ambas direcciones, y no sistemática hacia arriba o hacia abajo (como ocurre con otros sistemas), haciendo que la media de las diferencias con el método de comparación se aproxime a cero, pero que haya saltos significativos entre los estratos de clasificación de los pacientes. En general, las diferencias en la estratificación de los pacientes siguen la misma dirección que encontrábamos en el análisis de medias o en la regresión de Passing Bablok: el sistema SynchronLX20®-Beckman infraestima el cHDL y clasifica hacia abajo a los pacientes, mientras que los sistemas Modular P®-Roche sobreestiman el cHDL y clasifican hacia arriba a los pacientes. No obstante, es frecuente una amplia dispersión de resultados, que se observa, sobre todo en el grupo que con el método de precipitación queda clasificado entre 40-60mg/dL, de manera que los índices kappa obtenidos son relativamente bajos. Este hecho es importante, sobre todo si tenemos en cuenta que las concentraciones bajas de cHDL son un factor de riesgo independiente de las concentraciones de cLDL. Dentro de este contexto, cabría incluir la muy baja concordancia entre el sistema SynchronLX20®-Beckman y el método de comparación para magnitudes de la concentracion de cHDL en el rango de 40-60mg/dL; esta baja concordancia podría ser debida a un efecto aleatorio en el que la mayoría de las muestras seleccionadas dentro de este rango quedasen en la franja 40-50mg/dL, lo cual añadido a la infraestimación del cHDL por este sistema explicaría la elevada discordancia, que no se da en el resto de estratos de cHDL. Uno de los factores descritos que pueden influir en las diferencias de resultados entre los métodos directos es su diferente reactividad frente a la fracción HDL rica en apoE. La evaluación correcta de este factor y su estandarización es una necesidad clínica ya que no existe ninguna prueba rutinaria capaz de discriminar este tipo de partículas.
Otra posible causa de las diferencias entre métodos es la posible no commutabilidad de los materiales de referencia utilizados por los fabricantes. Una solución sería que los programas de intercomparación externos utilicen materiales commutables y con valores asignados por el método de referencia.
Por último, quedaría por explicar la sensibilidad de los métodos de Roche (ambas plataformas estudiadas y en la misma dirección) a la concentración de triglicéridos.Para ello, hay que tener en cuenta que el método de precipitación (en el formato utilizado en el estudio), y de acuerdo con datos previos17, no falló en ninguna de las muestras utilizadas y que las interferencias detectadas fueron específicas de las plataformas indicadas. Este es un efecto de una intensidad relativamente pequeña, pero que es significativa y contínua entre los diferentes estratos de concentración de triglicéridos. Si bien no existe ningún dato concreto en qué basarse, el hecho de que la composición de la HDL probablemente cambie al aumentar la concentración de triglicéridos, podría ser una de las razones de este hecho.
ConclusionesLos métodos homogéneos más utilizados en nuestro medio muestran imprecisiones que solo en un caso superan el 4%, considerado como uno de los requisitos de calidad necesarios para esta determinación. Hemos constatado que el método de precipitación utilizado como método de comparación, tiene una imprecisión alta (6,52%) y un sesgo frente al valor verdadero de 2,02% (-1,08 a 4,46%), con un ET que entra dentro de las especificaciones de calidad aceptables (NCEP). Los errores mas importantes que hemos detectado en nuestro medio han sido: los procedimientos de Modular P-reactivo® Roche producen sesgos positivos muy altos (en relación al método de comparación) de +9,86 y +14,9%, y en el método de Polianión/polímero de Beckman en el analizador Beckman LX20® que produce un sesgo negativo de (-16,5%).
Todos estos resultados nos hacen pensar que siguen existiendo importantes discrepancias técnicas en los métodos homogéneos utilizados actualmente en la cuantificación del cHDL, probablemente generadas por una elevada inexactitud en algunos de ellos, y que necesitamos mejorar la calidad analítica para cumplir los requerimientos clínicos. Estos métodos han solucionado el problema de la imprecisión pero no la exactitud. Probablemente sería necesario un programa similar al del CDC para que los laboratorios puedan verificar la exactitud de los métodos mediante la comparación con el método de referencia con materiales de origen humanos congelados para evitar el efecto matriz.
Por otra parte, es conveniente que los laboratorios conozcan las caracteristicas de imprecisión y sesgo del metodo directo que utilizan con respecto al de referencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.