La interpretación de las magnitudes bioquímicas durante la gestación requiere de intervalos de referencia específicos para dicha etapa, dados los cambios fisiológicos que se producen durante el embarazo. El objetivo de este estudio fue obtener el intervalo de referencia de la concentración sérica de ácido úrico, biomarcador asociado a un incremento del riesgo de desarrollo de preeclampsia en gestantes residentes en el Área 2 de Salud de la Región de Murcia (España).
Material y métodosEstudio prospectivo, longitudinal y consecutivo en el que la población de referencia estuvo finalmente formada por 270 gestantes sanas en las que se midió la uricemia durante los tres trimestres de gestación. Las recomendaciones del Clinical and Laboratory Standards Institute se utilizaron para la obtención de los intervalos de referencia.
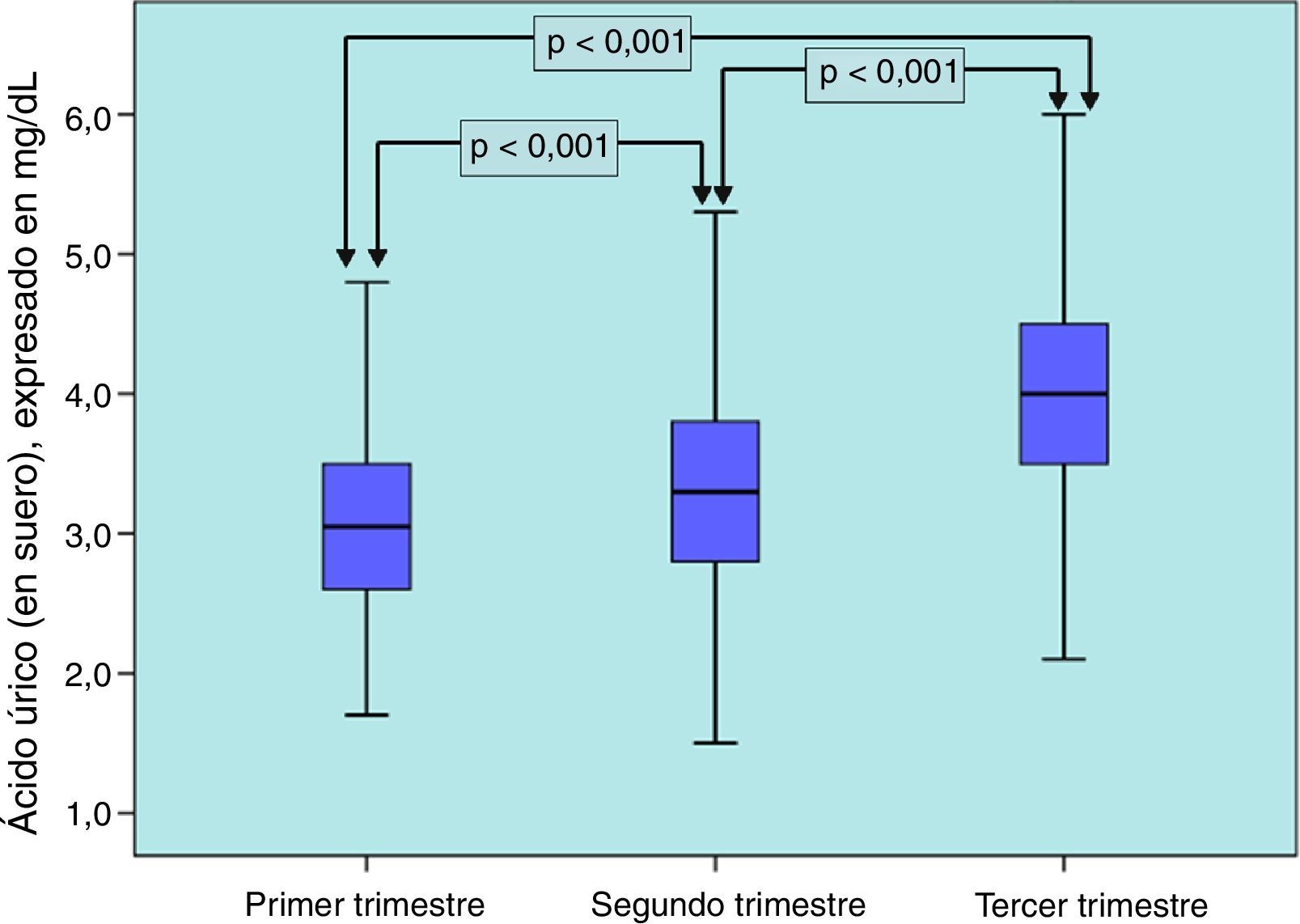
ResultadosLa uricemia aumentó de forma significativa durante la gestación, alcanzando una concentración marcadamente superior durante el tercer trimestre. Se definieron los siguientes intervalos de referencia: primer trimestre: 2,0-4,6mg/dl, segundo trimestre: 2,0-4,7mg/dl y tercer trimestre: 2,6-5,7mg/dl.
ConclusiónLa interpretación de la uricemia durante la gestación requiere de intervalos de referencia específicos para este estado fisiológico, estratificados por trimestres. Los intervalos obtenidos en nuestro estudio son una herramienta útil en la interpretación de la uricemia durante la gestación para la identificación de aquellas gestantes con un riesgo incrementado de preeclampsia.
Interpretation of biochemical variables during pregnancy requires reference intervals specific to that state, due to the physiological changes that occur during pregnancy. The objective of this study was to obtain the reference range of serum uric acid, biomarker associated with an increase in the risk of developing preeclampsia, in pregnant women of the Area 2 of the Region of Murcia (Spain).
Material and methodsThis is a consecutive longitudinal prospective study in which the reference population finally included 270 healthy pregnant women, in which serum uric acid was measured during the three trimesters of pregnancy. Recommendations of the Clinical and Laboratory Standards Institute were used to obtain reference intervals.
ResultsSerum uric acid levels increased significantly during pregnancy, reaching a concentration notably higher during the third trimester. The following reference intervals were defined: first trimester: 2,0-4,6mg/dl, second trimester: 2,0-4,7mg/dl and third trimester: 2,6-5,7mg/dl.
ConclusionInterpretation of serum uric acid levels during pregnancy requires reference intervals specific to this physiological state, stratified by trimesters. The ranges obtained in our study are a useful tool to identificate those pregnant women with an increased risk of preeclampsia.
La generación de valores de referencia para las magnitudes bioquímicas es una de las tareas esenciales del laboratorio clínico1, a fin de garantizar una interpretación correcta de aquellas por parte del clínico. La medida de determinadas magnitudes bioquímicas durante el embarazo es necesaria para el diagnóstico o exclusión de ciertas condiciones patológicas, con repercusión tanto sobre la madre como sobre el feto.
La disponibilidad de intervalos de referencia obtenidos en embarazos no complicados es un requisito esencial para la toma de decisiones en patologías como la preeclampsia, alteraciones de la coagulación, cuadros infecciosos, etc. Aunque algunos estudios y revisiones proporcionan estos intervalos para ciertas magnitudes bioquímicas que experimentan cambios durante la gestación2,3, la utilización de los mismos presenta limitaciones por las diferentes metodologías utilizadas y la población analizada.
La hiperuricemia es un hallazgo común en las gestantes con preeclampsia4, que a menudo precede a la hipertension arterial y la proteinuria., manifestaciones habitualmente utilizadas en el diagnóstico de este trastorno5. Incluso algunos autores propugnan la implicación del ácido úrico como factor que contribuye a la patogénesis de la preeclampsia, dada su capacidad para inducir inflamación, estrés oxidativo y disfunción endotelial, que condicionarían tanto el desarrollo como la función de la placenta4,6–8. Por ello, su concentración medida en las primeras etapas de la gestación puede asociarse a mayor riesgo de desarrollar preeclampsia9–11, aunque hay autores que cuestionan este valor12. La hiperuricemia adquiere un papel relevante como marcador útil en el diagnóstico diferencial con la hipertensión gestacional, equivalente al clásico de la proteinuria13,14, así como marcador de riesgo fetal o de pronóstico de eventos adversos materno-fetales15,16, aunque para otros su valor predictor es controvertido17–19. Por lo tanto, la interpretación de la concentración sérica de ácido úrico de la disponibilidad de valores de referencia obtenidos requiere la metodología utilizada para su medida y en una muestra representativa de la población atendida.
Algunos autores abogan por la introducción en las guías clínicas de la cuantificación de ácido úrico en distintas etapas de la gestación6. Así, en España, su determinación en el segundo trimestre de gestación como un signo de alerta de preeclampsia en mujeres normotensas está incluida en la Guía de práctica clínica de atención en el embarazo y puerperio recientemente editada por el Ministerio de Sanidad, Servicios Sociales e Igualdad20. Sin embargo, la citada guía establece esta recomendación sin referirse a valores de referencia o niveles séricos de alerta. En la literatura reciente existe una llamativa ausencia de valores de referencia específicos durante la gestación, en especial en un metabolito como el ácido úrico, tan dependiente de la función renal.
El objetivo de este estudio ha sido establecer valores de referencia de ácido úrico estratificados en los tres trimestres en mujeres gestantes con embarazos no complicados, como herramienta para el control de la gestación en nuestra área de salud.
Material y métodosDiseño del estudioEstudio prospectivo, longitudinal y consecutivo, realizado en el Servicio de Análisis Clínicos del Hospital Universitario Santa Lucía, que presta su actividad asistencial para el Área 2 de Salud de la Región de Murcia. Se incluyeron las gestantes a las que, como parte del seguimiento del embarazo, y de acuerdo con el Programa Integral de Atención a la Mujer de la Región de Murcia (14), se les solicitó el estudio analítico recogido en dicho protocolo, que incluye la medida de ácido úrico durante los trimestres primero (10-13 semanas), segundo (24-26 semanas) y tercero (33-36 semanas). Los criterios de exclusión fueron: pérdida al seguimiento, embarazo gemelar, patología sistémica previa a la gestación, patología obstétrica (diabetes gestacional, estados hipertensivos del embarazo) y crecimiento intrauterino retardado y prematuridad (parto en edad gestacional inferior a la semana 37). El período de inclusión de gestantes fue el comprendido entre diciembre de 2013 y mayo de 2014, completándose el seguimiento hasta octubre de 2014.
Dado que la medida de ácido úrico forma parte del proceso asistencial a la gestante en nuestra Área de Salud no se solicitó consentimiento informado.
Métodos de laboratorioA todas las gestantes se les extrajo mediante venopunción una muestra de sangre en un tubo sin anticoagulante con gel separador. A su llegada al laboratorio, las muestras fueron centrifugadas a 3.500rpm durante 5 min, siendo el suero procesado seguidamente para la cuantificación, entre otras magnitudes bioquímicas, de ácido úrico. Las mediciones fueron realizadas mediante el método de la uricasa/peroxidasa en un analizador Advia 2400 (Siemens Healthcare Diagnostic, Los Ángeles, CA, EE. UU.), con un límite de detección de 0,5mg/dl y un rango de medida entre 0,5 y 20,0mg/dl. Para el control interno de calidad se utilizó el material de control Liquid Assayed Multiqual (Bio-Rad), con un coeficiente de variación analítico que osciló entre 3,48 y 4,87% durante el período de estudio. Además, la determinación de ácido úrico estuvo incluida en el Programa de Garantía de Calidad de los Laboratorios Clínicos organizado por la Sociedad Española de Bioquímica Clínica y Patología Molecular, siendo el error total durante los meses del estudio inferior a las especificaciones de calidad establecidas por el propio laboratorio (17%)21, certificado de acuerdo a la Norma ISO 9001: 2008.
Análisis estadísticoSe aplicó el test de Kolmogorov para comprobar la normalidad de las variables continuas. Se analizó la presencia de valores atípicos para su exclusión mediante el test de Tukey, previo a la obtención de los valores de referencia, y se compararon las concentraciones de ácido úrico en los tres trimestres mediante el análisis de varianzas para medidas repetidas (ANOVA de una vía), con la corrección de Bonferroni para comparaciones múltiples. Para la obtención de los intervalos de referencia se aplicó el método no paramétrico basado en percentiles descrito en el documento CLSI C28-A3c22. El análisis estadístico fue realizado con los programas MedCalc 14.8.1 y SPSS versión 20.0. Se consideró como significativo un valor de p<0,05.
ResultadosDurante el período del estudio se incluyeron 374 gestantes que se encontraban en el primer trimestre de gestación. Después de completar el seguimiento y, tras la aplicación de los criterios de exclusión, previa revisión de la historia clínica por dos especialistas en Ginecología y Obstetricia, la muestra de referencia estuvo formada por 270 gestantes, con una edad mediana de 31 años (amplitud intercuartil: 7; rango: 17-42 años).
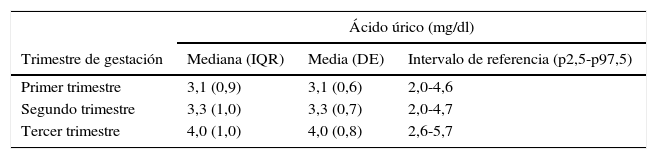
Se observó un incremento significativo (p<0,001) de la concentración de ácido úrico durante el trascurso de la gestación, que fue ligero en el segundo trimestre y marcado en el tercero (fig. 1), respecto a los valores del primer trimestre. En la tabla 1 se muestran los intervalos de referencia estratificados por trimestres, junto con las medidas de centralización y dispersión. Dichos intervalos fueron inferiores a los habitualmente utilizados en nuestro laboratorio para población adulta no gestante.
Intervalos de referencia de ácido úrico en suero durante la gestación
| Ácido úrico (mg/dl) | |||
|---|---|---|---|
| Trimestre de gestación | Mediana (IQR) | Media (DE) | Intervalo de referencia (p2,5-p97,5) |
| Primer trimestre | 3,1 (0,9) | 3,1 (0,6) | 2,0-4,6 |
| Segundo trimestre | 3,3 (1,0) | 3,3 (0,7) | 2,0-4,7 |
| Tercer trimestre | 4,0 (1,0) | 4,0 (0,8) | 2,6-5,7 |
Para la conversion de unidades (mg/dl) a unidades del sistema internacional (SI) (μmol/l), multiplicar por el factor de conversión (59,48).
DE: desviación estándar; IQR: amplitud intercuartil; p2,5: percentil 2,5; p97,5: percentil 97,5.
La interpretación clínica de una magnitud biológica requiere del conocimiento de las concentraciones de la misma en una muestra representativa de la población sana a la que pertenece el individuo. Dados los cambios fisiológicos que se producen durante la gestación, la disponibilidad de valores de referencia obtenidos en esta población es esencial para la toma de decisiones.
En nuestro estudio hemos obtenido los valores de referencia del ácido úrico en suero de gestantes con embarazos no complicados. A pesar de la abundante investigación sobre la asociación de ácido úrico sérico y preeclampsia, es llamativa la escasa literatura reciente estableciendo intervalos de referencia de ácido úrico en suero en gestantes sanas. Estudios con un diseño longitudinal que pueden ser ya considerados como históricos23,24, incluso utilizando métodos de medida ya no habituales en la actualidad, muestran resultados similares a los hallados en nuestro estudio respecto a los cambios que se producen en las concentraciones de ácido úrico durante la gestación no complicada, con un incremento progresivo de las mismas hasta alcanzar valores similares a los de la población no gestante al final del tercer trimestre.
Ya en la última década, se describen valores de referencia para el ácido úrico en suero, obtenidos de forma experimental, en los estudios de Larsson et al.2, con un diseño longitudinal incluyendo 52 gestaciones normales, y de Berruguilla et al.25, con un diseño transversal, utilizando ambos la misma metodología para la medida de ácido úrico y con una población con similares características a la seleccionada en nuestro estudio. En ambos estudios el hallazgo más significativo es similar al del nuestro, observándose un incremento significativo de la concentración sérica de ácido úrico durante la gestación, especialmente durante el tercer trimestre, lo que obliga a contar con intervalos estratificados en función de la edad gestacional. Los intervalos de referencia finalmente establecidos fueron muy similares (tabla 2). Nuestro trabajo tiene como principales ventajas su diseño longitudinal, durante los tres trimestres, y además aporta un importante número de gestantes, superior al referido en los estudios previos con embarazos normales2.
Comparación de los intervalos de referencia para ácido úrico en suero con estudios previos
| Ácido úrico (mg/dl) | |||
|---|---|---|---|
| Estudio | Primer trimestre | Segundo trimestre | Tercer trimestre |
| [2] | 2,0-4,2 | 2,4-4,9 | 3,1-6,3 |
| [25] | 1,5-4,5 | 2,1-4,7 | 2,5-5,3 |
| [a] | 2,0-4,6 | 2,0-4,7 | 2,6-5,7 |
Para la conversion de unidades (mg/dl) a unidades del sistema internacional (SI) (μmol/l), multiplicar por el factor de conversión (59,48).
[a] Intervalos de referencia obtenidos en nuestro estudio.
El aumento de la concentración de ácido úrico en distintas etapas de la gestación se asocia a un incremento del riesgo de desarrollar posteriormente preeclampsia. Así, elevaciones por encima de 3,56mg/dl en el primer trimestre, concentración inferior a la descrita en nuestro estudio como límite superior del intervalo de referencia (4,6mg/dl), se han descrito como un factor de riesgo para el desarrollo posterior de preeclampsia10. De forma similar, Wolak et al.11 demostraron que elevaciones de ácido úrico antes de la semana 20 de gestación por encima de 5,5mg/dl estaban asociadas a un aumento de la incidencia de preeclampsia. En el segundo trimestre, concentraciones superiores a 4,09mg/dl, también inferior a la descrita como límite superior del intervalo de referencia en nuestra población (4,7mg/dl), se asociaron a un aumento del riesgo de preeclampsia26. Sin embargo, la comparación de los resultados obtenidos en nuestro estudio con los puntos de corte descritos en los anteriormente citados está limitada por la diferente metodología utilizada, ya que aquellos se basaron en el cálculo del riesgo relativo. Recientemente, el estudio de Álvarez-Fernández et al27, concluyó que una concentración sérica de ácido úrico de 5,7mg/dl, igual al límite superior del intervalo de referencia definido en nuestro estudio para el tercer trimestre, permitía identificar con una elevada especificidad, entre mujeres que acudieron a un Servicio de Urgencia Obstétrica por hipertensión gestacional, aquellas con mayor riesgo de presentar preeclampsia o de desarrollarla a corto plazo.
En conclusión, nuestro estudio confirma la necesidad de estratificar los valores de referencia de ácido úrico según la edad gestacional, según trimestres. Los intervalos de referencia obtenidos contribuyen a una interpretación correcta de la concentración de ácido úrico durante la gestación en la población gestante atendida en nuestra área. De esta manera podemos establecer estrategias con el grupo de gestantes cuyos valores superan el percentil 97,5, y que pueden ser consideradas más vulnerables, siendo de especial utilidad en los estados hipertensivos del embarazo, y en la prevención, seguimiento o pronóstico de la preeclampsia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.