Ante la necesidad de estandarizar los procedimientos de recogida, transporte, manejo y análisis de muestras de orina de 24 h, se han elaborado guías internacionales con una serie de recomendaciones que deberían ser adaptadas a cada laboratorio según sus circunstancias.
ObjetivoConocer el grado de cumplimiento de estas recomendaciones en laboratorios españoles.
Material y métodos. Se realizó una encuesta a través de la página web de la Sociedad Española de Bioquímica Clínica y Patología Molecular sobre los diferentes procesos preanalíticos en el manejo de la orina de 24 h.
ResultadosSe obtuvieron respuestas de 50 laboratorios, dos de los cuales no eran españoles. Aunque mayoritariamente los laboratorios proporcionan información acerca de la recogida de la muestra, existe variabilidad en la forma de hacerlo. Estas diferencias se observan en aspectos como el acceso de los pacientes a los contenedores de recogida de orina con y sin conservante, la forma de entregar la muestra, el registro de la información asociada y los criterios de rechazo de una muestra no recogida de forma correcta.
ConclusionesExiste variabilidad en el cumplimiento de las recomendaciones internacionales. Un posible sesgo de esta encuesta es que los participantes en ella sean los que más motivados estén por este tema, y por tanto más fieles al cumplimiento de estas normas, por lo que la variabilidad detectada podría ser aún mayor. Finalmente, se revisan las principales recomendaciones para la estandarización de todo el proceso, con el fin de obtener una muestra de calidad que asegure unos buenos resultados.
Given the need to standardise procedures for the collection, transportation, handling, and analysis of 24-hour urine specimens, international guidelines have been developed with a series of recommendations that should be adapted to each laboratory depending on its circumstances.
ObjectiveTo determine the level of compliance to these recommendations in Spanish laboratories.
Material and methodsA survey was carried out, through the website of the Spanish Society of Clinical Biochemistry and Molecular Pathology, on the different pre-analytical procedures in the management of 24hour urine specimens.
ResultsA total of 50 laboratories responded, two of which were not Spanish. Although most laboratories provide information about the collection of the specimen, there is variability in how this is done. Differences were observed in areas such as, patient access to containers for collecting urine without preservative, how to deliver the specimen, recording the associated information, and rejection criteria of a specimen not collected correctly.
ConclusionsThere is variability in compliance with international recommendations. A possible bias of the survey is that the participants were those who are more motivated by this issue, and therefore more faithful compliance with these standards, thus the variability detected could be even higher. Finally, the main recommendations for the standardisation of the entire procedure is reviewed in order to obtain a specimen quality to ensure good results.
Una orina a tiempo controlado es aquella orina que se recoge durante un tiempo determinado en relación con otra actividad como puede ser la duración del día, la duración de la noche, la ingestión de algún nutriente o una intervención terapéutica. La muestra de orina de 24 h es la más común, recogiéndose todas las micciones que se producen en un periodo de 24 h.
Debido al carácter intermitente de la excreción de determinados solutos en orina, para algunos metabolitos solo se consideran aceptables las orinas recogidas durante un periodo no inferior a 24 h con el objeto de obtener un espécimen homogéneo y representativo de lo excretado a lo largo de un día.
El análisis bioquímico de la orina a tiempo controlado debería ser llevado a cabo siempre sobre la base de una necesidad médica concreta. La solicitud de un análisis de orina debería incluir una descripción adecuada del tipo de muestra e informar al laboratorio de la necesidad clínica, con el fin de facilitar la correcta selección de los procedimientos de análisis e interpretación de los resultados1.
La obtención de la orina, a diferencia de otros tipos de muestra, depende fundamentalmente de la colaboración del paciente. Por este motivo, resulta fundamental instruirle respecto de las condiciones óptimas de recogida, y transmitirle la responsabilidad de la obtención de una orina de calidad que repercutirá en los resultados que de ella se deriven. La instrucción del paciente, por tanto, será clave para permitir la obtención de una muestra adecuada, requiriéndose además procedimientos estandarizados para producir intervalos de referencia consistentes, y límites de decisión para la interpretación armonizada de los resultados.
Debido a los avances tecnológicos los errores más frecuentes no se producen en el análisis de la muestra sino en su recolección, transporte y procesamiento preanalítico en el laboratorio1. Entre estos errores nos podemos encontrar con especímenes mal recogidos por exceso o por defecto, recipientes no adecuados y/o contaminados, muestras mal conservadas, no homogeneizadas, condiciones de recolección inadecuadas, etc.
El número de parámetros que pueden cuantificarse en orina es elevado y cada uno de ellos puede necesitar unas condiciones especiales de recogida, almacenamiento y conservación. El laboratorio es el máximo responsable de la calidad de las muestras, por lo que deberá jugar un papel principal en la gestión de todas las etapas de la fase preanalítica, incluyendo la cita del paciente, los contenedores y conservantes a utilizar, la información al paciente para la recogida de la orina, etc.
Ante la necesidad de estandarizar los procedimientos de recogida, transporte, manejo y análisis de las muestras de orina se elaboraron guías internacionales como la European Urinalysis Guidelines (2000) bajo el auspicio de la European Confederation of Laboratory Medicine1 o la GP16-a3 Urinalysis; Approved Guideline-Third Edition (2009) del Clinical and Laboratory Standards Institute2. Estas guías tienen el reconocimiento internacional y deben ser adaptadas a cada laboratorio según sus circunstancias. A nivel nacional, la Asociación Castellano-Manchega de Análisis Clínicos elaboró en el año 2005 un documento sobre preanalítica de muestras de orina en este mismo sentido3.
Al revisar la bibliografía no hemos encontrado datos sobre la implementación de estas normas en los laboratorios españoles, de modo que nos pareció interesante realizar un sondeo con diferentes cuestiones sobre la preanalítica de la orina de 24 h. La Comisión de Función Renal y Urianálisis de la Sociedad Española de Bioquímica Clínica y Patología Molecular (SEQC) elaboró y difundió una encuesta para conocer el grado de adopción de estas normas en los laboratorios españoles y, a la vista de los resultados, sacar conclusiones y proponer medidas de mejora.
Material y métodosEn el año 2015, la Comisión de Función Renal y Urianálisis realizó una encuesta dirigida a laboratorios clínicos a través de la página web de la SEQC, para conocer el estado actual de los procesos preanalíticos relacionados con la recogida de la orina a tiempo controlado. El cuestionario (fig. 1) recogía datos sobre el hospital y la comunidad autónoma a la que pertenecía el laboratorio y contenía nueve preguntas específicas sobre el tema en cuestión. Aunque hubieran sido interesantes otras cuestiones relacionadas con la petición o con el transporte de muestras, no se incluyeron para simplificarla al máximo y así facilitar la participación del mayor número de laboratorios.
La metodología empleada para la difusión y realización de la encuesta fue a través de un enlace de acceso al cuestionario, situado en la página principal de la web de la SEQC. Este enlace dirigía a un documento creado con la aplicación de formularios de Google. Además, para darle mayor difusión, la SEQC, que envía de forma periódica a sus socios información sobre las novedades de su página, incluyó el acceso a esta encuesta durante los meses en los que estuvo activa (abril-septiembre de 2015).
El análisis estadístico de los datos obtenidos se realizó mediante el programa SPSS versión 21. Para expresar los porcentajes se realizó un redondeo al alza.
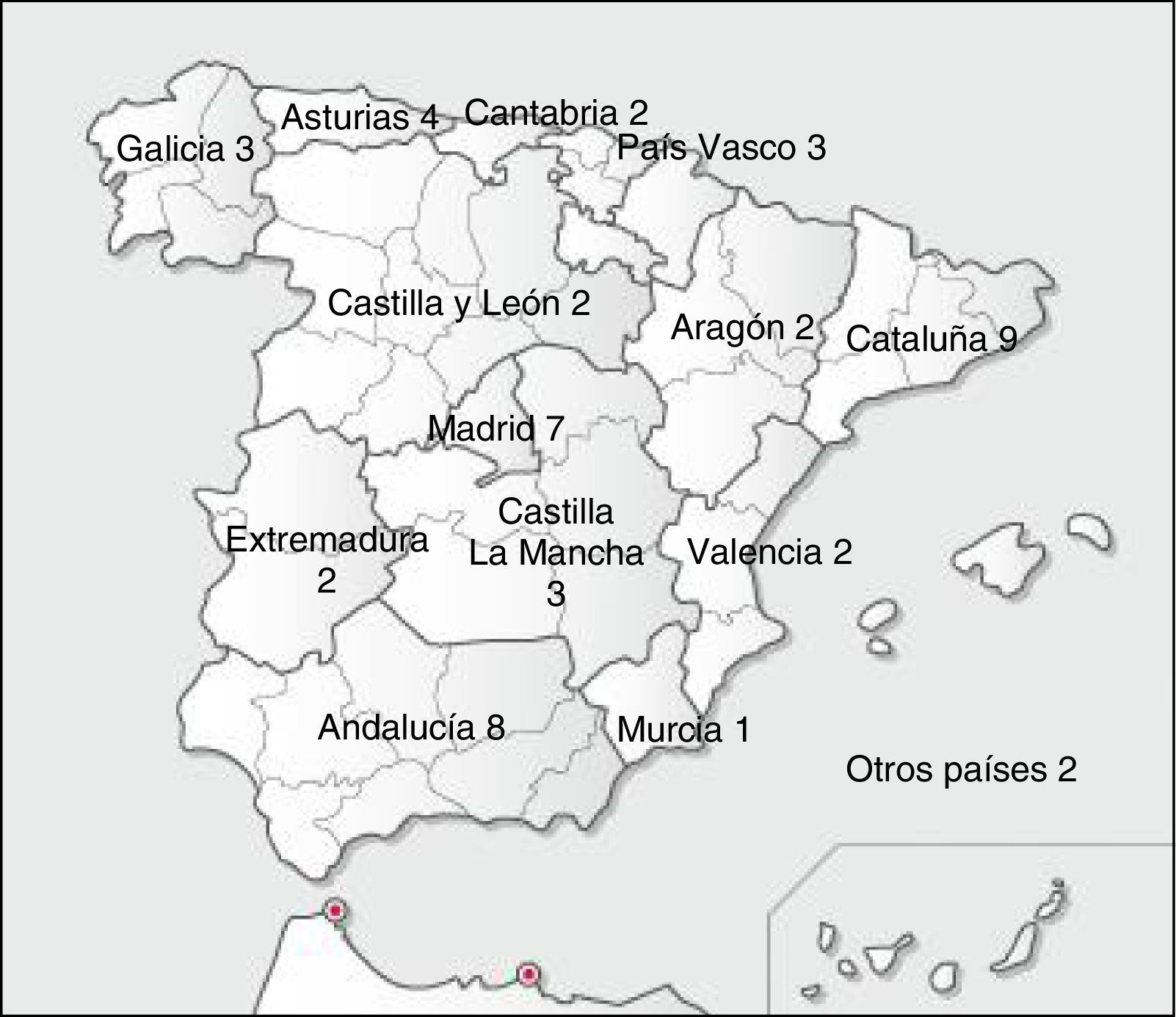
ResultadosCaracterísticas de los laboratoriosSe obtuvieron 50 respuestas al cuestionario de las que 48 pertenecían a laboratorios españoles, que fueron las que se consideraron para el tratamiento estadístico de la encuesta. Los resultados por comunidades se muestran en la figura 2. Respecto de la titularidad de los laboratorios, 46 eran públicos y 4 privados.
Instrucciones sobre recogida de la orinaEl 10% (n=5) de los laboratorios participantes no facilita a los pacientes instrucciones sobre recogida de la orina de 24 h. De los 43 (90%) laboratorios que sí la facilitan, solo 12 (28%) aportan información visual o gráfica además de la escrita en sus hojas de instrucciones, lo que representa el 25% de los laboratorios españoles participantes.
Registro de horas y conservación en neveraEl 83% (n=40) de los laboratorios no registra la hora de inicio y finalización de la recolección de la muestra, pero el 90% (n=43) sí recomienda que la orina sea mantenida en la nevera durante el período de recolección.
Contenedor de recogida de la orinaEl 17% (n=8) de los laboratorios no proporcionan al paciente el contenedor de recogida de la orina y el 35% (n=17) no proporciona el contenedor con el conservante apropiado cuando es necesario.
Entrega de la muestraEn el 75% (n=36) de los laboratorios se recibe el contenedor con la totalidad de la orina, y en el 25% (n=12) restante el paciente anota la diuresis y entrega alícuotas al laboratorio.
Registro del laboratorioEl 33% (n=16) de los laboratorios no certifica de ninguna manera la correcta recogida de la orina. De los 32 restantes (67%) que sí realizan alguna acción para evaluar la recolección de la muestra, la mayoría (50%, n=16) utilizan como criterio de rechazo la pérdida de micciones (tabla 1).
Criterios de rechazo utilizados por los participantes de la encuesta que utilizan algún criterio de rechazo. (N=32)
| Criterios de rechazo utilizados | Porcentaje (%) | Número de hospitales |
|---|---|---|
| Comentar con el paciente posibles incidencias en la recogida de muestra | 3,1 | 1 |
| Por contenedor inadecuado | 3,1 | 1 |
| En función de la eliminación diaria de creatinina (cálculo a partir de mg o mmol/kg/día) | 15,6 | 5 |
| En función del volumen (ej:< 400 o >3.000ml/día) | 6,3 | 2 |
| Incumplimiento del tiempo de recogida | 9,4 | 3 |
| La muestra se acepta pero con comentario de micción insuficiente | 3,1 | 1 |
| Pérdida de micciones | 50,0 | 16 |
| Combinación de criterios anteriores, en función de cada caso | 9,4 | 3 |
En primer lugar, es difícil conocer la representatividad de la encuesta ya que no existe un Catálogo Nacional de Laboratorios Clínicos. Si tomamos como base el Catálogo Nacional de Hospitales 2015 actualizado a 31 de diciembre de 20144 y consideramos los hospitales con más de 100 camas, tendríamos en España 460 hospitales. Si excluimos a los centros psiquiátricos, geriátricos y de larga estancia, ya que no suelen disponer de laboratorio propio, tendríamos una población teórica de 330 laboratorios clínicos hospitalarios, por lo que los 48 laboratorios que respondieron a la encuesta corresponderían a un 15%. Por tanto, aunque no podamos tomar en consideración los valores numéricos absolutos, este trabajo puede darnos una idea del estado actual de la preanalítica de la orina de 24 h en nuestro país.
Analizando los resultados obtenidos en la encuesta, parece que mayoritariamente (90%) los laboratorios proporcionan instrucciones para la recogida de la orina. Sin embargo, hay un pequeño porcentaje (10%) que no lo hacen. Esto puede llevar a estos laboratorios a recibir un mayor número de orinas de baja calidad. Por sí solo, el dar instrucciones de recogida de la orina no es garantía de éxito, pero si no se dan, la variabilidad en la recogida de la muestra será aún mayor. Estos laboratorios deberían hacer un esfuerzo por implicarse en las labores preanalíticas del procesamiento de la orina.
Lo que sí llama la atención es que, de esos 43 laboratorios que sí proporcionan información, el 75% no facilitan información gráfica o visual en las instrucciones de recogida como se recomienda en las guías. Esto puede llevar a que no se sigan las instrucciones de forma correcta, bien porque no se entiendan, por dificultades idiomáticas, por parecer demasiado extensa la lectura o por cualquier otra razón.
Es recomendable que cuando se entreguen los recipientes vayan acompañados siempre de instrucciones de recogida del espécimen de forma escrita. Las hojas de instrucciones deberán ser claras, con gráficos o dibujos que faciliten la comprensión, y dependiendo de la población atendida, en varios idiomas. Estas hojas pueden estar diseñadas por el laboratorio o utilizar como referencia alguna de las que aparecen en las guías1,3.
La persona encargada de entregarlas será además responsable de explicar de forma oral la forma correcta de recoger la orina asegurándose de su comprensión. Es necesario también que el paciente sea consciente de la importancia que tiene el seguir las instrucciones correctamente para obtener resultados representativos.
La mayoría de los laboratorios (83%) suministran a los pacientes el recipiente para la recogida de la orina. Sin embargo hay un 17% que no lo hacen, por lo que los recipientes no serán uniformes y puede que no reúnan las condiciones requeridas para cada tipo de recolección de orina.
En el caso de necesitar un recipiente con conservante, todavía es mayor el número de laboratorios que no hacen entrega de este tipo de contenedor con el aditivo correspondiente (35%).
Los recipientes y conservantes deberían ser suministrados de manera gratuita por el laboratorio o en quien se delegue, como en los puntos de extracción y/o citación, pero siempre por personal entrenado que conozca y tenga en cuenta las exigencias concretas que pueden requerir algunas determinaciones en orina. De esta manera el laboratorio podrá verificar que los contenedores reúnen las condiciones de esterilidad, capacidad y opacidad que requieren para las determinaciones solicitadas. Se puede aprovechar el momento de la entrega del recipiente para transmitir la información adecuada para la correcta recogida de la orina.
Se recomienda que los contenedores incorporen dispositivos de transferencia de la orina a tubos de recogida por sistema de vacío, ya que reúnen numerosas ventajas como la prevención de la contaminación biológica, derrame de la muestra, comodidad, optimización de procesos, etc. Es recomendable que la capacidad del contenedor sea al menos de 3 litros para que la mayoría de los pacientes tengan que utilizar un solo envase.
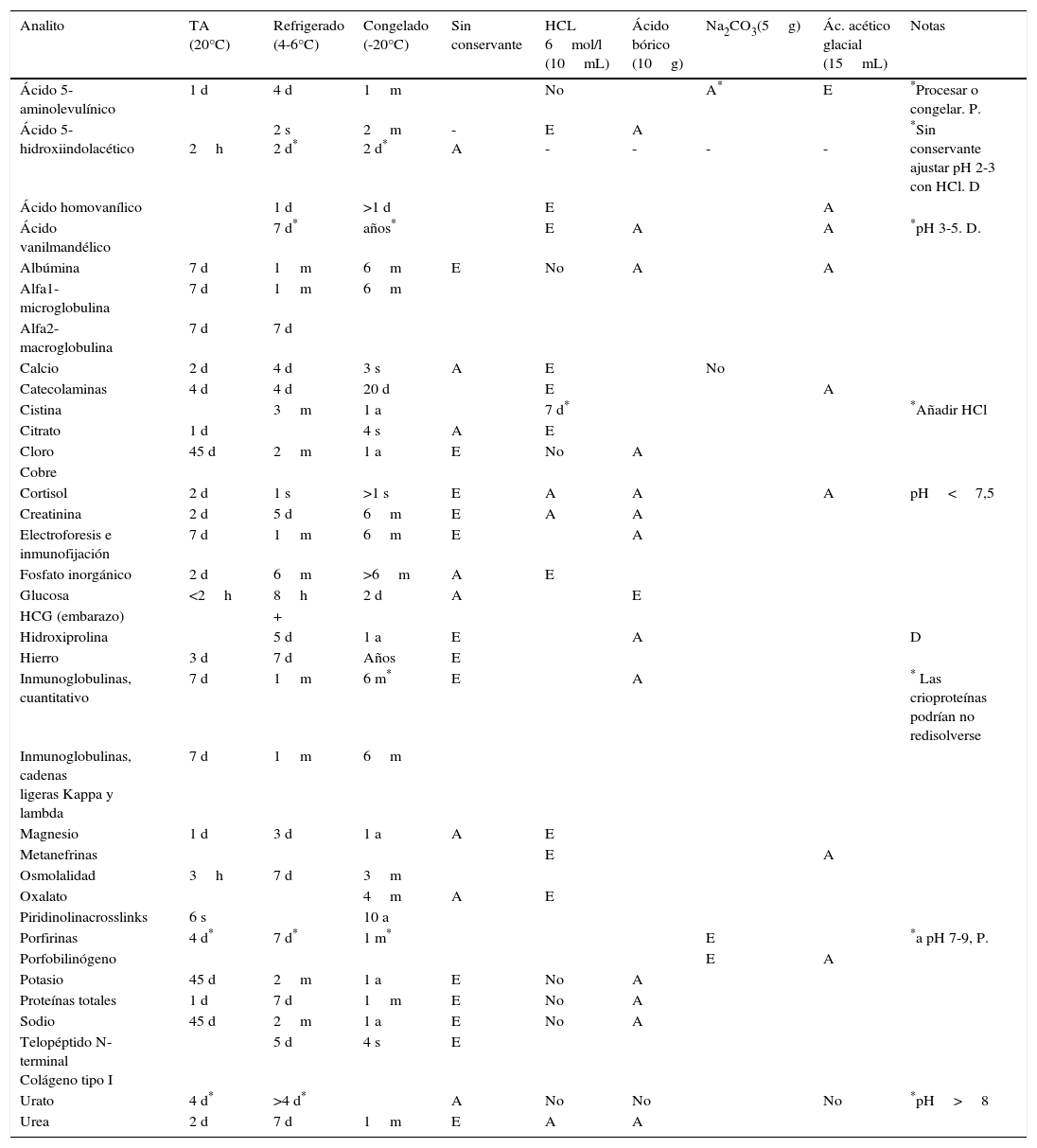
Los diferentes conservantes utilizados en la recogida y conservación de la orina así como los tiempos de estabilidad de los diferentes analitos se han resumido en la tabla 21,3,5–10. Si el médico solicita la cuantificación de componentes que requieren condiciones de recogida incompatibles debido a la necesidad de añadir diferentes conservantes, será necesario establecer diferentes días de cita aunque pueda resultar un poco incómodo para el paciente, recogiendo cada vez el espécimen que sea óptimo para cada prueba o grupo de pruebas.
Tiempos de conservación y utilización de conservantes de los analitos más habituales para orinas a tiempo controlado (expresado como el tiempo máximo de estabilidad que se encuentra documentado). Se asume la ausencia de infección bacteriana
| Analito | TA (20°C) | Refrigerado (4-6°C) | Congelado (-20°C) | Sin conservante | HCL 6mol/l (10mL) | Ácido bórico (10g) | Na2CO3(5g) | Ác. acético glacial (15mL) | Notas |
|---|---|---|---|---|---|---|---|---|---|
| Ácido 5-aminolevulínico | 1 d | 4 d | 1m | No | A* | E | *Procesar o congelar. P. | ||
| Ácido 5-hidroxiindolacético | 2h | 2 s 2 d* | 2m 2 d* | - A | E - | A - | - | - | *Sin conservante ajustar pH 2-3 con HCl. D |
| Ácido homovanílico | 1 d | >1 d | E | A | |||||
| Ácido vanilmandélico | 7 d* | años* | E | A | A | *pH 3-5. D. | |||
| Albúmina | 7 d | 1m | 6m | E | No | A | A | ||
| Alfa1-microglobulina | 7 d | 1m | 6m | ||||||
| Alfa2-macroglobulina | 7 d | 7 d | |||||||
| Calcio | 2 d | 4 d | 3 s | A | E | No | |||
| Catecolaminas | 4 d | 4 d | 20 d | E | A | ||||
| Cistina | 3m | 1 a | 7 d* | *Añadir HCl | |||||
| Citrato | 1 d | 4 s | A | E | |||||
| Cloro | 45 d | 2m | 1 a | E | No | A | |||
| Cobre | |||||||||
| Cortisol | 2 d | 1 s | >1 s | E | A | A | A | pH<7,5 | |
| Creatinina | 2 d | 5 d | 6m | E | A | A | |||
| Electroforesis e inmunofijación | 7 d | 1m | 6m | E | A | ||||
| Fosfato inorgánico | 2 d | 6m | >6m | A | E | ||||
| Glucosa | <2h | 8h | 2 d | A | E | ||||
| HCG (embarazo) | + | ||||||||
| Hidroxiprolina | 5 d | 1 a | E | A | D | ||||
| Hierro | 3 d | 7 d | Años | E | |||||
| Inmunoglobulinas, cuantitativo | 7 d | 1m | 6 m* | E | A | * Las crioproteínas podrían no redisolverse | |||
| Inmunoglobulinas, cadenas ligeras Kappa y lambda | 7 d | 1m | 6m | ||||||
| Magnesio | 1 d | 3 d | 1 a | A | E | ||||
| Metanefrinas | E | A | |||||||
| Osmolalidad | 3h | 7 d | 3m | ||||||
| Oxalato | 4m | A | E | ||||||
| Piridinolinacrosslinks | 6 s | 10 a | |||||||
| Porfirinas | 4 d* | 7 d* | 1 m* | E | *a pH 7-9, P. | ||||
| Porfobilinógeno | E | A | |||||||
| Potasio | 45 d | 2m | 1 a | E | No | A | |||
| Proteínas totales | 1 d | 7 d | 1m | E | No | A | |||
| Sodio | 45 d | 2m | 1 a | E | No | A | |||
| Telopéptido N-terminal Colágeno tipo I | 5 d | 4 s | E | ||||||
| Urato | 4 d* | >4 d* | A | No | No | No | *pH>8 | ||
| Urea | 2 d | 7 d | 1m | E | A | A |
Explicado en Notas en cada línea. A: aceptado; a: año; D: interferencia por dieta o fármacos; d: día; E: elección prioritaria; h: hora; HCl: ácido clorhídrico; m: mes; P: protegido de la luz; s: semana; TA: temperatura ambiente. Fuente: citas1,3,5–10.
Respecto a registrar la hora de inicio y finalización de la recogida de la orina, solo un 17% de los laboratorios lo hacen. Podría darse la circunstancia de que el laboratorio verifique si el paciente ha seguido el procedimiento estándar y solo en el caso de que no sea así dejarlo registrado. Hay protocolos que recomiendan que la recogida sea de 8 a 8 de la mañana del día siguiente por comodidad para el paciente, pero también son válidas las orinas que se recogen en otros horarios siempre que el periodo de recolección sea el convenido, generalmente 24 h.
Proponemos dos procedimientos de recogida de orina de 24 h según las recomendaciones de las diferentes guías:
- •
Procedimiento tradicional: habitualmente se recomienda que la recogida del espécimen de orina de 24 h se inicie al levantarse por la mañana del día anterior a la cita en el laboratorio. Esa primera orina se descartará en el váter y a partir de ese momento, durante las 24 h siguientes, el paciente deberá ir recogiendo en el contenedor toda la orina emitida, incluyendo la de la primera micción de la mañana del día de la cita en el laboratorio. Este procedimiento hace incompatible la entrega, en el mismo día de la cita, de orina de 24 h junto con la primera orina de la mañana.
- •
Procedimiento alternativo: este sistema permite la entrega de ambos especímenes (24 h y primera orina de la mañana) en la misma cita, y de este modo evita al paciente la molestia de tener que desplazarse dos días distintos al centro de extracción para entregar las dos orinas. Consiste en iniciar la recogida de la orina de 24 h en cualquier momento dos días antes de la fecha de la cita, por ejemplo al acostarse. Justo antes de irse a la cama, el paciente orinará directamente en el váter y anotará la hora exacta en el recipiente. A partir de ese momento iniciará la recogida completa de la orina durante 24 h. Al día siguiente antes de acostarse, exactamente a la misma hora en que se inició la recogida el día anterior, el paciente orinará por última vez incluyendo esta porción sobre el contenedor de 24 h. A la mañana siguiente, es decir, el día de la cita en el laboratorio, al levantarse de la cama recogería la orina de una micción, siguiendo el procedimiento habitual de porción media de la primera orina de la mañana tras lavado de genitales externos. Podría ser propuesto como único procedimiento de recogida de orina de 24 h para simplificar y facilitar la transmisión de la información, haya que recoger o no primera orina de la mañana.
Mientras el paciente recoge la muestra a lo largo del día es recomendable que la orina sea mantenida en la nevera para evitar su deterioro. Esta recomendación la hacen la mayoría de los laboratorios (90%), pero no conocemos el grado de cumplimiento ya que los pacientes son reticentes a poner su orina en el lugar donde hay comida. Esta es una de las cuestiones que debe de ser preguntada cuando el paciente entrega la orina ya que podría ser una causa de rechazo.
El paciente debe entregar en el laboratorio la totalidad de la orina recogida, y que sea el laboratorio el que mida la diuresis y haga las alícuotas correspondientes. Sin embargo, en un 25% de los casos son los pacientes los que miden el volumen, hacen las alícuotas y las entregan al laboratorio con los errores y riesgos que puede conllevar el que una persona no experimentada manipule, fraccione y homogeneice o no una orina.
En un tercio de los laboratorios participantes la orina es entregada sin que se tome ninguna medida para verificar que ha sido recogida correctamente. En los dos tercios restantes la pérdida de micciones (50%) es el criterio más ampliamente utilizado. Cabe destacar también que un importante número de laboratorios (16%) utiliza la excreción de creatinina por kg/día, y solo un 9% más de un criterio de rechazo.
Los requerimientos básicos para admitir una muestra incluyen entre otros que el tipo de espécimen sea el pertinente para el análisis solicitado, que esté correctamente identificado, y que las condiciones de recogida, transporte, preparación y conservación de la muestra sean las adecuadas.
Hay circunstancias que deberían utilizarse por norma como criterio de rechazo, debiendo solicitarse una nueva muestra:
- •
Incumplimiento del tiempo de recogida.
- •
Pérdida de micciones.
- •
Contenedor inadecuado.
- •
No conservación en nevera de la orina.
- •
Incidencias importantes en la recogida de la muestra.
Hay otra serie de causas potenciales de rechazo de muestra que el laboratorio tiene que valorar de manera individualizada:
- •
Eliminación diaria de creatinina.
- •
Volumen de diuresis <400 o >3.000mL/día.
- •
Medición de pH fuera de los límites.
El laboratorio debe comprobar, una vez recibida la muestra, si esta cumple con los requisitos mínimos imprescindibles para ser procesada. Si no fuera así se solicitará una nueva muestra, explicando y registrando el motivo del rechazo y la medida que se ha tomado.
Por otra parte, uno de los sesgos de este trabajo es que la encuesta era de libre acceso, no enviándose en particular a nadie para motivar su contestación, por lo que probablemente lo habrán hecho los que estén más implicados o preocupados por el tema. Aunque se ha obtenido un número importante de respuestas hubiéramos deseado que la participación fuese mayor dado que algunas comunidades autónomas no han tenido representación.
Si es cierta la hipótesis de que los laboratorios que han contestado son los más interesados por este tema, puede que sean también los que más adherencia tengan a la adopción de las normas publicadas por las guías, y la realidad se decantaría más hacia el no seguimiento de las recomendaciones existentes.
También hubiera sido interesante incluir en la encuesta preguntas relacionadas con la petición (tipo de volante), con la citación o con el transporte de muestras. No se incorporaron para simplificarla al máximo y así facilitar que contestaran el mayor número de participantes. Estas cuestiones podrían ser objeto de un futuro cuestionario, que además serviría para evaluar la efectividad de estas recomendaciones.
A continuación mencionamos algunas recomendaciones sobre los puntos no recogidos en la encuesta:
- •
Volantes.
Atendiendo a las sugerencias de las guías internacionales, los volantes de petición de pruebas deberían ser diseñados de forma que el médico sea consciente de la complejidad preanalítica de las determinaciones que está solicitando, haciéndole corresponsable de la petición y de los condicionantes que conlleva. Los programas de petición electrónica, cada vez más extendidos, son una herramienta muy útil con la que hacer partícipe al médico de estas exigencias, así como de la importancia de recoger el espécimen correctamente, en el recipiente idóneo y con el conservante adecuado. Para ello, el sistema de petición electrónica debería contemplar la introducción de filtros establecidos por el laboratorio y basados en los requerimientos preanalíticos para cada prueba.
En caso de no disponer de petición electrónica una alternativa sería la utilización de protocolos consensuados con los diferentes servicios para diseñar perfiles por patologías con características preanalíticas compatibles.
Una vez que el médico ha hecho la petición, será competencia del laboratorio el establecer las pautas a seguir por los servicios que citan los estudios analíticos. El personal encargado de citar deberá conocer y tener en cuenta los requerimientos preanalíticos exigidos por determinados analitos en cuanto a las condiciones de recogida, conservación y transporte, y si fuera necesario, desdoblar los volantes de petición en tantas citas como sean imprescindibles para asegurar la calidad e idoneidad del espécimen.
Otro aspecto a tener en cuenta es que la gestión de la agenda de citas del laboratorio se realice sobre la base de criterios de eficacia y distribución homogénea de la carga de trabajo.
En el caso de solicitudes complejas de análisis de orina deberán resolverse por personal especialmente formado en su manejo, consultando al facultativo de laboratorio responsable en caso de duda.
- •
Transporte.
Cuando las orinas se recojan en centros periféricos deberán trasladarse al laboratorio en las condiciones adecuadas de seguridad, tiempo y temperatura. El Agreementon Dangerous Goods by Road o acuerdo de transporte de mercancías peligrosas por carretera, siguiendo las recomendaciones de la OMS, clasifica a las orinas como sustancias infecciosas de categoría B dentro del grupo 3373 y que deberán cumplir con la instrucción de embalaje P65011.
En la actualidad no se indica ningún límite en cuanto a la capacidad de los recipientes primarios para transportar materias líquidas. No obstante, a efectos prácticos para evitar los riesgos asociados al transporte y manipulación de grandes y pesados recipientes llenos de orina, en el caso de especímenes de tiempo controlado se recomienda que se envíen desde los centros periféricos alícuotas correctamente homogeneizadas e identificadas, anotando en el lugar correspondiente el volumen total de la diuresis y el tiempo de recogida.
Se recomienda que el transporte sea lo más rápido posible y en sistemas refrigerados o neveras con control de temperatura.
ConclusionesLa variabilidad detectada en el procesamiento preanalítico de la orina de 24 h hace necesaria una estandarización del proceso y requiere de un esfuerzo en el cumplimiento de unas recomendaciones básicas:
- -
En la petición y citación de una analítica de orina deberán tenerse en cuenta los requerimientos de recogida, así como las incompatibilidades de diferentes analitos en un único recipiente.
- -
El laboratorio deberá entregar instrucciones escritas con información gráfica para la correcta recogida de la orina, así como proporcionar los envases de recogida adecuados.
- -
El laboratorio deberá asegurarse de que el paciente ha entendido esa información y de que este es consciente de la importancia de seguir las instrucciones.
- -
Las muestras de orina deberán ser entregadas en su totalidad al laboratorio y que este sea el encargado de su manipulación.
- -
En la recepción de las orinas el laboratorio deberá verificar que han sido recogidas correctamente, y tener descritos criterios de rechazo de las muestras.
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos al resto de los componentes de la Comisión de Función Renal su colaboración y sugerencias para la elaboración de la encuesta: Esther Barba Serrano, María José Diez de los Ríos Carrasco, Silvia Gracia García, Juan Ángel Jiménez García, Juan Miguel de Lamo Muñoz, Carlos Macías Blanco, Rosario Montañés Bermúdez, Esther Solé Llop y Salvador Ventura Pedret.