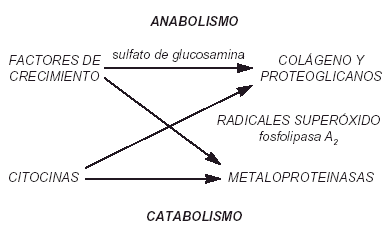
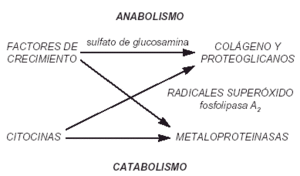
La artrosis es la afección musculoesquelética más prevalente entre la población. La artrosis primaria es más frecuente que la secundaria y en ella no se reconoce ninguna alteración que predisponga a su desarrollo. Se estima que entre el 25 y el 30% de los individuos de edades comprendidas entre 45 y 64 años, y más del 85% de los mayores de 65 años, presentan signos radiológicos de artrosis1,2. La artrosis es consecuencia del catabolismo progresivo de los componentes de la matriz del cartílago articular, debido a un desequilibrio entre la síntesis y la degradación de los mismos (Fig. 1). La degradación de la matriz se lleva a cabo, en parte, por enzimas llamadas metaloproteinasas secretadas por los condrocitos. Las citoquinas, producidas también por los condrocitos y fibroblastos sinoviales, aumentan en la artrosis3,4.
Figura 1. Mecanismo etiopatogénico de la artrosis3,4.
El descenso relativo de los proteoglicanos altera la afinidad de la matriz extracelular por el agua y, en este sentido, la capacidad de ésta para que fluya en la cavidad articular. Estos cambios estructurales repercuten en la viscoelasticidad, y tienen un impacto negativo en las propiedades biomecánicas del cartílago articular y del líquido sinovial, haciendo al cartílago vulnerable a la compresión, tensión y cizallamiento que ocurren durante el movimiento4.
Aunque los cambios iniciales se producen en el cartílago hialino, se van a afectar de forma secundaria las estructuras próximas: membrana sinovial, cápsula articular y hueso subcondral. Clínicamente, la artrosis se manifiesta por dolor, rigidez y limitación de la movilidad. Existen muchas opciones terapeúticas para el manejo de la artrosis, como son medidas físicas (pérdida de peso), tratamiento farmacológico (analgésicos, antiinflamatorios), inyección intraarticular de esteroides, tratamiento rehabilitador, desbridamiento artroscópico, osteotomías y sustitución protésica de la articulación. La viscosuplementación es un tratamiento alternativo para pacientes con artrosis sintomática. En este artículo de revisión, analizaremos los conceptos más actuales del papel que juega el ácido hialurónico intrarticular en el tratamiento de la artrosis de rodilla5.
PROPIEDADES DEL ÁCIDO HIALURÓNICO
El ácido hialurónico es una cadena de polisacáridos, constituida por unidades repetidas de disacáridos de N-acetilglucosamina y ácido glucurónico. Los sinoviocitos tipo B lo sintetizan y secretan a la cavidad articular6. La Tabla 1 resume las principales propiedades del ácido hialurónico7-13. La mayor parte del ácido hialurónico que se encuentra en la articulación consta de 12.500 unidades de disacáridos que proporcionan a la molécula un peso de aproximadamente 5 x 106 daltons (d). Una rodilla sana contiene 2 ml de líquido sinovial, con una concentración de ácido hialurónico de 2,5 a 4,0 mg/ml. En la artrosis dicha concentración se reduce de la mitad a un tercio del valor normal. El tamaño de la molécula también disminuye, así como la interacción entre las moléculas de ácido hialurónico. Esto se traduce en una pérdida de las propiedades reológicas, una menor densidad dinámica, una alteración de las propiedades elásticas y una disminución del efecto de filtro y barrera del líquido sinovial, que afecta a la nutrición del cartílago. La pérdida de la lubrificación produce un aumento de las fuerzas de tensión y ocasiona una disrupción en la malla de tejido colágeno, esencial para la integridad de la superficie articular. La inyección intra-articular de ácido hialurónico debería, teóricamente, contribuir a restaurar las propiedades reológicas del líquido sinovial (viscosidad, elasticidad y concentración de ácido hialurónico), y a proteger del deterioro a la articulación artrósica.
El ácido hialurónico regula diferentes actividades celulares a través de receptores específicos e interacciones con otras moléculas de la matriz extracelular14. Se ha identificado un receptor específico de membrana para el ácido hialurónico, perteneciente a la familia de glicoproteínas de adhesión CD44. Permite que las células se unan al ácido hialurónico, que se anclen los agregados de proteoglicanos a la membrana plasmática del condrocito, y juega además un importante papel en el metabolismo del ácido hialurónioco15. El ácido hialurónico puede ser degradado por un grupo de enzimas denominadas hialuronidasas. Las células del sistema retículo endotelial contienen receptores que se unen a las moléculas de ácido hialurónico, y son, por tanto, determinantes para el catabolismo del ácido hialurónico en sangre16.
Propiedades físicas
El ácido hialurónico posee propiedades viscosas y elásticas, y el que predomine una u otra depende de las fuerzas de cizallamiento aplicadas. Si éstas son elevadas, se produce un aumento de la elasticidad y una disminución de la viscosidad; si son bajas, sucede lo contrario. El ácido hialurónico proporciona al líquido sinovial «propiedades pseudoplásticas», absorbiendo el impacto durante los movimientos rápidos y actuando como lubricante durante los movimientos lentos7.
La evaluación directa de la cinética del ácido hialurónico dentro de la sinovial es difícil. Se han desarrollado ensayos con modelos animales para medir la vida media del ácido hialurónico inyectado tanto en articulaciones sanas como artríticas. En ovejas, la vida media intrasinovial fue de 20,8 horas, en comparación con 11,5 horas en articulaciones inflamadas8.
Efecto antiinflamatorio
El ácido hialurónico tiene, in vivo e in vitro, efectos sobre la función de los leucocitos. Éstos incluyen la inhibición de la fagocitosis, adherencia y la estimulación de la mitosis9,10. Hay que destacar que dichas propiedades dependen del tamaño molecular del ácido hialurónico12. En cambio, las moléculas tanto de alto como de bajo peso molecular no alteran otras funciones leucocitarias como la formación de radicales libres de oxígeno. La administración intraarticular de ácido hialurónico reduce los niveles de mediadores de la inflamación en el líquido sinovial de pacientes con artritis. In vitro existen evidencias de que el ácido hialurónico afecta a la liberación de ácido araquidónico de los fibroblastos sinoviales. Esta propiedad depende de la dosis y del peso molecular. El ácido araquidónico extracelular es captado por los lecucocitos de la sinovial y es convertido en mediadores de la inflamación, como por ejemplo prostaglandinas y leucotrienos17.
Efecto anabólico
La inyección intraarticular de ácido hialurónico puede afectar a la síntesis de ácido hialurónico estimulando a los fibroblastos sinoviales. En la articulación artrósica se produce ácido hialurónico en una menor proporción que en articulaciones sanas. En el estudio de Smith y Ghosh, se evalúa el efecto de varios preparados comerciales de ácido hialurónico en las articulaciones de pacientes con artrosis18. Tanto la concentración como el peso molecular de los mismos son importantes a la hora de estimular «de novo» la producción de ácido hialurónico. Un peso molecular superior a 5 x 105 d es más efectivo. Este hallazgo es compartido por otros autores, aunque hay que tener en cuenta que una concentración extracelular excesiva de ácido hialurónico puede tener efectos inhibitorios sobre los fibroblastos sinoviales.
Efecto analgésico
El efecto antiinflamatorio del ácido hialurónico dentro de la sinovial puede explicar, en parte, algunas de sus propiedades analgésicas. Ghosh ha demostrado un efecto analgésico directo en modelos animales11. En dicho estudio, el ácido hialurónico ha sido equiparable a la indometacina en cuanto a la reducción del dolor ocasionado por la administración intraarticular de bradiquininas. El autor concluye que el ácido hialurónico intraarticular modula el dolor mediante dos mecanismos: uno directo, a través de la inhibición de los nocicptores, y otro indirecto, a través de la sustancia P (péptido involucrado en la transmisión de la señal dolorosa).
Efecto condroprotector
En modelos animales, el ácido hialurónico ha demostrado tener un efecto condroprotector. En artrosis inducidas en perros mediante la sección de ligamento cruzado anterior, se observó un aumento en la producción de la matriz del cartílago, incluyendo al ácido hialurónico19. El significado de esta fase de reparación hipertrófica es desconocido, pero puede jugar un papel en la patogénesis de la artrosis. La inyección intraarticular de ácido hialurónico redujo precozmente este fenómeno en estudios en los que se emplean los mismos modelos animales20. No obstante hay que decir que a las 12 semanas no se observaron diferencias desde un punto de vista histológico entre la membrana sinovial artrósica de animales tratados y no tratados. En modelos animales de artrosis realizados con ovejas sometidas a una meniscectomía interna o externa, y tras la inyección semanal de cinco dosis de ácido hialurónico de elevado peso molecuar (2 x 106), se ha comprobado que no se detiene la formación de osteofitos o la lesión del cartílago, aunque mejora la movilidad21. Por tanto, los efectos condroprotectores del ácido hialurónico no están aún suficientemente demostrados.
VISCOSUPLEMENTACIÓN
Consiste en la inyección intraarticular de ácido hialurónico con el fin de restaurar la propiedades elásticas y viscosas del líquido sinovial, y así reconstruir la homeostasis alterada en la articulación artrósica22. Es una terapia indicada en pacientes que presentan sintomatología, a pesar de haber instaurado un tratamiento médico farmacológico y rehabilitador. Los pacientes con sobrepeso y con artrosis avanzada, experimentan peores resultados. Los efectos beneficiosos del ácido hialurónico no son permanentes, ya que el problema original continúa existiendo dentro de la articulación. El tratamiento es seguro y efectivo, pero requiere varias inyecciones para ser eficaz, ya que el ácido hialurónico exógeno es eliminado de la articulación23.
El uso del ácido hialurónico con fines terapéuticos tuvo lugar a finales de 1960. Se obtuvo de cordón umbilical humano y cresta de gallo, y pudo ser separado en fracciones inflamatorias y no inflamatorias. En modelos animales se demostró que la fracción no inflamatoria del hialuronato sódico era capaz de disminuir la inflamación sinovial y el dolor. Se comenzó a emplear en caballos de carreras con el nombre de Hyalartil-Vet24. Las características que una sustancia debe ofrecer para ser utilizada en la viscosuplementación se resumen en la Tabla 2.
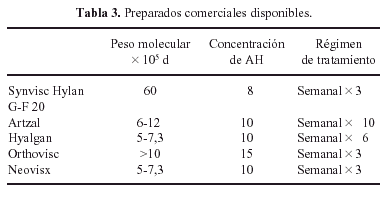
El peso molecular del ácido hialurónico fisiológico en la sinovial es aproximadamente 4-5 x 106 d. El peso molecular del ácido hialurónico empleado en la viscosuplementación afecta a varias propiedades relacionadas con su mecanismo de acción. Para aumentarlo, se ha desarrollado un proceso de entrecruzamiento de moléculas de ácido hialurónico mediante grupos hidroxilo terminal25. La Tabla 3 resume los preparados comerciales de ácido hialurónico de que disponemos hoy en día.
Efectos adversos
Aunque los preparados de ácido hialurónico se han empleado para el tratamiento de la artrosis de rodilla desde hace 20 años, la experiencia de su utilización ha sido más reciente. La incidencia global de efectos colaterales es de aproximadamente un 1% por inyección, y se recogen en la Tabla 4. Lo más frecuente son las reacciones locales, consistentes en dolor, calor y mínima tumefacción local26. No suelen durar más de 1 o 2 día. En un estudio retrospectivo realizado por Puttick, se observaron reacciones locales clínicamente significativas en un 11% de las inyecciones27. En una extensa revisión realizada en Canadá con Hylan GF, se detectaron reacciones locales en 42 (2,7%) de 1.537 inyecciones y en 28 (8,3%) de los 336 pacientes en total. De las 42 reacciones, 33 (79%) se resolvieron sin secuelas. Cinco pacientes tuvieron un total de 9 reacciones con secuelas, incluyendo tumefacción residual y dolor intermitente. Curiosamente, la proporción de efectos adversos por inyección fue superior (5,2%) cuando se realizaba un abordaje medial en rodillas parcialmente flexionadas.
En el estudio de Lussier et al no se describen reacciones sistémicas, aunque 28 pacientes tuvieron reacciones locales28. En el estudio de Wobig, no se objetivaron reacciones adversas locales, y sólo se describieron reacciones sistémicas transitorias leves en 3 pacientes: picores, calambres y hemorroides, aunque es cuestionable que éstas se deban a la inyección intraarticular de ácido hialurónico29. Se ha descrito también algún caso de pseudogota y condrocalcinosis tras la inyección intraarticular de ácido hialurónico30,31. Quizá las reacciones adversas mencionadas se deban a la inyección extraarticular accidental, que produciría una reacción local en los tejidos. También se piensa que una inyección técnicamente mal aplicada o la existencia de proteínas contaminadas en preparados de ácido hialurónies, pueden jugar un importante papel. Pacientes alérgicos a aves o proteínas de huevo, pueden tener una reacción al ácido hialurónico, por lo que no son candidatos al tratamiento.
EFICACIA CLINICA
Estudios en animales
Una amplia variedad de estudios animales han evaluado la eficacia y seguridad de la viscosuplementación para el tratamiento de la artrosis. En la mayoría de ellos, la artrosis es inducidada mediante la resección quirúrgica de estructuras que aceleran los cambios degenerativos. El modelo experimental de Pond-Nuki de artrosis en perros, es un ejemplo. En éste se secciona el ligamento cruzado anterior de la rodilla, produciéndose alteraciones en el cartílago parecidas a las que espontáneamente ocurren en la artrosis tanto en animales como en el hombre32,33. Se observa una disminución de la concentración de ácido hialurónico, que se piensa que es responsable de las alteraciones biomecánicas del cartílago artrósico.
La inyección intraarticular de ácido hialurónico tiene efectos beneficiosos en la preservación del cartílago articular y la membrana sinovial en conejos, ya que disminuye las erosiones, rotura y degeneración en dichos tejidos34. Estudios adicionales han demostrado que la administración de ácido hialurónico de alto peso molecular es más efectivo que el de bajo peso molecular35. Gosh et al tienen resultados similares en estudios efectuados con ovejas21. En el estudio de Armstrong et al sobre los efectos del ácido hialurónico intraarticular en el cartílago y hueso subcondral en ovejas con artrosis de corta evolución, se observó el efecto protector sobre el cartílago y el hueso subcondral36.
Gingerich et al evaluaron el efecto del ácido hialurónico exógeno sobre la función articular de caballos con artrosis. Los resultados eran dosis dependiente, siendo la dosis óptima de 20-40 mg37. La administración extraarticular de ácido hialurónico también ha demostrado tener efectos beneficiosos. Gannon obtuvo buenos resultados al administrar 10 mg de hialuronato sódico en el tratamiento de artritis y sinovitis38. En contraste con la mayoría de los estudios que mostraban los beneficios de la viscosuplementación en caballos, Pelso et al mostraron que la inyección intraarticular de ácido hialurónico no tenía efectos significativamente beneficiosos39. Smith et al observaron que la inyección de ácido hialurónico intraarticular en perros con artrosis no modificaba la evolución de la enfermedad y disminuía de forma significativa la concentración de proteoglicanos en las rodillas afectadas40.
Resultados en ensayos humanos
En 1974, Peyron y Balazs publicaron el primer ensayo clínico de la suplementación con ácido hialurónico como tratamiento de la artrosis en humanos. Cuarenta pacientes fueron distribuidos de forma aleatoria en dos grupos. Tras 4 meses de seguimiento, la mayoría de los pacientes del grupo que recibió tratamiento presentaba mejoría clínica41. Posteriormente, se han desarrollado múltiples estudios no controlados y un número limitado de ensayos controlados acerca de la administración intraarticular de ácido hialurónico.
En los estudios diseñados para valorar la eficacia del ácido hialurónico en el tratamiento de la artrosis de rodilla, se utilizan escalas de valoración estándar del dolor y función articular. Pero también se emplean instrumentos específicos, como el índice de Lequesne o el WOMAC (Western Ontario and McMaster Universities Ostheoarthritis Index)42,43. La escala de Lysholm empleada en el ensayo de Dahlberg et al no es específica de la artrosis, pero se usa con frecuencia en la evaluación de las lesiones ligamentosas de la rodilla44. Lo mismo sucede con la escala de Larson utilizada por Graf et al45.
Dixon et al encontraron que 11 inyecciones de ácido hialurónico por paciente en un período de 23 semanas, producía una mejoría estadísticamente significativa (p < 0,01) del dolor de rodilla, pero no en las actividades de la vida diaria o el dolor mecánico46. Dougados et al observaron que el ácido hialurónico era significativamente mejor (p < 0,03) que el placebo para aliviar el dolor y mejorar la actividad funcional valorada por el índice de Lequesne47.
En un estudio doble ciego, Altman et al encontraron beneficios estadísticamente significativos (p < 0,05) con un preparado de ácido hialurónico en comparación con placebo en un estudio de análisis de eficacia (análisis de los datos de aquellos pacientes que completaron el estudio)48. El dolor y la incapacidad valorados mediante el índice WOMAC también demostraba diferencias estadísticamente significativas (p = 0,041). En un estudio realizado por Scale et al de 12 semanas y 26 de seguimiento telefónico, se observaba una mejoría con Hylan G-F 20. En este ensayo también se comparaba el régimen de administración de tres inyecciones de tratamiento, con dos inyecciones, encontrándose mejoras significativas a favor del primero. En un ensayo de 52 semanas de duración, en el que se administraba ácido hialurónico en pacientes con dolor clínicamente significativo de rodilla, radiografías normales y cambios artrósicos precoces demostrados artroscópicamente, no mostraron beneficios clínicos comparado con el placebo44.
El ácido hialurónico también ha sido comparado con otros agentes terapéuticos. En un estudio simple ciego, Graf et al compararon 7 inyecciones de ácido hialurónico con 13 de mucopolisacárido MPA. Había una mejora significativamente superior (p < 0,05) en el índice de Larson (principalmente en el alivio del dolor) en el grupo tratado con ácido hialurónico a las 6 semanas, pero no a los 6 meses45. En otro estudio, Jones et al demostraron que los corticoides intraarticulares y el ácido hialurónico tenían una eficacia similar49. En el estudio realizado por Altman et al se comparó el ácido hialurónico con naproxeno 500 mg 2 veces al día, concluyendo que su eficacia era similar48. La Tabla 5 resume los resultados de la viscosuplementación con respecto a otras modalidades terapéuticas.
CONCLUSIÓN
El principal objetivo del tratamiento de la artrosis es disminuir el dolor y mantener o mejorar la función articular. En los últimos años se han desarrollado numerosos estudios que investigan el potencial de agentes condroprotectores, sustancias que son capaces de aumentar la actividad anabólica de los condrocitos, mientras que, simultáneamente, suprimen los efectos destructivos de las citoquinas en el cartílago. Parece que tales agentes, entre los que se encuentra el ácido hialurónico, permiten reparar el cartílago articular o al menos, detener su deterioro progresivo.