El resultado de los vástagos no cementados con recubrimiento poroso y anclaje metafisodiafisario que se empezaron a implantar a partir de los años 1983-1984 está siendo muy satisfactorio1,2. Sin embargo es aceptado que uno de los riesgos de este tipo de fijación es la reabsorción ósea periprotésica que según los autores varía entre el 7% y el 56%3. Bobyn4, en recientes estudios con prótesis experimentales no cementadas en perros, estableció claramente que la longevidad del vástago es mayor en los implantes porosos que en los lisos; además encontró en la interfaz de los implantes lisos partículas de desgaste del polietileno, mientras que los implantes porosos tenían un efecto protector de esta migración de las partículas de desgaste por presentar mayor osteointegración. Según estudios de Geesing5 esta integración se mejora con el recubrimiento por biomateriales como la hidroxiapatita (HA) y en las pruebas mecánicas demostró que este tipo de implante se fijaba con más fuerza al tejido óseo. Nuestro trabajo refleja los resultados clínicos y radiográficos obtenidos después de 8 años de seguimiento, con el vástago femoral CRM (Seipi-Bioimplant, Italia) recubierto en sus dos tercios proximales de 80 micras de biovidrio. Este biovidrio comercializado con el nombre de Biovetro® fue desarrollado por el grupo de estudio GSB en colaboración con la Stazione Sperimentale del Vetro de Murano (Italia).
MATERIAL Y MÉTODO
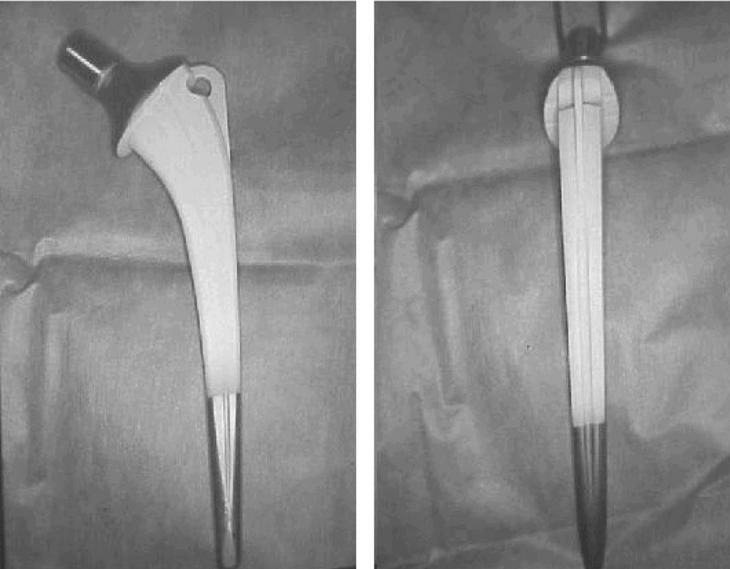
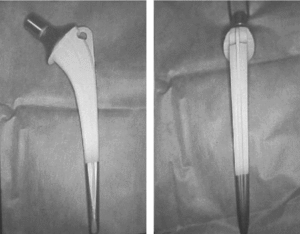
Se inició nuestra relación con el biovidrio implantando 70 prótesis totales de cadera no cementadas con vástago femoral recubierto en sus dos tercios proximales de biovidrio y cotilo impactado recubierto de malla de titanio. En 1994 se implantó a 41 pacientes y en 1995 a 26, que suman en total 67 pacientes. El vástago femoral es de aleación de titanio (TiAlVa), con cono morse 12/14, curvo y de sección rectangular con suavizamiento de los ángulos en su cara medial proximal, con collarete y pequeña aleta de estabilización a nivel de trocánter mayor y perforada para en caso necesario facilitar su extracción. Presenta canales longitudinales en su cara anterior, posterior y lateral que aumentan la superficie de contacto. Está afilado y biselado distalmente para evitar el efecto punta; con recubrimiento poroso en sus dos tercios proximales y recubierto en esta zona porosa con plasma-spray de biovidrio de 80 micras; la composición química de este plasma-spray de revestimiento de biovidrio es la siguiente: SiO2 (46-63%), Na2O (7-24%), K2O (2-8%), CaO (9-20%), MgO (0,1-2%), Al2O3 (0,1-2%), P2O5 (4-8%) Este vástago femoral se denomina CRM y está fabricado por Seipi-Bioimplant (fig. 1).
Figura 1. Vástago CRM: se aprecia su sección rectangular, el recubrimiento de biovidrio, la aleta estabilizadora, el orificio de extracción y los canales longitudinales.
El cotilo fue siempre impactado recubierto de malla de titanio con opción al atornillado y fabricado por Osteal-Ceraver (Francia). El par de fricción fue en todos los casos cerámica-polietileno, con cabeza de 28 mm.
De los 67 pacientes intervenidos han podido ser revisados de forma adecuada, tanto desde el punto de vista clínico como radiográfico, 59. A otros tres fue imposible localizarlos y 5 habían fallecido por causas ajenas a la intervención. Por tanto el presente estudio refleja los resultados de estos 59 pacientes a los que se implantaron 62 vástagos recubiertos de biovidrio.
Entre las causas etiológicas que motivaron la intervención destaca la coxartrosis con 54 casos (87%) y la necrosis avascular con 8 casos (13%) confirmados mediante estudio anatomopatológico; el número de varones fue de 30 (51%) y el de mujeres 29 (49%); la cadera derecha fue intervenida en 34 ocasiones (55%) y la izquierda en 28 (49%). La edad media de los pacientes intervenidos fue de 63 años con un máximo de 74 años y un mínimo de 35. Los controles de revisión postoperatoria se realizaron al mes, mes y medio, 3, 6 y 12 meses y luego anualmente, siendo revisados todos los pacientes durante finales de 2002 y principios de 2003.
A todos los pacientes se les realizó profilaxis antibiótica con cefonid 2 g intravenoso en el momento de bajar a quirófano y 1 g intravenoso a las 24 horas de la intervención; la profilaxis tromboembólica se inició con heparina subcutánea de bajo peso molecular, nadroparina de 0,3 ml, 12 horas antes de la intervención, continuando posteriormente cada 24 horas hasta 10 días más a partir de la fecha del alta hospitalaria.
Todos los pacientes fueron intervenidos por tres cirujanos del servicio habituados a la cirugía de la cadera, utilizando en todos los casos la vía de Hardinge. Las complicaciones intraoperatorias fueron las siguientes: tres fracturas de trocánter mayor y 8 fisuras diafisarias a nivel del calcar, tres de las cuales precisaron cerclaje alámbrico.
Entre las complicaciones postoperatorias hay que señalar: tres luxaciones (4,8%) que se solucionaron de forma incruenta y no han modificado el resultado final; dos flebitis (3,2%); dos infecciones (3,2%), una superficial que cedió con tratamiento antibiótico y otra en la que fue precisa la extracción y recambio del implante en dos tiempos.
En este estudio nos hemos encontrado con una estancia media elevada comparada con las estancias actuales, de 17 días con una máxima de 39 y una mínima de 9 días.
El cotilo fue impactado en los 62 casos (100%), sin tornillos en 48 (77%) y atornillado en 14 (23%). Existen 6 tamaños de vástago CRM, siendo el más implantado el número 3, en el 48% de los casos.
El drenaje se mantuvo durante 48 horas; los pacientes iniciaron sedestación al retirar el mismo y al tercer día se produjo la deambulación con carga parcial y dos bastones durante mes y medio. En aquellos pacientes en que hubo fractura de trocánter o fisuras femorales el apoyo se demoró tres semanas.
La evaluación clínica se realizó mediante la escala de Merle D'Aubigné6, que es quizá la más usada en Europa y que valora la ausencia de dolor con 6 puntos, la movilidad de más de 90° y sin actitudes viciosas con 6 puntos y la marcha normal e ilimitada con 6 puntos. Una puntuación excelente es la que suma 18 puntos; el resultado muy bueno suma 17 puntos, el bueno anota 15-16, el regular 13-14 y el malo 12 puntos o menos.
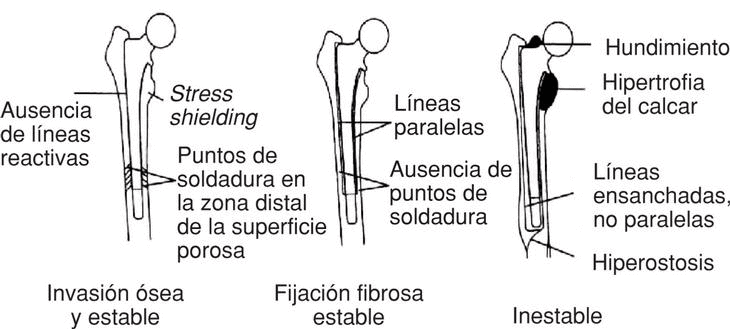
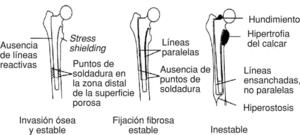
El estudio radiográfico se valoró según la clasificación de Engh7 para los vástagos no cementados (fig. 2), que los clasifica en: estable con invasión ósea cuando no existen líneas reactivas, no existe pedestal y cuando existen puntos de soldadura en la zona distal de la superficie porosa (fig. 3); implante estable con fijación fibrosa cuando existe una línea radiolúcida de menos de 1 mm de anchura alrededor de la circunferencia de la prótesis, no existen puntos de soldadura en el límite distal de la capa porosa y hay un pequeño pedestal; e implante con inestabilidad fibrosa cuando no existen signos de invasión ósea pero existe un pedestal distal, hipertrofia del calcar, líneas divergentes alrededor de la prótesis o clara migración del componente7. El análisis estadístico de supervivencia se realizó por el método actuarial.
Figura 2. Clasificación de Engh para los vástagos no cementados.
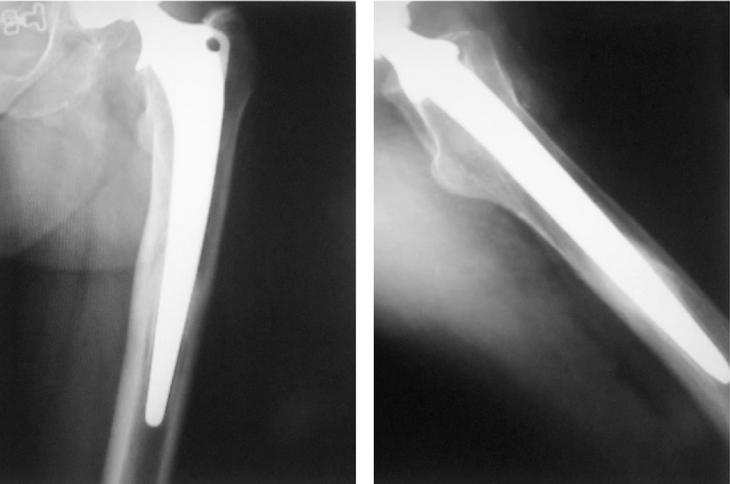
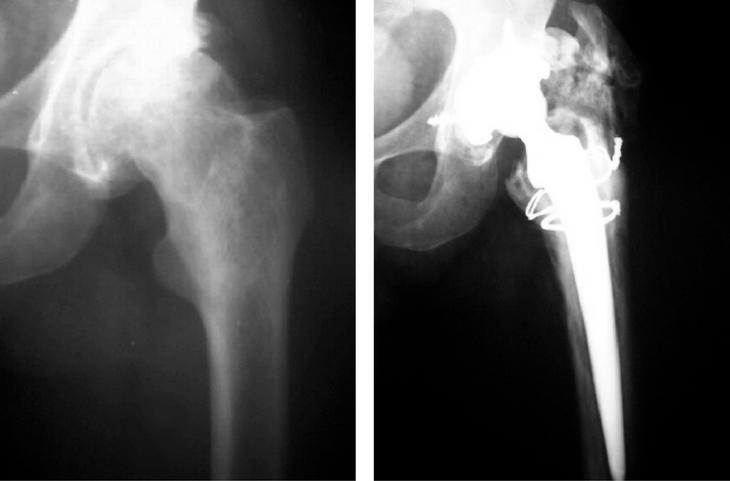
Figura 3. Vástago estable con puntos de soldadura en la zona distal de la superficie porosa y del biovidrio.
RESULTADOS
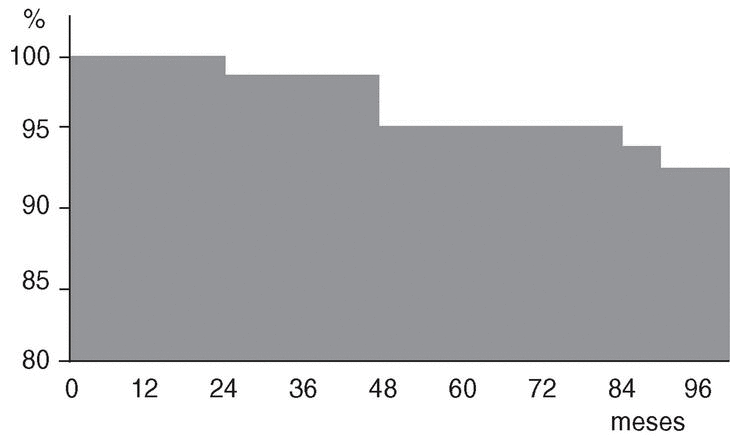
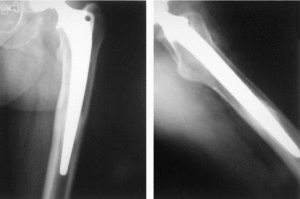
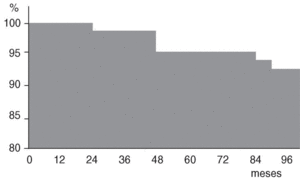
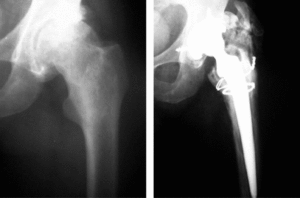
La curva de supervivencia del vástago CRM fue del 91,9% a los 8 años (fig. 4). En la valoración inicial y final realizada para este estudio se aplicó la escala de Merle D'Aubigné6 para las 62 artroplastias, encontrando una valoración clínica media preoperatoria de 2,34, 2,81 y 2,83 puntos para el dolor, la marcha y la movilidad respectivamente y una valoración final de 5,53, 5,66 y 4,94. Esta valoración corresponde a: 19 pacientes (30%) con resultado excelente, 17 (28%) con muy buen resultado, 12 (20%) con buen resultado, 7 (11%) regular y 7 (11%) malo (tabla 1). En estos malos resultados se incluyen a los 5 pacientes cuyo vástago ya había sido revisado por aflojamiento aséptico y en uno de los cuales se había producido una fisura femoral y la necesidad de cerclaje durante el acto quirúrgico, lo cual pudo influir en el mal resultado por la inexistencia de una adecuada fijación primaria inicial; el sexto paciente con mal resultado fue por infección profunda que obligó a extraer ambos componentes, y el séptimo paciente con mal resultado se detectó al realizar este estudio: presenta calcificaciones periarticulares grado III, un hundimiento y aflojamiento aséptico del vástago y está pendiente de revisión (fig. 5). No hemos tenido pacientes con dolor en el muslo, síntoma frecuente sobre todo con los primeros vástagos no cementados. Este punto favorable está posiblemente en relación con que el vástago sea de titanio, tenga una elasticidad más cercana a la del hueso y presente un extremo distal afilado y biselado.
Figura 4. Curva de supervivencia del vástago femoral CRM.
Figura 5. Vástago inestable y flojo con calcificaciones grado III y hundimiento e imagen preoperatoria del mismo caso.
El estudio radiográfico realizado a los tres meses de la intervención se utilizó como base para la comparación con el último estudio radiográfico. Se apreció la existencia de calcificaciones en una proporción elevada (41,9%). La distribución según la clasificación de Brooker es la siguiente: grado I, 16 casos (26% ), grado II, 6 casos (10% ), grado III, 4 casos (6% ) y grado IV ningún caso, lo que totalizan 26 casos (42%). Uno de nuestros pacientes con calcificaciones grado III y aflojamiento del vástago presentaba pérdida de la movilidad, seguramente achacable a dichas calcificaciones (fig. 5).
Aplicando la valoración radiográfica de Engh8 para los vástagos no cementados, a los 62 de este estudio recubiertos de biovidrio, se encontraron los resultados referidos en la tabla 2. Descontando el vástago revisado por infección profunda (que no ha sido por fallo del vástago en sí) y considerando el vástago pendiente de cambiar, se encontraron fallos de 5 vástagos, lo que supone una curva de supervivencia del 91,9% del vástago CRM al cabo de 8 años (fig. 4). En los tres casos en que hubo sólo aflojamiento aséptico del vástago uno ocurrió a los dos años, otro a los 4 años y el tercero está pendiente de revisión; en los otros dos casos hubo aflojamiento aséptico del cotilo y del vástago, ocurriendo uno a los 4 años y otro a los 7. En todos los vástagos revisados por aflojamiento aséptico se apreció en el acto operatorio la existencia de una membrana de interfaz y la desaparición en mayor o menor proporción del recubrimiento de biovidrio.
Se han encontrado vástagos infradimensionados en 16 casos (26%) de los 62 en estudio, tanto en pacientes con resultado excelente y bueno (11 casos), como en pacientes con resultado regular y malo (en los 5 casos restantes). La osteoporosis difusa metafisaria por disfuncionalidad se apreció en 14 casos (22%), no constituyendo ninguna merma funcional ni influyendo en el resultado clínico final.
En 6 casos (9%) se encontró hueso denso en la punta del vástago sin constituir un pedestal completo y sin ninguna repercusión clínica. La reabsorción del calcar se produjo en 8 casos (13%), sobre todo en pacientes con buen resultado clínico y radiográfico, que según algunos autores9 sería la expresión de fenómenos de adaptación del hueso al implante femoral.
DISCUSIÓN
Existen estudios experimentales sobre el comportamiento del biovidrio, pero no podemos valorar si nuestros resultados sobre la evolución del vástago CRM se asemeja o no a los de otras series publicadas, puesto que no se tiene referencia de ningún otro estudio sobre el resultado de vástagos femorales recubiertos de biovidrio.
Se apreció la existencia de calcificaciones heterotópicas en una proporción elevada (41,9%), mayor que en la mayoría de trabajos publicados y muy por encima de la media que está en torno al 15%, aunque dependiendo de las series9,10 se señala un 4,1% en prótesis no cementadas de tipo isoelástico a un 81% en prótesis cementadas de tipo Charnley. Estas calcificaciones las achacamos a la vía de abordaje de Hardinge, donde parece que son más frecuentes, y también a la agresividad de las fresas metafisarias que presentan una sección rectangular con estrías como dientes de sierra, y por tanto con unos ángulos muy agresivos para el tejido muscular vecino.
Probablemente alguno de los fallos de este vástago recubierto de biovidrio haya sido por defecto de técnica. En los primeros casos, al dimensionar bien el vástago dentro del canal se forzó el fresado y se produjeron fisuras femorales, que pudieron dar lugar a una mala fijación primaria del implante, ya que su estabilidad inicial es el principal factor para inducir el crecimiento de hueso sobre él12; también el cotilo pudo tener alguna influencia, puesto que en dos casos se apreció primero el aflojamiento del cotilo y posteriormente el del vástago.
La osteointegración de un implante ha sido definida como el contacto directo, sin interposición de partes blandas de tejido conectivo, cuando se examina al microscopio óptico13, entre el hueso viable que está remodelándose y el implante. Hay numerosos factores que modifican esta osteointegración influyendo de forma importante en las características del implante14. Con respecto a la biocompatibilidad del material, la aleación de TiAlVa parece la ideal para sustituir a las prótesis cementadas15 al tener un módulo de elasticidad relativamente bajo que evita el efecto protector de la carga que se produce en aleaciones como la de acero inoxidable o la de Cr Co Mb. El Ti ha mostrado mayor crecimiento óseo en su superficie que otras aleaciones, por lo que presenta la mejor biocompatibilidad. Se ha mostrado no tóxico e inerte en el medio fisiológico. Por todo ello se considera actualmente la aleación de Ti como la ideal junto con un recubrimiento bioactivo en su superficie.
Por lo que se refiere a la porosidad de la superficie, hay estudios comparativos4 que demuestran que los implantes lisos son más susceptibles que los porosos de formar una cavidad periimplante de tejido fibroso por donde además migran las partículas de desgaste del polietileno y facilitan la formación de granulomas; los implantes porosos permiten una mayor fijación histológica y mecánica del implante.
Con respecto a la rugosidad de la superficie, una rugosidad de 4 a 6 micras en los implantes produce mucho más crecimiento óseo, según Feighan13, que en los implantes de superficie pulida y encontró resultados significativamente mayores en la prueba de extracción.
Por lo que se refiere a los recubrimientos bioactivos de superficie, entre ellos destaca la HA, que es el material sustituto del hueso más estudiado5,16, empleado para relleno de defectos óseos, así como material de recubrimiento de prótesis de cadera. Por otra parte existen biovidrios y biovidriocerámicas14 que tienen en común la característica de poder formar una capa de hidroxil-carbonatoapatita en su superficie por medio de una reacción química cuando están en contacto con el tejido óseo viviente. La propiedad que distingue al biovidrio de la HA es que el primero sufre una biodegradación, esto es, favorece de inmediato la reabsorción y simultáneamente la osteoconducción17. El biovidrio en contacto con el tejido óseo presenta una transformación físico-química en 9 pasos de hidroxilación que finalizan con la formación de un lecho de gel de sílice sobre el cual se produce la aposición de cristales de fosfato cálcico (apatita) y de tejido conjuntivo que sirven de guía para la neoformación de tejido osteoide. El biovidrio se reabsorbe completamente y no interfiere en el proceso de remodelación ósea. La reabsorción de la HA es mucho más lenta, perdurando años como se ha demostrado en estudios en cadáver.
Paralelamente al inicio de esta serie de implantes de vástago femoral CRM con recubrimiento de biovidrio se elaboró una tesis doctoral14,17 que consistió en el implante en el fémur de 6 ovejas de características semejantes de 54 cilindros de TiAlVa de 10 mm de longitud y 3 mm de diámetro suministrados por Seipi-Bioimplant; eran implantes de superficie lisa, de los cuales la mitad estaban recubiertos de biovidrio y la otra mitad de HA, todos mediante el sistema de plasma-spray y con un espesor de recubrimiento de 80 micras. Todos los cilindros estaban perforados en uno
de sus extremos para poder fijar un dispositivo de tracción.
Su valoración al sacrificar esas ovejas a las 2, 4, 6, 8, 12 y 16 semanas estableció que si bien la porosidad del biovidrio era muy superior a la de la HA, lo que en principio debería favorecer una mayor osteointegración, la fuerza de unión al hueso de los implantes revestidos de biovidrio fue muy inferior a la conseguida con la HA. La fuerza necesaria para «hacer saltar» estos cilindros del fémur de la oveja fue siempre superior para los revestidos de HA y los valores máximos se produjeron al tercer mes, obteniéndose valores de 39,7 megapascales (Mpa) necesarios para arrancar los cilindros de HA, frente a los 8,2 Mpa para los cilindros recubiertos de biovidrio14,17.
A la vista de estos resultados se decidió suspender el implante de nuevos vástagos revestidos de biovidrio y observar su evolución a lo largo de los años. Se inició otra serie con este mismo vástago femoral pero revestido de HA que será objeto de estudio comparativo, con el CRM, a los 8 años de su implante.
Como conclusión se considera que actualmente existen ya series muy amplias, como la de Furlong18, con vástagos recubiertos de HA y con una supervivencia cercana al 100%. En la serie de D'Antonio19 en pacientes menores de 50 años y con seguimiento de 7 años se revisó algún vástago, pero en ningún caso por aflojamiento aséptico. Estas y otras series superan los resultados de nuestra pequeña serie de vástagos con recubrimiento de biovidrio, por lo que creemos que hoy día son mejores los resultados de los vástagos femorales recubiertos de HA que los recubiertos con biovidrio, y en particular con la composición, ya señalada en párrafos anteriores, que presenta este biovidrio.
En nuestra opinión existe una peor osteointegración del biovidrio por las siguientes razones: la rápida biodegradación del biovidrio favorece su reabsorción, que empieza ya a las pocas horas de su implante; no produce, en nuestra opinión, la estimulación suficiente para desencadenar la osteoconducción y la consiguiente osteointegración; la aparición de interfase fibrosa con reacción macrofágica a cuerpo extraño observada en los vástagos revisados; la escasa mineralización del hueso formado, posiblemente por una proporción elevada de aluminio que interfiere con el proceso normal de mineralización del osteoide y que en el biovidrio es de 0,1% a 2%, estando actualmente aceptado que el máximo porcentaje de Al2O3 que tiene que tener el biovidrio para que no pierda su bioactividad debe estar en 1%-1,5%; y el diseño del vástago CRM y su aleación, que permiten una buena estabilidad primaria del implante, han influido, en nuestra opinión, en que los resultados no hayan sido peores.
Conflicto de intereses. Los autores no hemos recibido ayuda económica alguna para la realización de este trabajo. Tampoco hemos firmado ningún acuerdo por el que vayamos a recibir beneficios u honorarios por parte de alguna entidad comercial. Por otra parte, ninguna entidad comercial ha pagado ni pagará a fundaciones, instituciones educativas u otras organizaciones sin ánimo de lucro a las que estemos afiliados.