Introducción
Por algún tiempo, la transmisión de enfermedades infecciosas y la alosensibilización humoral han sido los principales focos de atención de los esfuerzos investigadores en medicina transfusional. Sin embargo, algunas investigaciones han sugerido que la inducción de inmunotolerancia, anergia o hiporrespuesta (inmunomodulación) por las transfusiones de sangre homóloga (TSH) es un fenómeno que ocurre más frecuentemente que la alosensibilización. Los mecanismos implicados en esta inmunomodulación aún no han sido totalmente esclarecidos, barajándose actualmente 2 hipótesis: 1) la inducción por parte de los leucocitos del donante de una respuesta celular TH2 en el receptor de la transfusión, lo que originaría una inmunosupresión al bloquear las respuestas TH1; y 2) La inducción de un estado de anergia en el receptor al ser estimuladas las células T de éste por los leucocitos del donante en ausencia de las señales coestimuladoras adecuadas.12,38 Esta inmunomodulación, junto con las alteraciones que se producen en los eritrocitos durante el almacenamiento y que pueden provocar alteraciones de la microcirculación y de la oxigenación tisular,25,39 pueden originar un estado de susceptibilidad a la infección postoperatoria y/o la recidiva tumoral en el paciente que recibe una TSH.1,6
Dado que en las intervenciones de cirugía ortopédica es frecuente la utilización de TSH, se han realizado diversos estudios, tanto prospectivos como retrospectivos, encaminados a comprobar si existía una correlación entre las TSH perioperatorias y una mayor incidencia de infecciones postoperatorias. Así, Fernández y cols.13 realizaron un estudio retrospectivo sobre 376 pacientes intervenidos de cirugía de cadera, rodilla o columna y constataron que la incidencia global de infecciones postoperatorias fue del 6,1% (23/376). Sin embargo, cuando analizaron la incidencia de infecciones en función del tipo de sangre transfundido observaron que ésta fue del 6,9% en los que recibieron sangre homóloga (5/72), del 5% para los transfundidos con autóloga (7/140), del 4,9% en los pacientes no transfundidos (6/122) y del 11,9% en los que recibieron ambos tipos de sangre (5/42). Por tanto, la incidencia de infecciones fue de un 8,8% en los pacientes que recibieron sangre homóloga o sangre homóloga + autóloga (10/114). Esto es, casi un 45% más de infecciones que los que no habían recibido sangre hómologa (no transfundidos o sólo sangre autóloga). Triulzi y cols.37 han encontrado diferencias aún mayores en una serie de 102 pacientes sometidos a 109 intervenciones de artrodesis vertebral. Los pacientes con TSH presentaron una incidencia de infección postoperatoria del 20,8% (5/24), frente al 3,3% en los pacientes que recibieron sangre autóloga (2/60) o al 4% en los que no fueron transfundidos (1/25).
Recientemente se han publicado 2 grandes estudios en los que se han incluido casi 20.000 pacientes que vienen a confirmar los resultados antes citados y parecen dejar claro que la transfusión perioperatoria de sangre homóloga en cirugía ortopédica se asocia con un incremento del riesgo de infección postoperatoria. En el primero de ellos, Carson y cols.8 realizan un estudio retrospectivo (1983-1993) sobre 9.598 pacientes consecutivos con fractura de cadera y mayores de 60 años. El análisis de los datos reveló que, una vez eliminados los otros factores de riesgo, la transfusión de sangre homóloga se asoció a un 35% de aumento en el riesgo de padecer una infección postoperatoria grave y un 52% de aumento en el riesgo de padecer neumonía, siendo además este aumento dosis-dependiente.
En el estudio de Carson y cols.,8 dado que cubre un período de 10 años, pueden existir interferencias por cambios en las prácticas médicas y en él sólo se incluyen pacientes con fractura de cadera lo que, obviamente, impide la entrada de los pacientes en un progama de predepósito de sangre autóloga. Por el contrario, en el segundo de ellos, Bierbaum y cols.5 estudiaron prospectivamente 9.482 pacientes sometidos a cirugía programada de rodilla o cadera entre septiembre de 1996 y junio de 1997, el 60% de los cuales realizaron predepósito de sangre autóloga (media 1,7 U/paciente). Al analizar la incidencia de infecciones en función de las transfusiones recibidas, observaron que dicha incidencia fue del 7% en los que recibieron sangre homóloga, del 4% en los que recibieron sangre autóloga y del 3% en los que no fueron transfundidos. Esto es, los pacientes que recibieron sangre homóloga tuvieron un 47% más de infecciones postoperatorias que los que no la recibieron (p < 0,01), mayor incidencia de tromboflebitis y de sobrecarga de volumen y una mayor estancia hospitalaria, mientras que no hubo diferencias entre los que recibieron sangre autóloga y los que no fueron transfundidos,
Los resultados de estos estudios parecen constatar los beneficios de la implantación de programas que, como los de autotransfusión, eviten la exposición del paciente a TSH. Por ello, el objetivo del presente trabajo ha sido evaluar la efectividad de un programa de autotransfusión basado en la donación preoperatoria de sangre autóloga a corto plazo (DPSA) y en la recuperacion y reinfusión de la sangre de los drenajes postoperatorios, empleadas solas o combinadas, para evitar o reducir las TSH y los riesgos derivados de la misma en pacientes sometidos a cirugía de columna lumbar intrumentada.
Material y Método
Se ha realizado un estudio prospectivo randomizado abierto en el que inicialmente se incluyeron 140 pacientes programados para practicarles una artrodesis vertebral lumbar o lumbosacra instrumentada (Allospine, Sulzer, Suiza) con injerto autólogo de cresta ilíaca, comprendiendo de 2 a 4 niveles y con o sin descompresión de los elementos neurológicos mediante microcirugía. Todas las intervenciones fueron realizadas por el mismo cirujano, entre febrero de 1997 y mayo de 2000. Los pacientes fueron divididos en 4 grupos iguales de acuerdo con el tipo de estrategia transfusional que se iba a aplicar: Grupo A (control) constituido por los pacientes en los que no se planeó hacer ningún tipo de autotransfusión y que recibieron TSH según necesidad; Grupo B (ATP) constituido por los pacientes en los que se reinfundió la sangre de los drenajes postoperatorios como única fuente de sangre autóloga; Grupo C (DPSA) pacientes en los que se utilizó la sangre donada preoperatoriamente como única fuente de sangre autóloga; y Grupo D (DPSA+ATP) constituido por los pacientes que recibieron ambos tipos de autotransfusión.
En 18 de los 140 pacientes no se realizó instrumentación, por lo que fueron excluidos del estudio. En 4 pacientes del Grupo B no se recogieron un mímino de 250 ml de sangre, por lo que no fueron reinfundidos y pasaron al grupo control. Finalmente, 4 pacientes inicialmente incluidos en el Grupo C llegaron a quirófano con hemoglobinas bajas y tuvieron un sangrado mayor de lo previsto, lo que aconsejó el uso del recuperador y pasaron al Grupo D.
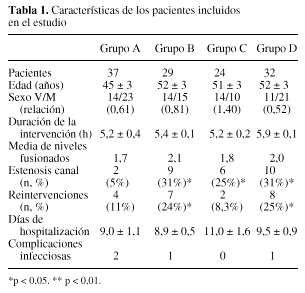
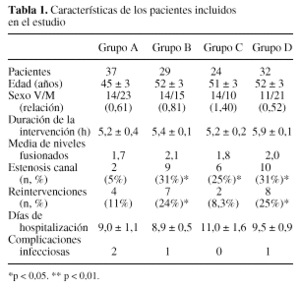
De este modo, la distribución de los 122 pacientes del estudio en los distintos grupos fue: Grupo A (Control, n = 37), Grupo B (Autotransfusión postoperatoria, ATP, n = 29); Grupo C (Autotransfusión preoperatoria, DPSA, n = 24) y Grupo D (Autotransfusión pre y postoperatoria, n = 32). No hubo diferencias significativas entre los grupos en cuanto a la edad, duración de la intervención, número de niveles fusionados, días de hospitalización o complicaciones postoperatorias, aunque sí en la relación varones/mujeres y en la incidencia de estenosis de canal y de reintervenciones (tabla 1).
Las intervenciones se realizaron bajo anestesia general y todos los pacientes recibieron 1,5 g de cefuroxima intraoperatoria y heparina de bajo peso molecular (Dalteparina 5.000 UI/24 h, 2-3 días) y antibióticos (Cefuroxima 750 mg/6 h, 3-4 días) postoperatoriamente como profilaxis de complicaciones tromboembólicas e infecciosas. Además, durante toda la intervención se realizaron lavados del campo quirúrgico con soluciones salinas conteniendo gentamicina (80 mg gentamicina/250 ml suero salino).
Al igual que estudios anteriores,33,34 la estimación de las pérdidas y la reposición hemática intraoperatorias fueron realizadas por el anestesiólogo, mientras en el postoperatorio la estimación del sangrado y la decisión de transfundir correspondió al cirujano. En todos los grupos, los pacientes fueron transfundidos si la hemoglobina bajaba de 8-9 g/dl, salvo que la sintomatología aconsejase hacerlo antes. La sangre homóloga se transfundió en forma de concentrados de hematíes, mientras que la autóloga se transfundió como sangre completa.
En todos los pacientes se aplicaron los criterios de inclusión y exclusión del protocolo de autotransfusión preoperatoria establecido por CRTS de Málaga, entre los que destaca la obtención de consentimiento informado, una Hb > 11 g/dl o un Hto > 34%, la ausencia de bacteriemia, sepsis, hepatitis o sida y la ausencia de procesos cardio-respiratorios graves, hipertensión arterial severa o antecedentes comiciales. La presencia de neoplasia no fue criterio de exclusión, aunque ninguno de los pacientes era portador de tumor maligno o benigno conocido.
Los pacientes de los grupos C y D donaron preoperatoriamente 2 unidades de sangre (400 ml/U) en bolsas con CPD-A (KBD-450 CAP, Kawasumi Laboratories, Japón), de acuerdo con el siguiente protocolo: la primera unidad se obtuvo 3-10 días antes de la intervención (generalmente 7 días); y la segunda 24 horas antes de la misma, realizándose una reposición del volumen extraído mediante la administración de soluciones de cristaloides (hemodilución normovolémica preoperatoria diferida).
La etiqueta de las bolsas utilizadas indica claramente el origen de la sangre mediante las palabras «sangre autóloga» y dispone además de espacio para anotar los datos de filiación del donante-paciente, la fecha de extracción, el grupo y una fotografía del mismo. Las unidades se conservaron sin fraccionar a 4 °C desde su extracción hasta su utilización intraoperatoria o en el postoperatorio inmediato, utilizando un frigorífico distinto al empleado para las unidades de sangre homóloga.
De acuerdo con la legislación española (RD 1854/1993), se realizaron las pruebas para la detección de agentes infecciosos (serología de sífilis, antígeno de superficie del virus de la hepatitis B y anticuerpos frente a virus de la hepatitis C, VIH-1 y VIH-2) no pudiendo utilizarse para transfusión autóloga las donaciones que hayan dado resultado positivo en alguna de ellas. Igualmente, las unidades no utilizadas para transfusión autóloga, fueron descartadas. Antes de la reinfusión de cualquiera de la unidades autólogas predepositadas, se realizaron las pruebas cruzadas de rutina.
La evaluación del programa de donación preoperatoria de sangre autóloga se realizó valorando la efectividad (% de pacientes que evitan la TSH), el rendimiento (% de unidades reinfundida) y la seguridad (% de pacientes que experientaron efectos adversos relacionados con la realización de la DPSA).9
En los pacientes de los grupos B y D se recuperó la sangre de los drenajes postoperatorios mediante un dispositivo de recolección-reinfusión, provisto de detector de seguridad para la fuga de aire y pérdida de vacío y de un filtro interior de 200 micras (ConstaVac CBC II, Stryker, USA). El sistema se conecta a los drenajes profundos en el quirófano; operación realizada por el cirujano o la enfermera en condiciones de máxima esterilidad. La presión de aspiración inicial fue de 89 mm Hg y, una vez que el paciente se encontraba en la sala de recuperación, se bajó a una presión de aspiración de 25 mm Hg.
Se recogió la sangre aspirada sin solución anticoagulante durante un máximo de 6 horas, transcurridas las cuales el contenido del reservorio colector fue transferido, desde la parte inferior del mismo, a una bolsa de transfusión con igual capacidad. Los últimos 80 ml de sobrenadante permanecieron en el reservorio con el fin de no retransfundir grasa. Siempre que el volumen recuperado fue mayor de 250 ml, la sangre fue reinfundida intercalando un filtro de 20-40 mm (SQ40SJKL, RC100KLE o LeukoGuard, Pall, Reino Unido), indepedientemente del nivel de hemoglobina del paciente.
En este caso, el rendimiento representa el porcentaje de equipos de recuperación instalados en los que se recupera un volumen mínimo para ser transfundido, mientras que, al igual que en la DPSA, la efectividad se mide por el porcentaje de pacientes que evitan la TSH y la seguridad por el porcentaje de pacientes que experimentan efectos adversos en relación a la ATP.
No fueron incluidos en un programa de autotransfusión postoperatoria con sangre filtrada, no lavada, aquellos pacientes en los que se dio alguna de las siguientes circunstancias: insuficiencia renal, función hepática alterada, trastornos de la coagulación, utilización de agentes hemostáticos locales o irrigación del campo quirúrgico con soluciones inadecuadas (povidona yodada, agua oxigenada), seropositivos, patología séptica o neoplásica o negativa del paciente a aceptar la técnica.
Para transformar el volumen de sangre recuperado en unidades (U), se aplicó la expresión: U = Vol drenado (ml) · Hto drenaje (%) / 400 (ml) · Hto preoperatorio donde: Vol. drenado es el volumen recogido en reservorio colector durante las 6 primeras horas del postoperatorio y 400 ml sería el volumen de sangre que se extrae para una unidad.
Todos los pacientes recibieron ferroterapia oral con 120 mg de Fe ferritínico/día (Ferroprotina, 3 sobres/día; Iquinosa) desde 3 semanas antes hasta un mes después de la intervención.
En todos los pacientes de recogieron los siguientes datos clínicos: número de historia, edad, sexo, fecha de la intervención, duración de la intervención, sangrado intraoperatorio, sangrado postoperatorio, sangrado total, unidades predepositadas, transfusiones intraoperatorias homólogas, transfusiones intraoperatorias autólogas, transfusiones postoperatorias homólogas, transfusiones postoperatorias autólogas, transfusiones totales, volumen reinfundido y su equivalente en unidades, hemoglobina preoperatoria, hemoglobina postoperatoria, hemoglobina al alta, complicaciones y días de hospitalización. El protocolo de recogida de datos y la supervisión de su cumplimentación, así como la recopilación y análisis de los datos obtenidos, fueron realizados por los autores no directamente implicados en el manejo clínico de los pacientes (MM y JJGV). Para el análisis de las necesidades transfusionales en cada grupo de asumió que un concentrado de hematíes homólogos era igual a una unidad de sangre autóloga, puesto que contienen aproximadamente la misma cantidad de hemoglobina.
Todos los resultados se expresaron como la media ± error estándar de (n) determinaciones. El estudio estadístico se realizó mediante t de Student para datos no apareados para la comparación de medias entre los grupos, con el paquete informático SPSS.
Resultados
Sangrado y reposición hemática de los pacientes
La población de estudio ha estado constituida por 122 pacientes con patología degenerativa de columna lumbosacra intervenidos consecutivamente por un mismo cirujano. En esta cirugía de artrodesis vertebral instrumentada, el volumen medio de sangrado ha oscilado entre 1.100 y 1.700 ml, siendo significativamente mayor en los grupos B y D, fundamentalmente a costa del sangrado intraoperatorio (tabla 2). En estos 2 grupos de pacientes hubo más estenosis de canal y más reintervenciones y, aunque no hubo diferencias significativas, sí se apreció una tendencia a un mayor número de niveles artrodesados y a una mayor duración de las intervenciones (tabla 1).
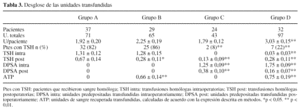
Para compensar el volumen perdido por sangrado, se realizó reposición hemática intra y/o postoperatoria en todos los grupos, si bien la tasas de transfusiones intraoperatorias fue mayor en el grupo D con respecto a los grupos A, B y C (p < 0,01), mientras que las postoperatorias fueron mayores que las de los grupos A (p < 0,05) y C (p < 0,01) (tabla 3). No obstante, no se encontraron diferencias significativas en las cifras de hemoglobina postoperatoria ni al alta (tabla 2) y tampoco en los días de hospitalización (tabla 1).
El número de complicaciones infecciosas postoperatorias fue bajo (4/122; 3,27%) y sin diferencias entre los grupos, no existiendo ningún caso de infección profunda de la herida quirúrgica (Grupo A: una infección urinaria y un seroma con cultivo positivo a E. coli; Grupo B: una neumonía; Grupo D: una infección urinaria) (tabla 1).
En el grupo control (Grupo A), constituido por 37 pacientes que no recibieron ningún tipo de autotransfusión, se transfundieron una media de 1,92 unidades de sangre homóloga/paciente (U/pte) (tabla 3). En este grupo 32 pacientes (86,5%) recibieron THS con la siguiente distribución (unidades/% pacientes): 1/18,9; 2/37,8; 3/24,3; 4/2,7 y 5/2,7; mientras que 5 de ellos no fueron transfundidos (13,5%).
En el grupo B, constituido por los pacientes en que sólo se utilizó como fuente de sangre autóloga la sangre del drenaje postoperatorio, pudieron recuperarse y reinfundirse 19 unidades de sangre completa, calculadas de acuerdo con la expresión descrita en métodos. Esto es, se ha conseguido la recuperación de 11.350 ml de sangre (74% de las pérdidas postoperatorias) y la reinfusión de una media de 405 ± 29 ml/pte, lo que ha supuesto una reducción del 60% en los requerimientos de sangre homóloga postoperatoria con respecto al grupo control (0,67 vs. 0,28 U/pte, respectivamente; p < 0,05). En este grupo, la tasa total de transfusión fue de 2,25 U/pte y sólo 4 pacientes (13,8%) evitaron la TSH (tabla 3). Los 25 pacientes restantes (86,2%) recibieron THS además de la ATP y la distribución de las unidades homólogas fue (unidades/% pacientes): 1/34,5; 2/34,5; 3/17,2. Esto es, con respecto al grupo A, aunque no disminuye el porcentaje de pacientes que reciben TSH (efectividad: 13,8%) sí aumenta el porcentaje de los pacientes que reciben sólo una unidad y disminuye el de los que reciben 3 unidades. El rendimiento es esta serie fue del 86,2%, ya que en 4 de los 33 recuperadores instalados no se recogió sangre en cantidad suficiente para ser reinfundida.
La DPSA requerida (2 unidades/paciente) a los pacientes de los grupos C y D fue realizada práticamente en el 100% de los casos, sin que se presentasen efectos adversos, salvo un caso de hipotensión en una paciente, en la que luego se comprobó que presentaba una hemoglobina de 10,5 g/dl previa a la extracción. Un paciente del grupo C donó sólo una unidad, mientras que otro del grupo D donó por error 3 unidades. Ninguna unidad fue desechada por positividad en las pruebas de detección de agentes infecciosos.
En el grupo C se recolectaron 47 unidades de DPSA, de las cuales se reinfundieron 40 (1,63 U/pte; Rendimiento: 85%) y se necesitaron 3 unidades de concentrados de hematíes en 2 pacientes (Efectividad 92%). La tasa global de transfusión en este grupo fue la más baja del estudio con 1,79 U/pte (tabla 3).
En el grupo D, se disponía de 64 U de DPSA y, además, se recuperaron 24 U de los drenajes postoperatorios (14.125 ml; 58% del sangrado postoperatorio). En este grupo, al presentar un mayor sangrado total, además de la administración de 1,90 U/pte de DPSA (61 U; Rendimiento: 95%) y de 428 ± 19 ml/pte de sangre recuperada (0,75 U/pte) fueron necesarias 9 unidades de concentrados de hematíes homólogos, con lo que la tasa media de transfusión fue de 3,03 U/pte (tabla 3). Por ello, en este grupo la efectividad de la autotransfusión fue inferior a la del grupo C ya que 7 pacientes recibieron sangre homóloga (Efectividad:78%).
Discusión
La implantación de un programa de autotransfusión en pacientes de cirugía ortopédica programada debe realizarse teniendo en cuenta las características del paciente, el sangrado previsto en la intervención, la seguridad de la programación quirúrgica y los medios disponibles en el hospital donde se realiza.
En el caso concreto de la cirugía instrumentada de columna lumbar, la información obtenida en el estudio realizado previamente por Sebastián y cols.33 para valorar la calidad de la sangre recuperada del campo quirúrgico y de los drenajes postoperatorios y la revisión de la casuística de este grupo quirúrgico señalaban que: 1) estos pacientes tienen una edad media de 45-50 años, con un sangrado intraoperatorio que se sitúa en 700-900 ml lo que cuestiona seriamente la autotransfusión intraoperatoria como medida coste-efectiva, y un sangrado total de 1.000-1.500 ml que hace que se transfundan una media de 2 U/pte; 2) La Clínica Parque San Antonio, donde se ha realizado este estudio, es una institución privada que permite una seguridad en la programación quirúrgica cercana al 100% y cuenta con un Servicio de Hematología y Hemoterapia, lo que permitía la instauración de un programa de DPSA; y 3) el coste de la unidades de recuperación de sangre ConstaVac CBC II (Striker, USA), cuya facilidad de manejo y seguridad, así como la calidad de la sangre recuperada, ya habían sido constatadas en un estudio previo,34 y la colaboración del personal de UCI de dicho Centro posibilitaban la utilización de la autotransfusión postoperatoria.
En base a estos datos, se inició el programa de autotransfusión con el empleo de los recuperadores post-operatorios (Grupo B, n = 29). Puesto que no se utilizó recuperación intraoperatoria, la postoperatoria se realizó a partir de sangre de drenaje no lavada, sobre cuyo uso existe cierta controversia,19,24 aunque estudios recientes han demostrado que es una excelente fuente de eritrocitos viables y funcionantes.25,33,34
En el grupo control (Grupo A) se transfundieron una media de 1,92 unidades de sangre homóloga/paciente (tabla 3), siendo esta tasa de transfusión menor que la publicada por otros grupos españoles,32 pero similar a la informada por otros autores.18,33,34
En el grupo de pacientes en que se utilizó como fuente de sangre autóloga la sangre del drenaje postoperatorio (Grupo B), la tasa media de transfusión fue de 2.25 U/paciente, sin diferencias significativas con respecto al grupo control (tabla 3). En este grupo, la reinfusión de sangre del drenaje postoperatorio redujo los requerimientos postoperatorios de TSH (0,67 vs 0,28 para los grupos A y B, respectivamente, p < 0,05) y, aunque no disminuyó el porcentaje de pacientes que requirieron TSH (tabla 3), sí redujo el número de unidades transfundidas por paciente y, por tanto, el impacto inmunológico de las mismas.8 En este sentido, convendría recordar que entre las contraindicaciones para el uso de la ATP es la presencia de infección o tumoración maligna en el foco quirúrgico por el peligro de diseminación.41 Sin embargo, dada la importancia que puede tener la asociación de la TSH sobre la recivida tumoral se han desarrollado procedimientos de irradiación o filtrado que permiten la total eliminación de células tumorales con capacidad proliferativa en la sangre recuperada, ya que el lavado de la misma no es suficiente.10,15,16,30 Igualmente, la infección en el foco quirúrgico puede ser una contraindicación relativa siempre que la reinfusión se haga con una amplia cobertura antibiótica y bajo una estrecha vigilancia.20
Los resultados obtenidos con la ATP en este estudio, similares a otros ya publicados para una serie de pacientes intervenidos de columna,4,34 confirman la efectividad de este procedimiento dentro de un programa de cirugía espinal sin sangre, aunque ésta sea menor a la que tiene en cirugía protésica de cadera o rodilla.17 Por ello, se decidió utilizar también la donación preoperatoria de sangre autóloga (DPSA), sola (Grupo C, n = 24) o en combinación con ATP (Grupo D, n = 32).
Para implantar un protocolo de donación preoperatoria de sangre autóloga es necesario decidir, primero, cuantas unidades debe donar el paciente y, segundo, con qué pauta temporal. En este sentido, de acuerdo con los resultados de distintos estudios, el número de unidades de sangre autóloga requeridas para evitar el uso de sangre homóloga en el 80-90% de los pacientes sometidos a cirugía vertebral oscila entre 2 y 4 unidades/paciente.7,18,21,23,26,32,35,36 Con estos datos y la experiencia acumulada en cirugia vertebral lumbar del grupo, se concluyó que el predepósito de 2 unidades sería suficiente para evitar el uso de sangre homóloga en la mayoría de estos pacientes.
El siguiente aspecto de la cuestión radicaba en cúando debería realizarse la DPSA. Generalmente, se acepta una pauta semanal de donación, realizando la última una semana antes de la intervencíon, para estimular la eritropoyesis y permitir que el paciente recuperase, al menos parcialmente, su valores hematimétricos.36 Sin embargo, existen algunos estudios que sugieren que la capacidad inmunodepresora de las transfusiones depende no sólo de su origen alogénico, sino también del tiempo de conservación en el banco por liberación de sustancias bioactivas por leucocitos y plaquetas.28 Dado que la desleucocitación de la sangre previa al almacenamiento como medida útil para disminuir estas complicaciones no ha sido aún implantada, parecía lógica la realización de la DPSA lo más cercana posible a la fecha de la intervención, ya que, además, así se consigue una mayor capacidad de oxigenación de la sangre almacenada.21,25 Finalmente, la donación preoperatoria de sangre autóloga induce una cierta hemodilución que, junto con la mayor capacidad fibrinolítica del plasma autólogo,3 puede contribuir a una menor incidencia de trombosis venosa profunda tras cirugía ortopédica, como se ha demostrado en la cirugía de PTR.2
En base a estos antecedentes, se decidió la implantación de un protocolo mixto consistente en la predonación de una unidad 3-12 días antes de la intervención (7 días en la mayor parte de los casos) y de una segunda unidad 24 horas antes de la intervención, sustituyendo el volumen extraído en esta última mediante una solución cristaloide (Hemodilución normovolémica preoperatoria diferida).21,29
La efectividad de las distintas estrategias utilizadas en el programa de autotransfusión estuvo condicionada por las diferencias en las necesidades transfusionales observadas en los distintos grupos. Estos diferentes requerimientos de reposición hemática pueden explicarse en función del volumen de sangrado que fue significativamente superior en los grupos B y D (tabla 2). Entre las razones que pueden justificar el mayor sangrado, podrían incluirse un mayor número de niveles artrodesados y una mayor duración de las intervenciones en estos grupos con respecto a los grupos A y C, aunque la diferencia no ha sido significativa; una mayor incidencia de estenosis de canal, sobre todo con respecto al grupo A, y una mayor incidencia de reintervenciones en estos grupos. Condiciones todas ellas que hacen aumentar el sangrado intraoperatorio (tabla 1). El mayor sangrado intraoperatorio no es atribuible a la llamada «curva de aprendizaje» puesto que este grupo viene utilizando esta instrumentación desde 1995, del mismo modo que el aumento del sangrado postoperatorio del grupo D no puede ser atribuido a la reinfusión del drenaje, puesto que en el grupo B no se produce.
Por otra parte, otro factor que ha influido en la tasa de transfusión ha sido la presencia de una relación varones/mujeres en el grupo D (0,52) menor que la de los grupos B (0,93) y C (1,40), aunque similar a la del grupo A (0,61) (tabla 1). Las mujeres, dada su menor corpulencia y su mayor proporcion de grasa corporal, presentan un volumen circulante menor (4-4,5 l) que el de los varones (5-6 l), lo que hace que toleren peor una misma pérdida hemática.27 Así mismo, las mujeres presentan niveles de hemoglobina más bajos que los varones y, por tanto, el predepósito induce en ellas una mayor hemodilución, lo que puede llevar aparejado una mayor tendencia al sangrado, dado el papel hemostático de los hematíes sobre las plaquetas. Esta mayor incidencia de mujeres en el grupo D, es importante al valorar el promedio de transfusiones realizadas en este grupo. Todo lo contrario ocurre en el grupo C, en el que se conjugan una mejor ratio varones/mujeres y un menor número de reintervenciones, para hacer de él el grupo menos transfundido.
En conclusión, a la vista de los datos mostrados en la tabla 3 y de acuerdo con los resultados recopilados en una revisión reciente, puede concluirse que el programa de DPSA implantado ha conseguido unas cotas de efectividad (84%) similares a las obtenidas en ésta y otras modalidades de cirugía ortopédica, tanto en estudios realizados en España (87%) como en el extranjero (91%), pero con un rendimiento superior (89, 74 y 60%, respectivamente).24
No obstante estos buenos resultados, se considera que aún sería posible mejorar el programa de DPSA con una mejor selección de los pacientes teniendo en cuenta peso, sexo y hemoglobina preoperatoria, así como el tipo de intervención y el sangrado previsto.9,27,31 Así mismo, consideramos que la combinación de DPSA con ATP podría ser útil en aquellos casos en los que no pueden recolectarse el número de DPSA requeridas o se desea disminuir el número de éstas y en aquellos en los que se espera un sangrado postoperatorio abundante.11
Finalmente, dado el reducido número de pacientes estudiados, no se ha podido observar diferencias significativas en la aparición de complicaciones infecciosas postoperatorias entre los distintos grupos, si bien su incidencia es menor que la de otros estudios,5,13,37 ni en la duración de la estancia hospitalaria, aunque la evolución subjetiva de los pacientes ha sido mejor en los grupos autotransfundidos. Se necesitan estudiar series prospectivas más largas para valorar adecuadamente estos aspectos.