Muchos de los mecanismos del desarrollo embrionario se pierden al llegar al estado adulto, aunque se conserva cierta capacidad regenerativa que va desde la cicatrización de heridas, a la regeneración estructural y funcional de algunas partes del cuerpo. La capacidad que tienen algunos vertebrados inferiores para regenerar tejidos especializados y órganos1,2 permite estudiar ciertas capacidades regenerativas en los organismos superiores mientras se conservan otras.
La regeneración puede desencadenarse por dos mecanismos: la desdiferenciación de células ya diferenciadas capaces de multiplicarse y diferenciarse ulteriormente en otras estirpes celulares, y la existencia de células madre que permanecen sin diferenciarse desde la época embrionaria para ser usadas con posterioridad. Ambos caminos están regulados por moléculas como factores de crecimiento, citoquinas, hormonas, etc.
La reparación ósea es un auténtico proceso regenerativo, pues hay una serie de factores endógenos y exógenos3,4 que conducen a la formación de un blastema de reparación por activación de células madre que formarán un callo por un proceso semejante al desarrollo embrionario, dejando finalmente la estructura reparada en forma y tamaño5.
A veces, el fallo de una respuesta da lugar a un fracaso total, expresado como retraso en la consolidación, o bien, como no consolidación o pseudoartrosis6. Resecciones óseas amplias o enfermedades genéticas como la osteogénesis imperfecta, causadas por una mutación del gen que codifica para el colágeno I7, interfieren en la biología normal del hueso, y por tanto en su reparación.
Estos problemas, salvo los de origen genético, son la suma de una falta de células madre o de algún factor bioactivo que regule alguno de los pasos que suponen su discurrir por el linaje osteoblástico. De todas las posibles alteraciones contenidas en esas dos causas generales, hoy sólo sabemos con certeza que el número de células madre del linaje osteogénico disminuye con la edad de forma muy significativa8.
Las falta de células, la deficiencia de factores de crecimiento y la incapacidad genética permiten adivinar que los caminos a seguir para la mejora de las diferentes situaciones patológicas podría ser:
1) Ante la escasez de células madre se pueden seleccionar las existentes, amplificarlas (multiplicarlas) in vitro y reinyectarlas en los lugares en los que se las necesita9.
2) Ante la deficiencia de factores de activación, las propias células madre cultivadas y amplificadas in vitro podrían ser inducidas ex vivo para posteriormente introducirlas, con su programa osteogénico corregido, en los lugares y pacientes que precisan la reposición de la facultad osteogénica perdida10,11. También puede actuarse, identificados los factores deficientes, haciendo llegar los mismos a los lugares donde las propias células del huésped podrían ser inducidas12.
3) Las deficiencias genéticas podrán ser tratadas transfectando las células osteoprogenitoras, in vivo o ex vivo, con vectores que pueden ser diseñados para que transporten el gen normal de la deficiencia13-15 (fig. 1).
Figura 1. Esquema que representa la terapia celular y génica que puede llevarse a cabo a partir de células de médula ósea. De estas células extraídas de un paciente aquejado de alguna patalogía esquelética se aíslan las células madre mesenquimáticas y se multiplican in vitro. Estas células pueden transfectarse con un gen para compensar una capacidad perdida, tras lo cual pueden reinstalarse en el mismo individuo para que restablezcan esa incapacidad (parte izquierda del esquema). De la misma forma, las células amplificadas pueden inducirse hacia el linaje osteogénico mediante agentes bioquímicos. Después pueden transferirse, con el material osteoconductor apropiado, a las lesiones esqueléticas correspondientes (parte derecha del esquema). FC: factores de crecimiento; BMP: proteína morfogenética ósea.
En la acumulación de conocimientos en los aspectos reseñados está la clave para un mejor entendimiento futuro de las distintas patologías óseas16.
Células madre, factores de crecimiento y materiales osteoconductores
El aislamiento y cultivo in vitro de las células madre mesenquimáticas (CMM) ha abierto la posibilidad de estudiar los mecanismos celulares y moleculares básicos de la mesengénesis (diferenciación celular a partir de MSC para dar todos los tipos celulares mesenquimáticos) y de desarrollar toda una tecnología que permita el uso clínico de estas células en clínica9,17,18.
La reparación ósea supone un auténtico proceso regenerativo sobre el que se están produciendo importantes avances. Esta reparación supone la organización de un blastema constituido por células capaces de proliferar y diferenciarse en el camino adecuado (fig. 2). Las CMM19-21 pueden encontrarse como pobladoras habituales de diferentes tejidos mesenquimáticos, sobre todo y como lugares más accesibles, el periostio y la médula ósea (MO)9, no habiéndose aclarado si las CMM adquieren el fenotipo de cada tejido antes de salir de estos lugares o después de llegar a cada microambiente tisular, así como tampoco si son éstas las únicas fuentes de células progenitoras de los tejidos mesenquimáticos.
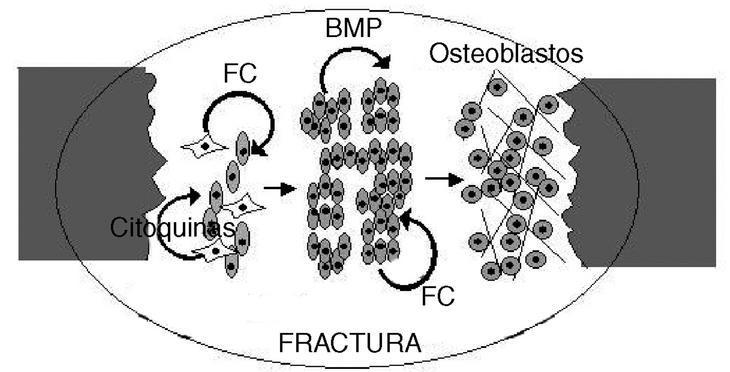
Figura 2. Reparación y regeneración ósea. La fractura de un hueso dispara la síntesis de factores de crecimiento y citoquinas, probablemente en las células estromáticas de la médula (células estrelladas). Estas sustancias estimulan a las células osteoprogenitoras (las células ovaladas aparentan ser células madre mesenquimatosas) a producir proteínas osteoinductoras (factores de crecimiento [FC] y proteína morfogenética ósea [BMP]). Estas proteínas inducen la proliferación y diferenciación de tales células, dando lugar primero a un blastema regenerativo, del que se diferenciará el linaje osteoblástico (células redondeadas) que reconstruirá el tejido óseo.
El aislamiento de CMM a partir de la MO, donde también se encuentran las células madre de la línea sanguínea, ha dado lugar a la distinción, dentro de la médula, entre el tejido hematopoyético y el no hematopoyético, este último ubicado en el estroma. Se ha comprobado que existe una independencia entre los procesos hemo y no hemopoyéticos22,23, aunque no se descarta cierta interrelación21. De este modo, los vertebrados conservarían la capacidad de reparar sus huesos, cartílagos, tendones, músculos, el propio estroma medular, el tejido adiposo y cualquier tejido conectivo, a partir de las CMM residentes fundamentalmente en la MO17, cuya diferenciación está regulada por factores de crecimiento (FC) (fig. 3).
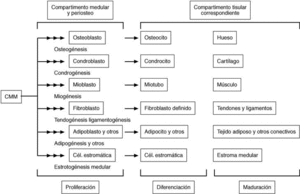
Figura 3. En este esquema se representan los linajes celulares del proceso mesengénico procedentes de una célula madre mesenquimatosa (CMM) de médula ósea o periostio. Los precursores de cada linaje iniciarían su procesamiento (proliferación y primeras etapas de su diferenciación) en la propia médula, para terminarlo en la ubicación tisular correspondiente a cada tipo, donde adquirirían su maduración definitiva. Hoy día no se descarta la presencia de tales céulas madre en otras localizaciones del individuo adulto, como otros tejidos conectivos y sangre periférica y del cordón umbilical, además, naturalmente, del embrión. Esquema adaptado de Caplan20.
Los FC son moléculas polipeptídicas que sintetizan las células, cuya misión general es transmitir señales entre unas células y otras para modular su actividad. Si bien el término «factores de crecimiento» se presta a confusión, ya que no todos afectan al crecimiento celular, está universalmente aceptado en sentido general, para referirse a aquellas moléculas que estimulan o inhiben la división celular, su diferenciación, la migración y expresión génica. Otras moléculas que forman grupos separados, aunque afectan a las mismas funciones, son las hormonas polipeptídicas y las citocinas. Las primeras son aquellas sustancias que se producen en glándulas endocrinas, se transportan por la circulación sanguínea y ejercen su acción a cierta distancia. El término citocina o citoquina en la práctica se reserva para este tipo de sustancias que están implicadas en la biología del sistema inmune24,25.
Los diferentes tipos de FC realizan su misión a determinadas concentraciones mediando receptores específicos en las células diana. Pueden actuar de manera autocrina, paracrina, endocrina, yuxtacrina, intracrina o mediada por componentes de la matriz extracelular. Las principales familias de FC se agrupan bajo los nombres TGF-β (Transforming Growth Factor), EGF (Epidermal Growth Factor), NGF (Nerve Growth Factor), PDGF (Plateled Derived Growth Factor), FGF (Fibroblast Growth Factor) e IGF (Insuline-like Growth Factor).
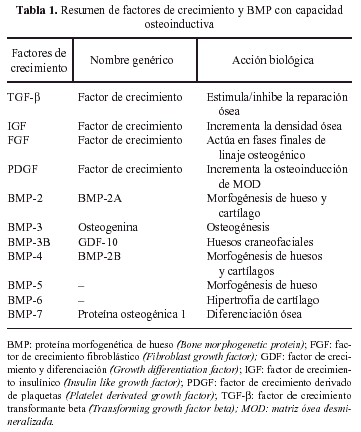
Estas familias de FC constituyen un extenso número de tipos y subtipos que se ve cada día aumentado por la descripción de algún nuevo componente. De todos ellos han sido varios los implicados en la reparación ósea, aunque no todos con la misma intensidad e importancia. A los IGF, PDGF, FGF y TGF-β les ha sido reconocida alguna acción en este proceso. A todos ellos hay que añadir un grupo de agentes bioactivos con personalidad propia: las proteínas morfogenéticas de hueso (BMP), las cuales, aunque genéticamente pertenecen a la familia de los TGF-β, tienen una capacidad osteoinductiva ampliamente demostrada26. La tabla 1 resume los factores de crecimiento y BMPs con capacidad osteoinductora 25,27-31.
De todos los datos presentes en la literatura, quizás emergen dos hechos claramente contrastados: los TGF-β estimulan la proliferación y reclutamiento de precursores osteoblásticos en los lugares de reparación y, por el contrario, parecen ser menos necesarios, o incluso inhibir, los últimos pasos del proceso32. Otro hecho interesante, aportado recientemente, es la posibilidad de un cierto sinergismo entre TGF-β y BMPs; los primeros serían ciertamente necesarios, sobre todo como mitogénicos y puede que también como inductores de CMM, mientras que en las últimas etapas de la osteogénesis necesitarían el concurso de BMP, razón por la cual, en experimentos in vitro, la presencia exclusiva de TGF-β podría tener un efecto inhibitorio, al no ocurrir ese sinergismo natural detectado33, 34.
El uso terapéutico del TGF-β es más un deseo que una realidad. Las inyecciones subperiósticas de este factor o su aplicación directa en fracturas han dado como resultado, a veces, incrementos en la formación de huesos y mejoría en la estabilidad mecánica. La difícil evaluación de resultados da lugar a una gran variabilidad35. Todo ello determina la necesidad de más investigaciones que clarifiquen la acción de los TGF-β en la osteogénesis, antes de poder extender su uso terapéutico.
Proteínas morfogenéticas del hueso
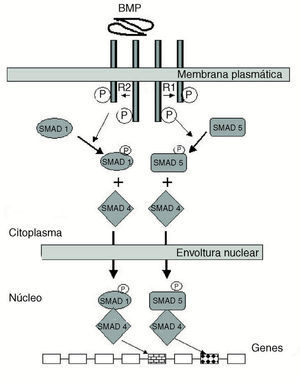
El trabajo de Urist36 en 1965 debe ser considerado como el que inició lo que hoy es un mundo complejo de proteínas que regulan los más variados procesos morfogenéticos en animales. La capacidad osteogénica que Urist encontró ligada a la matriz ósea desmineralizada (MOD) dio lugar a que se postulara que en la matriz orgánica del hueso deberían encontrarse factores, seguramente proteicos, capaces de inducir en las células vecinas su encauzamiento hacia el linaje osteogénico. Nació entonces lo que hoy es una superfamilia de productos génicos con capacidad de regulación pleiotrópica, es decir, que tienen acción en múltiples funciones: quimiotaxis, mitosis, diferenciación, apoptosis, etc.37 Por técnicas moleculares se han identificado y clonado diversos componentes de la familia, que incluye en mamíferos desde el BMP-2 al BMP-1626, cuyas acciones biológicas van más allá de la morfogénesis ósea: desarrollo del corazón, riñón, mantenimiento de tejidos adultos, inducción mesodérmica, gastrulación, etc. El mecanismo de acción general de las BMPs se ejerce a través de los receptores de membrana (BMPR-I y II) induciendo en el núcleo de la célula la activación de la maquinaria transcripcional. La complejidad de la respuesta intracelular inducida por la unión de las BMPs a sus receptores, a través de las proteínas Smad, está lejos de ser entendida en su totalidad38 (fig. 4).
Figura 4. Receptores de las proteínas morfogenéticas óseas (BMP). Representación esquemática de la cascada de acontecimientos moleculares que tienen lugar en las células tras la unión de BMP a sus receptores transmembranales I y II. El receptor II provoca la fosforilación del I. La cooperación entre ambos receptores desencadena la señal de transducción citoplasmática a través de los sustratos SMAD-1, 4 y 5, respectivamente, los cuales entran en el núcleo de la célula y desencadenan la respuesta génica correspondiente. SMAD: proteínas Smad.
La presencia de BMPs en la reparación de las fracturas está documentada39. BMP-2, BMP-4 y BMP-7 se expresan tanto en la osificación intramembranosa como endocondral, con diferente intensidad espacio-temporal40,41. La presencia de BMPs en la reparación ósea y su capacidad osteoinductiva está probada por varios procedimientos experimentales. Las pruebas realizadas en animales han demostrado que la inyección de BMP-2 recombinante humano (rhBMP-2) en fracturas de fémur de rata acelera el proceso de reparación, sin alterar significativamente la secuencia de acontecimientos5. La misma proteína, utilizada con colágeno como soporte y transportador en osteotomías de cúbito de conejo, propició una aceleración de la reparación frente a los controles. Resultados similares se han obtenido con BMP-7 en diferentes modelos experimentales42,43.
Estos resultados experimentales han disparado la puesta en marcha de experimentos clínicos en humanos, aunque preliminares44.
Clásicamente se viene utilizando el autoinjerto como la mejor manera de reparar un defecto óseo incapaz de repararse por sí mismo. El tejido óseo colocado en un entorno óseo vivo, bien vascularizado y en circustancias biomecánicas favorables, es rápidamente colonizado por células incorporadas al hueso trasplantado. El injerto actúa como osteoinductor y como osteoconductor. De la osteoinducción son reponsables los factores (difusibles o no) de la matriz que influyen en las células vecinas, mientras que de la osteoconducción se encargan los componentes estructurales (colagénicos y/o minerales) del hueso.
La cualidad osteoconductora de la matriz ósea se ha tratado de mimetizar con sustancias biológicas o artificiales, que han dado lugar a la fabricación de materiales con la textura y la porosidad del hueso25,45-49.
Modelos experimentales: procesamiento in vitro de células osteogénicas
El progreso en el estudio de la biología del tejido óseo pasa por la conjunción de varios factores y circunstancias: células competentes, biofactores osteoinductores y materiales osteoconductores, unidos a un determinado microambiente tisular, sin olvidar el sometimiento a las condiciones biomecánicas propias de cada localización particular. El fallo de alguno o varios de ellos conduce al fracaso del proceso en las situaciones patológicas o traumáticas conocidas.
El manejo de esos «factores y circunstancias» nos irá proporcionando las claves para el control del proceso. Dentro de los avances habidos estos últimos años en el manejo de CMM in vitro, nuestro grupo ha desarrollado un sistema experimental para la capacitación osteogénica de dichas células50,51.
Mardon et al52, en 1987, demostraron la capacidad de formación de hueso por las células del estroma de la MO. Su implantación en animales vivos en cámara de difusión, que aprovechan los factores humorales del huésped pero impiden la entrada de células del mismo, da lugar a la formación de hueso en el interior de dichas cámaras. No obstante, el cultivo in vitro de estas células no conduce a la diferenciación osteogénica, salvo que se añadan «agentes» externos. La adición a los cultivos de dexametasona y la suplementación con β-glicerofosfato (β-GF) como fuente exógena de fosfato53, o bien la adición de «agentes bioactivos» primitivamente aislados de la matriz ósea desmineralizada54, ha dado lugar a la inducción de diferenciación osteogénica en dichos cultivos, manifestada por cambios morfológicos y expresión de marcadores de hueso, como fosfatasa alcalina, colágeno I, osteocalcina, deposición de calcio, etc.
El uso combinado de dexametasona, β-GF y polvo de MOD, ha permitido diferenciar dos poblaciones celulares en los cultivos de MO de rata, una que crece y se diferencia en la primera semana de cultivo y otra que lo hace en la segunda y tercera semanas. Cuando las células proceden de animales viejos esta distinción desaparece paulatinamente, mostrándose que sólo la segunda de las poblaciones queda con capacidad de inducción osteogénica. Con ello se demostró que las células de MO con capacidad osteogénica disminuyen selectivamente con la edad, viendo que esa población puede ser amplificada in vitro e inducida a expresar marcadores óseos cuando se pone en contacto con factores movilizados de la MOD54.
En un intento de hacer una catalogación molecular de las CMM en distintos estadios de cultivo a lo largo del linaje osteoblástico, Bruder et al han obtenido diferentes anticuerpos monoclonales que reaccionan con la superficie de las CMM humanas en diferentes estadios de dicho linaje55. Los anticuerpos pueden usarse para localizar CMM y su progenie durante el desarrollo de huesos largos y del cráneo.
A medida que se van aislando y caracterizando las moléculas que participan en la osteogénesis, la mayoría de ellas presentes en la MOD, usada indiscriminadamente como agente osteoinductor, tanto in vitro como in vivo, se va diseccionando cuidadosamente el proceso. El TGF-β1 y varias BMPs son las más estudiadas, aunque no siempre con resultados coherentes. El efecto del TGF-β1 sobre la diferenciación osteoblástica in vitro es el que está produciendo resultados más conflictivos y, a veces, contradictorios.
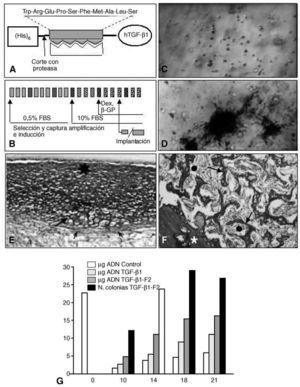
A finales de los años ochenta una serie de trabajos demostraban que el TGF-β1 puede tener un efecto estimulante de la proliferación y expresión de marcadores propios de diferenciación ósea, en diferentes tipos celulares cultivados in vitro; otros demostraron su efecto contrario, es decir, inhibición de la expresión de fosfatasa alcalina, osteonectina y osteocalcina, así como falta de efecto sobre la proliferación celular. Tampoco faltan trabajos que achacaron estos resultados a un posible efecto bifásico del TGF-β no bien estudiado o a diferencias en los resultados, probablemente debidas a cambios en las condiciones de cultivo56. Nuestro grupo50 ha demostrado que el TGF-β1 tiene, sobre todo, efecto mitogénico y formador de colonias sobre células de MO cultivadas en geles de colágeno, siendo escasa pero apreciable la capacidad de esas células para expresar marcadores óseos. Estas capacidades del TGF-β1 se magnifican cuando se usa un TGF-β1 al que se le añade un dominio molecular de unión específica al colágeno I (TGF-β1-F2). Estas células expandidas e inducidas in vitro bajo el influjo de este factor, llegan a producir tejido cartilaginoso y óseo cuando se las implanta en animales en cámaras de difusión11,50 (fig. 5).
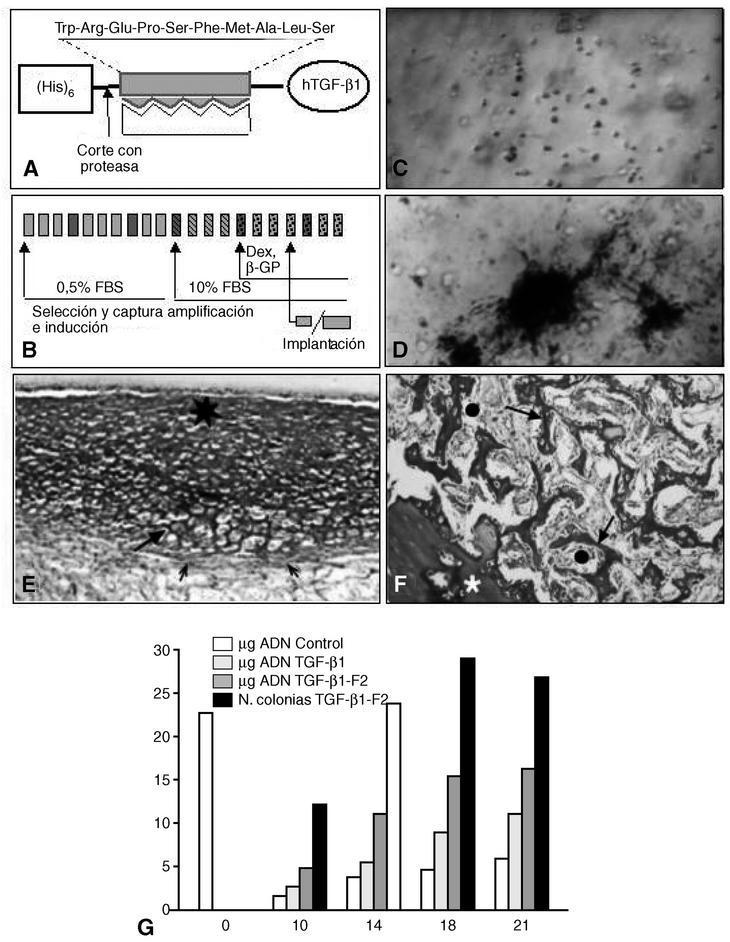
Figura 5. Capacitación de células osteogénicas. (A) Construcción molecular de un TGF-β1 recombinante humano con un dominio molecular de unión al colágeno I (rhTGF β1-F2) expresado en E. coli. (B) Las células de médula ósea se cultivan in vitro para seleccionar y capturar las CMM, amplificarlas e inducirlas hacia el linaje osteogénico, mediante factores de crecimiento y/o BMP. Cada recuadro representa un día de cultivo; los recuadros más oscuros representan el cambio de medio. (C) Células de médula ósea cultivadas durante la fase de amplificación (×50; en fresco. Contraste de fase). (D) Colonias mineralizadas al final del período de inducción. Las células fueron tratadas con rhTGF-β1-F2 (× 50; Von Kossa). (E) Las células implantadas in vivo en cámaras de Millipore forman nódulos con aspecto cartilaginoso (flecha grande) u osteoide (asterisco). Las flechas pequeñas representan la envuelta fibrilar de los nódulos (pericondrio) (×80; rojo sirio-hematoxilina). (F) Las células implantadas in vivo en cámaras de MOD forman trabéculas óseas típicas (flecha grande), entre las que quedan espacios ocupados por tejido medular (círculos). El asterisco representa la pared de la cámara (×70; rojo sirio-hematoxilina). (G) A lo largo de los días de cultivo el número de células evoluciona como se expresa por la cantidad de ADN, según las condiciones de cultivo. Sólo en presencia de rhTGF-β1-F2 se forman colonias, que indican un mayor grado de diferenciación.
Las BMP-2 y BMP-7 (OP-1) han demostrado ampliamente su capacidad para promover diferenciación osteoblástica in vitro57,58. En algún caso se ha demostrado incluso la existencia de dos poblaciones celulares en la MO cuando se les aplica BMP-2 y dexametasona in vitro. Una de rápida diferenciación, y otra que precisa la exposición a los factores inductores durante más tiempo. Estos resultados concuerdan con nuestros trabajos50,51, en relación con la inducción ejercida por las partículas de MOD sobre células de MO54. Otras BMPs, sobre todo, BMP-3, 4 y 6, sin olvidar otros FC (FGF, IGF y PDGF), han mostrado diferentes efectos sobre osteoinducción y diferentes tiempos de expresión durante la reparación ósea59,60.
El proceso regenerativo que subyace, por tanto, bajo la osificación o la regeneración ósea, es un proceso multimodulado en el que las células osteogénicas responden a distintos factores y circunstancias, desde el estadio de células madre multipotenciales. La dirección molecular de dicho proceso y la profundización en el conocimiento del control de la expresión genética para dichos factores son el futuro de la aplicación clínica de tales avances.
PERSPECTIVAS TERAPÉUTICAS
Los conocimientos sobre la caracterización, clonación, expresión y purificación de varias BMP han propiciado su utilización directa en casos clínicos concretos donde se necesita un estímulo osteogénico suplementario, con resultados dispares pero alentadores5,43.
Esta aplicación, no obstante, plantea problemas como son la falta de control sobre el tiempo que la proteína administrada permanece en la lesión, actividad de la misma y necesidad de células osteogénicas o los efectores últimos de la acción inductora en el lugar de aplicación. Consecuentemente, en aquellos casos en los que la falta de células sea el problema fundamental, la aplicación directa y esporádica de factores osteoinductores no producirá los resultados esperados61. Por ello, una línea de trabajo actual con gran proyección futura consiste en el aporte de células osteoprogenitoras a los lugares necesitados de reparación, bien directamente, o a través de un transportador, sin descartar la posibilidad de inyección sistémica en determinadas condiciones.
A finales de los años noventa se han empezado a utilizar de modo experimental las CMM cultivadas y manipuladas ex vivo para su uso en reparaciones óseas9,21. Los avances más significativos se han obtenido cultivando y multiplicando in vitro CMM procedentes de médula ósea embebidas en cilindros de hidroxiapatita (HA) de uno u otro tipo y colocadas en defectos segmentarios.
Los resultados conseguidos por este procedimiento mejoran a los obtenidos con la utilización directa de las BMPs adsorbidas sobre HA, aunque, en cualquier caso, no se asegure que ésta quede infiltrada de hueso nuevo tras 12 semanas de implantación. Además de estos resultados, parcialmente satisfactorios, debe tenerse en cuenta que, en muchas de las situaciones en las que se producen defectos de la osificación en la clínica humana, se dan también trastornos metabólicos generales o locales que se traducen, no sólo en una falta de células osteocompetentes, sino también en una deficiente presencia de factores bioactivos.
El conocimiento de todos los detalles celulares y moleculares de este proceso, unido al desarrollo del material osteoconductor apropiado para cada circunstancia, permitirá el avance de una auténtica bioingeniería tisular que ofrecerá inmensas posibilidades terapéuticas.
Un futuro próximo será el desarrollo de lo que hoy ya es un hecho en otros campos, la terapia génica, adaptada a las circunstancias propias de este caso. Es posible transfectar (cambiar unos genes por otros) los cultivos de CMM expandidas (multiplicadas en su número), con genes específicos que tratan de sustituir un gen anómalo, como el de la osteogénesis imperfecta, o reparar una función perdida en estas células como puede ser la expresión de BMP o FC, como los β transformantes (TGF-β), mediante la inserción del gen activo o el fragmento activador correspondiente. La reinyección de estas células modificadas en el mismo huésped del que proceden podrá restablecer la disfunción padecida.
La terapia génica también puede aplicarse in vivo, por ejemplo, en una fractura, transfectando las células in situ mediante la introducción directa del fragmento de ADN deseado en un vector, a través de una matriz activada, como el colágeno. Por este procedimiento el gen transfectado se incorpora al núcleo de las células de la fractura, las cuales transcriben la proteína para la que se introdujo el gen, elevando localmente la concentración de la misma. Este procedimiento es menos eficaz que la transfección ex vivo, a la vez que menos controlable, pero en ambos casos existen experimentos piloto que avalan sus posibilidades terapéuticas a costes muchos más bajos que la producción de proteínas recombinantes para su uso directo62-64. El hecho de que las células transfectadas permanezcan en el huésped poco tiempo (algunas semanas), lejos de ser un inconveniente como lo es en otros tratamientos, en reparación ósea puede coincidir con la desaparición de su necesidad una vez concluido el proceso.
Una mención especial merece el uso de este procedimiento para el tratamiento de la osteoporosis. En la medida en que esta es una enfermedad sistémica en la que se produce un desequilibrio entre formación y reabsorción ósea, en perjuicio de la primera, se puede teorizar que el suministro sistémico de células osteocapacitadas in vitro en tales enfermos podría reacomodar la ecuación ósea en el camino de la normalización. Se trataría de cultivar las CMM del paciente, multiplicarlas y osteoinducirlas ex vivo para reinstalarlas en el enfermo con la esperanza de que repueblen el tejido óseo del mismo. El descubrimiento de una secuencia peptídica de la sialoproteína de hueso (BSP) mediadora de la unión específica de los osteoblastos a la hidroxiapatita, podrá ayudar en la orientación de las células reinyectadas hacia el tejido óseo65.
Así pues, según progrese nuestro conocimiento el proceso multirregulado de la reparación ósea podrá ser remediado con la aportación de los factores bioactivos apropiados en el momento pertinente. Una alternativa a la inyección directa podría incluir la colección de MO, seguida de una selección, multiplicación y estimulación de sus CMM hacia la vía osteogénica, mediante FC y/o BMP in vitro. Estas células comprometidas pueden ser reimplantadas, con material osteoconductor apropiado, en las áreas a reparar.
En humanos, mientras el número de células madre hematopoyéticas varía muy poco con la edad, el de CMM varían enormemente; si en el recién nacido se encuentra una CMM por cada 10.000 células de médula ósea, a los 80 años de edad, sólo se puede encontrar una por cada dos millones23. La respuesta a la implantación de médula ósea desmineralizada decrece en ratas viejas, siendo estimulada por la administración de células osteoprogenitoras singénicas66.
El descenso de la actividad anabólica observada en huesos de individuos de más edad no es debido únicamente a la incapacidad de los osteoblastos y sus progenitores a progresar, puesto que éstos lo hacen en cultivo54,67. Con la edad disminuye enormemente el número de células susceptibles de diferenciación osteoblástica, además de apreciarse una cierta dificultad de progreso por falta de factores e incapacidad de las propias células para responder a los mismos.
El aislamiento de CMM y su tratamiento ex vivo con TGF-β propicia una gran población de células, que forman colonias, cuya inducción a diferenciarse hacia el linaje osteoblástico mediante BMP llevaría a una población de osteoblastos muy superior a la inicial, siendo ésta una forma eficaz de promover la osteogénesis. Conocemos la capacidad osteoinductiva de varias de ellas (BMP-2, 3, 4, 6 y 7) en distintas condiciones experimentales, su expresión durante el proceso normal de reparación ósea, pero ignoramos la distribución espacio-temporal de los factores en el proceso de regeneración del hueso para actuar con precisión.
En nuestro trabajo50, de selección, amplificación (multiplicación) y diferenciación de CMM basado en la acción de morfógenos (sustancia química capaz de provocar una respuesta biológica) y en el cultivo de las células en geles de colágeno, hemos obtenido interesantes resultados utilizando un FC modificado con un dominio molecular de unión específica al colágeno I, como es el TGF-β1-F2 recombinante humano para controlar mejor su tiempo de actuación. De nuestros resultados, se deduce que con el rhTGF-β1-F2 se selecciona una población celular que prolifera más activamente y forma colonias capaces de mineralizarse, y al implantarlas in vivo dan lugar a cartílago y sustancia osteoide en cámaras de difusión, y a hueso en cámaras de MOD11. De aquí puede inferirse que lo que les falta a las células seleccionadas y amplificadas por el rhTGF-β1-F2, se lo aporta la matriz ósea desmineralizada y las BMPs. Parece lógico, por tanto, avanzar la hipótesis de la necesidad de selección y amplificación celular mediante rhTGF-β1-F2 y osteinducción con rhBMP de forma sinérgica.
Una aplicabilidad inmediata de la ingeniería tisular a la cirugía ortopédica y traumatología del raquis podría centrarse en la consecución de artrodesis en las inestabilidades. La artrodesis posterolateral intertransversa (API) es el tipo de fijación intervertebral más frecuente para la columna lumbar degenerativa, fenómeno que suele ocurrir en edades avanzadas de la vida. El fracaso de la fusión alcanza el 35% de no consolidaciones, y en la morbilidad de la zona donante cuando se utiliza autoinjerto, lo cual llega a ocurrir en el 30% de los pacientes68,69.
La utilización actual de autoinjertos o aloinjertos en cirugía raquídea presenta ventajas e inconvenientes. El aloinjerto permite disponer de una cantidad ilimitada, con riesgo de contagio muy reducido. Sin embargo, el inconveniente fundamental consiste en la incorporación mucho más lenta y de menor cuantía que la que poseen los autoinjertos, siendo los injertos congelados en fresco aún mucho más inmunogénicos70.
Como alternativas al autoinjerto se han probado experimentalmente las BMP68,71. La combinación de un material osteoconductor, como el hueso desmineralizado, con un osteoinductor, como las BMP, se está configurando hoy como la base de esta nueva forma de estimular la osteogénesis, en el caso de la artrodesis posterolateral72. El osteoconductor ideal debe ser un material biocompatible, de fácil disponibilidad, que no produzca compresión muscular debido a su tamaño, amoldable a la zona posterolateral de la columna y capaz de permitir la rápida invasión de células mesenquimáticas, reabsorbiéndose y remodelándose a medida que el hueso neoformado va madurando68, entre otras razones por el referido problema de espacio.
En clínica una alternativa consiste en instrumentar solamente un lado e introducir el material promotor de la osteogénesis sin provocar así compresión musculocutánea. La instrumentación unilateral, sin embargo, presenta serios incovenientes, como la tendencia de la barra a romperse cuando la instrumentación se extiende hasta la región lumbar, con mayor frecuencia que cuando lo hace solamente a nivel torácico73,74.
Pero además del problema de espacio, los modelos experimentales actuales son muy incompletos y con diseños metodológicos de escasa calidad72,75. Los estudios en conejos no utilizan instrumentación de osteosíntesis, además realizan la fusión en un solo nivel, lo cual es excesivamente favorable dada la facilidad del conejo para la osteogénesis. La baja edad del conejo y, por tanto, su proclividad a la osteogénesis tampoco sitúa el experimento en condiciones de inferir conclusiones72. No obstante, los estudios más recientes sobre experimentación animal siguen esta línea76.
Los trabajos en primates77 para estudiar la eficacia de la rhBMP-2 administrada mediante un transportador, se realizan sobre muestras muy pequeñas. Por último, los estudios en humanos78 añadiendo cerámica como osteotransportador no tienen en cuenta las variables para un tamaño muestral adecuado, no diseñan los grupos experimentales adecuadamente y se utiliza una combinación de hueso autólogo con aloinjerto a los que se añaden bloques de cerámica. Los autores, en definitiva, concluyen que no es necesario añadir injerto de cresta ilíaca cuando se dispone de un transportador como la cerámica de fosfato cálcico bifásico.
Así pues, los planteamientos actuales para conseguir artrodesis ósea raquídea están enfocados a la combinación de instrumentación junto con diversas formas de promover la osteogénesis. Sin embargo, según se ha dicho, la estrategia más adecuada sea añadir FC al foco de fusión y células madre en cantidad suficiente, capacitadas in vitro con FC que las induzcan a diferenciarse en células osteoprogenitoras con estabilidad primaria lo más rígida posible. La experiencia quirúrgica ha mostrado que las células fabrican hueso sobre hueso, por lo cual es fundamental la preparación meticulosa del lecho receptor. La posibilidad de transferir las células capacitadas en una suspensión de colágeno líquido, poco inmunogénico, que gelifica a la temperatura corporal, mezclado con fragmentos de material osteoconductor reabsorbible, previamente infiltrado también de las mismas células, parece interesante a priori.
La aplicación de los FC como método de mejorar la osteointegración está poco estudiado en las artroplastias. Para conseguir una fijación duradera, en las artroplastias de cadera y rodilla no cementadas, es necesario un proceso de reparación ósea donde, tras la estabilización mecánica del implante mediante fijación rígida (estabilidad primaria) aparezca una fijación suficiente consistente en una verdadera fusión tisular entre el implante y el hueso, estabilidad secundaria80-82. Existen trabajos aislados, como los de Lind et al83, que evalúan los efectos de la OP-1 colocada en defectos óseos de 3 mm con y sin HA. La OP-1 aumenta la fijación mecánica de los implantes de HA sobre el colágeno o control, estimulando tres veces más la osteointegración y la osificación en el espacio, si se compara con el control, aunque no hubo diferencia con los tratados con matriz colagénica.
PROBLEMAS METODOLOGICOS EN LA TRANSFERENCIA DE RESULTADOS
Antes de plantear la transferencia de resultados de la ingeniería tisular ósea a la clínica humana conviene establecer tres aspectos fundamentales que no se deben olvidar.
1) Nivel celular y molecular. Según se ha expuesto, la capacidad de regeneración del tejido óseo no depende de los FC en sí mismos sino de las células osteoformadoras. Los FC no forman hueso, sino que regulan la multiplicación y diferenciación de las células que por sí, o mediante sus descendientes, producirán la sustancia osteoide. Por tanto, es mucho más importante para el resultado biológico la concentración definitiva de células osteogénicas que la presencia de FC, aun siendo ésta importante para la acción de aquéllos.
Deben seguir buscándose nuevas fuentes de FC de acceso más fácil y menos cruento que la MO. La singular arquitectura del tejido óseo propicia el desarrollo del mundo de los materiales biosintéticos osteoconductores. Este camino permitirá no sólo mejorar la reparación ósea de cualquier etiología, sino que hará posible la «fabricación» ex vivo de piezas óseas de un determinado tamaño que serán de gran utilidad para afrontar reparaciones postraumáticas de cierta extensión.
2) Biomecánica y microambiente. La propia osteogénesis necesita de las condiciones biomecánicas adecuadas, no debiendo obviarse conceptos actuales como osteosíntesis rígida, osteosíntesis dinámica, estabilidad primaria, etc. Dependiendo de estas condiciones, de las características de la fractura, del hueso en que se produce y de la edad, entre otros factores, se liberan unos mediadores bioquímicos u otros que llevarán a la formación de hueso, cartílago o tejido fibroso, o lo que es lo mismo, a consolidación, no consolidación hipertrófica o no consolidación atrófica.
Fabricar tejido con características químicas y citohistológicas similares al hueso no es hacer hueso funcional susceptible de osteointegración morfológica y funcional. El hueso es el resultado de la conjunción eficaz de factores biológicos y físicos. El conocimiento de estos últimos precisa de avances importantes para que el final del proceso de reparación sea en todo comparable a la situación normal. Uno de los detalles de este microambiente físico-químico lo constituye la vascularización. La osteogénesis es altamente exigente de angiogénesis. Sabemos más de CMM, TGF-β y BMP que de angiogénesis; la ingeniería tisular no avanzará suficientemente si no mejoramos nuestro conocimiento de la vascularización. La biología de las células endoteliales, los pericitos y los FC implicados como el VEGF (Vascular Endothelial Growth Factor) es otro campo que precisa expansión. La conjunción de estas líneas de actuación, células, FC, biomateriales, angiogénesis y entorno físico es fundamental. Por ejemplo, conocemos que la diferencia entre no consolidación atrófica e hipertrófica es un problema básicamente de angiogénesis de los fragmentos. El control de la vascularización es un campo de investigación muy activo en los últimos años, tanto por su importancia para la progresión del crecimiento tumoral como para la viabilidad de injertos variados. El bloqueo de VEGF en tumores o su activación en injertos parecen, a priori, formas de control de ambos procesos. Pero la promoción indiscriminada de uno u otro parece inadecuada por la pérdida del control clínico del proceso. Sin embargo, en lo que a la mejoría de la vascularización de implantes o injertos óseos se refiere, creemos puede abrirse una puerta experimental con posibilidades: el uso de FC recombinantes (VEGF, FGF, etc.) con dominios moleculares específicos que los conduzca y mantenga en un lugar determinado84,85. Así, en nuestro grupo pretendemos disponer de estos factores con capacidad de unión específica al colágeno I y a la HA, lo que permitirá su uso controlado en el tiempo y el espacio en lesiones óseas o de otro tipo.
Estos aspectos bioquímicos de la vascularización están en relación directa con la técnica de aplicación de terapéuticas como osteosíntesis o artroplastias, donde se han ido desarrollando técnicas instrumentales e implantes cada vez más respetuosos con la vascularización del hueso.
3) Diseño epidemiológico. Por último, un aspecto esencial en la transferencia de resultados básicos a la clínica es su evaluación, basada en el diseño epidemiológico y estadístico adecuado de grupos de pacientes que confieran validez externa a dicha transferencia merced a la planificación de proyectos prospectivos.
Paradójicamente, el auge de las ciencias básicas ha venido a mostrar que la validación estadística de los hechos, como acreditación de calidad de los resultados de investigación, ha sido ignorada a veces por la investigación básica sin que ello supusiera para ésta una rémora para su desarrollo.
Al estar basadas las ciencias básicas y clínica en el método científico, parece necesario resolver el problema conceptual que supone la ausencia de un procedimiento unitario que compatibilice la aceptación de las hipótesis básico-experimentales y clínicas, haciendo necesario el que investigadores básicos, cirujanos y epidemiólogos deban discutir problemas de metodología y resolver cómo la transferencia de resultados básicos a la clínica se considerará exitosa o fracasada.
4) Un último aspecto que no debe obviarse es el de la proyección social que los hallazgos recientes están teniendo, lo que supone y supondrá, a buen seguro, una gran cantidad de condicionantes de carácter ético y legal, aun cuando sean legítimas e incluso necesarias. Por un lado, la búsqueda de células madre del adulto para propiciar los avances en medicina regenerativa, sin necesidad de acudir a las células madre embrionarias, sean procedentes de clonación con fines terapéuticos, o de otro origen, posibilitará el avance sin condicionantes éticos o morales, y por otro, las células madre del cordón umbilical se presentan como una fuente prometedora de estas células, con posibilidades de «manipulación» ad libitum.
Agradecimientos
Este trabajo ha sido financiado por la CICYT (SAF99/ 0133), Fondo de Investigación Sanitaria (FIS: 96/0262 y 98/1174) Plan Andaluz de Investigación (PAI 2000-2003), Junta de Andalucía (CVI/0217), Consejería de Salud de la Junta de Andalucía (2000-2001), Servicio Andaluz de Salud (SAS) 1999 y 2000, Fundación Rey Fahd (Hospital Costa del Sol) y Fundación Mapfre Medicina 1999-2000.