Describimos un algoritmo para el manejo de las metástasis espinales en el que la importancia de los parámetros individuales varía dependiendo del momento en el que se contemplan.
Cada paciente sigue su propio proceso secuencial «personal» que no necesariamente considera todos los parámetros cada vez, ya que algunos pueden ser irrelevantes a la hora de elegir el tipo de tratamiento para ese individuo. Por ejemplo, un paciente en mal estado general con una puntuación ASA alta generalmente no es candidato para la cirugía, independientemente de la naturaleza del tumor primario o del número de metástasis. Para este paciente, el elemento más importante sería la sensibilidad del tumor al tratamiento adyuvante. Del mismo modo, un paciente con lesión aguda y progresiva de la médula espinal se sometería a descompresión quirúrgica y estabilización sin considerar una intervención más agresiva.
We described an algorithm for the management of spinal metastases in which the importance of single parameters varies depending on when they are contemplated.
Each patient follows his own «personal» sequential process which does not necessarily consider all the parameters each time as some may be irrelevant for the purpose of choosing the type of treatment for that single individual. For instance, a patient in general poor condition with a high ASA score is usually not a candidate for surgery, regardless of the primary tumor nature or the number of metastases. For this patient, the most important element would be the sensitivity of the tumor to adjuvant treatment. Similarly, a patient with acute and progressive spinal cord injury would undergo surgical decompression and stabilization without considering a more strenuous intervention.
En este documento describimos un algoritmo para el manejo de las metástasis de columna en el que la importancia de los parámetros individuales varía dependiendo del momento en que se contemplan (fig. 1).
La Organización Mundial de la Salud (OMS) calcula un incremento ascendente de la incidencia del cáncer, con 29,4 millones de nuevos casos en 20401.
Las localizaciones más frecuentes de las metástasis del cáncer son pulmón, hígado y hueso, y el segmento esquelético más frecuentemente afectado es la columna vertebral.
De hecho, se calcula que más del 10% de los pacientes con tumores desarrollan metástasis sintomáticas en la columna, y el 70% tienen evidencia de enfermedad metastásica en el momento de su muerte2. Ello se debe a la rica vascularización de los cuerpos vertebrales. Existe evidencia de que la sangre procedente de muchos sitios anatómicos drena directamente en el esqueleto axial. En un estudio post mortem destacado, Batson3 demostró que la sangre venosa de la mama y la pelvis no fluía solo a la vena cava sino también al plexo venoso que se extiende desde la pelvis a las venas epidural y perivertebral. Ello puede explicar, al menos en parte, la tendencia de la mama, de la próstata, del riñón y del pulmón a producir metástasis en el esqueleto axial.
La esperanza de vida de los pacientes con cáncer se ha incrementado considerablemente durante las últimas décadas, lo cual causa un incremento de la población que puede desarrollar potencialmente metástasis de columna.
La presencia de metástasis vertebrales y su tratamiento no solo afecta a la calidad de vida, sino también a la esperanza de vida. Hasta la fecha, no existe aún una línea terapéutica universalmente aceptada, dada la gran variedad de histotipos de los tumores primarios y de los métodos de metastatizarse. Sin embargo, lo que está universalmente aceptado es que la metástasis ósea es solo un elemento de la enfermedad sistémica y, por tanto, el manejo de los pacientes requiere un enfoque multidisciplinar que implica al oncólogo y al radiólogo.
La presentación clínica más frecuente de un paciente afectado por las localizaciones vertebrales de la enfermedad es el dolor4. Normalmente se trata de un dolor que es poco receptivo a muchos analgésicos, que normalmente se subestima y atribuye a problemas de tipo degenerativo, demorando el diagnóstico correcto y la clasificación terapéutica del paciente. El mecanismo patológico que determina el dolor se debe normalmente a uno de los mecanismos siguientes, o a la combinación de algunos de ellos:
- •
Expansión del hueso cortical con estrechamiento perióstico y activación de los nociceptorores.
- •
Compresión directa ejercida por el tumor en la médula espinal o las raíces nerviosas.
- •
Reemplazo progresivo de tejido sano por tejido patológico, que, no teniendo las mismas propiedades biomecánicas que el hueso sano, puede causar inestabilidad vertebral.
- •
Presencia de fracturas patológicas, que se manifiestan normalmente con aparición de dolor agudo, en ausencia de traumatismo aparente.
Otra modalidad de presentación de las metástasis vertebrales, aunque menos frecuente que el dolor, son los síntomas de tipo neurológico. Estos pueden derivarse de la compresión directa de la médula espinal o de las raíces nerviosas, o de la compresión ejercida por los fragmentos o deformidades óseas que surgen tras una fractura patológica.
El primer paso para el manejo correcto del paciente con metástasis vertebrales es realizar el diagnóstico correcto.
Las metástasis vertebrales pueden tener tres patrones diferentes de presentación: osteolítico (lítico, destructivo), osteoblástico (blástico, productivo) o mixto. Las lesiones líticas son destructivas, reflejan pérdida de hueso trabecular y cortical, y normalmente están bien delimitadas. Las lesiones blásticas, por otro lado, tienen un aspecto hiperdenso y son normalmente expansivas y con bordes débilmente definidos. Las lesiones mixtas tienen características líticas y blásticas combinadas.
Las lesiones líticas pueden debilitar la estructura vertebral, causando una fractura inminente, mientras que las lesiones blásticas pueden causar problemas neurológicos, al ejercer compresión en la médula espinal y las raíces. La TAC permite evaluar y clasificar las lesiones como líticas, blásticas o mixtas.
En diversos estudios se ha demostrado la importancia de una mejor evaluación de la calidad ósea, reflejando que solo existe un 2,3% de riesgo de fractura patológica cuando se compromete <50% del hueso cortical, y sin embargo un 80% de riesgo cuando se compromete >75% del hueso cortical5.
Sin embargo, las técnicas de imagen en el proceso diagnóstico son suficientes para una serie de lesiones patognomónicas (p.ej., osteoma osteoide), y las pruebas de laboratorio son útiles para otras lesiones (p.ej., mieloma múltiple), pero el diagnóstico histológico es necesario para la mayoría de ellas.
Por tanto, es necesario obtener una muestra tisular, y la biopsia transpedicular guiada por TAC es la mejor opción, ya que es la que menor riesgo de diseminación local tiene y permite, si se indica, la extirpación quirúrgica del tracto de la biopsia.
Los tratamientos terapéuticos modernos (quimioterapia, terapia hormonal, inmunoterapia) y la radioterapia han incrementado ciertamente la supervivencia de muchos pacientes que padecen tumores sólidos y hematológicos, aunque, sin embargo, no son capaces a menudo de controlar con efectividad el dolor y el deterioro funcional. Es posible que los nuevos biomarcadores tumorales y la epigenética tumoral, junto con las nuevas terapias hormonales e inmunoterapéuticas, inclinen aún más las curvas de supervivencia, de manera positiva, dado el mejor control de la enfermedad.
El objetivo de la cirugía en el manejo de las metástasis de columna podría ser uno de los siguientes, o la combinación de algunos de ellos:
- •
Preservación de la función neurológica o recuperación del déficit neurológico.
- •
Alivio del dolor.
- •
Restauración de la estabilidad de la columna.
- •
Control local del tumor.
Aun cuando el control local del tumor es el objetivo del tratamiento de las metástasis, no siempre se logra quirúrgicamente. De hecho, la amplia variedad de histotipos que pueden depositarse en la columna difiere en cuanto a sensibilidad a los tratamientos no quirúrgicos (tales como radioterapia, terapia hormonal e inmunoterapia). Además, es intuitivo que cuanto mayor sea la supervivencia prevista del paciente mayor será la posibilidad de recidiva de la enfermedad (con compresión eventual de la médula espinal y/o fractura patológica), y de ahí la importancia diferencial de lograr un control local duradero.
Es importante que el cirujano sea consciente de las diversas opciones disponibles para lograr el control local de los diversos histotipos, ya sean estas opciones de tipo quirúrgico o de otro tipo.
Desde nuestra perspectiva, las técnicas quirúrgicas para las metástasis de columna pueden resumirse como: 1)descompresión y estabilización; 2)resección intralesional (curetaje o citorreducción), y 3)resección en bloque, siguiendo a estos dos últimos métodos los procedimientos reconstructivos (con diversas técnicas). Todas estas operaciones pueden ser realizadas con enfoques anterior, posterior o combinado6.
- 1.
Descompresión y estabilización. Es el procedimiento quirúrgico más rápido y menos agresivo. Puede realizarse anterior o posteriormente mediante abordajes abiertos mínimamente invasivos. Los abordajes combinados no se utilizan de manera frecuente en este contexto. La laminectomía descompresiva con o sin eliminación del tumor epidural se combina con la estabilización posterior. Los autores creen que es imperativo estabilizar la columna vertebral al mismo tiempo. Este procedimiento está indicado para los pacientes con pronóstico a corto plazo que pudieran tener compromiso neurológico y/o fractura patológica. La familiaridad y la eficiencia del cirujano con estas técnicas permiten que este procedimiento sea realizado en un contexto urgente o emergente. La descompresión anterior y la estabilización están más comúnmente asociadas a complicaciones viscerales y vasculares. Por ello, pocos centros recomiendan este enfoque. La embolización arterial selectiva preoperatoria puede reducir la hemorragia asociada a tumores vasculares tales como el cáncer de células renales y el cáncer de tiroides.
- 2.
Resección intralesional (curetaje o citorreducción). El tumor se aborda de manera directa, bien anteriormente, posteriormente o circunferencialmente, y se extirpa de manera gradual, a fin de lograr una descompresión circunferencial de la médula espinal y reducir la carga tumoral. Este procedimiento se realiza a menudo como parte de un enfoque multidisciplinar, y está precedido por una embolización arterial selectiva preoperatoria para seleccionar los tumores. Dicha operación está indicada para metástasis no sensibles a la radioterapia asociadas a una fractura patológica, o para compresión de la médula espinal, o cuando está recomendada la reducción del tumor para mejorar los tratamientos oncológicos.
- 3.
Resección en bloque. Este procedimiento se realiza normalmente en pacientes con tumores óseos primarios malignos, y se recomienda ocasionalmente para los pacientes con pronóstico de medio a largo plazo y metástasis solitaria derivada un tumor relativamente resistente a la quimioterapia y a la radioterapia. La operación puede realizarse mediante abordaje posterior único, o enfoque combinado anterior y posterior. La resección en bloque está asociada a una menor tasa de recidiva local, aunque el ratio riesgo-beneficio es muy alto, dada la morbilidad de dichas operaciones prolongadas (8-16h). Se considera también la resección en bloque en tumores altamente vascularizados, ya que este tipo de resección puede causar menor hemorragia que la extirpación intralesional. En la mayoría de los casos, la metástasis de columna con invasión del canal muy relevante, que provoca compresión sintomática medular, no es idónea para la resección en bloque, debido a la falta de criterios quirúrgicos para la realización de tal procedimiento. El tratamiento adyuvante (es decir, radioterapia, terapia hormonal) puede reducir la incidencia de recidiva local y la progresión distante del tumor7.
Para elegir el tratamiento más adecuado hay que tener en cuenta diversos elementos: el pronóstico y las condiciones generales del paciente, el histotipo del tumor y su sensibilidad a las terapias adyuvantes, la extensión de la enfermedad y las condiciones neurológicas.
En el pasado se han realizado muchos esfuerzos para intentar crear puntuaciones pronósticas que pudieran orientar al manejo quirúrgico. Con dichos sistemas se asigna una puntuación a cada parámetro, y la suma de dichas puntuaciones indica el tratamiento más adecuado.
Tokuhashi et al.8 reportaron en 1989 su Scoring system for preoperative evaluation of a patient's prognosis with metastatic spinal tumor (Escala para establecer el pronóstico del tumor metastásico espinal). Dicha escala se basó en los datos retrospectivos recopilados de 64 pacientes con metástasis de columna, analizados para desarrollar un sistema de puntuación amplio que identifica seis variables con las que se evalúa la estratificación pronóstica. En 2005 publicaron una versión revisada, en la que se modificó el ítem Primary site of cancer (sitio primario del cáncer). De acuerdo con esta escala, se calculan tres clases de manejo del tumor: manejo conservador (puntuación 0 a 8), cirugía paliativa (puntuación de 9 a 11) y cirugía excisional (puntuación >12), con predicción de supervivencia reportada a <6, >6 y >12meses, respectivamente9.
Tomita et al.10 propusieron en 2001 una escala pronóstica basada en tres factores: tasa de crecimiento del tumor primario, número de metástasis de la cirugía excisional y presencia/ausencia de metástasis viscerales. Con la suma de la puntuación de los tres componentes se obtiene una puntuación general que oscila de 2 a 10, que va de buen a mal pronóstico, respectivamente. Dichos autores no evaluaron el estado funcional, porque se consideró un reflejo de la carga tumoral.
A lo largo de los años se han desarrollado muchas otras escalas, pero ninguna ha reflejado un porcentaje mayor al 90% de consistencia entre el tiempo de supervivencia predicho y el real para poder utilizarse en la práctica clínica11.
Se analizaron los factores que influyen en la incidencia de complicaciones y supervivencia tras el tratamiento quirúrgico de las metástasis espinales y se observó que las condiciones neurológicas preoperatorias, la naturaleza del tumor primario y el alcance del compromiso espinal constituyen los principales factores determinantes. La extensión sistémica de la enfermedad, o la edad del paciente, afectan en menor medida al resultado del paciente12.
Por tanto, deben seleccionarse detenidamente tanto el tipo de paciente como el tipo de tratamiento quirúrgico propuesto.
En 2004, el autor principal (AG) propuso un algoritmo para el manejo de las metástasis de columna en el que varía la importancia de los parámetros individuales, dependiendo del momento en que se contemplan13 (fig. 1).
Cada paciente sigue su propio proceso secuencial «personal», que no considera necesariamente todos los parámetros a la vez, ya que algunos pueden ser irrelevantes a la hora de elegir el tipo de tratamiento para dicho individuo. Por ejemplo, un paciente con peor estado general y puntuación ASA alta no es normalmente candidato para cirugía, independientemente de la naturaleza del tumor primario o del número de metástasis. Para dicho paciente, el elemento más importante sería la sensibilidad del tumor al tratamiento adyuvante. De modo similar, un paciente con lesión aguda y progresiva en la médula espinal sería sometido a descompresión quirúrgica y estabilización, sin considerar una intervención más agresiva.
Por tanto, no se considera únicamente al paciente en términos de la enfermedad, reduciendo la elección del tratamiento a una escala matemática sobresimplificada, sino que se le estudia como un todo: considerando en primer lugar su estado general, y solo de manera subsiguiente los elementes relacionados con la enfermedad metastásica.
El algoritmo del tratamiento propuesto comienza con el diagnóstico de las metástasis espinales. Seguidamente, el primer paso sería la evaluación anestésica, durante la cual debe establecerse la operabilidad del paciente: si el paciente es inoperable (ASA alta), deberán considerarse las opciones no quirúrgicas. El siguiente paso toma en consideración el histotipo y su sensibilidad a las terapias adyuvantes: si el tumor no responde a ninguna forma de tratamiento, la única opción para el paciente sería la terapia contra el dolor.
Si el paciente es considerado operable, se evalúan la extensión de la compresión de la médula espinal y la severidad del daño neurológico. De existir déficit neurológico, se evalúa la posibilidad de recuperación, sobre la base del tiempo transcurrido desde el inicio de los síntomas (figs. 2 y 3).
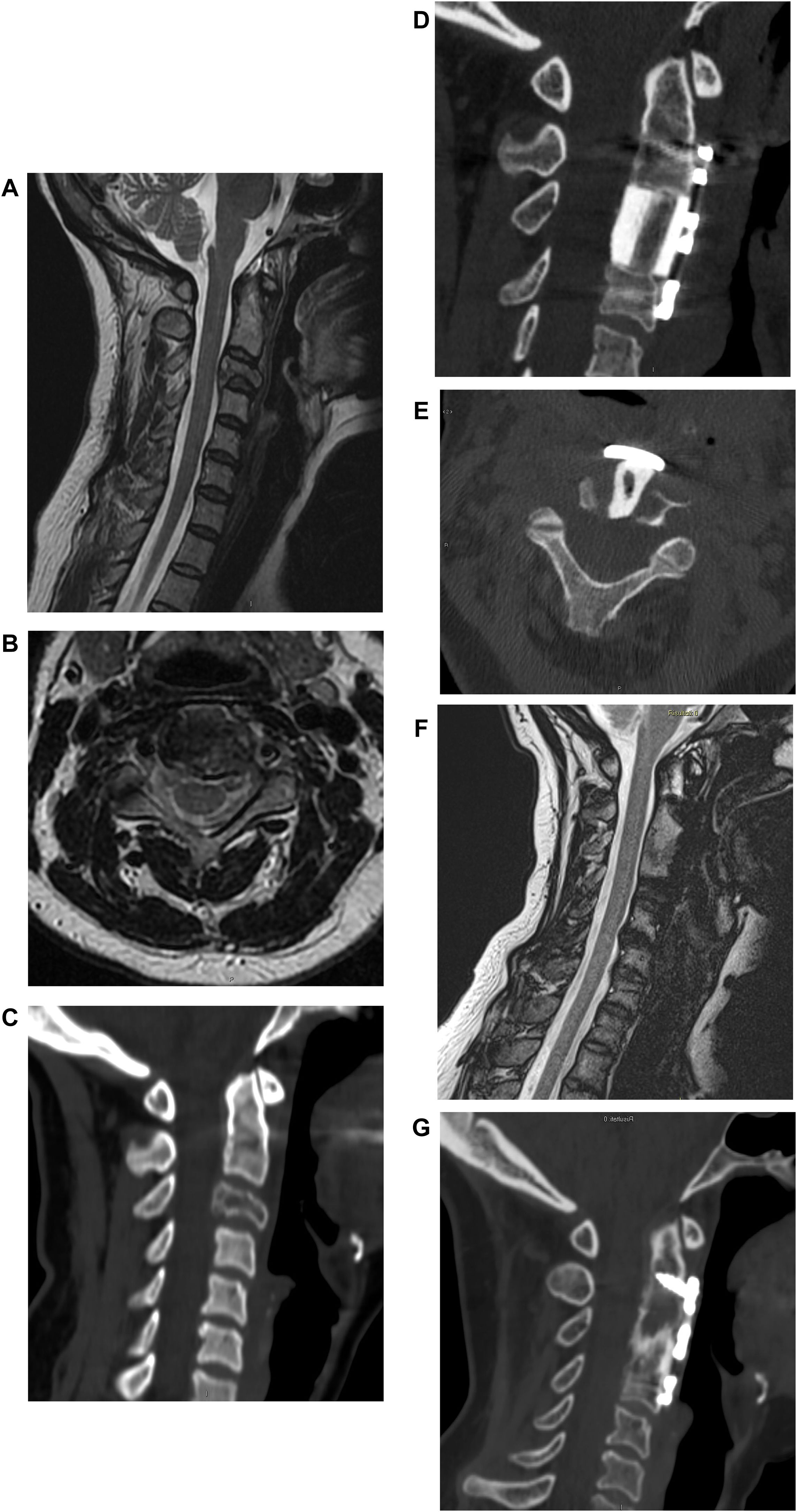
Mujer de 40 años. Fractura patológica en C3 derivada de metástasis espinal por cáncer de mama. Citorreducción en C3 mediante abordaje anterior, reconstrucción de la columna anterior con aloinjerto y placa de titanio. La imagen G muestra la fusión del injerto durante el seguimiento a un año.
Varón de 58 años. Metástasis espinal en L1 derivada de cáncer de próstata con compresión de la médula espinal de tipo2 de acuerdo con la clasificación de Bilsky, con deterioro de la función neurológica en los miembros inferiores. Descompresión, citorreducción y estabilización con instrumentación PEEK reforzada con fibra de carbono mediante abordaje posterior.
Si se excluye la recuperación neurológica en esta etapa, deberá reevaluarse la sensibilidad a los tratamientos adyuvantes. Por otro lado, si el paciente tiene una lesión aguda y progresiva en la médula espinal, deberá realizarse cirugía de urgencia.
De no existir déficit neurológico, o si el daño es estable, se evalúa la sensibilidad a los tratamientos adyuvantes. Si el tumor no es receptivo y solo existe una metástasis aislada, debe elegirse la resección de la lesión (fig. 4). En cambio, la descompresión quirúrgica y la estabilización están indicadas en el caso de que las metástasis sean múltiples y tratables. En caso de que no lo fueran, solo se administrará terapia contra el dolor.
Cuando no existe déficit, o la lesión es recuperable, y el tumor es receptivo a alguna forma de tratamiento adyuvante, se evalúa la fractura patológica (actual o inminente). De hecho, dicho parámetro es esencial a la hora de orientar a la elección entre la descompresión quirúrgica y la terapia de estabilización, o el tratamiento adyuvante en solitario. La resección del tumor puede realizarse en bloque con un margen amplio, o mediante citorreducción intralesional. En general, los autores sugieren la resección en bloque en caso de metástasis aisladas de histotipos no receptivos a la radioterapia y a la quimioterapia14.
Nivel de evidenciaNivel de evidencia IV.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.