La pelvis ósea constituye uno de los lugares del esqueleto donde con mayor frecuencia podemos encontrar lesiones tumorales. Sin embargo, estas lesiones habitualmente proceden de tumores de origen visceral (metástasis de carcinomas) o sanguíneo (leucemias, linfomas, mielomas). También es relativamente frecuente la infiltración de la pared ósea de la pelvis por tumores viscerales localizados en la cavidad pélvica (carcinoma de recto, de vejiga, de cuello uterino, etc).
Los sarcomas de la pelvis ósea (excluyendo por tanto el sacro) constituyen un subgrupo muy pequeño dentro de la patología tumoral ósea. No más del 10% de los sarcomas se localizan en el coxal. Al contrario de lo que ocurre en las series globales de sarcomas óseos, los tumores malignos de la pelvis, (exceptuando el de Ewing) afectan con frecuencia a pacientes adultos, a partir de la quinta década de la vida; y los subtipos histológicos más frecuentes tampoco coinciden con los de las series globales de sarcomas óseos. El sarcoma óseo más frecuente en las extremidades es el osteosarcoma, que típicamente se origina en la metáfisis de los huesos largos de adolescentes. En la pelvis, en cambio, el sarcoma óseo más frecuente es el de Ewing, que tiene una mayor predilección por el esqueleto axial que el osteosarcoma. También son frecuentes en esta localización el condrosarcoma y el histiocitoma fibroso maligno óseo, ambos típicos en el adultos. El condrosarcoma, además, puede asentar sobre una lesión benigna previa como el osteocondroma o el condroma que, precisamente en la pelvis, tienen una mayor facilidad para malignizar. El osteosarcoma de pelvis, a diferencia del de las extremidades, es más frecuente a partir de la quinta década de la vida y a menudo asienta sobre una lesión preexistente (malignización de un Paget, por ejemplo) o aparece como sarcoma radioinducido (por ejemplo tras la radiación de un carcinoma en esa localización). Otros tumores de origen vascular, como el hemangioendotelioma, son menos frecuentes. Además, no es frecuente encontrar en esta localización tumores de bajo grado histológico ya que casi todos los sarcomas de la pelvis son de alto grado.
Otra de las características propias de los sarcomas de la pelvis es la escasa supervivencia que tienen estos tumores. A diferencia de lo que ocurre con la mayoría de los sarcomas óseos1, los de la pelvis tienen un pronóstico más sombrío. Por último, hay que añadir que el resultado funcional tras la resección de los tumores de la pelvis ósea sigue siendo un gran reto para los cirujanos ortopedas especializados en esta patología. Los avances experimentados en el campo de la reconstrucción funcional de las grandes resecciones tumorales no han sido tan satisfactorios en esta localización como en los huesos largos.
La mayoría de los trabajos publicados sobre sarcomas excluyen la localización pélvica. Es difícil encontrar en la literatura trabajos en los que se mezclen sarcomas centrales con los de extremidades, precisamente porque no se comportan igual. Los sarcomas óseos de la pelvis tienen una serie de particularidades diagnósticas, pronósticas y terapéuticas, que los diferencian del resto de los sarcomas, y que a continuación vamos a analizar.
DIFICULTADES DIAGNOSTICAS
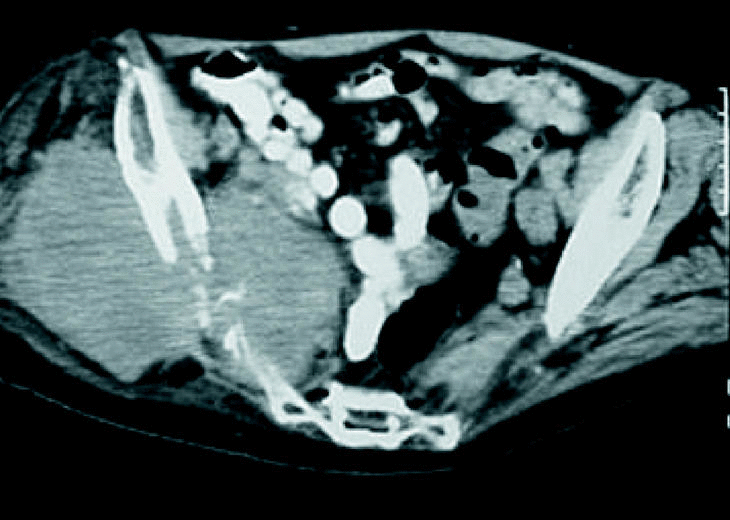
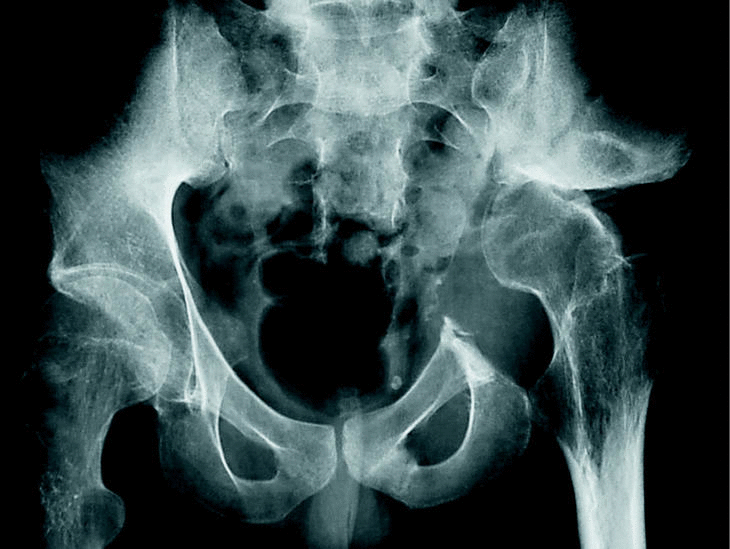
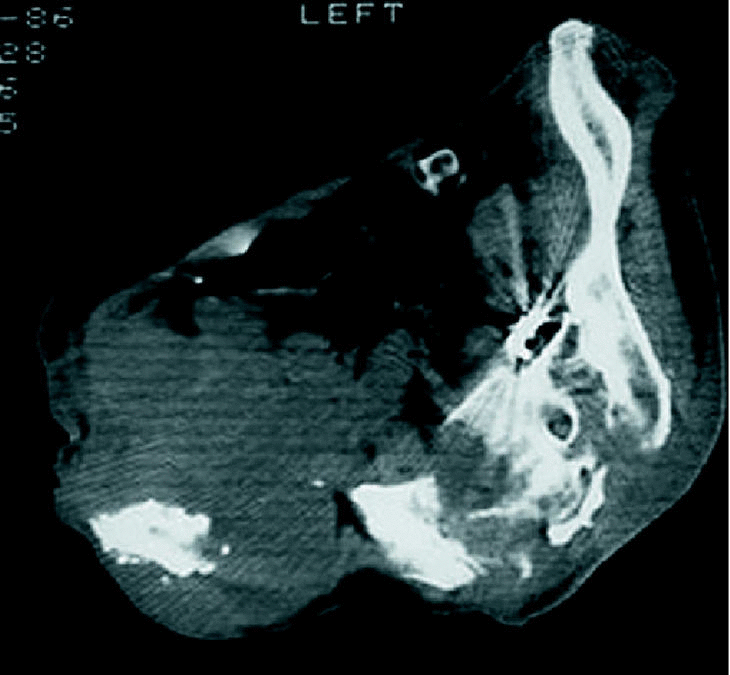
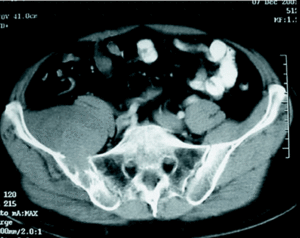
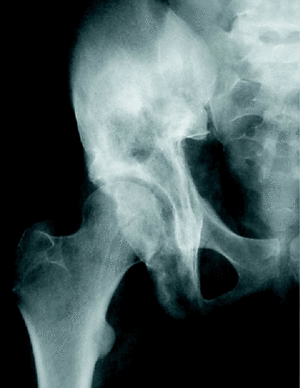
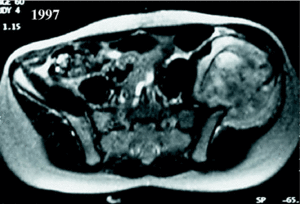
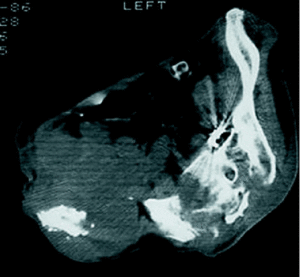
Cuando una tumoración asienta en una extremidad es más fácilmente detectable que cuando se localiza en la pelvis. El tumor en la pelvis tiene más «espacio» para crecer sin ser advertido por el paciente. El cuadro clínico es muchas veces superponible con el de la patología degenerativa lumbar, que constituye uno de los motivos más frecuentes de consulta para el cirujano ortopeda. Incluso el dolor nocturno (uno de los síntomas más alarmantes a la hora de sospechar la presencia de un tumor) puede confundirse en este caso con afecciones mucho más frecuentes como la hernia discal o con otras más raras como la compresión del nervio ciático en cualquier otra región anatómica (fig. 1). La sintomatología clínica puede inducir a error si no se piensa en esta posibilidad1. Además, como hemos comentado, la aparición de una lesión tumoral en la pelvis es con más frecuencia secundaria que primaria, y muchas veces la localización primaria puede permanecer asintomática, haciendo más difícil su sospecha clínica. En otras ocasiones se trata de una malignización de una lesión previa (por ejemplo una enfermedad de Paget), y puede no ser nada fácil llegar a la conclusión de que la transformación maligna ha ocurrido, puesto que también se puede atribuir la sintomatología a la lesión previa.
Figura 1. Paciente intervenida en dos ocasiones (liberación del ciático a nivel de la cabeza del peroné y discectomía lumbar) por presentar sintomatología sugerente de compresión del nervio ciático. Se trataba de un histiocitoma fibroso maligno de la pelvis.
Los estudios de imagen más comunes, como la radiología simple, tienen en esta localización una baja sensibilidad para las lesiones óseas, aunque con una aceptable especificidad. Por otro lado, permiten una escasa apreciación de las partes blandas. Por lo tanto, sólo resultan diagnósticos cuando el tumor ha alcanzado un gran tamaño. Con frecuencia los tumores osteolíticos en esta localización son confundidos con gases abdominales superpuestos con el hueso.
La tomografía axial computarizada (TAC) o la resonancia magnética (RM) tienen una mayor sensibilidad en esta zona anatómica. Además permiten realizar estudios de realce con contraste, lo cual aumenta considerablemente su especificidad. También sirven de guía para las biopsias por punción. En el seguimiento de estos pacientes tras los tratamientos, estos métodos de imagen se encuentran con mayores dificultades a la hora de distinguir una recidiva tumoral de alteraciones postquirúrgicas, hematomas, seromas, tejido de granulación, etc.
Por si todas estas dificultades en el diagnóstico de los tumores de la pelvis no fueran suficientes, hay que añadir que los estudios anatomopatológicos tampoco carecen de dificultad en esta zona. Como en otras localizaciones anatómicas, es necesario que la biopsia sea vista por patólogos con experiencia, dada la baja frecuencia de estas lesiones y su heterogeneidad. Pero además, en la pelvis puede ser más complicada la caracterización de estas lesiones, que adquieren en esta localización formas más variadas. Existen sarcomas de la pelvis que no son nada fáciles de «etiquetar», incluso para patólogos expertos en tumores óseos. Y hay otros sarcomas fácilmente confundibles entre sí. Por ejemplo: en esta zona, un osteosarcoma condroblástico puede ser particularmente fácil de confundir con un condrosarcoma, y el tratamiento de estas dos entidades es muy distinto.
CONNOTACIONES PRONOSTICAS
La pelvis ósea es una estructura muy bien vascularizada, a diferencia de los huesos largos. No hay que olvidar que las fracturas de la pelvis son potencialmente las más sangrantes del esqueleto, llegando incluso a comprometer la supervivencia de quienes sufren este tipo de traumatismos. Esta característica condiciona una mayor «receptividad» para el asiento de metástasis óseas de carcinomas que la que tienen los huesos largos y, a su vez, determina una mayor facilidad para la diseminación hematógena de los sarcomas originados en esa localización. Además de ser abundante, la vascularización de la pelvis es compleja. Existen gran cantidad de anastomosis entre distintos sistemas que hacen difícil saber de qué arteria principal puede depender un tumor que asiente en la pelvis. Y esto también dificulta la efectividad del tratamiento. La respuesta al tratamiento quimioterápico (en el caso de emplear quimioterapia intraarterial) puede ser menos positiva de lo que cabría esperar en otras localizaciones. Por este mismo motivo, la embolización prequirúrgica con intención de disminuir el sangrado operatorio puede no conseguir su objetivo en esta localización, aunque sea muy deseable realizarla cuando se espera un sangrado importante. Además, la complejidad anatómica de la zona hace que otros tratamientos adyuvantes, como la radioterapia, pierdan también efectividad en esta zona.
Algunos tipos específicos de sarcoma, propios de esta localización (como el osteosarcoma sobre enfermedad de Paget) tienen de por sí un pronóstico mucho peor que el resto de sarcomas de esa «familia». La respuesta al tratamiento, tanto quimioterápico como quirúrgico, es mucho peor y la supervivencia muy escasa. Y no es únicamente por su localización, sino por el tipo de tumor, que no responde al tratamiento. En un reciente estudio multicéntrico europeo en el que hemos participado, la sobrevida media de pacientes afectos de osteosarcoma sobre enfermedad de Paget (cuya localización más frecuente es la pelvis) fue de 9 meses.
Por otro lado, la presencia de metástasis al diagnóstico no solamente es más frecuente en los sarcomas de esta localización en comparación con los de los huesos largos sino que, además, supone un factor de muy mal pronóstico. Cuando un sarcoma de hueso largo comienza con metástasis pulmonares, la experiencia nos dice que la resección del primario y las metástasis puede todavía conseguir una relativamente alta tasa de curaciones. Desgraciadamente, en los tumores de la pelvis esto no suele ser así2.
DIFICULTADES TERAPÉUTICAS
La cirugía de los tumores de la pelvis es una de las más difíciles desde muchos puntos de vista. En otros casos de similar dificultad técnica, como los tumores de columna, con frecuencia se es consciente de las limitaciones que impone la presencia del saco dural, que muchas veces imposibilita una buena resección del tumor. En esos casos ya se parte de la base de que muchas veces no será posible una resección con márgenes, y se intenta una cirugía menos «radical» complementada con terapia adyuvante. Por decirlo de un modo gráfico, se «tira la toalla» antes de empezar. En la cirugía de la pelvis, en cambio, se sabe que resultará costosa y de gran dificultad, pero hay que intentar una resección con márgenes. En primer lugar, la resección de un tumor maligno en esta localización requiere un conocimiento anatómico muy profundo, no sólo del sistema musculoesquelético sino también de otros órganos y aparatos. Las estructuras vasculares, el aparato genitourinario, las asas intestinales, la inervación del periné y los esfínteres, etc. son, si cabe, más importantes que la estructura musculoesquelética que se pretende resecar y reconstruir. Por lo tanto, deben ser reconocidas y, en la medida de lo posible, respetadas. Las posibilidades de resección con márgenes de seguridad se ven mucho más reducidas en los de la pelvis que en los tumores de los huesos largos, precisamente porque están rodeados de estas otras estructuras.
El hecho de que la cirugía en esta zona sea tan complicada ha propiciado que se trate de facilitar mediante el empleo de distintas terapias adyuvantes. En muchos casos de osteosarcoma, por ejemplo, resulta muy útil el empleo de quimioterapia intraarterial, y también en la pelvis puede resultar eficaz. La radioterapia intraoperatoria o la braquiterapia disminuyen el riesgo de recidiva local en los sarcomas radiosensibles como el de Ewing. En las metástasis, por ejemplo, puede ser útil el empleo de la crioterapia, dependiendo de la localización, las perspectivas vitales, etc. La perfusión de factor de necrosis tumoral (TNF) es hoy en día técnicamente inaplicable a los sarcomas de la pelvis, pero esperamos en un futuro no muy lejano poder contar con esta arma que tan eficaz se ha mostrado en sarcomas de extremidad considerados irresecables. Es cierto que la recidiva tumoral no depende exclusivamente de los márgenes quirúrgicos.
La eficacia de los tratamientos neoadyuvantes también desempeña un papel muy importante en las posibilidades de recidiva. Pero en los sarcomas localizados en la pelvis es mayor, si cabe, que en otras localizaciones la necesidad de no rebajar las exigencias quirúrgicas confiando en la efectividad de otros tratamientos. Por ejemplo, aunque se reduzca mucho la masa de partes blandas acompañante al tumor, suele ser imprescindible resecar toda la masa ósea afecta, por muy eficaz que haya sido el tratamiento neoadyuvante, si se quiere conseguir la curación del paciente. Por otro lado, también estas terapias adyuvantes tienen una especial dificultad en esta zona: por ejemplo, la presencia de asas intestinales, la vejiga, el aparato genital, etc. pueden dificultar la estimación de los campos y dosis de radiación en un sarcoma de la pelvis, y disminuir así la eficacia de esta modalidad terapéutica. Además, los sarcomas de la pelvis, al contrario de los de extremidades, son más frecuentes a partir de la quinta a sexta década de la vida. Otro factor que condiciona la eficacia del tratamiento es la menor tolerancia de las personas mayores al tratamiento quimioterápico, que puede inducir a reducir las dosis o la duración del tratmiento.
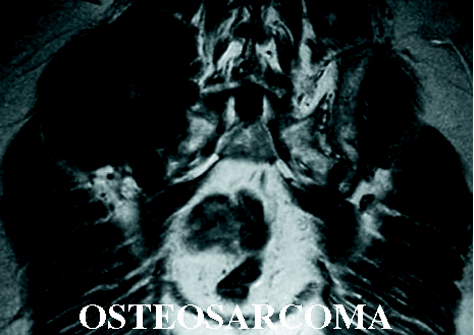
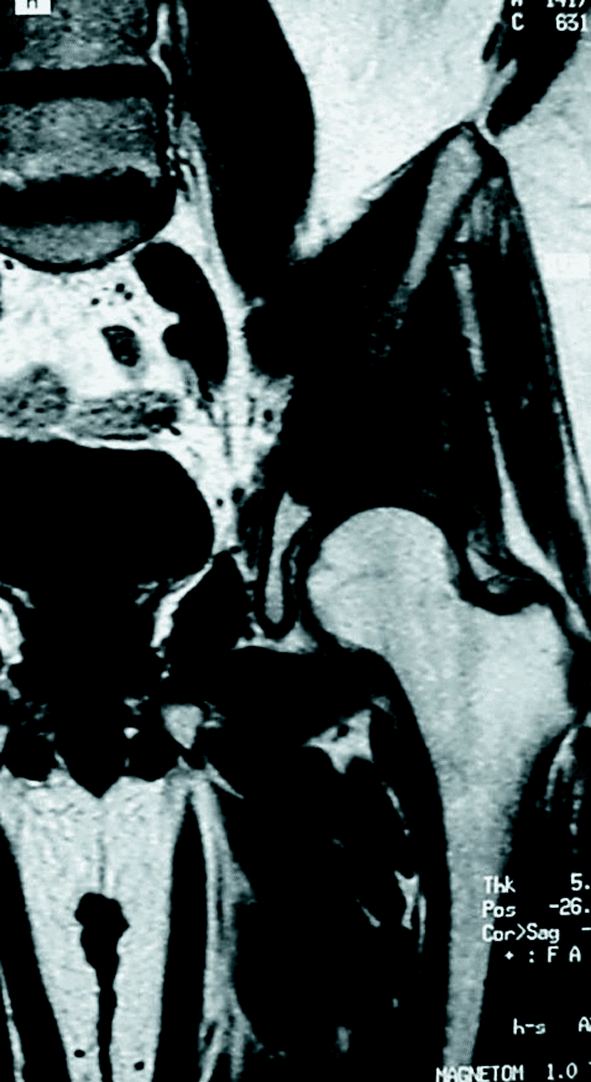
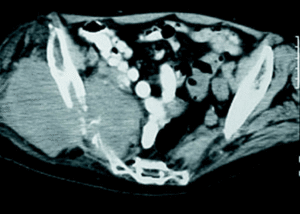
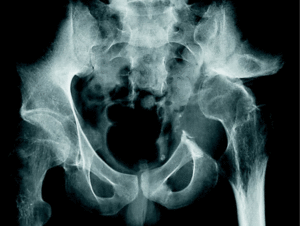
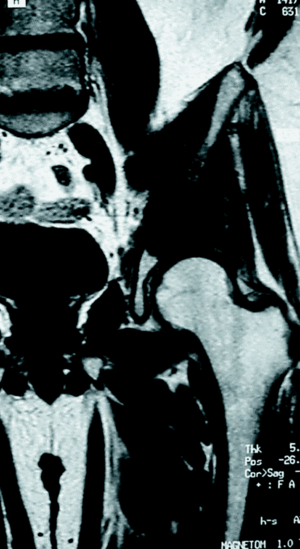
Para complicar un poco más las cosas, la articulación sacroilíaca, a diferencia de cualquier otra articulación del esqueleto, no representa una barrera al paso del tumor en más de la mitad de los casos (fig. 2), por lo que suele ser necesario incluir en la resección parte del ala sacra, cuando el tumor asienta en esa zona3. La duración de la intervención, el sangrado, etc. limitan también las posibilidades de éxito. La aparición de complicaciones postquirúrgicas es mucho más frecuente en esta localización anatómica. La tasa de infecciones se ve incrementada de modo proporcional a la duración de la intervención. Si a esto se añade el tamaño del tumor y el empleo con mayor frecuencia de tratamientos adyuvantes como la radioterapia, las dificultades quirúrgicas se ven aún más incrementadas. Por ejemplo: la radioterapia preoperatoria incrementa sensiblemente las posibilidades de trombosis de la vena ilíaca tras su manipulación quirúrgica. Cuando además no se trata de un primer intento quirúrgico sino de una reintervención por recidiva, las posibilidades de éxito se reducen drásticamente. Es decir: si alguien tiene alguna posibilidad de realizar una buena resección de un tumor pélvico, ese es el primer cirujano que lo opera.
Figura 2. La articulación sacroilíaca no suele ser una barrera al paso de los diferentes tipos de sarcomas pélvicos. HFM: histiocitoma fibroso maligno.
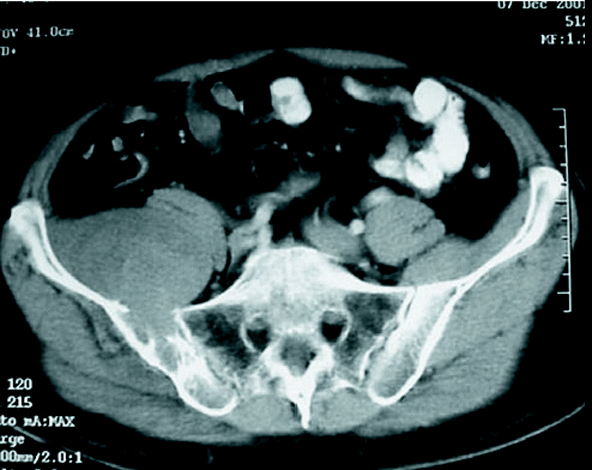
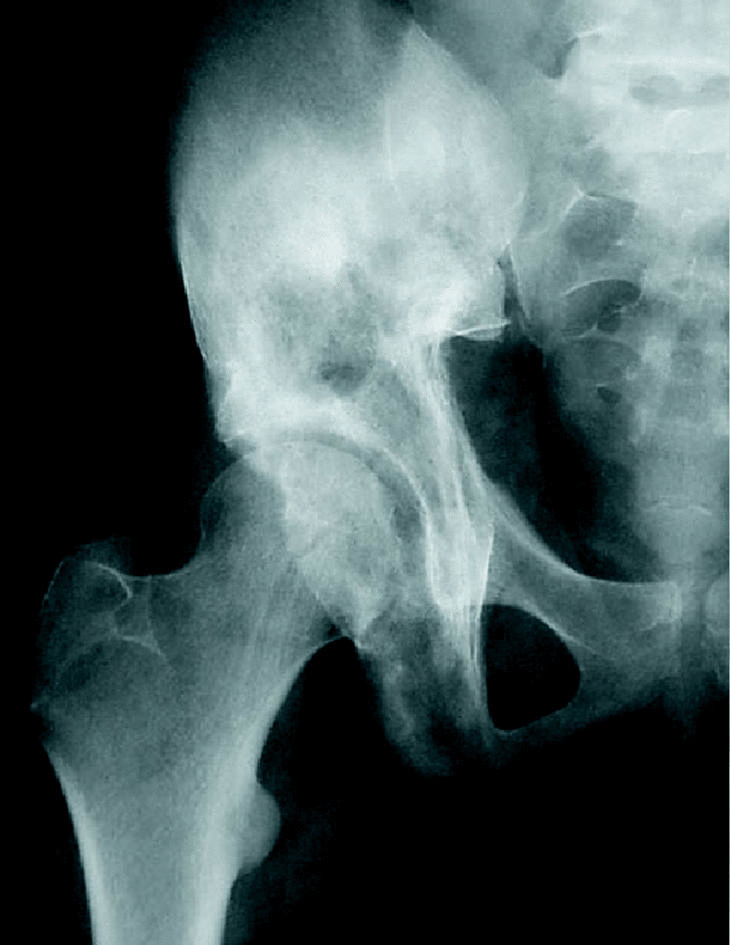
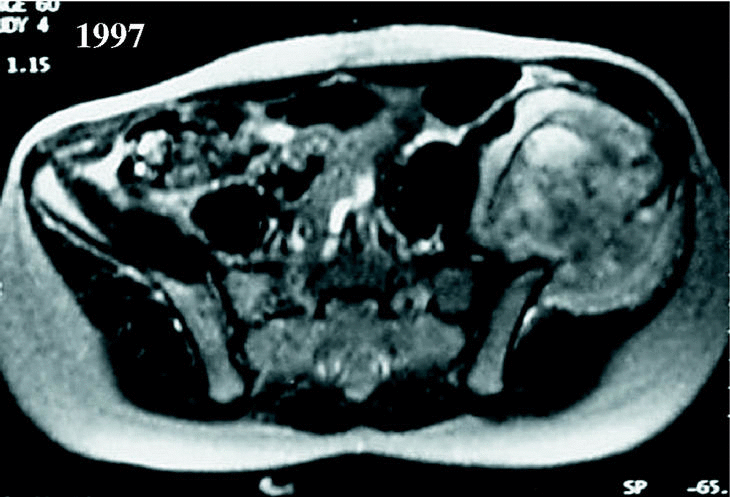
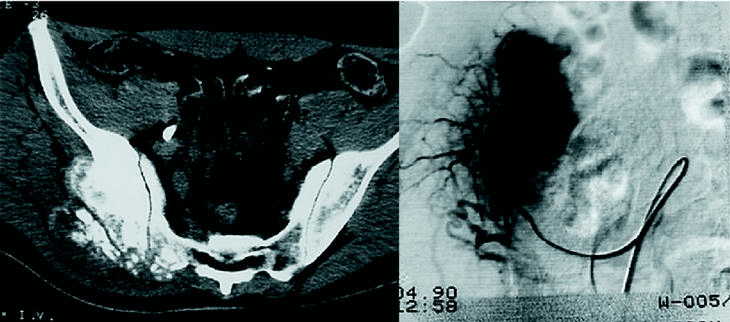
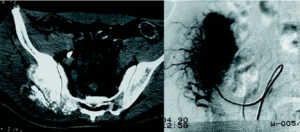
Este paso del tratamiento (la resección quirúrgica con márgenes) es de capital importancia en cuanto a las posibilidades de curación4,5. No cabe plantearse el tratamiento en función de otros parámetros, que pueden tener más o menos importancia, pero que no servirán de nada si el paciente no se cura. No parece lógico que se plantee la intervención quirúrgica para hacer una reconstrucción espectacular, técnicamente muy sofisticada, si antes no se ha conseguido una resección con márgenes. Y aquí desempeña un papel muy importante la biopsia (que debe ser realizada por el cirujano que tratará a ese paciente, aunque parezca técnicamente sencilla) (fig. 3), el abordaje empleado, etc. Sería de todo punto de vista inaceptable plantearse como objetivo tener una bonita radiografía postquirúrgica si el paciente no sobrevive a su enfermedad.
Figura 3. (A) Histiocitoma fibroso maligno de ilíaco, con masa de partes blandas en cara anterior. Le realizaron la biopsia por cara posterior, contaminando la musculatura glútea que antes de la biopsia no parecía estar infiltrada. Fueron necesarias transfusiones múltiples por sangrado en la biopsia. (B) La resección incluyó todo el trayecto de la biopsia previa. El sacrificio de la musculatura probablemente podría haberse evitado con otro tipo de biopsia. (C) La reconstrucción se llevó a cabo con autoinjerto.
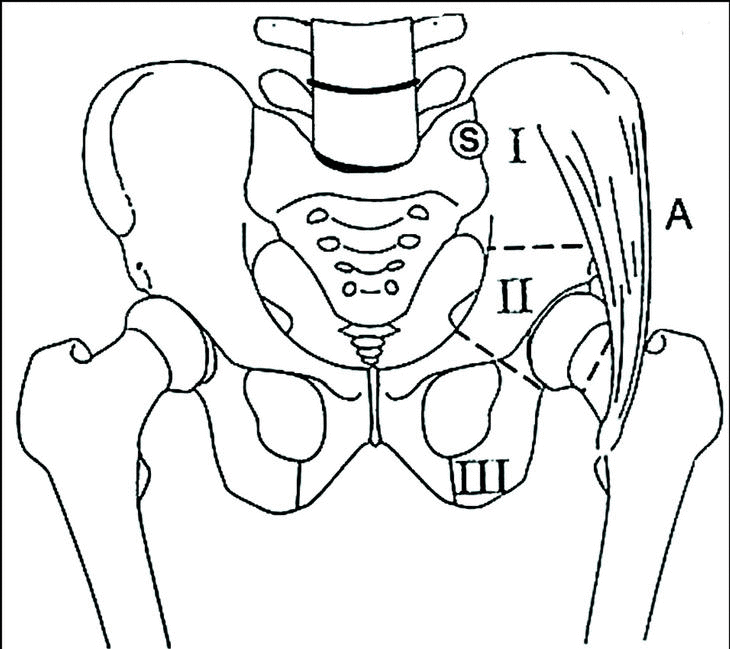
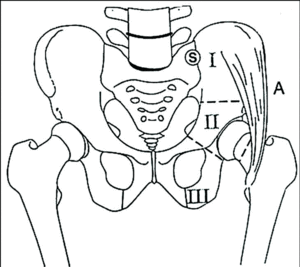
En función de las estructuras resecadas las técnicas de reconstrucción empleadas serán distintas. En los tumores de la pelvis es clásico el empleo de esquemas que distinguen las zonas más asequibles que pueden no necesitar reconstrucción quirúrgica alguna (cara anterior de la pala ilíaca, isquion, pubis), de las zonas más complejas (articulación sacroilíaca, acetábulo) que muchas veces requieren reconstrucción (fig. 4). Sin embargo, desgraciadamente la mayoría de los sarcomas de la pelvis afectan a alguna de esas estructuras de mayor dificultad quirúrgica (sacroilíaca o acetábulo) cuando no a las dos. En nuestra experiencia, sólo un 8% de los sarcomas de la pelvis asientan en estructuras fácilmente resecables, y que no requieren ningún tipo de reconstrucción. Clásicamente se empleaban técnicas muy mutilantes como la cuartectomía6, que además no estaban ni mucho menos exentas de complicaciones, incluida la recidiva local7.
Figura 4. El 32% de los sarcomas de la pelvis se localizaron en el área sacroilíca, el 35% en el acetábulo, y el 25% en ambas zonas. Sólo un 8% de los sarcomas de la pelvis se localizaron en áreas fácilmente resecables como la cresta ilíaca, isquion o pubis. (S, A, I, II, III: zonas más o menos asequibles de reconstrucción).
Cuando el tumor afecta a la línea innominada, la articulación sacroilíaca o el acetábulo, cabe la opción de no realizar reconstrucción (fig. 5), pero la función puede quedar muy limitada, no sólo por la falta de continuidad entre la extremidad y el tronco, sino también por el intenso acortamiento que puede quedar. Por este motivo, la mayoría de las veces se intenta algún tipo de reconstrucción, bien sea con autoinjerto (fig. 3), aloinjerto8 o prótesis para reinstaurar la continuidad entre la extremidad y el esqueleto axial. Unas veces se busca la artrodesis iliosacra o femorosacra9, otras veces se intenta reconstruir la articulación coxofemoral mediante artroplastias (fig. 6), y en muchas ocasiones hay que tratar de reconstruir esas dos articulaciones (fig. 7).
Figura 5. (A) Hombre de 19 años con osteosarcoma de acetábulo. Tras la quimioterapia intraarterial se resecó la lesión sin realizar reconstrucción. (B) Nueve años después no hay signos de recidiva.
Figura 6. Condrosarcoma de acetábulo. Reconstrucción con aloinjerto y prótesis de cadera.
Figura 7. (A) Sarcoma de Ewing que afecta a la articulación sacroilíaca y al acetábulo. (B) Resección de la tumoración con márgenes de seguridad. Se colocó un espaciador de cemento con gentamicina hasta finalizar la quimioterapia. (C) Reconstrucción con aloinjerto y prótesis.
La reconstrucción muchas veces prolonga una cirugía de por sí complicada, y tiene un especial riesgo de infección, que también distingue a los tumores de la pelvis de otras localizaciones más «accesibles». Por ejemplo, los grandes aloinjertos de la pelvis tienen una tasa tan alta de infecciones, incluso en centros con gran experiencia, que hace replantearse su empleo como método de reconstrucción en esta localización anatómica10. El problema está en que, en algunos casos, no existen muchas otras alternativas. La cobertura del método de reconstrucción empleado mediante colgajos musculares es de capital importancia para evitar una infección11 (fig. 8). No es infrecuente tras muchas horas de cirugía la aparición de zonas de necrosis cutánea en la incisión. En algunos casos puede ser útil el empleo de espaciadores con antibióticos tras la resección, en espera de realizar la reconstrucción en un segundo tiempo quirúrgico, una vez finalizado el período de quimioterapia (fig. 7). Además del riesgo de infección, la funcionalidad de la extremidad puede quedar muy comprometida por otras complicaciones en esta cirugía como la trombosis venosa o arterial, la posibilidad de daño neurológico del ciático o el crural, etc.
Figura 8. Sarcoma de Ewing tratado mediante injerto. (A) La cobertura del aloinjerto es fundamental para evitar infecciones. (B) Cinco años después el paciente está asintomático con una discreta báscula pélvica.
Todo lo expuesto hasta el momento puede incitar a plantearse renunciar a la parte quirúrgica del tratamiento en los tumores de la pelvis. Pero esto, más que una victoria atribuible a una retirada a tiempo, sería, continuando con el símil bélico, equivalente a una deserción. Las posibilidades de curación en los sarcomas de la pelvis pasan necesariamente por un tratamiento multidisciplinar que incluya una resección con márgenes sanos. Así como en otras localizaciones algunos tumores como el sarcoma de Ewing pueden curarse sin necesidad de cirugía, en la pelvis esto es algo casi imposible12. Ya hemos comentado que la complejidad anatómica de la zona también dificulta la efectividad del tratamiento radio y quimioterápico (además de incrementar los riesgos quirúrgicos). Pero todo esto no hace más que realzar el papel de la cirugía en estos tumores. En muchas ocasiones se emplean abordajes poco usuales en nuestra especialidad para intentar resecar bien un tumor de la pelvis (intra o extraperitoneales, anterior y posterior, etc). Si la resección no es completa, las posibilidades de rescate quirúrgico son casi nulas, puesto que el tumor puede estar diseminado por cualquiera de los territorios previamente abordados.
La supervivencia media sin cirugía es muy variable dependiendo del estadio al diagnóstico, el tipo de tumor, etc. Así, un sarcoma de Ewing de la pelvis puede llegar a vivir más de 2 años desde el diagnóstico, y un condrosarcoma puede llegar a sobrevivir más de 3 años; sin embargo, el osteosarcoma o el histiocitoma fibroso maligno raramente sobrepasan el año si no se consigue una buena resección con márgenes. Con una experiencia cercana al centenar de casos, el 40% de los sarcomas de pelvis de alto grado que fueron operados en nuestro centro permanecen vivos en la actualidad (con una media de seguimiento de 8 años), mientras que de aquellos que, por motivos muy distintos, no fueron operados no sobrevivió ninguno, por muy eficaz que fuera el tratamiento adyuvante. De los intentos de rescate quirúrgico en recidivas tras intervenciones previas, tampoco sobrevivió ninguno (fig. 9).
Figura 9. Condrosarcoma que había sido intervenido previamente en dos ocasiones en otro centro. La lesión recidivó y el paciente no sobrevivió.
Por lo tanto, hay que insistir en que la cirugía tiene un papel primordial, pero sólo el primer cirujano tiene alguna posibilidad de resultar eficaz. Cuando la resección es completa y el tratamiento adyuvante es adecuado, se puede aspirar a la curación de estos tumores (fig. 10), aunque las posibilidades hoy por hoy no son tan altas como en otras localizaciones (40% frente al 77% a los 5 años)13. Los avances que se están produciendo en el campo de la biología molecular abren un panorama muy esperanzador en el tratamiento de los sarcomas. Hace ya años que nadie duda que el cáncer es una enfermedad genética, no porque se transmita de padres a hijos (aunque a veces esto también ocurre) sino en cuanto a que se produce por una alteración en los genes que controlan la multiplicación celular.
Figura 10. El tratamiento adyuvante del osteosarcoma es fundamental. (A) La quimioterapia intraarterial fue de gran utilidad en este caso. (B) Doce años después de la intervención, el paciente está asintomático.
Hoy en día, contamos con técnicas muy precisas como la reacción en cadena de la polimerasa (PCR) para detectar esas alteraciones genéticas. Estos hallazgos son una indudable ayuda a la hora de establecer el diagnóstico (por ejemplo, la detección de la translocación entre el cromosoma 11 y el 22 en el sarcoma de Ewing) y el pronóstico de estas lesiones (por ejemplo, algunos tipos de transcrito en este mismo tumor tienen mejor pronóstico que otros). Todo esto que hasta ahora no desempeñaba un papel especialmente relevante en el tratamiento, comienza ya a tener sus aplicaciones terapéuticas. Se empiezan a definir dianas moleculares a las que poder «apuntar» con este nuevo armamento del que disponemos. Siguiendo con el ejemplo anterior, al igual que ocurre en algunas leucemias, algunos casos de sarcoma de Ewing expresan una oncoproteína intracelular (tirosinquinasa) fácilmente detectable. El STI571 o Gleevec es un ihibidor específico de la tirosinquinasa. Se trata del primer fármaco diseñado específicamente para actuar de forma selectiva sobre un error genético caracterizado por la mezcla de material entre cromosomas. En un futuro no muy lejano esperamos poder confirmar la eficacia de estos tratamientos en los sarcomas y, de modo muy especial, en los de peor pronóstico como son los de la pelvis.