El metotrexato es uno de los fármacos más empleados en pacientes con procesos reumatológicos, debido a su eficacia y perfil de seguridad. Sin embargo, los pacientes tratados con este fármaco son en ocasiones de edad avanzada, por lo que el riesgo de toxicidad aumenta, así como el de intoxicación por error en la toma de la medicación. Presentamos el caso de una paciente de 87 años, polimedicada, con antecedentes de deterioro cognitivo y escaso apoyo social que sufrió una intoxicación aguda grave por metotrexato. Además, describimos las características de los casos de toxicidad por este fármaco ingresados en nuestro Hospital en los últimos 7 años.
Methotrexate is one of the most widely used drugs in rheumatology due to its high efficacy-to-toxicity. However, patients treated with this drug are sometimes elderly, which increases toxicity risks, as well as mistakes in taking the medication. The case is presented of an 87 year-old patient, on multiple medications, with a history of cognitive impairment and low social support, who suffered acute methotrexate toxicity. A description is also presented on the characteristics of the toxicity cases due this drug admitted to this hospital in the last 7 years.
El metotrexato es uno de los fármacos más utilizados en Reumatología por su alta eficacia y baja toxicidad. A pesar de que los efectos tóxicos cuando aparecen suelen ser leves —manifestaciones gastrointestinales, anemia—, en ocasiones pueden ser más graves y producir una mielosupresión intensa, afectación hepática o pulmonar irreversible. La toxicidad depende de la dosis de fármaco y de los factores que intervienen en su absorción, distribución y excreción1,2. A pesar de que las directrices para la correcta utilización y la prevención de la toxicidad por metotrexato están bien establecidas1, siguen produciéndose en nuestros Hospitales ingresos por toxicidad, que en ocasiones tienen un desenlace fatal.
El caso que describimos es un ejemplo representativo de una paciente de alto riesgo de intoxicación aguda de metotrexato. Por ello, nos ha parecido de interés su comunicación, describiendo además las características de los casos de toxicidad por este fármaco que han ingresado en nuestro Centro en los últimos años.
Caso clínicoMujer de 87 años, dependiente para las actividades básicas de la vida diaria (escala de Barthel: 24), que vivía con su marido de edad similar. Se le había diagnosticado artritis reumatoide seropositiva 17 años antes y seguía tratamiento desde hacía 7 con metotrexato (15mg en dosis única semanal), ácido fólico (5mg semanales) y metilprednisolona (2mg diarios). Dos años antes se le había diagnosticado deterioro cognitivo moderado de tipo mixto (GDS: 5; Minimental: 16/30), osteoporosis, hipertensión arterial y dislipidemia. Seguía tratamiento con furosemida, galantamina, alopurinol, ácido acetilsalicílico, omeprazol, atorvastatina, lormetazepam, risperidona, calcifediol y denosumab.
Acudió a Urgencias por un cuadro de varios días de evolución de deterioro del estado general, con postración, fiebre, lesiones cutáneas y mucosas, disfagia y deposiciones melénicas. En la exploración física destacaba: afectación del estado general, fiebre de 39°C, dificultad respiratoria, hipotensión y taquicardia. Presentaba una mucosa oral sangrante con erosiones en el paladar y la faringe y hematomas extensos en la espalda y extremidades. En la analítica destacaba: 0,5×103 leucocitos/μL, con 0% de neutrófilos; Hb: 6g/dL y 11×103 plaquetas/μL; Cr: 1,02mg/dL (1-1,18mg/dL); ALT: 51U/L (2-40U/L); GGT: 266U/L (11-50U/L) y FAL: 143U/L (46-116U/L). La radiografía de tórax y la ecografía abdominal fueron normales. Se diagnosticó probable intoxicación por metotrexato, con mucositis, pancitopenia severa y hepatitis leve. Se pautó ácido folínico, factor estimulante de colonias granulocíticas, ácido tranexámico, transfusión de concentrados de plaquetas y hematíes y antibioterapia empírica. La paciente evolucionó favorablemente con recuperación completa de la aplasia tras 14 días de tratamiento, normalización de la función renal y hepática y desaparición de las lesiones mucocutáneas. A los 6 meses del episodio, la paciente permanece asintomática. Se reinterrogó a los familiares y se constató un error en la administración del metotrexato, con una sobredosificación por la toma de los comprimidos diariamente en vez de semanalmente, debido al deterioro cognitivo de la paciente y la falta de supervisión del entorno familiar.
Material y métodosSe recogieron de forma retrospectiva los datos de los pacientes dados de alta en nuestro Centro con el diagnóstico de toxicidad por metotrexato durante un periodo de 7 años (desde el 01/01/2011 hasta el 31/12/2017). Se seleccionaron inicialmente 44 pacientes, excluyéndose 19 de ellos al no poderse asegurar la existencia de una relación directa con el fármaco, por presentar otras causas que podían justificar sus manifestaciones clínicas o por no haberse suspendido el tratamiento con metotrexato tras el alta. Las variables analizadas se recogen en la tabla 1.
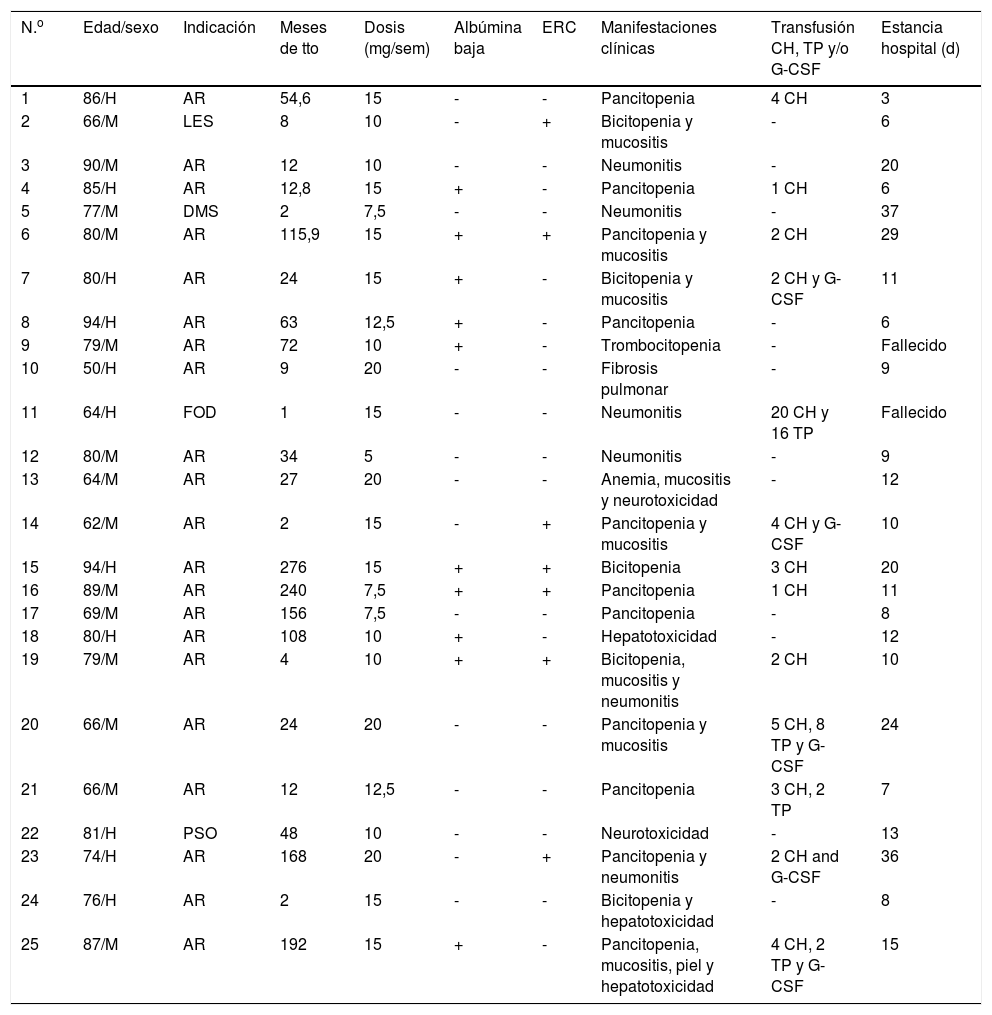
Características de los pacientes y datos clínicos
| N.o | Edad/sexo | Indicación | Meses de tto | Dosis (mg/sem) | Albúmina baja | ERC | Manifestaciones clínicas | Transfusión CH, TP y/o G-CSF | Estancia hospital (d) |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 86/H | AR | 54,6 | 15 | - | - | Pancitopenia | 4 CH | 3 |
| 2 | 66/M | LES | 8 | 10 | - | + | Bicitopenia y mucositis | - | 6 |
| 3 | 90/M | AR | 12 | 10 | - | - | Neumonitis | - | 20 |
| 4 | 85/H | AR | 12,8 | 15 | + | - | Pancitopenia | 1 CH | 6 |
| 5 | 77/M | DMS | 2 | 7,5 | - | - | Neumonitis | - | 37 |
| 6 | 80/M | AR | 115,9 | 15 | + | + | Pancitopenia y mucositis | 2 CH | 29 |
| 7 | 80/H | AR | 24 | 15 | + | - | Bicitopenia y mucositis | 2 CH y G-CSF | 11 |
| 8 | 94/H | AR | 63 | 12,5 | + | - | Pancitopenia | - | 6 |
| 9 | 79/M | AR | 72 | 10 | + | - | Trombocitopenia | - | Fallecido |
| 10 | 50/H | AR | 9 | 20 | - | - | Fibrosis pulmonar | - | 9 |
| 11 | 64/H | FOD | 1 | 15 | - | - | Neumonitis | 20 CH y 16 TP | Fallecido |
| 12 | 80/M | AR | 34 | 5 | - | - | Neumonitis | - | 9 |
| 13 | 64/M | AR | 27 | 20 | - | - | Anemia, mucositis y neurotoxicidad | - | 12 |
| 14 | 62/M | AR | 2 | 15 | - | + | Pancitopenia y mucositis | 4 CH y G-CSF | 10 |
| 15 | 94/H | AR | 276 | 15 | + | + | Bicitopenia | 3 CH | 20 |
| 16 | 89/M | AR | 240 | 7,5 | + | + | Pancitopenia | 1 CH | 11 |
| 17 | 69/M | AR | 156 | 7,5 | - | - | Pancitopenia | - | 8 |
| 18 | 80/H | AR | 108 | 10 | + | - | Hepatotoxicidad | - | 12 |
| 19 | 79/M | AR | 4 | 10 | + | + | Bicitopenia, mucositis y neumonitis | 2 CH | 10 |
| 20 | 66/M | AR | 24 | 20 | - | - | Pancitopenia y mucositis | 5 CH, 8 TP y G-CSF | 24 |
| 21 | 66/M | AR | 12 | 12,5 | - | - | Pancitopenia | 3 CH, 2 TP | 7 |
| 22 | 81/H | PSO | 48 | 10 | - | - | Neurotoxicidad | - | 13 |
| 23 | 74/H | AR | 168 | 20 | - | + | Pancitopenia y neumonitis | 2 CH and G-CSF | 36 |
| 24 | 76/H | AR | 2 | 15 | - | - | Bicitopenia y hepatotoxicidad | - | 8 |
| 25 | 87/M | AR | 192 | 15 | + | - | Pancitopenia, mucositis, piel y hepatotoxicidad | 4 CH, 2 TP y G-CSF | 15 |
AR: artritis reumatoide; CH: concentrados de hematíes; DMS: dermatomiositis; ERC: enfermedad renal crónica (FG<60ml/min/m2; albumina<3g/dl); FOD: fiebre de origen desconocido; G-CSF: factor estimulante de colonias granulocíticas; H: hombre; LES: lupus eritematoso sistémico; M: mujer; PSO: psoriasis; TP: pool de plaquetas.
Cuatro de los 25 casos analizados presentaban una intoxicación aguda debida a un error en la administración del fármaco, como ocurrió en nuestra paciente.
La media de edad de los pacientes fue de 76,7 años, con un rango comprendido entre 50-94 años. En el 84% de los pacientes el motivo del tratamiento fue una artritis reumatoide. La dosis de metotrexato osciló entre los 5 y 20mg semanales y la media de duración del tratamiento fue de 65 meses (tabla 1).
La mayoría de los pacientes presentaban otras enfermedades asociadas. Un 60% (15/25) presentaba un índice de comorbilidad de Charlson de 3 puntos o superior y en 4 pacientes constaba en su historia clínica el diagnóstico de deterioro cognitivo previo.
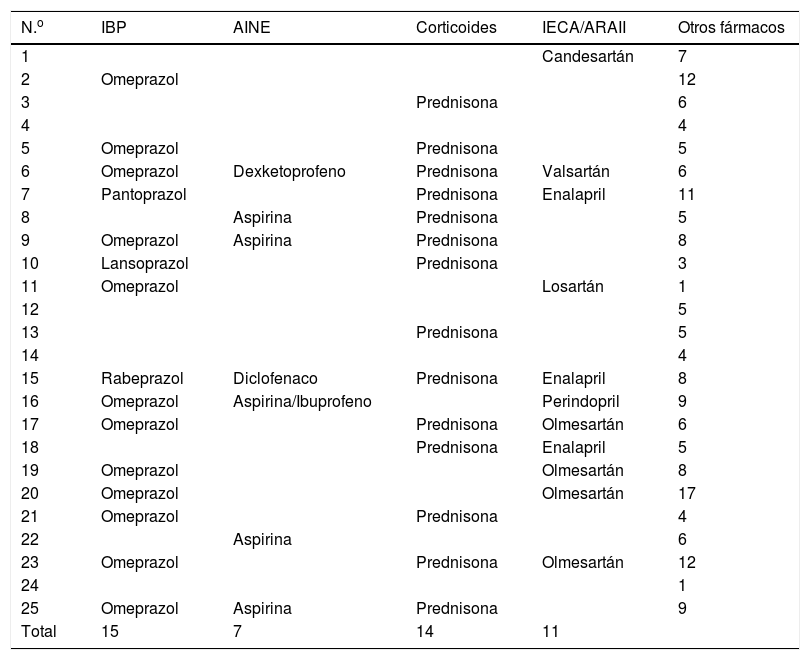
La mayoría de los pacientes realizaban tratamientos con otros fármacos, siendo la media de fármacos por paciente de 9,4. Un 40% consumía más de 10 comprimidos diferentes cada día. Además, era frecuente el uso concomitante de fármacos que pueden favorecer la toxicidad del metotrexato: el 60% tomaba inhibidores de la bomba de protones (IBP), 44% IECA o ARA II, 56% glucocorticoides y un 28% antiagregantes o AINE (tabla 2).
Otras medicaciones utilizadas
| N.o | IBP | AINE | Corticoides | IECA/ARAII | Otros fármacos |
|---|---|---|---|---|---|
| 1 | Candesartán | 7 | |||
| 2 | Omeprazol | 12 | |||
| 3 | Prednisona | 6 | |||
| 4 | 4 | ||||
| 5 | Omeprazol | Prednisona | 5 | ||
| 6 | Omeprazol | Dexketoprofeno | Prednisona | Valsartán | 6 |
| 7 | Pantoprazol | Prednisona | Enalapril | 11 | |
| 8 | Aspirina | Prednisona | 5 | ||
| 9 | Omeprazol | Aspirina | Prednisona | 8 | |
| 10 | Lansoprazol | Prednisona | 3 | ||
| 11 | Omeprazol | Losartán | 1 | ||
| 12 | 5 | ||||
| 13 | Prednisona | 5 | |||
| 14 | 4 | ||||
| 15 | Rabeprazol | Diclofenaco | Prednisona | Enalapril | 8 |
| 16 | Omeprazol | Aspirina/Ibuprofeno | Perindopril | 9 | |
| 17 | Omeprazol | Prednisona | Olmesartán | 6 | |
| 18 | Prednisona | Enalapril | 5 | ||
| 19 | Omeprazol | Olmesartán | 8 | ||
| 20 | Omeprazol | Olmesartán | 17 | ||
| 21 | Omeprazol | Prednisona | 4 | ||
| 22 | Aspirina | 6 | |||
| 23 | Omeprazol | Prednisona | Olmesartán | 12 | |
| 24 | 1 | ||||
| 25 | Omeprazol | Aspirina | Prednisona | 9 | |
| Total | 15 | 7 | 14 | 11 |
AINE: antiinflamatorio no esteroideo; ARAII: antagonista receptor angiotensina II; IBP: inhibidor bomba de protones; IECA: inhibidor enzima angiotensina.
Siete pacientes presentaban una enfermedad renal crónica previa al ingreso y en 10 pacientes se observó la existencia de hipoalbuminemia.
La toxicidad más frecuente fue la hematológica (72%), seguida de la afectación cutánea (32%). La mitad de los pacientes precisaron transfusión de hemoderivados. La neumonitis por toxicidad se observó en 7 pacientes y hubo 3 casos de hepatitis tóxica. Dos pacientes presentaron manifestaciones neurológicas, que se resolvieron tras la retirada del fármaco (tabla 1)
La estancia media hospitalaria fue de 14,1 días. La mayoría de los pacientes evolucionaron favorablemente, falleciendo únicamente 2 pacientes, uno debido a una neumonitis tóxica y otra paciente por una sepsis secundaria a neumonía.
Tal y como hemos comentado, se recogieron 4 casos de intoxicación aguda por error de administración en la dosis de metotrexato (tabla 1). La media de edad de estos pacientes fue de 78,3 años y los 4 tomaban otros medicamentos de manera concomitante (>7 fármacos). Tres de ellos tomaron por error el medicamento a diario y otro había abandonado el suplemento de ácido fólico.
DiscusiónEn nuestra serie hay un sesgo en la selección de los casos ya que solo se incluyeron los que requirieron ingreso debido a la toxicidad por su gravedad. Esto explica que el efecto adverso más frecuente en nuestro estudio fuera hematológico, precisando ingreso y en el 70% de ellos transfusión de componentes sanguíneos y/o factores estimuladores de colonias granulocíticas. La toxicidad hematológica (anemia, trombocitopenia o leucopenia) es poco frecuente y se estima en alrededor del 3% de los tratamientos crónicos con metotrexato, y la pancitopenia en el 1% de los casos3.
La edad media de los pacientes fue cercana a la octava década de la vida, confirmando lo que se describe como uno de los factores de riesgo más importantes de toxicidad4. La desnutrición y la enfermedad renal crónica también son más frecuentes en estos pacientes, junto con la polifarmacia (empleo de 3 a 5 fármacos al mismo tiempo), que por sí sola aumenta el riesgo de reacciones adversas medicamentosas y de interacciones farmacológicas5.
La excreción del metotrexato es inhibida por la presencia de ácidos débiles, como el ácido acetilsalicílico y AINE, y disminuida por otras medicaciones nefrotóxicas (IECA, ARA II). Sin embargo, el tratamiento con omeprazol es un factor de riesgo más debatido6. En nuestro estudio más de la mitad de los pacientes tomaban alguno de estos fármacos.
Las diferentes sociedades científicas han publicado reiteradamente recomendaciones para el seguimiento de los pacientes en tratamiento con metotrexato, recomendando controles analíticos periódicos7. Con este estudio queremos resaltar la importancia de que se sigan y cumplan estas recomendaciones, realizándose una monitorización si cabe más estrecha en los pacientes de edad avanzada, en los que conviene revisar regularmente los medicamentos que están tomando de forma crónica.
Se han notificado casos de toxicidades mortales relacionadas con la administración diaria involuntaria en lugar de semanal, especialmente en personas de edad avanzada. Por ello, en julio de 2004, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) emitió una nota informativa y realizó una actualización de la ficha técnica y del prospecto del metotrexato y una modificación del envase de presentación del fármaco, incluyendo mensajes sobre la dosificación semanal del fármaco por vía oral8. En julio de 2011 la AEMPS emitió una nueva alerta9. Sin embargo, continúan publicándose nuevos casos de intoxicación por error de dosis10, como sucede en nuestra revisión, en la que detectamos otros 4 pacientes.
En el caso que describimos, la paciente reunía varios factores de riesgo para presentar toxicidad por el fármaco y era una candidata idónea para que se produjera un error en la toma del mismo. Se le había diagnosticado deterioro cognitivo 2 años antes. Tenía escaso apoyo familiar, ya que vivía con su marido de edad similar y tomaba múltiples medicamentos. Durante su seguimiento, los diferentes médicos que la atendieron no se plantearon en ningún momento la conveniencia de seguir o no con el mismo esquema terapéutico.
A los pacientes se les receta un medicamento adecuado en un momento de su vida, pero a medida que envejecen y aparecen nuevas comorbilidades, creemos importante revalorar estos tratamientos y los fármacos concomitantes, para evitar en la medida de lo posible la aparición de nuevos casos.
Por ello, con el caso que presentamos nos gustaría llamar la atención sobre el hecho de que, aunque el metotrexato es un fármaco relativamente seguro, su uso debería ser estrechamente vigilado en aquellos pacientes que puedan ser más propensos a cometer errores en su administración, como puede ser el caso de los pacientes mayores, con comorbilidades y polimedicados.