Información de la revista
Vol. 18. Núm. 4.
Páginas 268-271 (julio 1999)
Vol. 18. Núm. 4.
Páginas 268-271 (julio 1999)
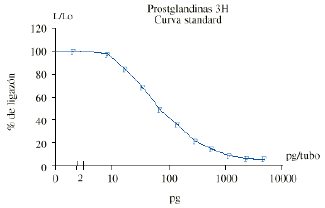
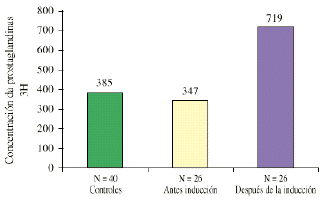
Prostaglandina E2 plasmática en mujeres embarazadas sometidas a inducción del trabajo de parto con aplicación endocervical de gel
PLASMA PROSTAGLANDIN E2 IN PREGNANT WOMEN UNDERGOING LABOR INDUCTION WITH ENDOCERVICAL GEL APPLICATION
Visitas
4187
M C. Siqueira, J. Neves, M P. Arteaga, M. Bicho, A. Silva Cruz
Este artículo ha recibido
Información del artículo
Opciones para acceder a los textos completos de la publicación Revista Española de Medicina Nuclear e Imagen Molecular
Socio
Si es usted socio de la Sociedad Española de Medicina Nuclear e Imagen Molecular (SEMNIM) puede acceder al texto completo de los contenidos de la Revista Española de Medicina Nuclear e Imagen Molecular desde los enlaces a la revista publicados en la web de la SEMNIN (enlace a https://semnim.es/iniciar-sesion/), previo inicio de sesión como socio. Si tiene problemas de acceso puede contactar con la Secretaría Técnica de la SEMNIM en el correo electrónico secretaria.tecnica@semnim.es o en el teléfono: + 34 619 594 780
Suscriptor
Suscribirse
Contactar
Teléfono para suscripciones e incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h
Llamadas desde España
932 415 960
Llamadas desde fuera de España
+34 932 415 960
E-mail