Los primeros estudios que ensayan el etidronato en la osteoporosis posmenopáusica datan del año 19711. Esta terapia administrada en forma continua, presentaba el inconveniente de producir efectos nocivos en la mineralización ósea. Posteriormente en 1984, Anderson et al2 aplicando las bases del tratamiento coherente propugnado por Frost3 observaron que la pauta de tratamiento cíclico con etidronato aumentaba notablemente el volumen trabecular en las biopsias de cresta ilíaca de 5 pacientes con osteoporosis posmenopáusica, sin encontrar trastornos de la mineralización ósea. Estas observaciones supusieron el punto de partida para la realización de diversos estudios para valorar la eficacia del etidronato en la osteoporosis.
En el año 1990, dos estudios publicados en New England Journal of Medicine4,5, valoran la efectividad del tratamiento cíclico con etidronato en la preservación de la masa ósea y en la reducción del riesgo de fractura vertebral en mujeres con osteoporosis posmenopáusica establecida. Estas dos publicaciones y otras posteriores proporcionaron en ese momento una evidencia suficiente para que este bifosfonato fuera aprobado en muchos países, con la indicación mencionada.
Actualmente la aparición de dos nuevos bifosfonatos, el alendronato y el risedronato, con indicación en la osteoporosis y con una actividad biológica superior al etidronato, plantean la pregunta de si éste continúa constituyendo una opción terapéutica de primera línea. Ya que no existen estudios comparativos entre estos fármacos que nos permitan dar una respuesta definitiva, nos referiremos, en esta revisión, a aquellos efectuados con el alendronato y el risedronato, que por la similitud de las poblaciones de estudio ha permitido comparar los resultados con los del etidronato.
Objetivos
Los objetivos de esta revisión han sido valorar la eficacia y seguridad del etidronato en la prevención y tratamiento de la osteoporosis posmenopáusica y la corticoide. Para ello, se han considerado los estudios que nos proporcionan una evidencia indirecta de la eficacia con la densidad mineral ósea (DMO) y los que valoran las fracturas óseas.
La seguridad se ha valorado con los efectos del etidronato en el tejido óseo, mediante los estudios histomorfométricos y la tolerancia en el aparato digestivo, que es la causa más frecuente de abandonos con este tipo de fármacos.
Se ha efectuado una búsqueda en MEDLINE (PubMed) desde el año 1990 hasta diciembre de 2000, aplicando los criterios de selección con la mayor evidencia que podemos exigir a los estudios de intervención terapéutica, es decir: prospectivos, controlados, aleatorizados y a doble ciego.
Osteoporosis posmenopáusica
Tratamiento cíclico con etidronato en la osteoporosis posmenopáusica establecida
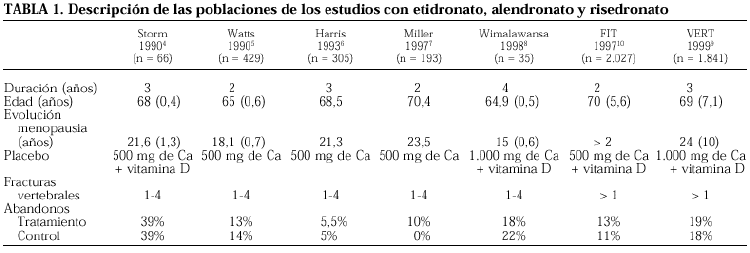
Densidad mineral ósea. Revisaremos cinco estudios4-8 que reúnen los criterios de selección mencionados y que presentan unas características basales muy similares: edad, tiempo de evolución de la menopausia y entre 1-4 fracturas vertebrales en el momento de iniciar el estudio. En el estudio de Miller et al7, únicamente se han valorado los resultados del sexto y séptimo años, correspondientes a la fase de doble ciego y la comparación se ha efectuado entre los grupos con un tratamiento acumulado de etidronato de 7 años y 2 años, respectivamente, por considerar que reúnen características similares a los otros estudios revisados. Estos estudios con etidronato superan a los 3 años el 5% de incremento de la DMO lumbar. El estudio de Wimalawansa et al8 pone de manifiesto que la DMO sigue aumentando cuando el tratamiento se prolonga durante más de 3 años. Estos resultados son equiparables a los obtenidos en el estudio de Harris et al (VERT)9 con el risedronato (5,4% [0,3]), e inferiores al del estudio de Black et al (FIT)10 con el alendronato (7,9% [0,1]), que presentan unas características de población muy similares de edad y evolución de la menopausia y todas las pacientes presentaban al menos una fractura vertebral osteoporótica a la entrada del estudio, lo que permite efectuar una relación de comparación con los de etidronato (tabla 1).
En el fémur también se observan, en las pacientes tratadas con etidronato, incrementos con respecto al punto de partida y las diferencias con los controles presentan valores significativos en el cuello femoral, triángulo de Ward y trocánter, y en la valoración femoral total8. La magnitud de las diferencias con respecto a los controles son superiores en los estudios con el alendronato10 y el risedronato9.
Fracturas. De los distintos trabajos revisados, los episodios de fracturas vertebrales incidentales se han valorado los resultados referentes al número de pacientes que presentan al menos una fractura vertebral, ya que diversas fracturas en un individuo no representan hechos independientes.
La reducción del riesgo relativo de mujeres con fracturas vertebrales en tratamiento con el etidronato resulta significativa en los estudios de Watts et al y Miller et al5,7, con una reducción del riesgo, con respecto a los controles, del 56 y el 88%, respectivamente. A pesar de que estas cifras son superiores a las encontradas en el estudio FIT10 y VERT9 (47 y 41%, respectivamente), hemos de tener presente que estos estudios con etidronato presentan un número escaso de participantes y el objetivo principal ha sido valorar los cambios en la DMO. Los estudios que aquí nos referimos con los otros dos bifosfonatos han sido diseñados para poder valorar fundamentalmente la reducción de fracturas vertebrales.
Tomando como patrón el diseño del estudio FIT10, para obtener una potencia metodológica del 99%, se precisa de una población de estudio del orden de 2.000 mujeres para observar reducciones de riesgo de fractura vertebral en un 40%, para un supuesto de incidencia anual de fracturas vertebrales en el grupo sin intervención del 6,5%. Los estudios revisados con el etidronato, en el mejor de los casos, presentan un poder por el referente (FIT) del 56%5.
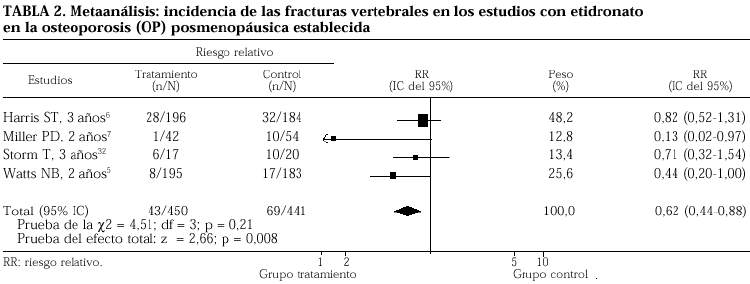
Con la finalidad de obtener un mayor peso en la evidencia del tratamiento cíclico con etidronato en la reducción de fracturas vertebrales, y dada la homogeneidad de las poblaciones de estos estudios con etidronato, hemos podido agrupar los resultados y realizar un metaanálisis. El peso estadístico obtenido ha sido suficiente para poder diferenciar un menor riesgo de fracturas vertebrales en las mujeres posmenopáusicas en tratamiento con etidronato al compararlo con los controles (tabla 2). La reducción del riesgo relativo de fractura ha resultado del orden del 40% (p = 0,008), muy similar al del alendronato10 y el risedronato9. Según estos resultados y en esta población de posmenopáusicas con osteoporosis establecida, el número de mujeres a tratar (NNT) durante 3 años para evitar al menos un episodio de fractura vertebral es de 17 para el etidronato y de 15 y 20 para el alendronato y risedronato, respectivamente9,10.
Es obvio que los estudios revisados con el etidronato carecen de los requisitos suficientes para poder valorar el efecto del etidronato en las fracturas no vertebrales. En un amplio estudio observacional de cohortes, realizado por Van Staa et al11, que reúne la información obtenida de 550 médicos generalistas del Reino Unido, un total de 7.977 pacientes de ambos sexos con tratamiento cíclico con etidronato fue comparado con un igual número de osteoporóticos apareados según edad y sexo y que no tomaban etidronato. La reducción de todas las fracturas no vertebrales fue del 20% y, atendiendo únicamente a las de cadera, la reducción fue del 34%. Aunque el tipo de estudio no es un ensayo clínico con un diseño previo para cumplir este objetivo y obtener unas conclusiones definitivas, nos proporciona una valiosa información de la eficacia del etidronato en las fracturas no vertebrales, especialmente la de cadera.
Tratamiento cíclico con etidronato en la prevención de la posmenopausia reciente
Estudios más recientes12-15, realizados en mujeres con una menopausia poco evolucionada y durante el seguimiento de 2 años, ponen de manifiesto que la terapia con etidronato es efectiva en la preservación de la masa ósea en la zona lumbar y en la cadera, a diferencia de los controles que al final del período de estudio presentan un balance negativo. En el estudio de Herd et al13, los resultados en la zona lumbar son más efectivos durante los primeros 3 años de la menopausia (etidronato +1,73% [0,8] frente a control 3,30% [0,7]) y pasados los 7 años (+3,42% [0,6] frente a 0,38% [0,7]). Meunier et al14 observan que al cabo de un año de finalizar el tratamiento con etidronato, la DMO de las pacientes desciende en la misma proporción que en el grupo control, aunque persisten valores superiores a los del inicio del estudio. El comportamiento de los marcadores del remodelado óseo, en estos estudios revisados, evidencia reducciones con respecto al estado basal de hasta el 25%, tanto para los de resorción como para los de formación ósea, lo que subraya la efectividad del etidronato en este período, en el que la pérdida de masa ósea es tan importante.
Osteoporosis corticoide
Tratamiento cíclico con etidronato en la prevención y tratamiento de la osteoporosis corticoide
Los corticoides a dosis elevadas están claramente implicados en el metabolismo óseo16,17; su utilización a dosis bajas durante períodos prolongados también está relacionada con una DMO baja y fracturas. En la prevención y el tratamiento de la osteoporosis corticoide se han ensayado diversos fármacos utilizados habitualmente en la osteoporosis involutiva, entre ellos el etidronato.
Los estudios revisados18-23, incluyen tres estudios de prevención y tres de tratamiento en pacientes con terapia crónica con corticoides. Las poblaciones de estudio se refiere a pacientes de ambos sexos, con enfermedades que requieren tratamiento corticoide: colagenosis, vasculitis, hepatopatías y neumopatías.
Prevención (DMO). Los tres estudios de prevención que revisamos18-20 incluyen a pacientes que habían iniciado el tratamiento corticoide, durante los 3 meses previos al seguimiento. La duración de éstos fue de un año y las dosis medias de corticoides durante el estudio oscilaron entre 2,9 (0,9) y 13 (10) mg/día de prednisona. En todos ellos el grupo control, que estaba suplementado con 500 mg de calcio diario experimentó descensos de la DMO lumbar, entre el 2,7 y el 3,7% al final del estudio, mientras que los pacientes con etidronato mantuvieron incrementos discretos con respecto al inicio. Las diferencias de DMO lumbar entre los grupos con intervención y los controles resultaron significativas. En el fémur, únicamente en el estudio de Adachi et al19, la diferencia con el grupo control resultó significativa en el trocánter (4,14% [0,9]) (p = 0,02). Los resultados de los estudios en la prevención de la osteoporosis corticoide, en la columna, con el alendronato24 son superiores al etidronato (2,9% [0,3] frente a 0,61% [0,54]) y similares a los del risedronato25 (0,6% [0,5]). En el fémur tanto el alendronato24 como el risedronato25 presentaron mayor eficacia en todas las localizaciones.
Tratamiento (DMO). En los pacientes con tratamiento prolongado de corticoides22-24, la DMO lumbar aumentó significativamente entre el 4,8 y el 5,1% a los 2 años de tratamiento con etidronato, observándose respuestas a los 6 meses. El estudio de Pitt et al22 es el único en el que el grupo control incrementa significativamente la DMO lumbar y también es el único de éstos en que el grupo control tomaba suplementos con 400 U de vitamina D.
En el fémur, menos en el estudio de Guesens et al23, el alendronato y el risedronato evidencian una efectividad superior al etidronato.
Fracturas. En el estudio de prevención de Adachi et al19, el etidronato demuestra ser efectivo en la reducción del riesgo de fracturas vertebrales (RR = 0,15), al igual que en el estudio de Saag et al con el alendronato24, en el subgrupo de pacientes posmenopáusicas. El risedronato26 resulta efectivo en la reducción de las fracturas vertebrales en el conjunto de la población de estudio, varones, mujeres pre y posmenopáusicas con tratamiento crónico con corticoides.
Estudios comparativos con otros fármacos
Hay estudios que comparan el etidronato con otros bifosfonatos: pamidronato y clodronato, con la THS, con la calcitonina y con el flúor. En la osteoporosis posmenopáusica el etidronato, en alguno de éstos, es menos efectivo que la THS27. Con respecto al flúor, es inferior en cuanto a la DMO, pero con una efectividad comparable en la reducción de fracturas vertebrales28.
En la osteoporosis corticoide los resultados son similares al pamidronato y al clodronato y superiores a la calcitonina29,30.
Como hemos podido observar en esta revisión, hay evidencias que demuestran al etidronato efectivo en la preservación de la DMO de la osteoporosis posmenopáusica y corticoide, aunque el alendronato y risedronato evidencian una efectividad superior en el fémur. Es interesante comentar que en la osteoporosis posmenopáusica, de los estudios revisados, del 15 al 20% de los pacientes en tratamiento con etidronato no aumentan la DMO durante el tiempo de estudio frente a un 5% en el estudio FIT con alendronato. La tasa de pacientes que incrementan la DMO en la osteoporosis corticoide es del 60-78% en los estudios con el etidronato frente a un 80% con el alendronato. Los estudios revisados con el risedronato no nos proporcionan dicha información.
El resultado del metaanálisis nos proporciona una base suficiente para pensar en un estudio de gran envergadura, y poder concluir definitivamente sobre la efectividad del etidronato en la reducción de fracturas vertebrales. En los estudios de prevención de la osteoporosis corticoide los resultados en la reducción de fracturas son parecidos a los del alendronato. El risedronato presenta una mayor eficacia en los pacientes con tratamiento crónico con corticoides.
Seguridad
Seguridad ósea
Los estudios de seguridad ósea, mediante histomorfometría7,32,34, en períodos de seguimiento largos, como el de Miller et al7 durante 7 años, son unánimes en concluir que no hay criterios de osteomalacia, observando disminución de la frecuencia de activación de las unidades de remodelado, así como disminución de la profundidad de resorción, mecanismos que pueden explicar la efectividad de los bifosfonatos en la DMO y las fracturas.
Efectos gastrointestinales
Los efectos adversos del etidronato en el tracto gastrointestinal, frecuentes con este tipo de fármacos, ha sido valorada en los ensayos clínicos presentados. La disposición de un amplio estudio posmárketing34, que nos proporciona una información real de lo que pasa en el día a día de nuestras consultas, nos permite ser concluyentes en observar unos efectos adversos similares en los pacientes osteoporóticos, de ambos sexos, tratados y no tratados con etidronato. Tampoco se observaron diferencias atendiendo a la toma de medicación concomitante (antiinflamatorios no esteroides y corticoides).
Todo ello nos reafirma la opinión de la gran tolerancia digestiva del etidronato con este régimen de administración cíclica.
Conclusiones
Con las premisas de selección efectuadas en esta revisión, podemos concluir que existe evidencia suficiente de la eficacia del etidronato en la preservación y restauración de la DMO en la osteoporosis posmenopáusica y corticoide, aunque los estudios con el alendronato y el risedronato presentan una mayor acción en la zona femoral.
En la osteoporosis posmenopáusica establecida, el etidronato presenta un efecto antifractura vertebral en algún estudio, aunque la potencia estadística de ellos es muy débil. El resultado encontrado en el metaanálisis nos proporciona una base sólida para inducirnos a efectuar un estudio de mayor envergadura que los existentes. También reduce la tasa de fracturas en mujeres posmenopáusicas que inician tratamiento con corticoides.
Los resultados del amplio estudio observacional atribuyen al etidronato una eficacia en la reducción de las fracturas no vertebrales, especialmente las de cadera.
La seguridad ósea esta avalada por los estudios histomorfométricos, durante largos períodos de tratamiento.
Los estudios de tolerancia gastrointestinal presentan el etidronato como un fármaco seguro con efectos adversos equiparables a los controles.