Introducción
La artritis reumatoide (AR) es una enfermedad sistémica inflamatoria que afecta fundamentalmente a las articulaciones y que suele seguir un curso crónico con fluctuaciones. La inflamación persistente en la membrana sinovial es capaz de producir un deterioro irreversible en el cartílago articular y en el hueso subcondral que limita la funcionalidad de la articulación y que puede llevar al paciente a un grado de incapacidad importante en pocos años. En la última década, se ha hecho especial hincapié en la conveniencia de realizar un diagnóstico temprano y de instaurar un tratamiento eficaz que controle la enfermedad, eliminando o reduciendo al máximo la sinovitis crónica. El pronóstico de los pacientes con AR ha mejorado con la disponibilidad de fármacos modificadores de la enfermedad (FAME) que pueden controlar la actividad de la enfermedad en un gran número de enfermos, si bien su remisión completa es infrecuente.
La leflunomida (LFN) es un fármaco incorporado recientemente al arsenal terapéutico de la AR. Es un derivado isoxazólico que actúa fundamentalmente como inhibidor selectivo de la síntesis de novo de las pirimidinas en las células de la respuesta inmune, en particular, los linfocitos T activados. El metabolito activo de la LFN, el A77 1726, inhibe de forma reversible la dihidroorotato deshidrogenasa, un enzima mitocondrial esencial en la síntesis de novo de pirimidinas1. Se ha demostrado la eficacia de LFN tanto en modelos animales como en ensayos clínicos y en la práctica habitual en pacientes con AR2.
La actividad de la enfermedad y la respuesta terapéutica se pueden evaluar de forma cuantitativa; en este sentido, se recomienda medir una serie de parámetros en cada paciente3, a partir de los cuales se obtienen distintos índices y criterios de respuesta: criterios ACR 20 o 50%4 y criterios EULAR5 basados en el índice DAS (Disease Activity Score)6. Ambos criterios de mejoría presentan un alto nivel de concordancia entre ellos y se ha demostrado su validez para discriminar entre distintos tratamientos y una asociación significativa con la progresión radiológica de la enfermedad7.
Existe un grupo de enfermos con AR que no responden a distintos FAME, en unos casos por ineficacia, en otros por mala tolerancia y en algunos por mal cumplimiento terapéutico. No existen estudios publicados en los que se evalúe la eficacia de la LFN en la AR refractaria empleando ambos criterios de respuesta. El objetivo del presente estudio fue conocer la eficacia y seguridad de la LFN en pacientes con AR refractaria, en condiciones asistenciales reales.
Metodología
Se realizó un estudio abierto, no controlado, longitudinal y prospectivo para valorar la respuesta clínica a la LFN en pacientes con AR refractaria, entendiendo como tales a aquellos que hubieran recibido al menos tres FAME previamente o bien dos siempre que uno de ellos hubiera sido metotrexato y que mantenían, a juicio del reumatólogo, una actividad inflamatoria inaceptable que justificaba el cambio de medicación.
Se empleó LFN en monoterapia, siguiendo la pauta de dosificación habitual, es decir, una dosis de carga de 100 mg/día durante los tres primeros días y 20 mg/día como dosis de mantenimiento. Se permitía la reducción de la dosis a 10 mg diarios en aquellos pacientes que lo requirieran por efectos secundarios.
El estudio se inició en mayo de 2000 y se recogieron datos de todos los enfermos que recibieron LFN a lo largo de un año. Participaron los 6 médicos reumatólogos y la enfermera especializada del servicio. La recogida de datos se llevó a cabo en las consultas externas con revisiones cada tres meses. Los parámetros evaluados fueron los siguientes:
Eficacia
Índice de Ritchie.
Recuento del número de articulaciones dolorosas (NAD).
Recuento del número de articulaciones tumefactas (NAT).
Valoración del dolor por el paciente, según escala analógica visual (EAV de 0-100 mm).
Valoración global de la actividad de la enfermedad por el paciente (EAV de 0-100 mm).
Valoración global de la actividad de la enfermedad por el médico (EAV de 0-100 mm).
Duración de la rigidez matutina en minutos.
Clase funcional según la clasificación de Steinbroker de I a IV.
Reactantes de fase aguda: VSG, proteína C reactiva (PCR) o ambas.
Valoración de la capacidad funcional, mediante el cuestionario Health Assessment Questionnaire (HAQ) modificado, de 8 ítems. En un subgrupo de pacientes seguidos en consulta de enfermería a partir de diciembre de 2000 también se recogió el cuestionario HAQ de 20 ítems.
La variable principal de medición de eficacia fue el porcentaje de pacientes con respuesta a la LFN. Para ello se utilizaron los criterios siguientes:
Criterios EULAR5, que valoran la eficacia en tres grados de respuesta: mejoría, respuesta moderada y no mejoría. Se basan en los índices compuestos DAS6 y DAS288. En el primero se tiene en cuenta el recuento de dolor a la palpación en 53 articulaciones y presencia de tumefacción en 44 articulaciones. En el DAS28 se tienen en cuenta sólo 28 articulaciones en ambos recuentos.
Criterios ACR20 y ACR50, que valoran la eficacia según el porcentaje de pacientes que consiguen una respuesta del 20 o del 50% de un conjunto de parámetros clínicos, funcionales y analíticos4.
Otras variables de eficacia valoradas fueron la variación cuantitativa de los índices DAS y DAS28 y el porcentaje de retiradas de LFN por ineficacia.
En el estudio de eficacia sólo se tuvieron en cuenta aquellos pacientes que llevaban al menos dos meses de tratamiento con LFN y se les hubiera practicado la evaluación inicial y al menos una evaluación evolutiva.
Tolerancia
Las determinaciones de laboratorio (hematología y bioquímica renal y hepática) para el control del medicamento se efectuaron con periodicidad mensual. Se recomendó a los pacientes vigilar su presión arterial (PA). La notificación de reacciones adversas de la medicación se llevó a cabo en las revisiones programadas o en el momento de producirse, pudiendo contactar el paciente con los médicos a través de la consulta de enfermería. Quedaba a juicio del reumatólogo determinar si la reacción adversa podía ser achacada presumiblemente a LFN y la gravedad de la misma. Según el mismo criterio, se aconsejaba la continuación de la medicación, la disminución de la dosis a 10 mg/día o la suspensión temporal o definitiva del fármaco.
La variable de medición primaria de seguridad fue el porcentaje de retiradas de LFN por efectos adversos.
En el estudio de tolerancia se incluyeron todos los pacientes que recibieron al menos una dosis de LFN y se disponía de alguna evaluación posterior.
Análisis estadístico
Por tratarse de un estudio abierto y no controlado, el análisis estadístico de los datos de eficacia y seguridad tuvo fundamentalmente un carácter descriptivo. Se emplearon pruebas paramétricas y no paramétricas de comparación de medias (t de Student y U de Mann-Whitney) para relacionar los índices de eficacia con las variables sexo, edad, años de evolución de la enfermedad, seropositividad, número de FAME y de tratamientos combinados previos. Se empleó la prueba de la χ2 de Pearson para explorar la asociación entre variables cualitativas. La base de datos se realizó en un archivo File Maker Pro PC y el tratamiento estadístico se llevó a cabo con el programa SPSS, versión 10.0 para Windows.
Resultados
Eficacia
En el período comprendido entre mayo de 2000 y mayo de 2001 recibieron LFN un total de 46 pacientes con AR. Tres no cumplían los criterios de refractariedad. Tres pacientes se excluyeron del estudio de eficacia por disponer sólo de los datos de la consulta basal: dos no acudieron a revisión y a una paciente, que abandonó el tratamiento por ineficacia subjetiva, no se le realizaron las mediciones para calcular los índices DAS y ACR. Cinco pacientes abandonaron el tratamiento con LFN por efectos adversos antes de los dos meses. Las características de los 35 pacientes restantes que cumplían los criterios de inclusión en el estudio de eficacia se presentan en la tabla 1. El 77% eran mujeres y la media de la edad fue de 56,8 años. La media de duración de la enfermedad fue de 16,9 años. En el 77% de los casos el factor reumatoide (FR) era positivo. Habían recibido una media de 4,7 FAME en monoterapia y 1,5 tratamientos FAME combinados previamente. El 46% de los pacientes permanecían en una clase funcional III y el 51% en una clase funcional II de la clasificación de Steinbrocker. La media de duración del tratamiento con LFN fue de 6,5 meses.
En la tabla 2 se indica la respuesta a LFN según los criterios de mejoría EULAR. Diecinueve pacientes (54%) experimentaron mejoría o bien una respuesta moderada al tratamiento, mientras que en 16 pacientes (46%) no hubo respuesta según el índice DAS. Éste se redujo desde una media inicial de 3,84 (DE: 0,8) hasta un valor final medio de 3,06 (DE: 1,0) (p < 0,001). Trece pacientes (37%) alcanzaron un valor final del índice DAS menor de 2,4, lo que se considera inactividad. Por el contrario, 8 pacientes (23%) tuvieron valores finales de DAS superiores a 3,7, lo que se considera enfermedad activa. El porcentaje de respondedores según el DAS28 fue similar: 19 pacientes (54%) con mejoría o respuesta moderada y el 46% sin respuesta, si bien el número de pacientes con mejoría fue menor dos pacientes (5%) y el de respuesta moderada mayor que con el índice DAS, 17 pacientes (49%). El DAS28 descendió desde cifras iniciales de 5,1 (DE: 0,9) hasta un valor medio final de 4,2 (DE: 1,9) (p < 0,001). No hubo diferencias entre los respondedores y no respondedores en cuanto al sexo, años de evolución de la enfermedad, seropositividad, número de FAME previos, número de tratamientos combinados previos ni actividad (DAS) al inicio del tratamiento. En los pacientes de mayor edad se observó una tendencia no significativa a mejorar según criterios EULAR (p = 0,058).
Catorce pacientes (40%) alcanzaron una mejoría según el índice ACR20 y cuatro (11%) mejoraron según el índice ACR50 (tabla 3). Tampoco hubo diferencias entre los respondedores y no respondedores al comparar la respuesta según las variables referidas anteriormente para los criterios EULAR y, al igual que en este caso, también hubo una tendencia a mejorar según ACR20 en los pacientes de más edad (p = 0,058).
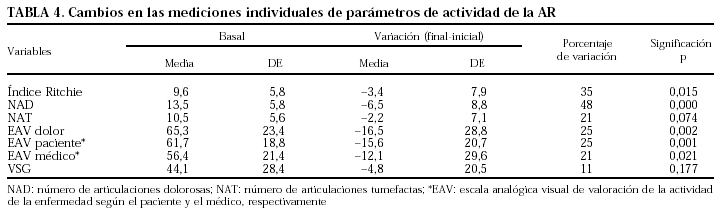
En la tabla 4 se exponen las diferencias entre las distintas mediciones individuales realizadas al inicio y al final del tratamiento en los 35 pacientes analizados. Hubo diferencias significativas en las variables índice de Ritchie, NAD, EAV de actividad del paciente y del médico, EAV del dolor según el paciente y duración de la rigidez matutina. No hubo diferencias significativas entre los valores iniciales y finales de NAT y VSG.
Tolerancia
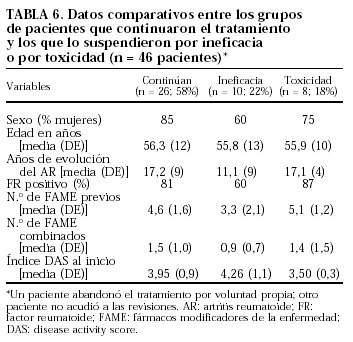
Una paciente se excluyó del estudio de tolerancia ya que no acudió a ninguna revisión. De los 45 pacientes restantes, 26 (58%) continuaban el tratamiento con LFN tras una media de 7,1 meses. Entre ellos, en 7 casos hubo de reducirse la dosis de LFN a 10 mg/día por distintos efectos adversos leves o pasajeros. Diecinueve pacientes (41%) suspendieron la LFN: una paciente lo hizo por voluntad propia tras un cumplimiento muy irregular; 10 pacientes (22%) abandonaron la LFN por ineficacia tras una media de 5,9 meses de tratamiento; 8 pacientes (18%) suspendieron el tratamiento por efectos adversos al cabo de una media de 3,1 meses. En la tabla 5 se recogen los motivos que obligaron a la suspensión de LFN en estos pacientes. Se observaron otros efectos secundarios que no requirieron la suspensión definitiva, sino la reducción en algunos casos de la dosis de LFN a 10 mg/día. Estos efectos secundarios fueron: cefalea (1), astenia (2), pérdida de peso (1), deposiciones diarreicas pasajeras (2), temblor (1), prurito leve (1), alopecia (1), hipertensión arterial controlada con medicación (1), elevación transitoria de las transaminasas (1) y leucopenia leve (1). En la tabla 6 se indican las características diferenciales de los pacientes que continuaron el tratamiento, los que abandonaron por ineficacia y los que lo hicieron por toxicidad. No hubo diferencias significativas entre estos grupos en cuanto al sexo, la edad, los años de evolución de la AR, la seropositividad, el número de tratamientos previos ni la actividad de la enfermedad medida con el índice DAS al inicio del tratamiento.
Discusión
En el presente estudio, realizado en condiciones de práctica clínica habitual, se ha evaluado la eficacia de LFN en el control de la actividad inflamatoria en un grupo de pacientes con AR caracterizados por una larga duración de la enfermedad y una pobre respuesta a tratamientos previos con otros FAME. Se consideró que los pacientes tenían una AR refractaria si no habían mejorado al menos con tres fármacos o bien dos de ellos siempre que uno fuera metotrexato. Para cuantificar la respuesta al tratamiento con LFN de forma objetiva se utilizaron tanto los criterios europeos como los americanos.
Las características de los pacientes de nuestro estudio coinciden en general en la edad, distribución por sexos y presencia de FR con las de los estudios controlados publicados sobre la eficacia de LFN en la AR. Sin embargo, se diferencian tanto en la duración media de la enfermedad (16,9 años) como en el número de terapias previas con FAME (4,7). Así, en un estudio en fase II de búsqueda de dosis eficaces9 en 402 pacientes con AR, la duración media de la enfermedad fue de 8,3 años. En el estudio de Strand et al10, que comparaban LFN con metotrexato y placebo en 482 pacientes, la duración media de la AR fue de 6,7 años y el número de tratamientos previos ineficaces fue de 0,8. En el estudio del Grupo Europeo de Estudio de la Leflunomida publicado por Smolen et al11 en 358 pacientes comparando la eficacia de LFN con sulfasalacina y placebo, la duración media de la AR fue de 7 años y el 41% de los pacientes tenían una enfermedad de menos de dos años de evolución. Entre el 40 y el 53% de los pacientes no habían recibido ningún FAME previamente. Finalmente, en el trabajo del Grupo Multinacional para el Estudio de la Leflunomida publicado por Emery et al12 en 999 pacientes con AR activa que comparaba la eficacia de LFN con metotrexato, la duración media de la enfermedad fue de 3,5 a 3,8 años según los grupos y la media de FAME previos fue de 1,1. En nuestro estudio todos los pacientes tenían una AR de más de 4 años de evolución y los propios criterios de inclusión exigían al menos dos terapias previas con FAME.
La eficacia de LFN en los estudios citados, medida en términos de porcentaje de respuesta ACR20, fue en general superior a la encontrada en nuestros pacientes. En el primer estudio en fase II, el porcentaje de respuesta fue del 50 y 59% en los pacientes tratados con 10 y 25 mg/día de LFN, respectivamente, frente al 28% de los pacientes que respondieron al placebo9. En el trabajo de Strand et al, el índice de respuesta ACR20 fue del 52 frente al 26% de respuesta en el grupo placebo10; en el estudio del grupo europeo el porcentaje de respuesta ACR20 con LFN fue del 55 frente a un 29% con placebo11, y en el estudio multinacional, el porcentaje fue del 50,5% tras el primer año de tratamiento12. Como se observa, hay una cifra consistente de respuesta ACR20 entre el 50 y el 55% de los pacientes en los ensayos clínicos; el porcentaje del 40% observado en nuestro estudio puede deberse al pequeño tamaño de la muestra, a la propia naturaleza del mismo, hecho en condiciones de práctica habitual, en las que la adherencia al tratamiento suele ser más irregular, y a las características señaladas de tratarse de pacientes con mayor duración de la enfermedad y mayor número de fracasos terapéuticos previos.
No existen publicaciones que ofrezcan específicamente el porcentaje de respuesta según el índice DAS en los ensayos clínicos mencionados. En un trabajo publicado en forma de resumen para la validación del índice SDAI (Simplified Disease Activity Index) empleando la base de datos de LFN, se muestra la diferencia entre el valor inicial y final del DAS28 en los tres ensayos clínicos principales. El DAS28 varió de 7 a 5,43 a los 6 meses en el estudio comparativo con sulfasalacina y desde valores de 6,3 y 6,99 hasta 4,9 al cabo de 12 meses en los estudios comparativos de LFN con metotrexato13. En nuestro estudio, el DAS28 descendió desde una media inicial de 5,1 hasta un valor medio final de 4,2. Se ha establecido que existe una buena correlación entre los índices de respuesta ACR20 y DAS, si bien este último parece detectar mejor las diferencias después de un tratamiento14. En nuestro estudio también encontramos asociación (p = 0,000) entre ambos criterios de respuesta, si bien hubo 6 pacientes que no alcanzaron una mejoría según ACR20 y sí lo hicieron con los criterios EULAR.
En el grupo de 35 pacientes valorados para eficacia, se produjo un descenso significativo en la mayoría de las variables individuales analizadas entre los valores iniciales y finales, con excepción del NAT y de la VSG. La VSG media se redujo un 11%. En el estudio comparativo de LFN con sulfasalacina se observó un descenso de sólo el 13% de la VSG al cabo de 6 meses en comparación con el descenso del 33% observado con la sulfasalacina11. En el estudio de Emery et al, la VSG media descendió al cabo de dos años un 27% con LFN frente al 51% con metotrexato12. No se observó tanta diferencia en el estudio de Strand et al, en el que los descensos en la VSG fueron del 16% con LFN y del 19% con metotrexato10. No obstante, se observa en general una disminución sólo moderada de la VSG, lo cual tiene cierta relevancia a la hora de valorar la respuesta según el índice DAS en el que la VSG figura como uno de los componentes del mismo.
En nuestro estudio, el 58% de los pacientes continuaban con el tratamiento de LFN al cabo de una media de 6,5 meses. El porcentaje de retiradas por toxicidad achacada a LFN fue del 18%. En un trabajo publicado en forma de resumen sobre la experiencia con LFN durante un año en una población americana de 119 pacientes con AR de características parecidas a las de nuestro estudio (duración media, 14,6 años; 4,2 FAME previos por paciente), al cabo de un año continuaban el tratamiento un 48% de los pacientes y se retiraron por toxicidad el 17% de los mismos15. En los tres grandes estudios comparativos reseñados, las cifras de retirada por toxicidad variaron entre el 14 y el 22% de los pacientes.
No se observó ninguna reacción adversa grave que pusiera en peligro la vida del paciente y que pudiera ser achacada directamente a la LFN. El caso más llamativo fue la aparición de una proteinuria en rango nefrótico coincidente con la retirada de metotrexato e inicio de la LFN en una paciente en la que se demostró finalmente la presencia de amiloidosis. La proteinuria fue disminuyendo al retirar la LFN y añadir clorambucil. En los dos casos de retirada por hepatotoxicidad, las transaminasas se normalizaron al suspender el tratamiento con LFN. En uno de estos casos existía una hepatitis crónica persistente demostrada por biopsia e historia de toxicidad hepática con otros FAME. Entre los efectos adversos menores, destaca el de una paciente que experimentó una gran mejoría con LFN pero presentó un cuadro de pérdida de peso importante, finalmente estabilizado, por lo que se decidió no suspender la medicación. Este efecto secundario de LFN ha sido confirmado recientemente16.
La tasa de retiradas por ineficacia en nuestro estudio fue del 22%, cercano al 17% de retiradas por este motivo en el estudio de Strand et al10 y superior a la observada en los trabajos del grupo europeo (8%)11 y del grupo multinacional (7%)12. Realmente, hasta hace pocos años y durante una década no había aparecido ningún FAME nuevo con eficacia demostrada para el control de la AR. Por tanto, la mayoría de las terapias, aunque no consiguieran un grado de mejoría aceptable, se mantenían durante un tiempo más prolongado en monoterapia o en asociación, en espera de conseguir con el tiempo un mejor control de la enfermedad, ya que no había otra alternativa. La aparición reciente de las terapias biológicas con fármacos anti-TNF, de eficacia demostrada tanto en el control de la inflamación como en el daño estructural17, hace que los FAME habituales, entre ellos la LFN, se retiren tras un período relativamente corto si no se consigue una mejoría suficiente. Tanto la Sociedad Española de Reumatología18 como la EULAR19, a través de paneles de expertos, han publicado recomendaciones en este sentido. En nuestro país, se ha definido la respuesta terapéutica satisfactoria y también el fracaso terapéutico, este último consistente en una respuesta inferior al índice ACR20 o la presencia de 6 o más articulaciones inflamadas o de inflamación en una articulación que por circunstancias del paciente le provoque una pérdida importante de su capacidad funcional18. Un Comité de Expertos de la EULAR reunidos en Viena consideró como una AR activa la presencia de 5 o más articulaciones inflamadas y dolorosas en un recuento de 28 articulaciones y al menos un reactante de fase aguda elevado o bien en presencia de una puntuación DAS28 mayor de 3,219. Se considera que el tiempo mínimo de tratamiento con LFN necesario para considerar que ésta no es eficaz es de tres meses18. Aunque estas recomendaciones se publicaron con posterioridad al inicio de nuestro estudio, 8 de los 10 pacientes que abandonaron el tratamiento con LFN por ineficacia reciben en la actualidad tratamiento con infliximab. Sólo se ha usado la combinación LFN y metotrexato en una paciente que no había alcanzado mejoría con LFN en monoterapia, comprobándose una mejoría importante de la actividad de la enfermedad sin aparecer efectos secundarios hasta la actualidad. Se ha demostrado la eficacia de esta combinación20, si bien hay que realizar estudios a largo plazo que demuestren las seguridad de dicha asociación.
En resumen, el tratamiento con LFN en un grupo de pacientes con AR refractaria atendidos en condiciones de asistencia reales demostró una eficacia moderada en el control de la actividad de la enfermedad. Más de la mitad de los pacientes continuaron con la medicación al cabo de 6 meses. La tasa de respuesta según el índice ACR20 fue del 40%; según los criterios EULAR, la tasa de mejoría o de respuesta moderada fue del 54%. La mayoría de los efectos secundarios observados fueron leves, si bien en el 18% de los casos obligaron a la suspensión del tratamiento por la intensidad o persistencia de los mismos. Creemos que la LFN es una posibilidad terapéutica aceptable que ha de ensayarse en un paciente con AR antes de considerar el uso de una de las terapias biológicas disponibles en la actualidad.
Agradecimientos
A Fayna Álamo Santana y Dolores Fiuza Pérez (Unidad de Investigación del Hospital de Gran Canaria Dr. Negrín) por su inestimable colaboración en el análisis estadístico de los datos.