Introducción
El etanercept es la proteína de fusión que combina la porción soluble, extracelular, del receptor p75 del factor de necrosis tumoral alfa (TNF-*) con dominios del fragmento Fc de la inmunoglobulina (Ig) G1 humana. Se sigue proporcionando información que confirma su eficacia y seguridad a largo plazo, así como nuevas perspectivas en su uso clínico, tanto en lo que se refiere a la pauta de dosificación como a su uso combinado con metotrexato en el tratamiento de la artritis reumatoide. Finalmente se conocen los resultados de investigaciones que han explorado otras vías de administración del fármaco, como es la vía intraarticular.
Eficacia
Desde el punto de vista de la eficacia, se dispone de datos de seguimiento, en extensión abierta a 5 años, de 1.442 pacientes con artritis reumatoide que recibieron, en Estados Unidos, etanercept en monoterapia, 25 mg por vía subcutánea 2 veces a la semana1. Al cabo de este largo período de seguimiento, el 29% de los pacientes presentaba un número de articulaciones dolorosas igual a 0, el 25% tenía un número de articulaciones inflamadas de 0, y en el 17% de los individuos la puntuación del Health Assessment Questionnary (HAQ) fue de 0. En Europa, un estudio abierto similar2 ha permitido observar, tras 4 años de tratamiento con etanercept a la misma dosis en 332 pacientes con artritis reumatoide, unas respuestas ACR 20, 50 y 70 del 79, 53 y 26%, respectivamente.
En sujetos con artritis reumatoide de reciente comienzo, el ensayo ERA, después de un período de doble ciego de 2 años, se continuó con una extensión abierta. En los pacientes inicialmente aleatorizados a etanercept, 25 mg por vía subcutánea 2 veces a la semana, que han completado el quinto año de tratamiento las respuestas ACR 20, 50 y 70 son del 68, 49 y 33%, respectivamente3. El 31% de estos sujetos, al final del quinto año, tiene un número de articulaciones dolorosas igual a 0. El 24% no tiene articulaciones inflamadas, y en el 32% el HAQ es de 0. La proteína C reactiva se ha normalizado en el 71% de los individuos, y el 73% de los mismos ha podido reducir o suprimir la dosis de glucocorticoides. La progresión del índice total de Sharp en estos pacientes ha sido de 1,14 (frente a 2,69 para el grupo que recibía metotrexato), 0,37, 0,41 y 0,42 en los años 2.º, 3.º, 4.º y 5.º, respectivamente.
Una prolongación de otro ensayo clínico4 permite conocer los datos de seguimiento de 61 pacientes con artritis reumatoide tratados en extensión abierta, una mediana de 56 meses, con la combinación de etanercept y metotrexato: el 61% disminuye o suprime el metotrexato; el 85%, los glucocorticoides; el 27% tiene un número de articulaciones dolorosas = 0; el 22%, un número de articulaciones inflamadas = 0, y el 15%, un HAQ de 0. A los 4 años de tratamiento las respuestas ACR 20, 50 y 70 son del 76, 45 y 18%, respectivamente5.
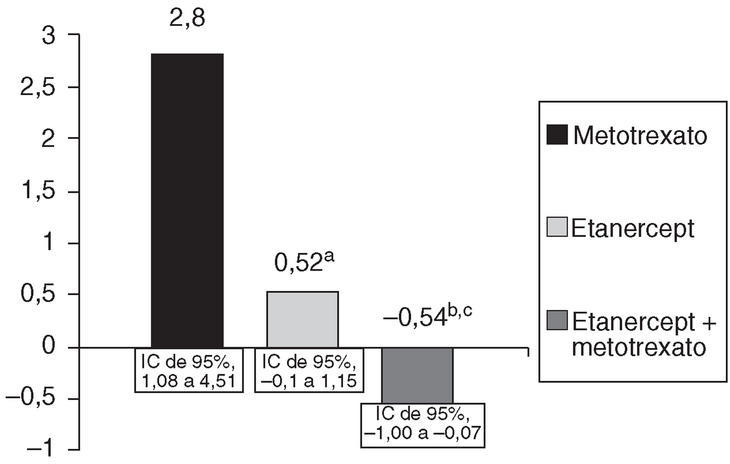
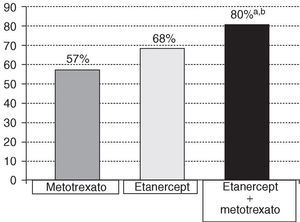
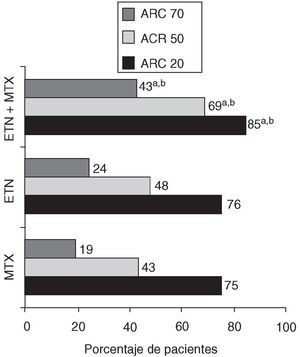
El estudio TEMPO6 es un ensayo clínico aleatorizado doble ciego en el que se ha incluido a 686 pacientes con artritis reumatoide activa de hasta 20 años de evolución, con el fin de evaluar la respuesta terapéutica, básicamente los cambios radiológicos, en 3 ramas de tratamiento: etanercept 25 mg por vía subcutánea 2 veces a la semana, metotrexato en escala rápida de dosis (hasta 20 mg/semana a las 8 semanas) y la combinación de los dos anteriores. Se incluyó a pacientes con enfermedad activa, con fallo previo a fármacos antirreumáticos modificadores de la enfermedad (FAME) distintos del metotrexato. La variable primaria de desenlace fue la progresión radiológica medida por el índice de Sharp total a las 52 semanas (cambio con respecto a la basal); 642 pacientes pudieron someterse a este análisis. Los resultados de este estudio se exponen en las figuras 1, 2 y 3. Como se puede observar en ellas, la combinación de etanercept y metotrexato origina, en comparación con los grupos que reciben monoterapia, un efecto superior en la inhibición de la progresión del daño estructural radiológico. También se observa para el grupo de terapia combinada una mayor reducción de la actividad de la enfermedad, de la capacidad para inducir la remisión clínica (DAS [Disease Activity Score] < 1,6) y un mayor efecto en la mejoría de la discapacidad.
Figura 1. Progresión del índice total de Sharp a las 52 semanas en el estudio TEMPO. ap < 0,05: etanercept frente a metotrexato; bp < 0,01: combinación de etanercept + metotrexato frente a metotrexato; cp < 0,01: combinación de etanercept + metotrexato frente a etanercept.
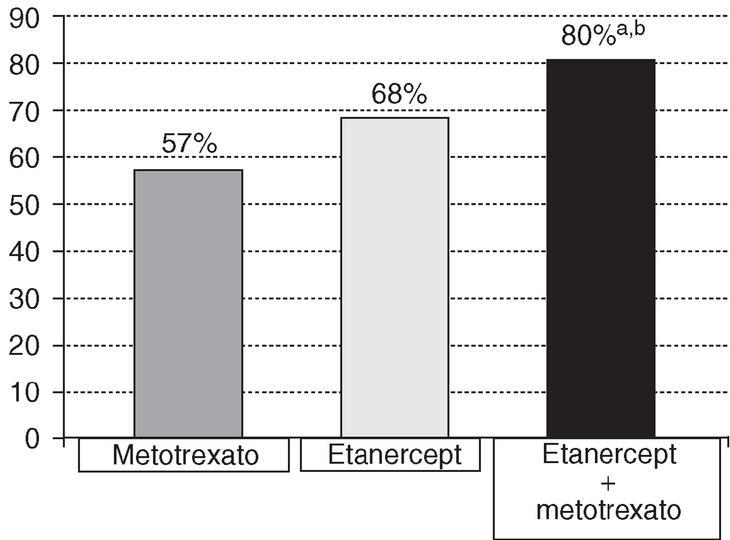
Figura 2. Porcentaje de pacientes sin progresión en el daño estructural radiológico (cambio en el índice total de Sharp inferior o igual a 0,5) en la semana 52. Estudio TEMPO. ap < 0,05: combinación de etanercept + metotrexato frente a etanercept; bp < 0,05: combinación de etanercept + metotrexato frente a metotrexato.
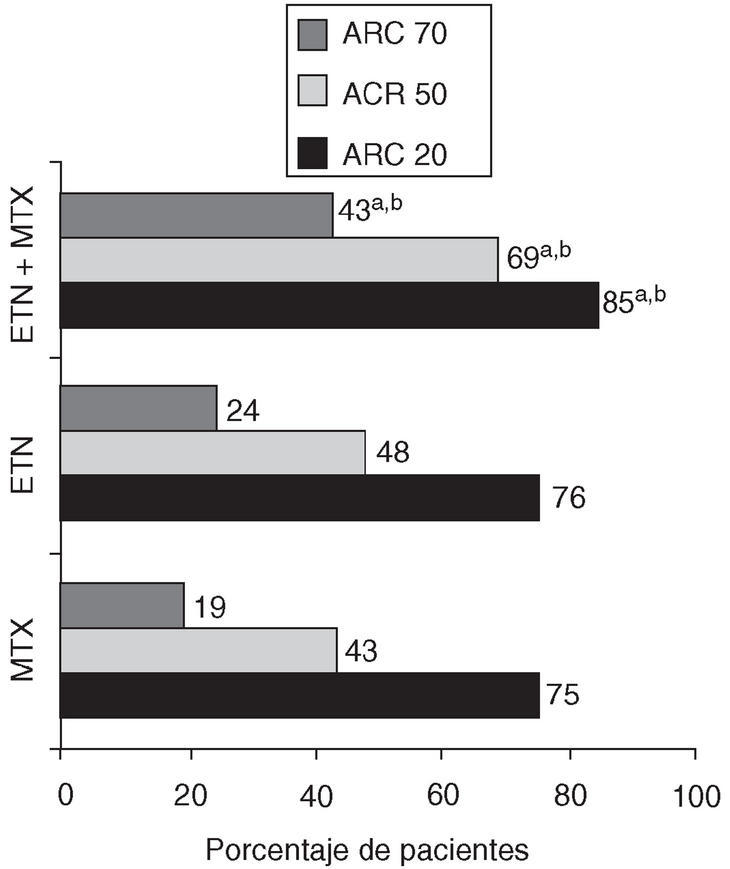
Figura 3.Respuestas ACR (porcentaje de pacientes) en la semana 52 en el estudio TEMPO. MTX: metotrexato; ETN: etanercept; ETN + MTX: etanercept + metotrexato; ap < 0,05: combinación de etanercept + metotrexato frente a metotrexato; bp < 0,05: combinación de etanercept + metotrexato frente a etanercept.
También disponemos desde fechas recientes de información relevante en lo que respecta a la posibilidad en el cambio de la pauta de dosificación del etanercept en la artritis reumatoide. Un ensayo clínico de fase III, doble ciego, aleatorizado, incluyó a 434 pacientes con artritis reumatoide activa que fueron aleatorizados (con esquema 1:4:3) a placebo, etanercept, 50 mg por vía subcutánea 1 vez a la semana, y etanercept, 25 mg por vía subcutánea 2 veces a la semana, respectivamente7. El objetivo primario del estudio fue la medición de la respuesta ACR 20 a las 8 semanas, momento en que se obtuvo una respuesta ACR 20 en el 19% de los pacientes tratados con placebo, en el 50% de los que recibieron etanercept, 50 mg, 1 vez a la semana y en el 49% de los que recibieron la pauta tradicional de dosificación. La mejoría media de la puntuación del HAQ fue también similar entre las dos ramas activas de tratamiento con etanercept. En base a estos hallazgos, la Food and Drug Administration (FDA) aprobó la posibilidad de utilizar etanercept con la pauta de 50 mg una vez a la semana por vía subcutánea para el tratamiento de la artritis reumatoide.
El etanercept ha sido combinado con otros FAME (sulfasalazina, hidroxicloroquina y oro parenteral) en estudio abierto en el que se incluyó a 119 pacientes con artritis reumatoide activa a pesar de recibir los anteriores fármacos8. Se obtuvo rescate en la eficacia con la adición de etanercept, 25 mg, por vía subcutánea 2 veces a la semana, tanto a las 24 como a las 48 semanas. Las combinaciones fueron, en general, bien toleradas, con una tasa de discontinuación por efectos adversos del 9%.
El etanercept es capaz de mejorar la capacidad laboral de los pacientes con artritis reumatoide. El estudio ECHO9 ha comparado el efecto de etanercept sobre variables de salud tras 12 meses de tratamiento, con respecto a pacientes con artritis reumatoide que no lo reciben. En 145 pacientes con artritis reumatoide (media de evolución de la enfermedad de 14 años) que recibieron etanercept, el número de días perdidos para el trabajo fue de 24,1, frente a 42,4 días perdidos en 133 pacientes con artritis reumatoide (media de evolución = 13 años) que no recibieron el fármaco. La utilización de etanercept es capaz, asimismo, de mejorar, la calidad de vida relacionada con la salud en los sujetos con artritis reumatoide. El programa ENLIVEN10 ha estudiado a 1.043 pacientes con artritis reumatoide tratados con etanercept en la práctica clínica. A los 6 meses de iniciado el tratamiento, la puntuación del componente mental del Short Form-36 (SF-36) pasó de 58 a 71,4, y la del de función física, de 30,3 a 50,8.
Seguridad
En extensiones abiertas de ensayos clínicos, realizadas tanto en Estados Unidos como en Europa, la tasa de infecciones graves, expresada en número de casos/pacientes-año, refleja a largo plazo (>= 4 años de seguimiento) una media de 0,05 para la monoterapia con etanercept en artritis reumatoide avanzada, de 0,03 en la artritis reumatoide de reciente comienzo y de 0,025 en la utilización combinada de etanercept + metotrexato11. En el estudio TEMPO6, al cabo de 52 semanas la frecuencia de infecciones graves fue similar entre las 3 ramas de tratamiento. El riesgo de aparición de infecciones graves parece asociarse al uso concomitante de glucocorticoides o inmunosupresores y a la diabetes mellitus12.
Según los datos comunicados al sistema de farmacovigilancia de la FDA (AERS-FDA) se puede calcular una tasa de incidencia de tuberculosis en pacientes que reciben etanercept de 14,7 casos/100.000 en el año 2001 y de 8,2 casos/100.000 en 2002 (la incidencia de tuberculosis en la artritis reumatoide en Estados Unidos es de 6,2 casos/100.000 habitantes)13. El 60% de los casos comunicados recibía simultáneamente inmunosupresores. La mediana de tiempo desde el inicio del etanercept y la aparición de tuberculosis fue de 11,5 meses. El 52% de los casos fueron tuberculosis extrapulmonares. Se han descrito otras infecciones granulomatosas en pacientes en terapia con etanercept14.
En 2.054 pacientes con artritis reumatoide avanzada y de reciente comienzo, seguidos durante 5 años, el número de tumores sólidos observados se correspondía con el esperado según las estimaciones para la población general (SEER del National Cancer Institute, ajustado para edad y sexo)15. El análisis de 1.442 pacientes con artritis reumatoide, con una mediana de exposición al etanercept de 3,7 años, no detectó un incremento en la incidencia de carcinoma cutáneo de células escamosas16. En un estudio de 19.072 pacientes seguidos longitudinalmente, desde 1998 hasta 2002, no parece observarse que la terapia con agentes anti-TNF, incluido el etanercept, se asocie al incremento en el riesgo de recurrencia del cáncer, aunque es aconsejable apreciar estos datos con prudencia y extremar la precaución en la indicación de este tipo de tratamientos en pacientes con artritis reumatoide e historia previa de neoplasias17.
Las comunicaciones espontáneas al sistema AERS-FDA, desde noviembre de 1998 a diciembre de 2000, permitieron estimar una incidencia de 19 casos de linfoma por cada 100.000 pacientes tratados con etanercept (18,3 casos/100.000 es la incidencia estimada de linfoma en la población general de Estados Unidos en el período 1992-1998)18. La vigilancia poscomercialización ha permitido registrar, hasta marzo de 2003, una tasa de linfoma/100 pacientes-año similar o inferior a la estimada para la población general (0,03)19. No parece existir un patrón claro de relación temporal ni asociación con ningún subtipo especial de linfoma o con los que aparecen tras el trasplante de órganos. Wolfe ha calculado una ratio estandarizada de linfoma de 3,8 para los pacientes con artritis reumatoide que reciben etanercept, frente a 1,9 que estima en la población con artritis reumatoide que no recibe terapia biológica20.
Menos del 5% de los pacientes con artritis reumatoide tratados con etanercept en ensayos clínicos desarrollan anticuerpos contra el fármaco, no neutralizantes. Estos anticuerpos no parecen afectar a la tolerabilidad y la eficacia del medicamento. Los casos descritos de recurrencia o de nueva aparición de enfermedad desmielinizante en pacientes tratados con etanercept desaconsejan su indicación en pacientes con antecedentes o historia familiar positiva para este tipo de procesos del sistema nervioso central21. Los ensayos clínicos realizados para investigar la eficacia del etanercept en el tratamiento de la insuficiencia cardíaca congestiva (ICC) no fueron capaces de demostrar que el uso de este agente redujera, frente al placebo, el riesgo de hospitalización o muerte por empeoramiento de la ICC22,23. Wolfe et al24 han estudiado a 13.171 pacientes con artritis reumatoide y 2.568 con artrosis, procedentes del National Data Bank of Rheumatic Diseases, buscando tasas de ICC, predictores y efectos de la terapia anti-TNF. Tras 2 años de seguimiento encuentran que la tasa media de ICC en la artritis reumatoide es del 3,5%, similar a la de la población general pero inferior a la de la artrosis (2,2%). Según los resultados de esta investigación, la actividad de la artritis reumatoide y su gravedad predicen el riesgo de ICC. Los pacientes con artritis reumatoide que reciben terapias anti-TNF tienen, en esta investigación, tasas más bajas de ICC, comparados con los que no la reciben, y no se observan diferencias entre el etanercept y el infliximab.
No se ha observado que el etanercept afecte a los resultados de las pruebas de inmunocompetencia (niveles de inmunoglobulinas séricas, función de los neutrófilos y marcadores de superficie de los linfocitos T y B) en un subgrupo de pacientes con artritis reumatoide durante ensayos clínicos, con respecto al placebo25. No se recomienda la vacunación con agentes vivos en pacientes que reciben etanercept. Se permite la administración de vacunas con agentes muertos o antígenos en pacientes adultos. De cualquier manera, la respuesta de anticuerpos frente a la vacunación en pacientes con artritis reumatoide que reciban etanercept debe ser estudiada con mayor profundidad26. Un estudio piloto27 parece sugerir que la adición de etanercept (25 mg por vía subcutánea 2 veces por semana) al tratamiento de la hepatitis C con ribavirina e interferón reduce los niveles de ARN viral, mejora la regresión de la fibrosis y disminuye la incidencia de efectos adversos. Los resultados de un estudio con pocos pacientes sugieren que el uso a corto plazo de etanercept, en pacientes con artritis reumatoide y hepatitis C, no afecta a las pruebas de función hepática ni altera la carga viral28. La traslación a la clínica de estos hallazgos necesita ser confirmada.
Administración por vía intraarticular
Se han explorado nuevas vías para la administración de etanercept en pacientes con artropatías inflamatorias. En concreto, se han comunicado resultados sobre el empleo de etanercept por vía intraarticular. Un ensayo clínico aleatorizado, controlado, doble ciego (para la dosificación) y ciego (para el observador), ha elegido 2 articulaciones inflamadas, bilaterales y simétricas: una articulación recibía la medicación y la otra actuaba como control29. En la parte I de este estudio se aleatorizó la dosis de inyección de etanercept a 2, 4 u 8 mg (doble ciego para la dosificación), y en la parte II todas las articulaciones se inyectaron con 8 mg. Se incluyeron 26 pacientes. Se evaluaron 16 muñecas, 6 articulaciones metacarpofalángicas, 6 interfalángicas proximales, 6 interfalángicas distales, 6 metatarsofalángicas, 2 codos y 2 tobillos. Las inyecciones intraarticulares se realizaron bajo control ecográfico. La eficacia se midió clínicamente (observador ciego independiente), por resonancia magnética y por eco-Doppler. Ningún paciente mejoró con las dosis de 2 y 4 mg intraarticulares de etanercept. La inyección intraarticular de 8 mg de etanercept disminuyó el dolor articular medido por escala analógica visual en 23 de 25 pacientes después de 1 semana, y en 14 de 25 después de 1 mes (ANOVA [analysis of variance between groups], p < 0,05); el número de DUS píxeles desciende después de 1 semana en 18 de 25 pacientes y después de 1 mes en 21 de 25 (ANOVA, p < 0,05). No se observaron estos cambios en las articulaciones control. Se sugiere, en este estudio, que las grandes articulaciones se deben infiltrar con una dosis mayor de 8 mg.
Un segundo ensayo clínico aleatorizado, doble ciego para la dosificación y con observador ciego, incluyó a pacientes con sinovitis activa de 2 o más articulaciones, preferiblemente simétricas, candidatas a inyección intraarticular con glucocorticoides, que fueron infiltradas con etanercept30. Una articulación se infiltra y la otra actúa como control. Se probaron varias dosis (2, 4 y 8 mg) en la fase inicial y luego todas se inyectan con 8 mg. Un observador ciego evaluó la eficacia clínica y se midió también la velocidad de sedimentación globular y la proteína C reactiva. Se inyectaron 28 articulaciones en 26 pacientes. Desde el punto de vista de la seguridad, sólo 1 paciente al que se le inyectaron 4 mg de etanercept en la muñeca presentó inflamación del dorso de la mano a los 2 días. No se detectó ningún otro acontecimiento adverso: no hubo reacciones locales en el punto de la inyección, no se produjeron infecciones ni reactivación de la enfermedad.
Un tercer estudio31 ha comparado la inyección intraarticular de 12,5 mg de etanercept frente a placebo (suero salino isotónico) en 20 pacientes con artritis reumatoide y artritis activa. Diez pacientes recibieron la inyección intraarticular de etanercept y los otros 10 se inyectaron con placebo. El diseño fue doble ciego. La inyección intraarticular de 12,5 mg de etanercept mejoró de forma estadísticamente significativa el dolor, la inflamación y la movilidad articular en estos pacientes, frente al placebo.