In the last three decades the species of Candida have been of great interest due to the high mortality rates that they cause in immunocompromised and hospitalized patients. These species are opportunistic pathogens and they have inhabited other environments long before colonizing human cells. Among these environments we find wastewater from mines, and water from aquifers and soils that contain high concentrations of precious metals as well as toxic and base metals.
AimsThe aim of this study was to assess whether Candida albicans and Candida glabrata are able to maintain homeostasis in the presence of zinc, copper, cobalt or silver.
MethodsTo achieve the objective, each of the Candida species was exposed to every single metal individually in a salt solution. Subsequently the treated cells were lysed to evaluate the compounds formed by means of Scanning Electron Microscopy-Energy Dispersive X-ray spectroscopy (SEM-EDS).
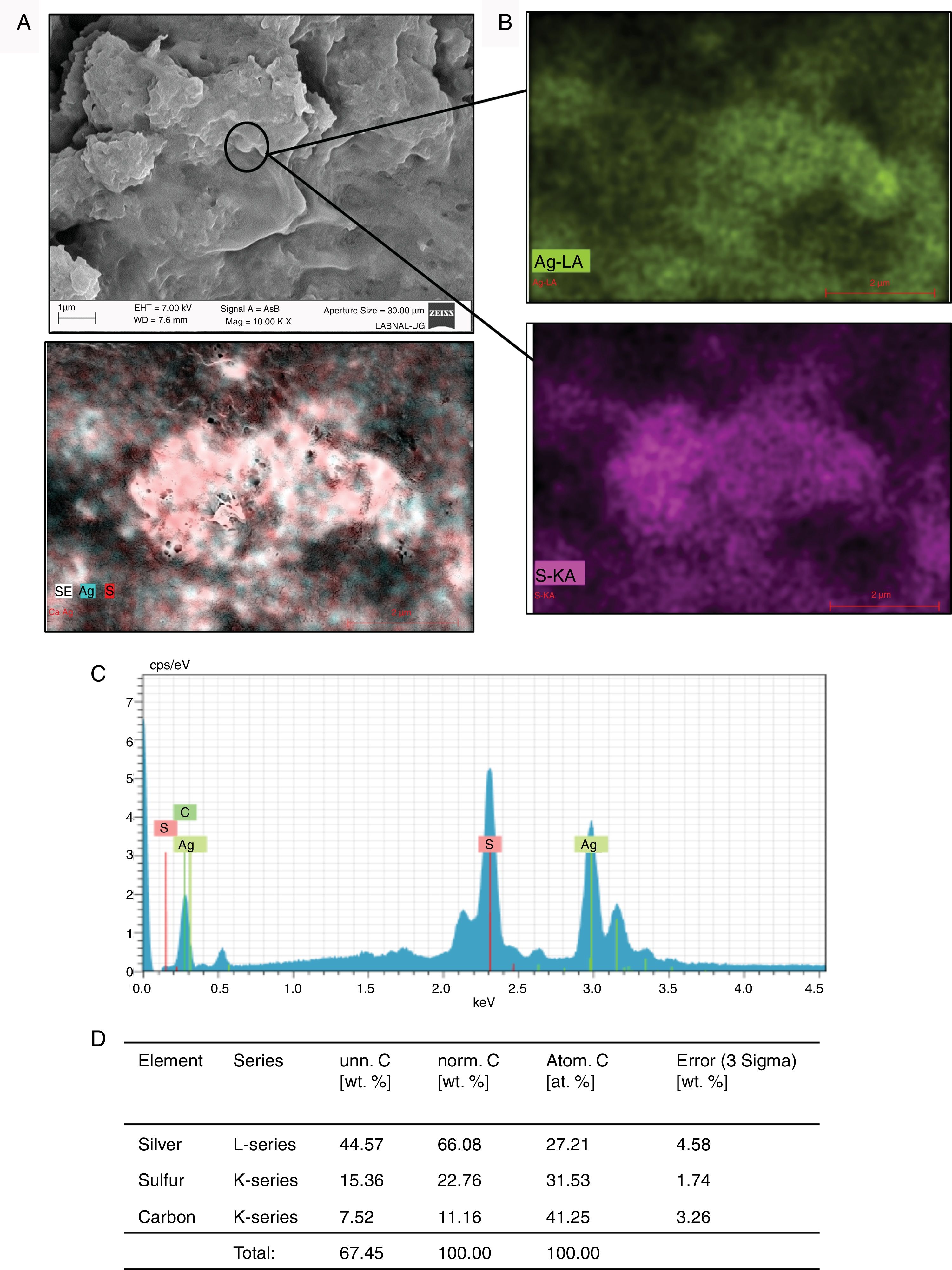
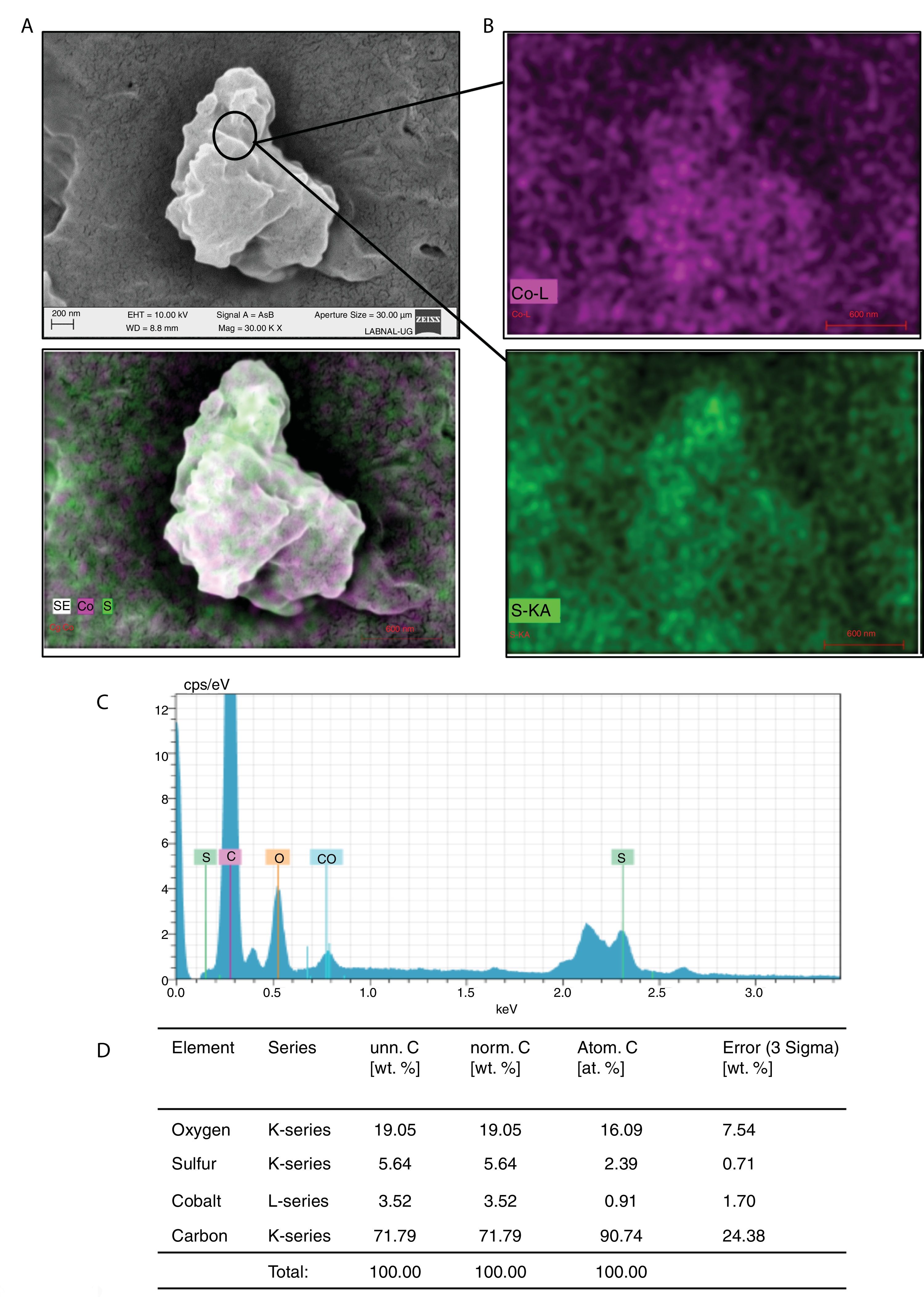
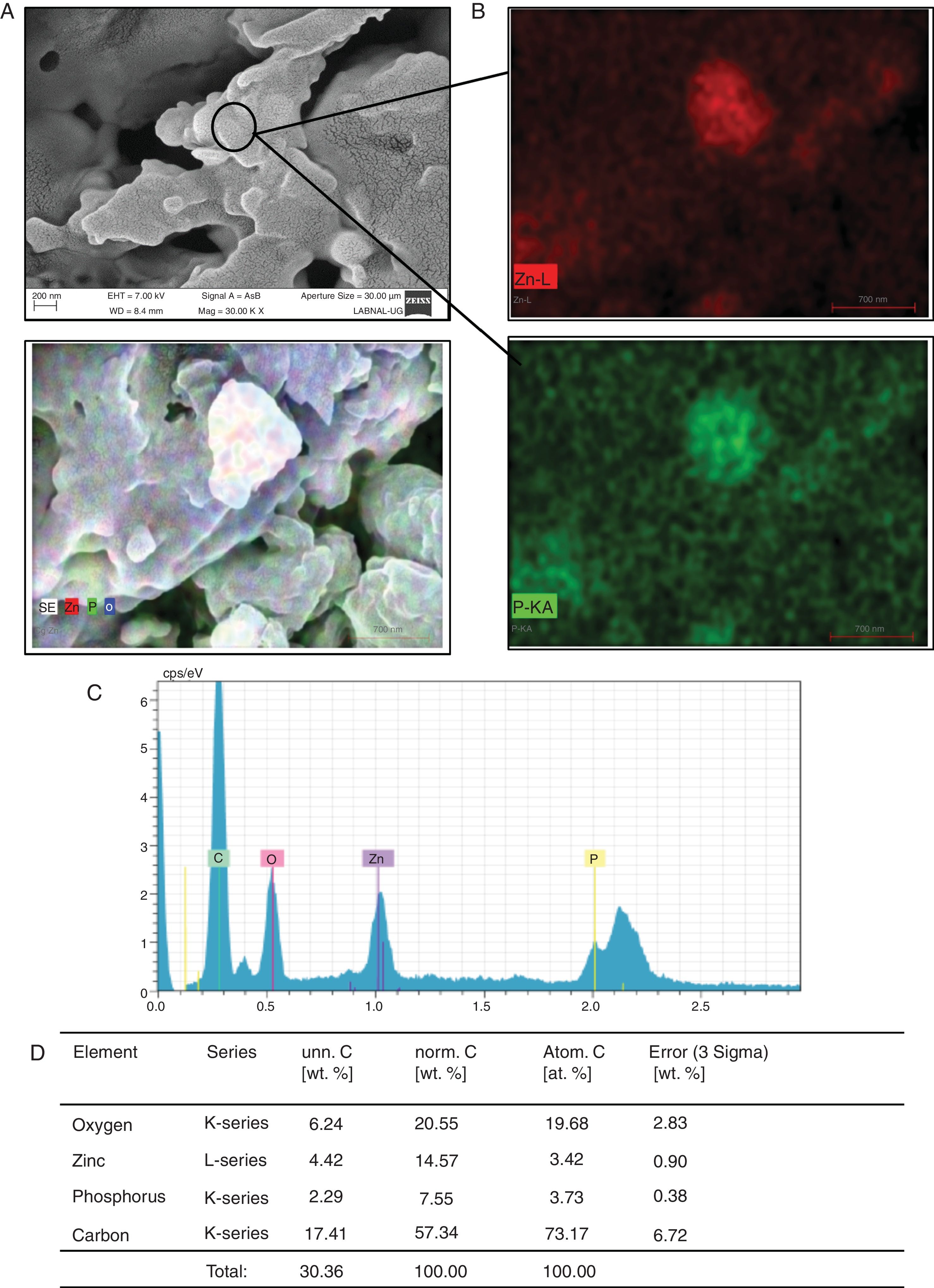
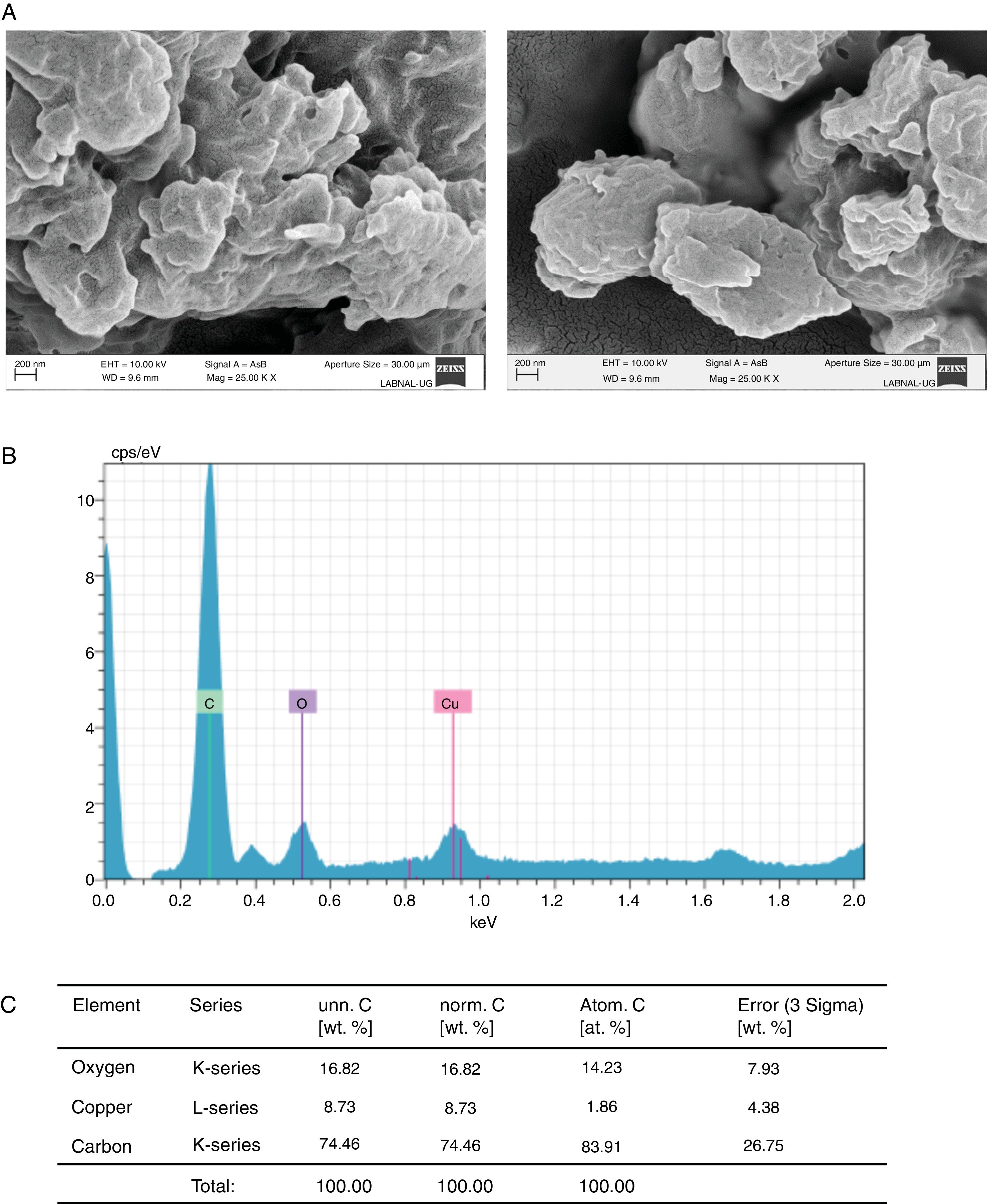
ResultsWhen analyzing the compounds that both C. albicans and C. glabrata formed in the presence of each of the metals, we found that they had synthesized silver sulfide (Ag2S), cobalt sulfate (CoSO4), zinc phosphate (Zn3(PO4)2), or copper oxide (CuO).
ConclusionsOur results indicate that both C. albicans and C. glabrata have enzymatic and non-enzymatic mechanisms that allow them to achieve homeostasis in a different specific manner for each of the single metals to which they were exposed. To our knowledge, this is the first work reporting that C. albicans and C. glabrata can reduce different metals, with the subsequent formation of sulfides, sulfates, phosphates and oxides. This ability, developed over time by these Candida species, is probably a kind of biochemical mechanism in order to survive and colonize many different environments, from water or soil to humans. For this reason, C. albicans and C. glabrata make up an excellent model of study, both from a medical and biotechnical point of view.
Las especies de Candida han cobrado gran interés en las últimas tres décadas debido a los altos índices de mortalidad que ocasionan en pacientes inmunodeficientes y hospitalizados. Estas especies son consideradas patógenas oportunistas y existen otros medios ambientes que estas levaduras han habitado mucho antes de haber colonizado al ser humano: aguas residuales de minas, agua de mantos acuíferos y suelos que contienen altas concentraciones de metales preciosos, metales tóxicos y metales comunes.
ObjetivosEl objetivo del presente trabajo fue evaluar si Candida albicans y Candida glabrata eran capaces de mantener la homeostasis en presencia de los elementos químicos cinc, cobre, cobalto y plata.
MétodosPara lograr el objetivo, las dos levaduras fueron expuestas a cada uno de los metales elegidos de manera independiente, y posteriormente las células tratadas fueron lisadas para permitir la evaluación por medio de microscopía electrónica de barrido con espectrometría de dispersión de energía de rayos X (SEM-EDS) del compuesto formado.
ResultadosAl analizar los compuestos que tanto C. albicans como C. glabrata formaron en presencia de cada metal, se encontró que habían sintetizado sulfuro de plata (Ag2S), sulfato de cobalto (CoSO4), fosfato de cinc (Zn3(PO4)2), u óxido de cobre (CuO).
ConclusionesNuestros resultados indican que tanto C. albicans como C. glabrata poseen mecanismos enzimáticos y no enzimáticos que les permiten alcanzar una homeostasis de manera específica para cada metal al que son expuestas. A nuestro entendimiento este es el primer trabajo que documenta que C. albicans y C. glabrata pueden reducir distintos metales, con la subsecuente formación de sulfuros, sulfatos, fosfatos y óxidos. Esta habilidad que pudieron desarrollar a lo largo del tiempo estas especies de Candida para poder sobrevivir y colonizar medios ambientes tan diferentes, que van desde el agua o los suelos hasta el ser humano, las convierte en un excelente modelo de estudio, tanto desde el punto de vista médico como biotecnológico.
Artículo
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora