Evaluar y comparar la eficacia de protocolos de craneopuntura con electroestimulación, lidocaína intravenosa (i.v.), ketamina i.v. y ozono en autohemoterapia como terapias complementarias al tratamiento habitual en la reducción del dolor y la mejora de la calidad de vida de pacientes con fibromialgia (FM).
DiseñoEnsayo clínico controlado, aleatorizado.
EmplazamientoHospital Universitario Reina Sofía de Córdoba (España).
ParticipantesPacientes (265) con FM confirmada clínicamente, divididos en 5 grupos.
IntervencionesCiclo de tratamiento especificado en cada protocolo: lidocaína i.v., ketamina i.v., autohemoterapia con ozono, craneopuntura con electroacupuntura, grupo control.
Mediciones principalesEscala total de dolor y cada uno de sus componentes, escala visual analógica y Cuestionario de Impacto de la Fibromialgia basales y a los meses 1, 3 y 6 de la terminación de las intervenciones.
ResultadosEl grupo de craneopuntura mostró diferencias significativas (p<0,05) en más variables, especialmente a los 6 meses, frente a los otros, seguido por el de ozono.
ConclusiónLos protocolos de craneopuntura y ozono en autohemoterapia presentaron una eficacia notablemente superior en el tratamiento de la FM a la de los protocolos de lidocaína y de ketamina.
To assess and compare the efficacy of scalp acupuncture with electroestimulation, intravenous lidocaine, intravenous ketamine and ozone autohemotransfusion as complementary therapies for alleviating pain and improving the quality of life in patients with fibromyalgia (FM).
DesignRandomized, controlled clinical trial.
LocationHospital Universitario Reina Sofía at Córdoba (Spain).
ParticipantsPatients (265) with clinically confirmed FM divided into 5 groups.
InterventionsFormalized cycles of treatment: intravenous lidocaine, intravenous ketamine; scalp acupuncture with electroacupuncture, autohemotransfusion of ozone, control group.
MeasurementsTotal pain scale and components, visual analogue scale and questionnaire on FM impact (CIF) before the interventions and on months 1, 3 and 6 after termination of the interventions.
ResultsThe scalp acupuncture group showed significant differences (p<0.05) on the variables compared to the other groups, especially al 6 months; it is followed by ozone group.
ConclusionsThe scalp acupuncture and ozone protocols showed a remarkably higher efficiency than the lidocaine and ketamine protocols for treating FM.
La fibromialgia (FM) es una enfermedad crónica y compleja que afecta a un 2,7% de la población española1. El 75% de los pacientes son mujeres con edades comprendidas entre 35 y 55 años2.
Actualmente no existen métodos satisfactorios de tratamiento, farmacológico o no, para la FM3–8. Algunos de los fármacos tienen efectos secundarios que pueden hacer inadecuado su uso en pacientes con FM, ya que suelen tolerarlos peor. Por ello, es preciso encontrar de forma perentoria nuevas estrategias coste-efectivas que reduzcan el dolor osteomuscular y mejoren el funcionamiento físico y emocional, así como la calidad de vida en pacientes con FM9.
Algunos estudios han sugerido que el uso de acupuntura y técnicas relacionadas de la Medicina Tradicional China puede ser un tratamiento eficaz, ya sea único o complementario10. Se ha estimado que aproximadamente un 20% de los pacientes con FM tratados en hospitales universitarios en Estados Unidos utilizaron acupuntura dentro de los 2 años del diagnóstico11.
La acupuntura se está integrando en las corrientes más importantes de tratamiento del dolor en los estudios del National Center for Complementary and Alternative Medicine (Estados Unidos) utilizando técnicas de imagen para observar sus efectos en el cerebro con el fin de intentar comprender las acciones neurobiológicas centrales y periféricas, así como las áreas del cerebro involucradas en la percepción del dolor12,13.
La British Medical Association ha animado al incremento del uso de la acupuntura para intentar mejorar la calidad del tratamiento14. La literatura médica sugiere que la acupuntura puede aliviar el dolor crónico15. Una reciente revisión incluyó 5 ensayos clínicos controlados sobre acupuntura en el tratamiento de la FM16 concluyendo que eran necesarios más estudios rigurosos, especialmente en el campo de la electroacupuntura17,18.
Los datos sobre la eficacia de la infusión de lidocaína para aliviar el dolor en FM son confusos19–21. Hay pruebas de que los antagonistas del NMDA (N-metil-D-aspartato), como ketamina y dextrometorfano pueden aliviar el dolor en FM22,23. Tanto la lidocaína como la ketamina deben ser aplicadas en ciclos semanales, ya que son poco efectivas como tratamiento aislado24.
El ozono está demostrándose útil en aquellas patologías25,26 en las que la hiperoxigenación resulta fundamental. Por ello, se presume que su aplicación en pacientes con FM eliminaría varias de sus manifestaciones27,28, al disminuir notablemente los síntomas dolorosos que habitualmente impiden la realización de los trabajos físicos recomendados para la recuperación, ya que tiene un importante efecto analgésico. Además, el tratamiento con ozono logra mejorar el estado general de la persona, devolviéndole la vitalidad y la energía, recuperando el buen estado de ánimo y restituyendo el sueño29–31.
Este estudio pretende profundizar en estas vías de tratamiento que, si se aplican correctamente, son muy baratas y carecen de efectos secundarios importantes; por lo que su difusión con indicaciones adecuadas ayudaría también a paliar el gasto farmacéutico de forma importante. Se ha procurado seguir las recomendaciones STRICTA32 y CONSORT33.
Pacientes y métodosEl estudio se ha llevado a cabo en la Unidad del Dolor del Hospital Universitario Reina Sofía de Córdoba a lo largo de los años 2011 a 2014. El objetivo general consistió en valorar la eficacia —por separado y comparada— de la craneopuntura con electroestimulación, lidocaína intravenosa (i.v.), ketamina i.v. y ozono en autohemoterapia como terapias complementarias al tratamiento habitual (grupo control) en la reducción del dolor y en la mejora de la calidad de vida de pacientes con FM frente al empleo del tratamiento farmacológico convencional en la provincia de Córdoba, a los 30 días, a los 3 meses y a los 6 meses de la finalización del tratamiento.
Los objetivos específicos fueron los siguientes:
- 1.
Evaluar el grado de alivio del dolor. Conocer en qué proporción disminuye el valor total de la escala de dolor y de la escala visual analógica (EVA) en estos pacientes.
- 2.
Evaluar el grado de reducción de la intensidad y frecuencia del dolor, de la disminución en el consumo de analgésicos, de la reducción de problemas relativos al sueño, de la reducción de la discapacidad. Conocer en qué proporción disminuye el valor de estos parámetros del dolor en estos pacientes tras un ciclo de tratamiento.
- 3.
Evaluar la mejora en la calidad de vida, medida a través de los test propuestos. Conocer en qué proporción disminuye el valor del Cuestionario de Impacto de la Fibromialgia (CIF).
Por un lado, se realizó un ensayo clínico controlado y aleatorizado con pacientes diagnosticados de FM y que cumplían los criterios de inclusión-exclusión (tabla 1), para comparar la eficacia de cada uno de los 4 tratamientos en el control de los síntomas de la FM. Se incluyó exclusivamente a pacientes entre 18 y 65 años, ya que a más edad hay más probabilidad de presentar enfermedades concomitantes.
Criterios de inclusión-exclusión
| Criterios de inclusión |
| Diagnóstico cierto de fibromialgia: |
| – Dolor generalizado o difuso que persiste más de 3 meses, presente a ambos lados del cuerpo, por encima y por debajo de la cintura, y en el esqueleto axial (columna cervical, torácica o lumbar, o cara anterior del tórax), junto con el índice de dolor generalizado y el índice de gravedad de síntomas39 |
| – Dolor a la presión digital en 11 de los 18 puntos dolorosos (9 pares): |
| 1. Occipitales: inserciones de los músculos suboccipitales |
| 2. Cervicales bajos: en la cara anterior de los espacios intertransversos C5 a C7 |
| 3. Trapecios: punto medio de sus bordes superiores |
| 4. Supraespinosos: en el nacimiento del músculo, por encima de la espina de la escápula, cerca del borde interno |
| 5. Segunda costilla: lateral a la segunda articulación condrocostal |
| 6. Epicondíleos: 2cm distal a los epicóndilos |
| 7. Glúteos: cuadrante superior y externo de las nalgas |
| 8. Trocantéreos: posterior a los trocánteres mayores |
| 9. Rodillas: en la bolsa grasa medial, proximal a la interlínea |
| Criterios de exclusión |
| Diagnóstico inexistente, incompleto o confuso |
| Embarazo |
| Enfermedad psiquiátrica grave en actividad |
| Grave deterioro del estado general |
| Tratamiento con corticoides |
| Dermopatía generalizada y grave |
| Rentofilia o litigio laboral por causa del dolor |
| Contusiones o traumatismos directos como causa primera de evolución<1 mes |
| Pacientes con patología reumática concomitante (artritis reumatoide, espondilitis anquilosante, artritis psoriásica, lupus eritematoso sistémico, artropatías microcristalinas o artrosis) |
| Inclusión en una lista de espera quirúrgica |
| Diabetes mellitus |
| Enfermedad oncológica |
| Anemia y enfermedades hematológicas |
| Enfermedad sistémica grave o descompensada (cardiopulmonar, neurológica, renal, febril) |
| Miedo a las agujas |
| Tratamiento previo con acupuntura |
| Pacientes que no puedan acudir a las visitas necesarias para llevar a cabo el estudio |
| Alergia al fármaco asignado |
| Participar en otro estudio de investigación |
Por otro lado, se realizó un estudio de grupos apareados antes-después con los mismos pacientes para evaluar la eficacia de la craneopuntura con electroestimulación, lidocaína i.v., ketamina i.v. y ozono en autohemoterapia, independientemente y en comparación con el tratamiento farmacológico convencional (grupo control) que estaban recibiendo.
Protocolo de lidocaínaInfusión i.v. de 3-7mg/kg peso en 100ml de suero fisiológico en 60min durante 5 días. Control en reposo durante otros 60min.
#· Día 1: 3mg/kg peso.
#· Día 2: 4mg/kg peso.
#· Día 3: 4mg/kg peso.
#· Día 4: 5mg/kg peso.
#· Día 5: 6mg/kg peso.
Protocolo de ketaminaDurante 5 días seguidos a dosis de 0,4mg/kg i.v. en 100ml de suero fisiológico durante 60min. Administración previa de 1mg de midazolam. Control en reposo durante otros 60min.
Protocolo de ozonoLos pacientes recibieron 7 sesiones de ozonoterapia i.v. Esta forma de aplicación se fundamenta en la autohemoterapia semanal de 120-150ml de sangre tratada, de manera que se extrae sangre al paciente (en bolsas, con filtro Millipore®) a la que se aplica ozono (3-4mg: 100ml de ozono a presión de 40μg/ml) y se devuelve al torrente circulatorio del paciente en 10min.
Protocolo de craneopunturaConsistió en la puntura bilateral de determinadas líneas, puntos y áreas, 2 días por semana, durante 5 semanas seguidas (10 sesiones) con electroestimulación (onda denso-dispersa con la intensidad que tolerara cada paciente) durante 20min.
- A)
Área de la sensibilidad (cartografía CC1).
- B)
Área sensitivo-motriz de los MMII o área de la marcha (CC1).
- C)
Línea central de la calota (CC3).
- D)
Área de la fortaleza (CC3).
- E)
Punto del pensamiento (CC2).
- F)
Línea mediofrontal (CC3).
- G)
Área de los sentimientos y la mente (CC3).
- H)
Punto de la memoria (CC2).
- I)
Punto de entendimiento del lenguaje (CC2).
- J)
Línea posterotemporal (CC3).
Distribución de las sesiones:
- –
A: sesiones 1 y 6.
- –
B: sesiones 2 y 7.
- –
C + D + E + F: sesiones 3 y 8.
- –
G + H: sesiones 4 y 9.
- –
I + J: sesiones 5 y 10.
El médico acupuntor que realizó las intervenciones es especialista en acupuntura tradicional china por The Third School of Clinical Medicine of Beijing Medical University y tiene más de 17 años de experiencia clínica en acupuntura.
Los pacientes se seleccionaron desde la unidad del dolor consecutivamente y se aleatorizaron (1:1:1:1:1) con el programa informático C4-SDP, manteniendo en todo momento oculta la asignación al evaluador externo. No fue posible cegar a los pacientes que recibieron ozono en autohemoterapia ni a los del grupo de craneopuntura o a quienes realizaban las técnicas.
El mantenimiento de la movilidad es muy importante en los pacientes con FM, por lo que se entregó una tabla de ejercicios aeróbicos34 —Guía de ejercicios para personas con fibromialgia, editada por la Asociación de Divulgación de Fibromialgia— para que los hicieran diariamente, además de andar de manera continuada 1h al día.
Para medir las variables, se realizó de forma presencial autoaplicable la valoración inicial con EVA, escala completa del dolor10 y CIF35 (al mes y a los 3 y 6 meses de haber terminado el tratamiento). Otras variables son edad, sexo, duración del dolor (cronicidad) y tiempo desde el diagnóstico de FM.
La EVA de intensidad consiste en una línea recta horizontal, de 10cm de longitud, donde los extremos marcan la gravedad del dolor. En el extremo izquierdo aparece la ausencia de dolor y en el derecho se refleja el mayor dolor imaginable. Permite medir la intensidad del dolor que describe el paciente con la máxima reproducibilidad entre los observadores.
La escala completa del dolor es una escala habitual de valoración del dolor (intensidad, frecuencia, consumo de analgésicos, discapacidad y sueño, puntuados entre 0 y 4) que presenta la ventaja de medir distintas variables de forma que, en conjunto, representan la característica de interés. Es un índice que, al combinar varias mediciones, mejora la precisión con la que se valora el alivio del dolor.
El CIF es una versión española del Fibromyalgia Impact Questionnaire (FIQ), actualizada en 2007 y de consenso, que se utiliza en España para la evaluación de los pacientes con FM y cuya puntuación media es de 70,5 puntos.
En el análisis de los datos (el método conocido como intención de tratar), los sujetos son analizados en el grupo al que inicialmente fueron asignados, independientemente de si recibieron de forma correcta o no la intervención que les tocó en suerte. Este análisis tiene 2 ventajas fundamentales. Es la única estrategia que conserva las ventajas que se adquieren mediante la asignación aleatoria de los participantes. Su valor esencial es que los grupos son comparables en su composición en todas las variables (edad, sexo, gravedad de la clínica, etc.) excepto en el factor de intervención que es objetivo del estudio. La asignación aleatoria consigue que muchas variables que son potenciales factores de confusión, conocidos o no, se distribuyan de manera equilibrada entre ambos grupos. De este modo, su efecto de confusión queda anulado.
Con un riesgo alfa del 5% y una potencia del contraste del 80%, resultaron ser necesarios 265 pacientes, con un tamaño del efecto de tipo medio (d=0,25) según la convención propuesta por Cohen36 para un análisis de varianza de medidas repetidas en un contraste bilateral con 5 grupos independientes a comparar, resultando grupos de 53 pacientes.
Se utilizó el paquete estadístico SPSS para el análisis de datos, y se llevó a cabo la prueba de Friedman (no paramétrica) para comparar las variables ordinales y el análisis de la varianza (paramétrica) para las variables cuantitativas en grupos apareados (antes-después) de pacientes para valorar la eficacia de cada tratamiento en comparación con el tratamiento farmacológico convencional. Se realizó la prueba de Kruskall-Wallis para las variables ordinales y el análisis de la varianza para las variables cuantitativas para la comparación entre los grupos. Los datos faltantes no se sustituyeron por el peor valor obtenido, sino por el valor medio.
En cuanto a los aspectos éticos, se respetaron los principios recogidos en la Declaración de Helsinki: los pacientes firmaron el documento de consentimiento informado específico y se obtuvo previamente el informe favorable del comité ético de investigación clínica. Toda la información obtenida está sujeta al mismo nivel de confidencialidad que la contenida en la historia clínica.
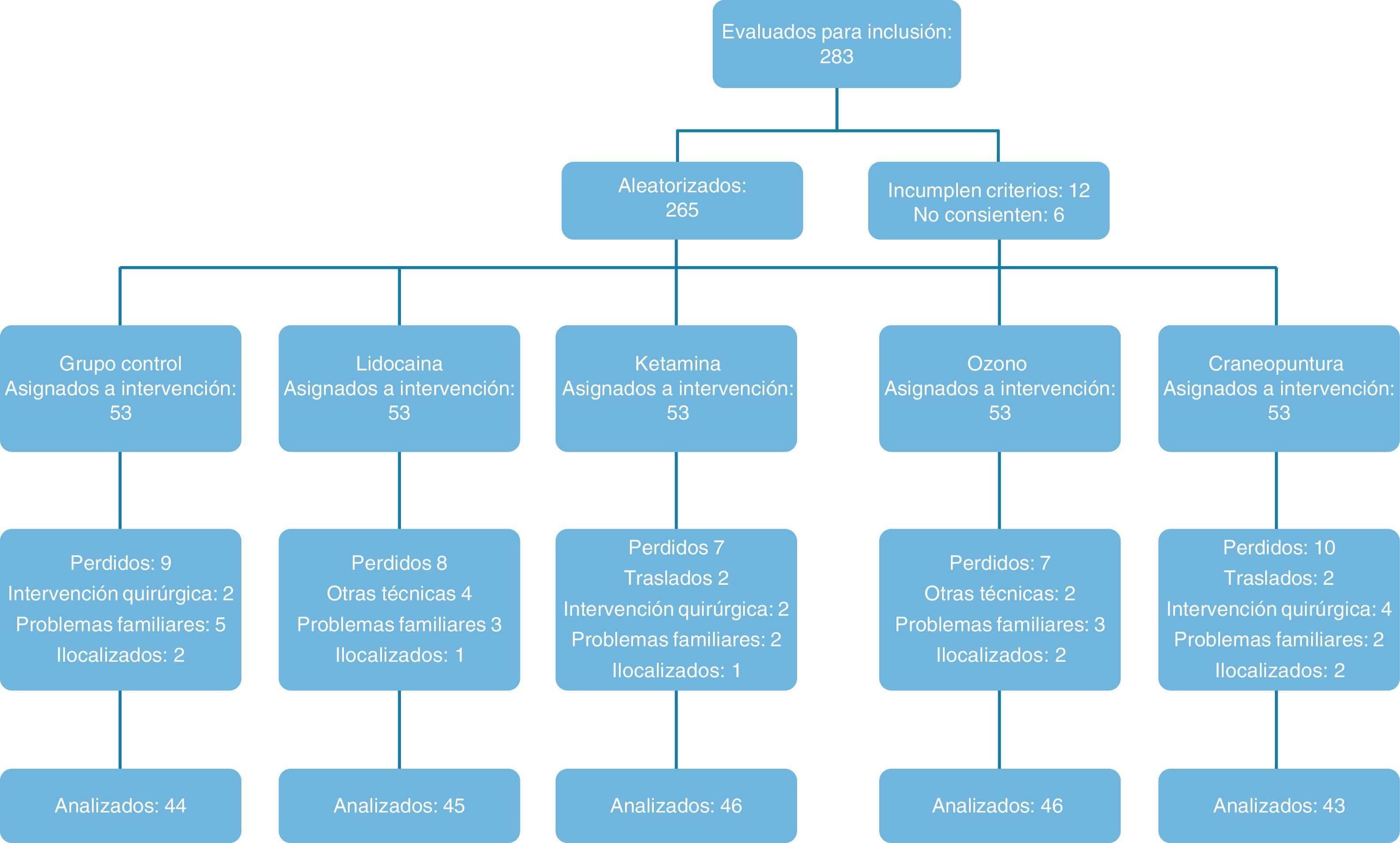
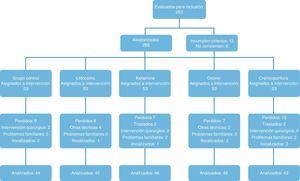
ResultadosEl 93% de los pacientes pertenecían al sexo femenino. Se les había diagnosticado de FM hacía 7,4 años, por término medio. La media de edad fue de 51 años (mínimo 20, máximo 65). Antes de las intervenciones, la media de la EVA era de 8,64/10 y la del CIF de 75,8. En la figura 1 se muestra el esquema del estudio 1.
No hubo diferencias significativas entre los grupos al inicio del estudio respecto a cualquiera de las variables, excepto para la incapacidad. A pesar de la aleatorización, se encontraron diferencias para la incapacidad al inicio en contra del grupo de ketamina y en comparación con los otros (p<0,01), especialmente con el de lidocaína.
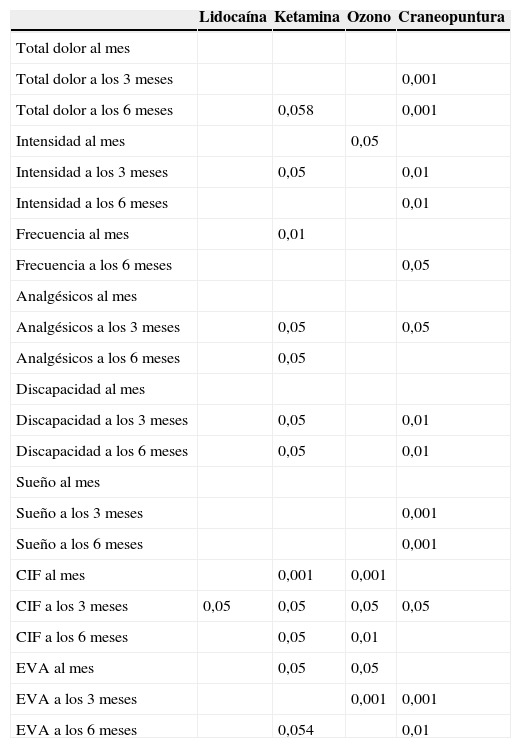
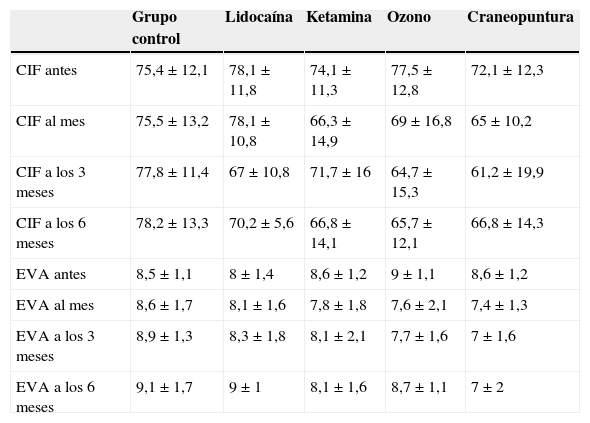
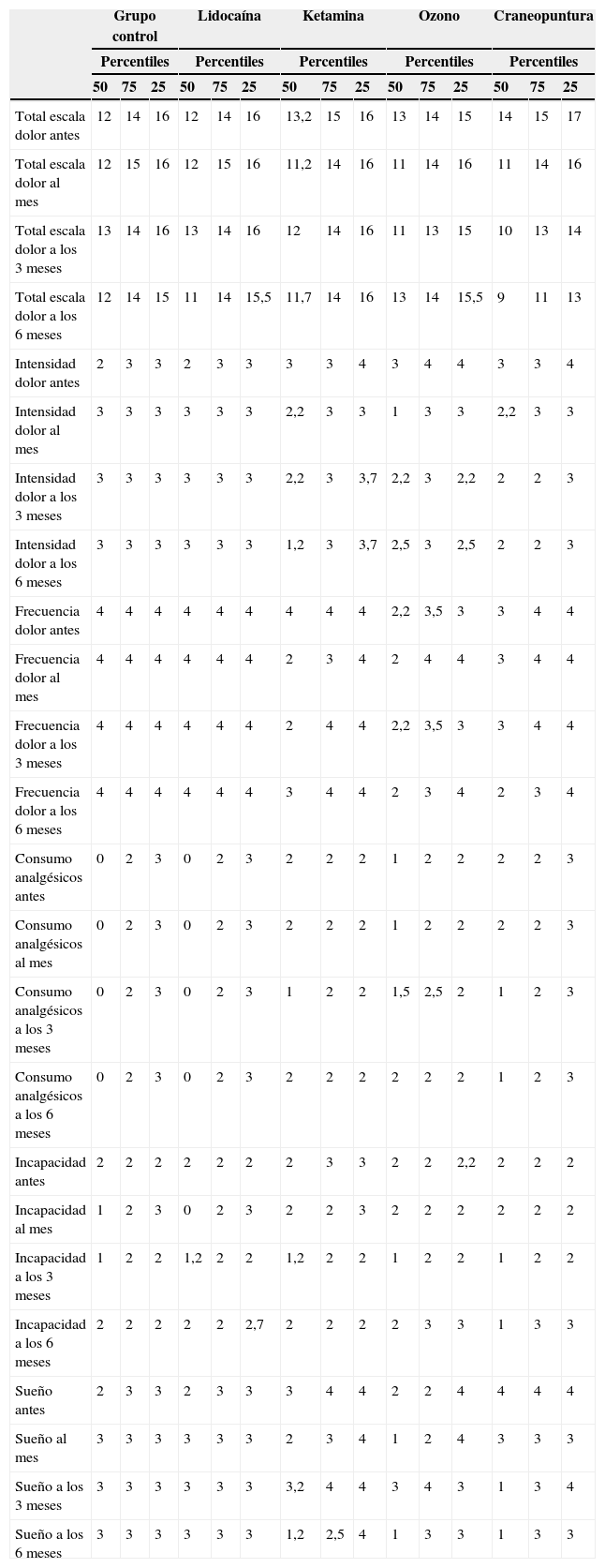
En la tabla 2 se presentan las diferencias estadísticamente significativas dentro de cada grupo y en la tabla 3 las diferencias entre los grupos. Las tablas 4 y 5 muestran los resultados para cada variable obtenidos en cada grupo.
Diferencias estadísticamente significativas dentro de cada grupo antes y después de la intervención*
| Lidocaína | Ketamina | Ozono | Craneopuntura | |
|---|---|---|---|---|
| Total dolor al mes | ||||
| Total dolor a los 3 meses | 0,001 | |||
| Total dolor a los 6 meses | 0,058 | 0,001 | ||
| Intensidad al mes | 0,05 | |||
| Intensidad a los 3 meses | 0,05 | 0,01 | ||
| Intensidad a los 6 meses | 0,01 | |||
| Frecuencia al mes | 0,01 | |||
| Frecuencia a los 6 meses | 0,05 | |||
| Analgésicos al mes | ||||
| Analgésicos a los 3 meses | 0,05 | 0,05 | ||
| Analgésicos a los 6 meses | 0,05 | |||
| Discapacidad al mes | ||||
| Discapacidad a los 3 meses | 0,05 | 0,01 | ||
| Discapacidad a los 6 meses | 0,05 | 0,01 | ||
| Sueño al mes | ||||
| Sueño a los 3 meses | 0,001 | |||
| Sueño a los 6 meses | 0,001 | |||
| CIF al mes | 0,001 | 0,001 | ||
| CIF a los 3 meses | 0,05 | 0,05 | 0,05 | 0,05 |
| CIF a los 6 meses | 0,05 | 0,01 | ||
| EVA al mes | 0,05 | 0,05 | ||
| EVA a los 3 meses | 0,001 | 0,001 | ||
| EVA a los 6 meses | 0,054 | 0,01 |
CIF: Cuestionario de Impacto de la Fibromialgia; EVA: escala visual analógica.
Diferencias estadísticamente significativas entre los grupos*
| Ketamina | Ozono | Craneopuntura | |
|---|---|---|---|
| Total dolor al mes | |||
| Total dolor a los 3 meses | p<0,05 | p<0,05 | |
| Total dolor a los 6 meses | p<0,05 | ||
| Intensidad al mes | |||
| Intensidad a los 3 meses | p<0,05 | p<0,05 | |
| Intensidad a los 6 meses | p<0,05 | ||
| Frecuencia al mes | |||
| Frecuencia a los 3 meses | |||
| Frecuencia a los 6 meses | |||
| Analgésicos al mes | |||
| Analgésicos a los 3 meses | |||
| Analgésicos a los 6 meses | |||
| Discapacidad al mes | |||
| Discapacidad a los 3 meses | |||
| Discapacidad a los 6 meses | p<0,05 | ||
| Sueño al mes | |||
| Sueño a los 3 meses | |||
| Sueño a los 6 meses | |||
| CIF al mes | p<0,01 | p<0,01 | |
| CIF a los 3 meses | |||
| CIF a los 6 meses | |||
| EVA al mes | |||
| EVA a los 3 meses | |||
| EVA a los 6 meses | p<0,05 |
CIF: Cuestionario de Impacto de la Fibromialgia; EVA: escala visual analógica.
Resultados en variables cuantitativas*
| Grupo control | Lidocaína | Ketamina | Ozono | Craneopuntura | |
|---|---|---|---|---|---|
| CIF antes | 75,4±12,1 | 78,1±11,8 | 74,1±11,3 | 77,5±12,8 | 72,1±12,3 |
| CIF al mes | 75,5±13,2 | 78,1±10,8 | 66,3±14,9 | 69±16,8 | 65±10,2 |
| CIF a los 3 meses | 77,8±11,4 | 67±10,8 | 71,7±16 | 64,7±15,3 | 61,2±19,9 |
| CIF a los 6 meses | 78,2±13,3 | 70,2±5,6 | 66,8±14,1 | 65,7±12,1 | 66,8±14,3 |
| EVA antes | 8,5±1,1 | 8±1,4 | 8,6±1,2 | 9±1,1 | 8,6±1,2 |
| EVA al mes | 8,6±1,7 | 8,1±1,6 | 7,8±1,8 | 7,6±2,1 | 7,4±1,3 |
| EVA a los 3 meses | 8,9±1,3 | 8,3±1,8 | 8,1±2,1 | 7,7±1,6 | 7±1,6 |
| EVA a los 6 meses | 9,1±1,7 | 9±1 | 8,1±1,6 | 8,7±1,1 | 7±2 |
CIF: Cuestionario de Impacto de la Fibromialgia; EVA: escala visual analógica.
Resultados en las variables cualitativas
| Grupo control | Lidocaína | Ketamina | Ozono | Craneopuntura | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Percentiles | Percentiles | Percentiles | Percentiles | Percentiles | |||||||||||
| 50 | 75 | 25 | 50 | 75 | 25 | 50 | 75 | 25 | 50 | 75 | 25 | 50 | 75 | 25 | |
| Total escala dolor antes | 12 | 14 | 16 | 12 | 14 | 16 | 13,2 | 15 | 16 | 13 | 14 | 15 | 14 | 15 | 17 |
| Total escala dolor al mes | 12 | 15 | 16 | 12 | 15 | 16 | 11,2 | 14 | 16 | 11 | 14 | 16 | 11 | 14 | 16 |
| Total escala dolor a los 3 meses | 13 | 14 | 16 | 13 | 14 | 16 | 12 | 14 | 16 | 11 | 13 | 15 | 10 | 13 | 14 |
| Total escala dolor a los 6 meses | 12 | 14 | 15 | 11 | 14 | 15,5 | 11,7 | 14 | 16 | 13 | 14 | 15,5 | 9 | 11 | 13 |
| Intensidad dolor antes | 2 | 3 | 3 | 2 | 3 | 3 | 3 | 3 | 4 | 3 | 4 | 4 | 3 | 3 | 4 |
| Intensidad dolor al mes | 3 | 3 | 3 | 3 | 3 | 3 | 2,2 | 3 | 3 | 1 | 3 | 3 | 2,2 | 3 | 3 |
| Intensidad dolor a los 3 meses | 3 | 3 | 3 | 3 | 3 | 3 | 2,2 | 3 | 3,7 | 2,2 | 3 | 2,2 | 2 | 2 | 3 |
| Intensidad dolor a los 6 meses | 3 | 3 | 3 | 3 | 3 | 3 | 1,2 | 3 | 3,7 | 2,5 | 3 | 2,5 | 2 | 2 | 3 |
| Frecuencia dolor antes | 4 | 4 | 4 | 4 | 4 | 4 | 4 | 4 | 4 | 2,2 | 3,5 | 3 | 3 | 4 | 4 |
| Frecuencia dolor al mes | 4 | 4 | 4 | 4 | 4 | 4 | 2 | 3 | 4 | 2 | 4 | 4 | 3 | 4 | 4 |
| Frecuencia dolor a los 3 meses | 4 | 4 | 4 | 4 | 4 | 4 | 2 | 4 | 4 | 2,2 | 3,5 | 3 | 3 | 4 | 4 |
| Frecuencia dolor a los 6 meses | 4 | 4 | 4 | 4 | 4 | 4 | 3 | 4 | 4 | 2 | 3 | 4 | 2 | 3 | 4 |
| Consumo analgésicos antes | 0 | 2 | 3 | 0 | 2 | 3 | 2 | 2 | 2 | 1 | 2 | 2 | 2 | 2 | 3 |
| Consumo analgésicos al mes | 0 | 2 | 3 | 0 | 2 | 3 | 2 | 2 | 2 | 1 | 2 | 2 | 2 | 2 | 3 |
| Consumo analgésicos a los 3 meses | 0 | 2 | 3 | 0 | 2 | 3 | 1 | 2 | 2 | 1,5 | 2,5 | 2 | 1 | 2 | 3 |
| Consumo analgésicos a los 6 meses | 0 | 2 | 3 | 0 | 2 | 3 | 2 | 2 | 2 | 2 | 2 | 2 | 1 | 2 | 3 |
| Incapacidad antes | 2 | 2 | 2 | 2 | 2 | 2 | 2 | 3 | 3 | 2 | 2 | 2,2 | 2 | 2 | 2 |
| Incapacidad al mes | 1 | 2 | 3 | 0 | 2 | 3 | 2 | 2 | 3 | 2 | 2 | 2 | 2 | 2 | 2 |
| Incapacidad a los 3 meses | 1 | 2 | 2 | 1,2 | 2 | 2 | 1,2 | 2 | 2 | 1 | 2 | 2 | 1 | 2 | 2 |
| Incapacidad a los 6 meses | 2 | 2 | 2 | 2 | 2 | 2,7 | 2 | 2 | 2 | 2 | 3 | 3 | 1 | 3 | 3 |
| Sueño antes | 2 | 3 | 3 | 2 | 3 | 3 | 3 | 4 | 4 | 2 | 2 | 4 | 4 | 4 | 4 |
| Sueño al mes | 3 | 3 | 3 | 3 | 3 | 3 | 2 | 3 | 4 | 1 | 2 | 4 | 3 | 3 | 3 |
| Sueño a los 3 meses | 3 | 3 | 3 | 3 | 3 | 3 | 3,2 | 4 | 4 | 3 | 4 | 3 | 1 | 3 | 4 |
| Sueño a los 6 meses | 3 | 3 | 3 | 3 | 3 | 3 | 1,2 | 2,5 | 4 | 1 | 3 | 3 | 1 | 3 | 3 |
El dolor es siempre una experiencia subjetiva, lo cual plantea problemas para emplear modelos teóricos e instrumentos de medición adecuados. Es muy difícil valorar todos los aspectos que entran a formar parte del dolor. Es importante tener en cuenta que la FM es una enfermedad crónica caracterizada por dolor recurrente en un período de meses o incluso más largo.
El hecho de no haber tenido en cuenta si el paciente realizaba intervenciones complementarias como gimnasia, taichi, yoga, psicoterapia, terapia ocupacional, rehabilitación, etc. puede constituir un sesgo, al igual que si un sujeto recibió tratamiento analgésico, antiinflamatorio, antidepresivo, etc. por una nueva patología crónica concomitante durante el período del estudio, dado que los sujetos pueden estar polimedicados. Al recoger los datos de forma autoaplicada, el sesgo de detección se igualó para todos los grupos.
Cada paciente constituyó su propio control antes-después del tratamiento asignado, por lo que se evitaron varios factores de confusión e interacción. El sesgo de selección se intentó evitar con la inclusión consecutiva de los pacientes remitidos que cumplían los criterios de inclusión, hasta que se completara el número necesario; por tanto, se considera que se incluye toda la población existente hasta un número determinado. El estudio pierde fuerza demostrativa debido a la pérdida de pacientes.
El cegamiento es especialmente importante en los estudios que utilizan medidas de resultado subjetivas como el dolor. El sesgo de realización era el sesgo principal que se podía cometer en este estudio ya que no es posible el cegamiento de la intervención y los participantes que eran conscientes de su grupo de asignación podrían cambiar su conducta. No obstante, los efectos observados por esta “contaminación” suelen estar más relacionados con comunicación de síntomas y efectos secundarios de fármacos.
Con un estudio antes-después se aporta la mejor evidencia en cuanto al efecto de una determinada intervención sanitaria en condiciones de práctica clínica, manteniendo el tratamiento habitual del paciente. El grupo de craneopuntura se muestra como el más eficaz (tabla 2) al haber obtenido más diferencias significativas entre los valores iniciales y a los 3 y 6 meses, seguido por el grupo de ketamina y el de autohemoterapia con ozono. Un estudio previo había mostrado la falta de eficacia de una sola dosis i.v. de ketamina en el alivio del dolor en pacientes con FM a los 2 meses24. Un protocolo con varias dosis como el usado en el presente trabajo ha conseguido algunas diferencias significativas en este sentido. El grupo de lidocaína obtuvo pobres resultados, lo cual confirma los resultados de otros estudios37.
Al haber obtenido más diferencias significativas, el grupo de craneopuntura se muestra también como el más eficaz (tabla 3) frente a los otros (especialmente a los 6 meses), seguido del de autohemoterapia con ozono (especialmente a los 3 meses). Los grupos de ketamina y lidocaína obtuvieron pobres resultados.
No hubo diferencias significativas entre los grupos para la incapacidad al mes, lo que implica que los sujetos del grupo de ketamina mejoraron notablemente en ese intervalo de tiempo, teniendo en cuenta que se encontraron diferencias para la incapacidad al inicio en contra del grupo de ketamina en comparación con los otros (p<0,01). Se observó una mejoría muy significativa de la incapacidad entre los meses 3 y 6 en el grupo de craneopuntura (tabla 5).
Los buenos resultados obtenidos en el grupo que recibió craneopuntura pueden deberse, en una medida importante, al uso de electroacupuntura. Un trabajo reciente en ratas sugiere que la electroacupuntura a alta y baja frecuencia es eficaz en la reducción de la hiperalgesia en un modelo de dolor muscular crónico38. Se desconoce la acción por la que la electroacupuntura y la craneopuntura actúan sobre la sensibilización patológica de los mecanismos del cerebro que integran las señales nociceptivas.
ConclusiónEn relación con las técnicas estudiadas se podría concluir que habría que utilizar como primera medida terapéutica el protocolo de craneopuntura y descartar el de lidocaína. La duda aparece acerca de cuál utilizar en segundo lugar, ya que el protocolo de ketamina parece eficaz pero tiene más efectos secundarios que la autohemoterapia con ozono.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Trabajo presentado parcialmente en el XI Congreso de la Sociedad Española del Dolor celebrado en Toledo del 22 al 24 de mayo de 2014.